名校
解题方法
1 . 亚硝酸钠(NaNO2)是一种工业盐,实验室可用如图装置(略去部分夹持仪器)制备。

已知:
① ;
;
② ;
;
③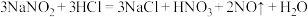 ;
;
④酸性条件下,NO和 都能与
都能与 反应生成
反应生成 和
和 ;
; 能使酸性高锰酸钾溶液褪色。
能使酸性高锰酸钾溶液褪色。
(1)加热装置A前,先通一段时间N2,目的是_______ ;
(2)装置A中发生反应的化学方程式为_______ ;
(3)实验结束后,B瓶溶液中溶质的主要成分是_______ (填化学式)。
(4)仪器C中盛放的药品为_______ (填名称)。
(5)充分反应后,检验装置D中产物的方法是:取产物少许置于试管中,_______ ,则产物是NaNO2 (注明试剂、现象)。
(6)装置F的作用是_______ ;
(7)为测定亚硝酸钠的含量,称取4.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,再向锥形瓶中加入0.1000molL酸性KMnO4溶液20.00mL,两者恰好完全反应。计算所得固体中亚硝酸钠的质量分数_______ 。(写出计算过程)

已知:
①
 ;
;②
 ;
;③
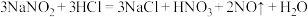 ;
;④酸性条件下,NO和
 都能与
都能与 反应生成
反应生成 和
和 ;
; 能使酸性高锰酸钾溶液褪色。
能使酸性高锰酸钾溶液褪色。(1)加热装置A前,先通一段时间N2,目的是
(2)装置A中发生反应的化学方程式为
(3)实验结束后,B瓶溶液中溶质的主要成分是
(4)仪器C中盛放的药品为
(5)充分反应后,检验装置D中产物的方法是:取产物少许置于试管中,
(6)装置F的作用是
(7)为测定亚硝酸钠的含量,称取4.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,再向锥形瓶中加入0.1000molL酸性KMnO4溶液20.00mL,两者恰好完全反应。计算所得固体中亚硝酸钠的质量分数
您最近一年使用:0次
2021-04-28更新
|
449次组卷
|
4卷引用:江苏省常熟市2020-2021学年高一下学期期中化学试题
名校
解题方法
2 . 亚硝酰硫酸(NOSO4H)主要用于染料、医药等工业。实验室用如下图装置(夹持装置略)制备少量NOSO4H,并测定产品的纯度。已知:NOSO4H遇水分解,但溶于浓硫酸而不分解。

(1)装置A利用Na2SO3和硫酸制取SO2,导管b的作用是___________ 。
(2)装置B中浓HNO3与SO2在浓H2SO4作用下化合制得NOSO4H,该反应为放热反应。
①该反应必须维持体系温度不得高于20℃,采取的措施除了冷水浴外,还可以采取的操作是______ 。
②开始反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速度明显加快,其原因是______ 。
(3)该实验装置存在可能导致NOSO4H产量降低的缺陷是___________ 。
(4)测定亚硝酰硫酸NOSO4H的纯度。
准确称取1.380g产品放入250mL的碘量瓶中,加入0.1000mol/L、60.00mL的KMnO4溶液和10mL25%H2SO4溶液,摇匀。然后将0.2500mol/L草酸钠(Na2C2O4)溶液滴入碘量瓶中,消耗草酸钠溶液的体积为20.00mL。
已知:
①配平下面的方程式:___________ 。
_______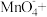 _______
_______ _______
_______ ______
______
 ______
______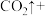 ______
______
②亚硝酰硫酸的质量分数=___________ 。(精确到0.1%)(写出计算过程)

(1)装置A利用Na2SO3和硫酸制取SO2,导管b的作用是
(2)装置B中浓HNO3与SO2在浓H2SO4作用下化合制得NOSO4H,该反应为放热反应。
①该反应必须维持体系温度不得高于20℃,采取的措施除了冷水浴外,还可以采取的操作是
②开始反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速度明显加快,其原因是
(3)该实验装置存在可能导致NOSO4H产量降低的缺陷是
(4)测定亚硝酰硫酸NOSO4H的纯度。
准确称取1.380g产品放入250mL的碘量瓶中,加入0.1000mol/L、60.00mL的KMnO4溶液和10mL25%H2SO4溶液,摇匀。然后将0.2500mol/L草酸钠(Na2C2O4)溶液滴入碘量瓶中,消耗草酸钠溶液的体积为20.00mL。
已知:

①配平下面的方程式:
_______
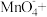 _______
_______ _______
_______ ______
______
 ______
______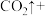 ______
______
②亚硝酰硫酸的质量分数=
您最近一年使用:0次
2023-04-10更新
|
458次组卷
|
2卷引用:江苏省苏州中学2022-2023学年高一下学期期中考试化学试题
名校
解题方法
3 . 三氯化铬( )在工业上主要用作媒染剂和催化剂,
)在工业上主要用作媒染剂和催化剂, 常用于颜料、陶瓷、橡胶等工业,实验室模拟工业上以
常用于颜料、陶瓷、橡胶等工业,实验室模拟工业上以 为原料制备
为原料制备 和
和 。
。
(1)制备 。取一定质量的
。取一定质量的 和对应量的水加入到三颈瓶中,水浴加热并搅拌,一段时间后同时加入过量浓盐酸和无水乙醇充分反应,生成
和对应量的水加入到三颈瓶中,水浴加热并搅拌,一段时间后同时加入过量浓盐酸和无水乙醇充分反应,生成 并放出
并放出 气体。
气体。
①上述反应的化学方程式为_______ 。
②上述反应中的乙醇与 投料的物质的量比例大约为3:8,原因是
投料的物质的量比例大约为3:8,原因是_______ 。
(2)测定 的质量分数。
的质量分数。
Ⅰ.称取样品0.3300g,加水溶解并配成250.0mL的溶液。
Ⅱ.移取25.00mL样品溶液于带塞的锥形瓶中,加热至沸后加入稍过量的 ,稀释并加热煮沸,再加入过量的硫酸酸化,将
,稀释并加热煮沸,再加入过量的硫酸酸化,将 氧化为
氧化为 ;再加入过量KI固体加塞摇匀,使铬完全以
;再加入过量KI固体加塞摇匀,使铬完全以 的形式存在。
的形式存在。
Ⅲ.加入1mL淀粉溶液,用0.0250 标准
标准 溶液滴定至终点,平行测定3次,平均消耗标准
溶液滴定至终点,平行测定3次,平均消耗标准 溶液24.00mL。
溶液24.00mL。
已知反应:
 (未配平)
(未配平)
 (未配平)
(未配平)
①滴定终点的现象是_______ 。
②计算 的质量分数(写出计算过程)
的质量分数(写出计算过程)_______ 。
(3)制备 。Cr(Ⅲ )的存在形态的物质的量分数随溶液pH的分布如图所示。
。Cr(Ⅲ )的存在形态的物质的量分数随溶液pH的分布如图所示。

请补充完整由 溶液制备
溶液制备 的实验方案:取适量
的实验方案:取适量 溶液,
溶液,_______ ,低温烘干,得到 晶体(实验中须使用的试剂:1
晶体(实验中须使用的试剂:1 NaOH溶液、0.1
NaOH溶液、0.1
 溶液、0.1
溶液、0.1
 溶液、蒸馏水)。
溶液、蒸馏水)。
 )在工业上主要用作媒染剂和催化剂,
)在工业上主要用作媒染剂和催化剂, 常用于颜料、陶瓷、橡胶等工业,实验室模拟工业上以
常用于颜料、陶瓷、橡胶等工业,实验室模拟工业上以 为原料制备
为原料制备 和
和 。
。(1)制备
 。取一定质量的
。取一定质量的 和对应量的水加入到三颈瓶中,水浴加热并搅拌,一段时间后同时加入过量浓盐酸和无水乙醇充分反应,生成
和对应量的水加入到三颈瓶中,水浴加热并搅拌,一段时间后同时加入过量浓盐酸和无水乙醇充分反应,生成 并放出
并放出 气体。
气体。①上述反应的化学方程式为
②上述反应中的乙醇与
 投料的物质的量比例大约为3:8,原因是
投料的物质的量比例大约为3:8,原因是(2)测定
 的质量分数。
的质量分数。Ⅰ.称取样品0.3300g,加水溶解并配成250.0mL的溶液。
Ⅱ.移取25.00mL样品溶液于带塞的锥形瓶中,加热至沸后加入稍过量的
 ,稀释并加热煮沸,再加入过量的硫酸酸化,将
,稀释并加热煮沸,再加入过量的硫酸酸化,将 氧化为
氧化为 ;再加入过量KI固体加塞摇匀,使铬完全以
;再加入过量KI固体加塞摇匀,使铬完全以 的形式存在。
的形式存在。Ⅲ.加入1mL淀粉溶液,用0.0250
 标准
标准 溶液滴定至终点,平行测定3次,平均消耗标准
溶液滴定至终点,平行测定3次,平均消耗标准 溶液24.00mL。
溶液24.00mL。已知反应:
 (未配平)
(未配平) (未配平)
(未配平)①滴定终点的现象是
②计算
 的质量分数(写出计算过程)
的质量分数(写出计算过程)(3)制备
 。Cr(Ⅲ )的存在形态的物质的量分数随溶液pH的分布如图所示。
。Cr(Ⅲ )的存在形态的物质的量分数随溶液pH的分布如图所示。
请补充完整由
 溶液制备
溶液制备 的实验方案:取适量
的实验方案:取适量 溶液,
溶液, 晶体(实验中须使用的试剂:1
晶体(实验中须使用的试剂:1 NaOH溶液、0.1
NaOH溶液、0.1
 溶液、0.1
溶液、0.1
 溶液、蒸馏水)。
溶液、蒸馏水)。
您最近一年使用:0次
2022-11-04更新
|
331次组卷
|
2卷引用:江苏省苏州市2022-2023学年高三上学期期中调研化学试题
名校
4 . 以SO2、软锰矿(主要成分MnO2,少量Fe、Al、Ca及Pb的化合物等)、氨水及净化剂等为原料可制备MnSO4溶液和Mn3O4,主要实验步骤如下:

步骤Ⅰ:如图所示装置,将SO2通入B中的软锰矿浆液中(MnO2+SO2 = MnSO4)。
步骤Ⅱ:充分反应后,在不断搅拌下依次向三口烧瓶中加入适量纯净的MnO2、MnCO3,最后加入适量Na2S沉铅等重金属。
步骤Ⅲ:过滤得MnSO4溶液。
(1)装置A用于制取SO2,反应的化学方程式为_____ 。
(2)装置B中反应应控制在90~100℃,适宜的加热方式是_____ 。
(3)装置C的作用是_____ 。
(4)“步骤Ⅱ”中加入纯净MnO2的目的是_____ ,用MnCO3调节溶液pH时,需调节溶液pH范围为_____ (该实验条件下,部分金属离子开始沉淀和沉淀完全的pH如下)。
(5)已知:①用空气氧化Mn(OH)2浊液可制备Mn3O4[6Mn(OH)2+O2 2Mn3O4+6H2O],主要副产物为MnOOH;反应温度和溶液pH对产品中Mn的质量分数的影响如下图所示:
2Mn3O4+6H2O],主要副产物为MnOOH;反应温度和溶液pH对产品中Mn的质量分数的影响如下图所示:

②反应温度超过80℃时,Mn3O4产率开始降低。
③Mn(OH)2是白色沉淀,Mn3O4呈黑色;Mn3O4、MnOOH中锰的质量分数理论值依次为72.03%、62.5%。
请补充完整由步骤Ⅲ得到的MnSO4溶液,并用氨水等制备较纯净的Mn3O4的实验方案:_____ ,真空干燥6小时得产品Mn3O4。

步骤Ⅰ:如图所示装置,将SO2通入B中的软锰矿浆液中(MnO2+SO2 = MnSO4)。
步骤Ⅱ:充分反应后,在不断搅拌下依次向三口烧瓶中加入适量纯净的MnO2、MnCO3,最后加入适量Na2S沉铅等重金属。
步骤Ⅲ:过滤得MnSO4溶液。
(1)装置A用于制取SO2,反应的化学方程式为
(2)装置B中反应应控制在90~100℃,适宜的加热方式是
(3)装置C的作用是
(4)“步骤Ⅱ”中加入纯净MnO2的目的是
| 金属离子 | Fe2+ | Fe3+ | Al3+ | Mn2+ |
| 开始沉淀pH | 7.04 | 1.87 | 3.32 | 7.56 |
| 沉淀完全pH | 9.18 | 3.27 | 4.9 | 10.2 |
 2Mn3O4+6H2O],主要副产物为MnOOH;反应温度和溶液pH对产品中Mn的质量分数的影响如下图所示:
2Mn3O4+6H2O],主要副产物为MnOOH;反应温度和溶液pH对产品中Mn的质量分数的影响如下图所示: 
②反应温度超过80℃时,Mn3O4产率开始降低。
③Mn(OH)2是白色沉淀,Mn3O4呈黑色;Mn3O4、MnOOH中锰的质量分数理论值依次为72.03%、62.5%。
请补充完整由步骤Ⅲ得到的MnSO4溶液,并用氨水等制备较纯净的Mn3O4的实验方案:
您最近一年使用:0次
2019-02-13更新
|
454次组卷
|
2卷引用:江苏省苏州市第一中学2019-2020高二下学期期中考试化学试题
名校
5 . 某兴趣小组模拟工业制漂白粉,设计了如下图所示的实验装置。
已知:①氯气与碱反应放出热量。②6Cl2+6Ca(OH)2=5CaCl2+Ca(ClO3)2+6H2O。
试回答下列问题:

(1)甲装置中仪器a的名称是________________________ 。
(2)装置乙中饱和食盐水的作用是________________________ 。
(3)装置丁中发生反应的化学方程式为_____________________ 。
(4)漂白粉在空气中失效的原因是______________ 、______________ (用化学方程式表示)。
(5)①该小组制得的漂白粉中n(CaCl2)远大于n[Ca(ClO)2],其主要原因是________ 。
②为提高Ca(ClO)2的含量。可采取的措施是___________ (任写一种即可)。
已知:①氯气与碱反应放出热量。②6Cl2+6Ca(OH)2=5CaCl2+Ca(ClO3)2+6H2O。
试回答下列问题:

(1)甲装置中仪器a的名称是
(2)装置乙中饱和食盐水的作用是
(3)装置丁中发生反应的化学方程式为
(4)漂白粉在空气中失效的原因是
(5)①该小组制得的漂白粉中n(CaCl2)远大于n[Ca(ClO)2],其主要原因是
②为提高Ca(ClO)2的含量。可采取的措施是
您最近一年使用:0次



