解题方法
1 . 某同学为了验证海带中含有碘,在实验室进行如下实验。下列说法正确的是
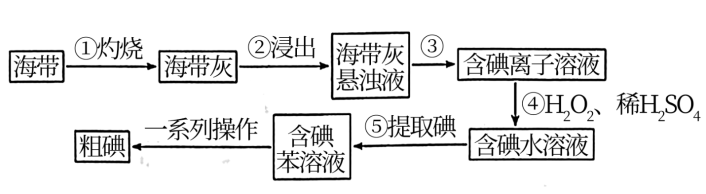

| A.步骤③所需玻璃仪器为漏斗、烧杯、玻璃棒 |
B.步骤④中 的作用为催化剂 的作用为催化剂 |
| C.步骤⑤含碘苯溶液从仪器的下口放出 |
| D.“粗碘”固体中含有少量硫酸钠固体,可采用升华的方法提纯获得碘单质 |
您最近一年使用:0次
2021-07-21更新
|
659次组卷
|
3卷引用:河北省张家口市2020-2021学年高一下学期期末考试化学试题
2 . 海洋资源的利用具有非常广阔的前景。回答下列问题:
Ⅰ.海水提溴
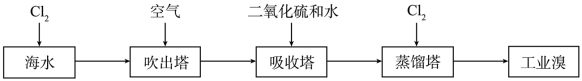
(1)溴元素在元素周期表中的位置为_______ 。
(2)吸收塔用二氧化硫和水吸收Br2的离子反应方程式:_______ 。
(3)蒸馏塔的蒸馏温度应控制在80-90°C最有利于生产,原因可能为:温度过高,_______ ;温度过低,_______ 。
Ⅱ.海水提镁
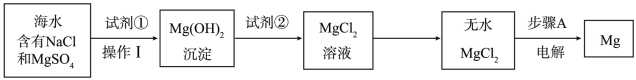
(4)工业上常用于沉淀Mg2+的廉价试剂①的俗名是_______ 。操作Ⅰ的名称是_______ 。
(5)步骤A的化学方程式为_______ 。
Ⅲ.海带提碘

(6)步骤B需搅拌、加热煮沸的目的是_______ 。步骤C中反应的离子方程式为_______ 。
Ⅰ.海水提溴

(1)溴元素在元素周期表中的位置为
(2)吸收塔用二氧化硫和水吸收Br2的离子反应方程式:
(3)蒸馏塔的蒸馏温度应控制在80-90°C最有利于生产,原因可能为:温度过高,
Ⅱ.海水提镁

(4)工业上常用于沉淀Mg2+的廉价试剂①的俗名是
(5)步骤A的化学方程式为
Ⅲ.海带提碘

(6)步骤B需搅拌、加热煮沸的目的是
您最近一年使用:0次
2022-07-10更新
|
351次组卷
|
2卷引用:湖北省新高考联考协作体2021-2022学年高一下学期期末考试化学试题
3 . 围绕海水的综合利用,化学课外兴趣小组进行下列实验:
(1)模拟工业制备氯气
装置如图所示,接通电源,当观察到石墨电极与滤纸接触的区域有细小的气泡产生时,停止通电。将pH试纸分别放在a、b处滤纸上,观察颜色变化。
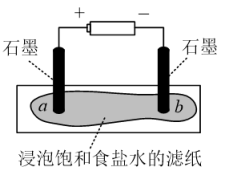
①在上述实验中观察a处pH试纸中心呈白色,边缘有一圈淡淡的红色,b处pH试纸呈___________ 色。
②实验结束后,将滤纸对折,使a、b处充分接触,可将a处残余的Cl2进一步处理。此时发生反应的化学反应方程式是___________ 。
(2)模拟反萃取法提取碘实验流程如下图:
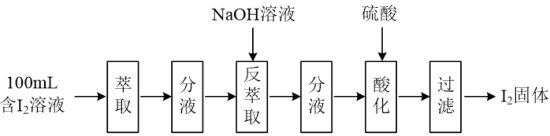
①“萃取”操作时须使用的玻璃仪器有烧杯、玻璃棒和___________ 。
②“反萃取”操作时溶液中有I-、IO 生成。“酸化”步骤发生反应的离子反应方程式为
生成。“酸化”步骤发生反应的离子反应方程式为___________ 。
(3)模拟浓海水提取镁实验流程如下图:
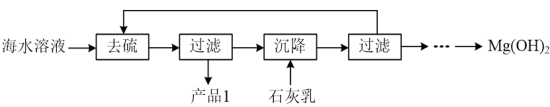
说明:模拟浓海水成分配制的“海水溶液”主要成分如下:
①产品1的化学式为___________ 。
②沉降阶段主要的化学反应方程式为___________ 。
(1)模拟工业制备氯气
装置如图所示,接通电源,当观察到石墨电极与滤纸接触的区域有细小的气泡产生时,停止通电。将pH试纸分别放在a、b处滤纸上,观察颜色变化。

①在上述实验中观察a处pH试纸中心呈白色,边缘有一圈淡淡的红色,b处pH试纸呈
②实验结束后,将滤纸对折,使a、b处充分接触,可将a处残余的Cl2进一步处理。此时发生反应的化学反应方程式是
(2)模拟反萃取法提取碘实验流程如下图:

①“萃取”操作时须使用的玻璃仪器有烧杯、玻璃棒和
②“反萃取”操作时溶液中有I-、IO
 生成。“酸化”步骤发生反应的离子反应方程式为
生成。“酸化”步骤发生反应的离子反应方程式为(3)模拟浓海水提取镁实验流程如下图:

说明:模拟浓海水成分配制的“海水溶液”主要成分如下:
| 离子 | Na+ | Mg2+ | Cl- | SO |
| 浓度/(g·L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
②沉降阶段主要的化学反应方程式为
您最近一年使用:0次
名校
解题方法
4 . 海带提碘是工业碘的主要来源之一,下列说法错误的是:
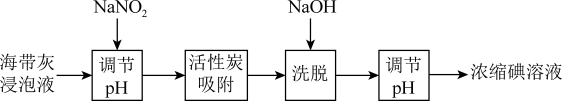

| A.NaNO2可将I-氧化为I2 |
B.“洗脱”时发生3I2+6OH-=IO +5I-+3H2O +5I-+3H2O |
| C.活性炭不仅能够吸附I2还可以循环使用 |
| D.浓缩碘溶液中的碘可以用酒精萃取 |
您最近一年使用:0次
2022-01-20更新
|
280次组卷
|
3卷引用:福建省福州市2021-2022学年高三上学期期末质量抽测化学试卷
福建省福州市2021-2022学年高三上学期期末质量抽测化学试卷(已下线)一轮巩固卷7-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(广东专用)湖南省株洲市醴陵市第一中学2021-2022学年高三下学期期中考试化学试题
名校
解题方法
5 . 海水提溴与海带提碘,共同点是
| A.浓缩方法 | B.采用热空气吹出 |
| C.四氯化碳萃取 | D.氧化剂可选择氯水 |
您最近一年使用:0次
2023-04-14更新
|
285次组卷
|
2卷引用:上海市建平中学2023-2024学年高一上学期期末教学质量检测化学试卷
名校
解题方法
6 . 海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
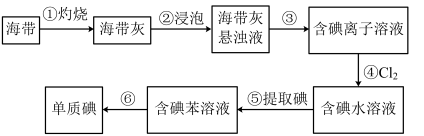
请填写下列空白:
(1)步骤③⑥的实验操作名称分别是_______ 和_______ 。步骤④反应的离子方程式是_______ 。除了氯水,从绿色化学角度考虑,最合适的试剂为_______ 。
A.浓硫酸 B.浓硝酸 C.KMnO4溶液 D.H2O2
(2)步骤⑤中,某学生选择用苯来提取碘的理由有:碘与苯不反应;苯与水不互溶:还有_______ 。从含碘水溶液中获得含碘苯溶液,该操作名称为_______ ,用到最主要仪器为_______ ,不能用酒精代替苯的理由是:_______
(3)向一容积为15 mL的试管中先加入3 mL碘水,再加入1 mL苯,充分振荡、静置后,下列图示现象正确的是_______

关于卤素氯、溴、碘的叙述,错误的是_______
a.单质易溶于有机溶剂中 b. X-的颜色逐渐加深
c.单质氧化性性逐渐减弱 d.X-的还原性逐渐增强

请填写下列空白:
(1)步骤③⑥的实验操作名称分别是
A.浓硫酸 B.浓硝酸 C.KMnO4溶液 D.H2O2
(2)步骤⑤中,某学生选择用苯来提取碘的理由有:碘与苯不反应;苯与水不互溶:还有
(3)向一容积为15 mL的试管中先加入3 mL碘水,再加入1 mL苯,充分振荡、静置后,下列图示现象正确的是

关于卤素氯、溴、碘的叙述,错误的是
a.单质易溶于有机溶剂中 b. X-的颜色逐渐加深
c.单质氧化性性逐渐减弱 d.X-的还原性逐渐增强
您最近一年使用:0次
7 . 海带中含有碘元素,可通过以下步骤提取:①灼烧海带成灰:②将海带灰转移,加入蒸馏水,搅拌,煮沸;③过滤,向滤液中滴入氯水,振荡;④将氧化后溶液转移,向其中加入CCl4振荡,静置。以上步骤不需要用到的仪器是
A.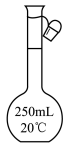 | B.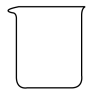 | C. | D.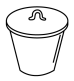 |
您最近一年使用:0次
名校
8 . 碘元素是我们人体不可或缺的微量元素,某化学兴趣小组在实验室模拟工业提碘,流程图如下,请回答下列问题:
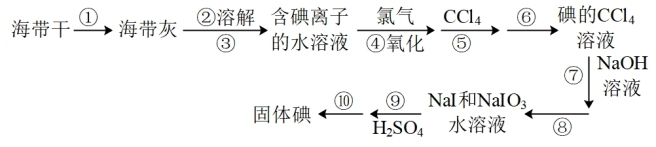
(1)请填写流程图中的操作步骤名称:③___________ ; ⑤___________ ;⑧___________ ;⑩___________ 。
(2)请填写该操作所需要的重要仪器名称:①___________ ;⑥___________ 。
(3)步骤①的目的是:___________ 。步骤④⑤⑥⑦⑧的目的是:___________ 。
(4)检验步骤③后的水溶液中是否含有碘离子的方法是___________ 。
(5)请写出步骤⑦发生的离子方程式:___________ 。
(6)为了获得更纯净的碘单质,针对固体碘可以进行的操作是___________。(填写编号)

(1)请填写流程图中的操作步骤名称:③
(2)请填写该操作所需要的重要仪器名称:①
(3)步骤①的目的是:
(4)检验步骤③后的水溶液中是否含有碘离子的方法是
(5)请写出步骤⑦发生的离子方程式:
(6)为了获得更纯净的碘单质,针对固体碘可以进行的操作是___________。(填写编号)
| A.加入干燥剂,加热升华 | B.蒸馏 |
| C.重结晶 | D.萃取、分液 |
您最近一年使用:0次
解题方法
9 . 某同学取干海带经下列加工流程,从中提取 。下列说法错误的是
。下列说法错误的是
 。下列说法错误的是
。下列说法错误的是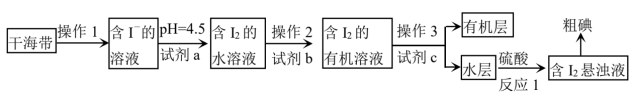

| A.操作1中至少包括灼烧、溶解、过滤等主要过程 |
B.试剂a可以是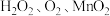 等氧化剂,试剂b可以是 等氧化剂,试剂b可以是 |
| C.操作2和3均用到分液漏斗,振荡萃取时分液漏斗下口要向下倾斜,并不断放气 |
D.反应1每得到127克碘,转移电子数约为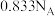 (NA为阿伏加德罗常数的值) (NA为阿伏加德罗常数的值) |
您最近一年使用:0次
2024-02-07更新
|
308次组卷
|
4卷引用:山东省威海市2023-2024学年高一上学期期末考试化学试题
山东省威海市2023-2024学年高一上学期期末考试化学试题(已下线)8.1自然资源的开发利用课后作业基础篇(已下线)8.1.1 金属矿物、海水资源的开发利用8.1.1金属矿物、海水资源的开发利用 课堂例题
10 . 实验室模拟工业从海藻中提取碘的流程如图:
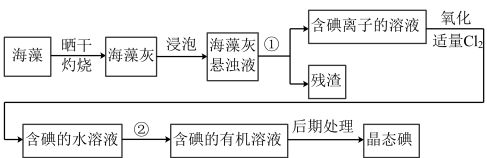
(1)选择合适实验操作名称填入流程图中:①_____ ,②_____ 。
A.溶解 B.过滤 C.萃取 D.分液
从“含碘的有机溶液”中回收溶剂,并得到碘单质,可选用如图装置完成。
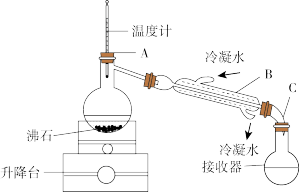
(2)装置中间部分是“冷凝管”,该装置中有一处明显的错误是_____ 。
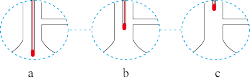
(3)装置A中,温度计所处的正确位置是_____ 。(选填编号)

(1)选择合适实验操作名称填入流程图中:①
A.溶解 B.过滤 C.萃取 D.分液
从“含碘的有机溶液”中回收溶剂,并得到碘单质,可选用如图装置完成。

(2)装置中间部分是“冷凝管”,该装置中有一处明显的错误是
(3)装置A中,温度计所处的正确位置是

您最近一年使用:0次



