9. CO
2是一种温室气体,对人类的生存环境产生巨大的影响,维持大气中CO
2的平衡对生态环境保护有着重要意义。
(1)CO
2加氢合成低碳烯烃技术能有效利用CO
2,以合成C
2H
4为例。该转化分为两步进行:
第一步:CO
2(g)+H
2(g)

CO(g)+H
2O(g)
Δ
H1=+41.3kJ/mol
第二步:2CO(g)+4H
2(g)

C
2H
4(g)+2H
2O(g)
Δ
H2=-210.5kJ/mol
CO
2加氢合成乙烯的热化学方程式为
__。
(2)利用CO
2和H
2合成甲醇又是一个有效利用CO
2的途径,反应如下:CO
2(g)+3H
2(g)

CH
3OH(g)+H
2O(g)
Δ
H3①在容积为2L的恒容密闭容器中,通入2molCO
2和3molH
2发生上述反应,下列说法能够表明该可逆反应达到平衡状态的是
__(填字母)
a.消耗1.5molH
2时,有0.5molCH
3OH生成
b.转移3mol电子时,消耗11.2L(标准状况下)CO
2c.体系中气体的密度不变
d.水蒸气的体积分数保持不变
e.单位时间内生成H
2与生成H
2O的物质的量之比为3:1
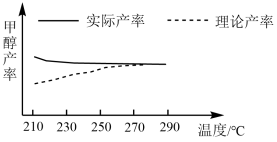
②研究温度对该反应甲醇产率的影响。在210℃~290℃,保持原料气中CO
2和H
2的投料比不变,按一定流速发生上述反应。得到甲醇平衡产率与温度的关系如图所示,Δ
H3__0(填“>”、“=”或“<”)。判断依据是
__。
③在一固定容积的密闭容器中发生上述反应。若要提高平衡时CH
3OH产率,则可以采取的措施是
__(填字母)。
a.升温
b.加入催化剂
c.增加CO
2的浓度
d.加入H
2加压
e.加入惰性气体
f.分离出甲醇
(3)在一定温度和催化剂作用下,也可将CO
2转化为燃料CH
4,反应方程式为CO
2(g)+4H
2(g)

CH
4(g)+2H
2O(g)。当30℃时,一定量的CO
2和H
2混合气体在容积为1L的恒容密闭容器中发生上述反应,5min后达到平衡,此时各物质的浓度如下表:
| 物质 | CO2(g) | H2(g) | CH4(g) | H2O(g) |
| 浓度/mol·L-1 | 0.2 | 0.8 | a | 1.6 |
则a=
__,该反应平衡常数
K=
__。
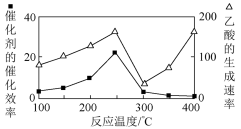
(4)以TiO
2/Cu
2Al
2O
4为催化剂,利用CH
4可以将CO
2直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系如图所示,乙酸的生成速率主要取决于温度影响的范围是
__。250~300℃时,温度升高而乙酸的生成速率降低的原因是
__。