23. 硝酸铜是重要的工业用品,可用作陶瓷的着色剂以及制备铜系催化剂等。
I.实验室可用如图装置制备硝酸铜,取一容积为300 mL的注射器与蒸馏烧瓶(500 mL)相连,向烧瓶中加入0.384g铜片和18mL 2.5mol/L的稀HNO
3溶液。
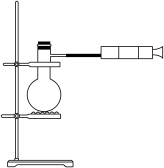
回答下列问题:
(1)欲加快铜与硝酸的反应速率,可采用多种不同的措施,若采用化学试剂法,下列试剂中可以使用的是
_______。
A.蒸馏水
B.无水醋酸钠
C.加入1mL浓H
2SO
4 D.AgNO
3溶液
(2)反应停止后,使生成的气体与液体间继续反应。若忽略液体体积变化,最终溶液中的

的物质的量浓度与开始时相比
_______(填“不变”、“变大”或“变小”)
II.工业上生产硝酸铜晶体的流程图如图l:
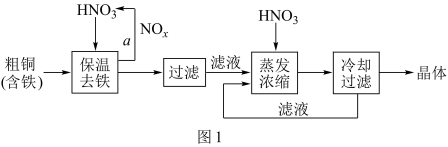
(3)若保温去铁反应生成气体是NO时,则离子方程式是
_______。
(4)蒸发浓缩时,要用硝酸调节溶液的pH=1,其目的是
_______(结合离子方程式说明)。
(5)如图2所示为硝酸铜晶体[Cu(NO
3)
2•nH
2O]的溶解度曲线(温度在30℃前后对应不同的晶体)从图中获取如下信息,不正确的有
_______(填字母)。

a.C点溶液为Cu(NO
3)
2的不饱和溶液
b.30℃时结晶可析出两种晶体
c.按上述流程最终得到的晶体是Cu(NO
3)
2•3H
2O
d.将A点溶液升温至30℃时,可以析出Cu(NO
3)
2•3H
2O晶体
(6)某些共价化合物(如H
2O、NH
3、N
2O
4等)在液态时发生了微弱的电离,如:

,则液态NH
3电离的方程式是
_______。液态N
2O
4电离得到电子数相差18的阴阳离子,因此可用Cu与液态N
2O
4反应制备无水硝酸铜,其反应的化学方程式是
_______