江西省赣州市十六县(市)十七校2020-2021学年高一下学期期中联考化学试题
江西
高一
期中
2021-05-07
327次
整体难度:
容易
考查范围:
常见无机物及其应用、化学与STSE、认识化学科学、化学反应原理、物质结构与性质、化学实验基础
江西省赣州市十六县(市)十七校2020-2021学年高一下学期期中联考化学试题
江西
高一
期中
2021-05-07
327次
整体难度:
容易
考查范围:
常见无机物及其应用、化学与STSE、认识化学科学、化学反应原理、物质结构与性质、化学实验基础
一、单选题 添加题型下试题
单选题
|
较易(0.85)
解题方法
1. 化学与生活、科技及环境密切相关。下列说法不正确的是
| A.2020年3月发射了北斗系统第五十四颗导航卫星,其计算机的芯片材料是高纯度硅 |
| B.为了防止感染“新冠病毒”,坚持每天使用无水酒精杀菌消毒 |
| C.硅胶常用作食品干燥剂,也可以用作催化剂载体 |
| D.葡萄酒中通常含有微量SO2,既可以杀菌又可以防止营养成分被氧化 |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
解题方法
2. 用NA表示阿伏加德罗常数的值,下列判断正确的是
A.常温常压下,18g 所含的中子数为9NA 所含的中子数为9NA |
| B.常温下,7.8g固体Na2O2中,含有的阴阳离子总数为0.4NA |
| C.常温常压下,17g氨气中含有非极性共价键为3NA |
| D.用金属铁、Cu片、稀硫酸组成原电池,当金属铁质量减轻5.6g时,流过外电路的电子为0.3NA |
您最近一年使用:0次
2021-04-25更新
|
150次组卷
|
2卷引用:江西省赣州市十六县(市)十七校2020-2021学年高一下学期期中联考化学试题
单选题
|
容易(0.94)
名校
3. 下列表示正确的是
A.原子核中有8个中子的氧离子: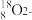 | B.次氯酸的结构式: |
C. 的比例模型 的比例模型 | D. 的电子式: 的电子式: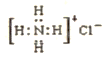 |
您最近一年使用:0次
2021-04-25更新
|
223次组卷
|
2卷引用:江西省赣州市十六县(市)十七校2020-2021学年高一下学期期中联考化学试题
单选题
|
适中(0.65)
解题方法
4. 下列反应的离子方程式或物质的形成过程正确的是
A.铜跟浓 反应: 反应: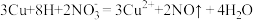 |
B.向 溶液中加入过量的 溶液中加入过量的 溶液: 溶液: 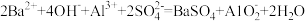 |
C.将氯气通入冷的氢氧化钠溶液中: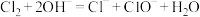 |
D.三氯化铁溶液中加入铜粉: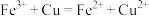 |
【知识点】 离子反应的发生及书写 离子方程式的正误判断解读
您最近一年使用:0次
单选题
|
较易(0.85)
解题方法
5. 下列实验操作规范且能达到目的的是
A.溶液的配制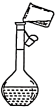 | B.氯气的净化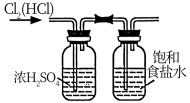 |
C.沉淀的过滤 | D.氨气的收集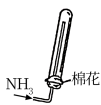 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
6. 推理是一种重要的能力。打开分液漏斗活塞,进行如图所示的探究实验,对实验现象的预测及分析错误的是
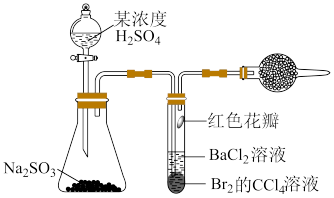
| A.试管内CCl4层溶液褪色,说明Br2具有氧化性 |
| B.试管中的红色花瓣褪色,说明SO2具有漂白性 |
| C.试管中产生大量气泡,说明Na2SO3被氧化产生SO3 |
D.一段时间后试管内有白色沉淀,说明有SO 生成 生成 |
【知识点】 二氧化硫的化学性质
您最近一年使用:0次
2021-01-25更新
|
2853次组卷
|
17卷引用:广东省2021年普通高中学业水平选择考适应性测试化学试题
广东省2021年普通高中学业水平选择考适应性测试化学试题江西省赣州市十六县(市)十七校2020-2021学年高一下学期期中联考化学试题山东省济宁市任城区2020-2021学年高一下学期期中考试化学试题湖北省武汉市蔡甸区汉阳一中2020-2021学年高一下学期5月月考化学试题辽宁省庄河市高级中学2021-2022学年高二上学期开学考试化学试题(已下线)专题14 无机综合运用(选择题)-2022年高考化学二轮复习重点专题常考点突破练(已下线)第11讲 硫及其化合物(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)专题24 实验分析设计型选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)第四章 非金属及其化合物 第21讲 硫酸 含硫物质的转化上海市复旦大学附属中学2022-2023学年高三下学期3月月考化学试题(已下线)专题03 硫酸和硝酸专讲(专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)陕西西安三中2022-2023学年高一下学期第二次月考化学试题(已下线)第3讲 硫及其重要化合物(已下线)第12讲 硫及其化合物(已下线)考点15 硫及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)江西省丰城市第二中学2023-2024学年高一上学期11月期中考试化学试题山西省大同市浑源七中2023-2024学年高一下学期第一次月考化学试题
单选题
|
较易(0.85)
名校
8. 银锌纽扣电池如图,电池反应式为: ,下列说法正确的是
,下列说法正确的是
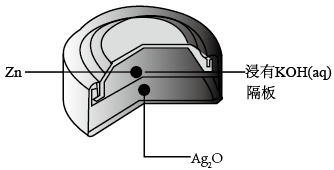
 ,下列说法正确的是
,下列说法正确的是
| A.锌作正极 |
| B.负极发生还原反应 |
C.负极的电极方程式为: |
D.电池工作时,电流从 经导线流向Zn 经导线流向Zn |
您最近一年使用:0次
2021-04-25更新
|
633次组卷
|
6卷引用:江西省赣州市十六县(市)十七校2020-2021学年高一下学期期中联考化学试题
单选题
|
适中(0.65)
解题方法
9. 根据光合作用原理,设计如图原电池装置。下列说法正确的是
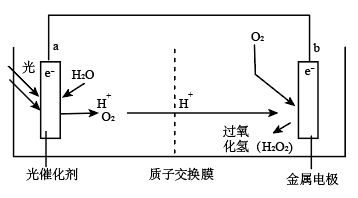

| A.a电极为原电池的正极 |
B.电子移动方向是 |
C.b电极的电极反应为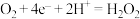 |
D.a电极上每生成 ,通过质子交换膜的 ,通过质子交换膜的 为2mol 为2mol |
【知识点】 原电池原理的应用 原电池电子流向判断及应用解读
您最近一年使用:0次
单选题
|
较易(0.85)
名校
解题方法
10. 中国首条“生态马路”在上海复兴路隧道建成,它运用了“光触媒”技术,在路面涂上一种光催化剂涂料,可将汽车尾气中45%的NO和CO转化成N2 和CO2。下列对此反应的叙述中正确的是
| A.使用光催化剂不改变反应速率 |
| B.该“光触媒”技术可以杜绝“光化学烟雾”的产生 |
| C.升高温度能加快反应速率 |
| D.改变压强对反应速率无影响 |
您最近一年使用:0次
2020-07-01更新
|
685次组卷
|
14卷引用:辽宁省六校2019-2020学年高一下学期期中考试化学试卷
辽宁省六校2019-2020学年高一下学期期中考试化学试卷辽宁省阜新市第二高级中学2019-2020学年高一下学期期末考试化学试题河北省邢台市第二中学2020-2021学年高二上学期开学摸底考试化学试题山西省临猗县临晋中学2020-2021学年高二9月月考化学试题(已下线)【浙江新东方】绍兴qw122(已下线)专题06 化学反应速率和化学平衡——备战2021年高考化学纠错笔记江西省赣州市十六县(市)十七校2020-2021学年高一下学期期中联考化学试题甘肃省庆阳市第六中学2020-2021学年高一下学期期中考试化学(理)试题浙江省丽水外国语学校高中部2021-2022学年高二上学期第一次月考(10月)化学试题海南省琼海市嘉积中学2021-2022学年高一下学期期末考试化学试题广东省深圳市宝安中学高中部2020-2021学年高一下学期期中考试化学试卷 辽宁省阜新市第二高级中学2022-2023学年高一下学期期末考试化学试卷广东省东莞市东华高级中学2023-2024学年高一下学期前段考试化学试题广东省广州市育才中学2023-2024学年高一下学期 期中考试化学试题
单选题
|
较易(0.85)
解题方法
11. 两气体A、B分别为0.6mol与0.5mol,在0.4L密闭容器中反应: ,经5min后达到平衡,此时气体C为0.2mol,在此时间内气体D的平均反应速率为0.1mol/(L∙min)。下列结论错误的是
,经5min后达到平衡,此时气体C为0.2mol,在此时间内气体D的平均反应速率为0.1mol/(L∙min)。下列结论错误的是
 ,经5min后达到平衡,此时气体C为0.2mol,在此时间内气体D的平均反应速率为0.1mol/(L∙min)。下列结论错误的是
,经5min后达到平衡,此时气体C为0.2mol,在此时间内气体D的平均反应速率为0.1mol/(L∙min)。下列结论错误的是| A.平衡时A的浓度为0.75mol/L | B.B的转化率为20% |
| C.C的平均反应速率为0.1mol/(L∙min) | D. |
【知识点】 化学反应速率计算解读 转化率的相关计算及判断解读
您最近一年使用:0次
单选题
|
较易(0.85)
解题方法
12. X、Y、Z、M、Q、R皆为前20号元素且原子序数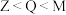 ,其原子半径与最高或最低化合价的关系如图所示。下列说法错误的是
,其原子半径与最高或最低化合价的关系如图所示。下列说法错误的是
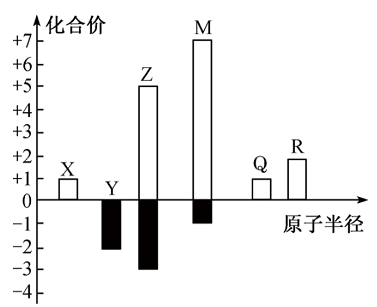
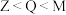 ,其原子半径与最高或最低化合价的关系如图所示。下列说法错误的是
,其原子半径与最高或最低化合价的关系如图所示。下列说法错误的是
| A.X、Y、Z三种元素组成的化合物可能是酸或碱 |
| B.R位于第四周期第ⅡA族 |
C.简单离子半径: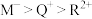 |
| D.Z与M的最高价氧化物对应的水化物均为强酸 |
您最近一年使用:0次
单选题
|
较易(0.85)
解题方法
13. 应用元素周期律的有关知识,可以预测我们不熟悉的一些元素的单质及其化合物的性质。下列预测中正确的是
①Li在氧气中剧烈燃烧,产物是Li2O2,其溶液是一种强碱
②第二周期非金属元素的气态氢化物溶于水后,水溶液可能为碱性
③砹(At)单质为有色固体,AgAt不溶于水也不溶于稀硝酸
④硫酸锶(SrSO4)是难溶于水的白色固体
⑤硒化氢(H2Se)是无色、有毒、比H2S稳定的气体
①Li在氧气中剧烈燃烧,产物是Li2O2,其溶液是一种强碱
②第二周期非金属元素的气态氢化物溶于水后,水溶液可能为碱性
③砹(At)单质为有色固体,AgAt不溶于水也不溶于稀硝酸
④硫酸锶(SrSO4)是难溶于水的白色固体
⑤硒化氢(H2Se)是无色、有毒、比H2S稳定的气体
| A.②③④ | B.①②④ | C.①③⑤ | D.②④⑤ |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
14. X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物的摩尔质量为17g/mol;W的质子数是X、Y、Z、M四种元素质子数之和的 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是| A.XZ2、M2Z2均为共价化合物 |
| B.原子半径:W>Z>Y>X>M |
| C.由X元素形成的单质硬度一定很大 |
| D.由X、Y、Z、M四种元素形成的化合物只含有离子键 |
【知识点】 根据原子结构进行元素种类推断解读
您最近一年使用:0次
2020-04-21更新
|
199次组卷
|
5卷引用:江西省临川第二中学2019-2020学年高一下学期期中线上调研考试化学试题
单选题
|
适中(0.65)
解题方法
15. 在两个恒温、恒容的密闭容器中进行下列两个可逆反应:(甲)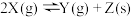 (乙)
(乙) 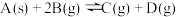 ,当下列物理量不再发生变化时:其中不能表明(甲)和(乙)都达到化学平衡状态是
,当下列物理量不再发生变化时:其中不能表明(甲)和(乙)都达到化学平衡状态是
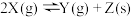 (乙)
(乙) 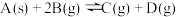 ,当下列物理量不再发生变化时:其中不能表明(甲)和(乙)都达到化学平衡状态是
,当下列物理量不再发生变化时:其中不能表明(甲)和(乙)都达到化学平衡状态是| A.混合气体的密度 |
| B.反应容器中生成物的百分含量 |
| C.反应物的消耗速率与生成物的消耗速率之比等于系数之比 |
| D.混合气体的压强 |
【知识点】 化学平衡状态的判断方法解读
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
16. 如图是氮氧化物 的储存还原的工作原理:NOx的储存过程与还原过程在不同时刻是交替进行的。下列有关说法
的储存还原的工作原理:NOx的储存过程与还原过程在不同时刻是交替进行的。下列有关说法不正确 的是

 的储存还原的工作原理:NOx的储存过程与还原过程在不同时刻是交替进行的。下列有关说法
的储存还原的工作原理:NOx的储存过程与还原过程在不同时刻是交替进行的。下列有关说法
| A.“储存”过程中,BaO转化为Ba(NO3)2 |
| B.在储存还原过程中,Pt作催化剂 |
C.在BaO转化为Ba(NO3)2过程中,参加反应的NO和 的物质的量之比为4∶1 的物质的量之比为4∶1 |
| D.若还原性气体为H2,则参加反应的H2与生成的N2的物质的量之比是5∶1 |
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-无机推断题
|
适中(0.65)
解题方法
17. 下表标出的是元素周期表的一部分元素,回答下列问题:
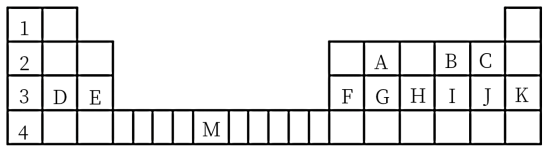
(1)除稀有气体外第三周期中原子半径最大的是___________ (填元素符号)
(2)表中用字母标出的12种元素中,化学性质最不活泼的是___________ (用元素符号表示,下同),非金属性最强的是___________ (用元素符号表示),属于过渡元素的是___________ (用表中的字母表示)。
(3)化合物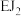 中含有的化学键为
中含有的化学键为___________ 。(填“离子键’”、“极性共价键”、“非极性共价键”)
(4)用电子式表示A的简单气态氢化物的形成过程___________ 。
(5)D、F元素最高价氧化物对应水化物相互反应的离子方程式为___________

(1)除稀有气体外第三周期中原子半径最大的是
(2)表中用字母标出的12种元素中,化学性质最不活泼的是
(3)化合物
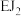 中含有的化学键为
中含有的化学键为(4)用电子式表示A的简单气态氢化物的形成过程
(5)D、F元素最高价氧化物对应水化物相互反应的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中(0.65)
解题方法
18. Ⅰ、(1)反应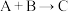 (吸热)分两步进行①
(吸热)分两步进行①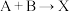 (放热);②
(放热);② (吸热)。下列示意图中,能正确表示总反应过程中能量变化的是
(吸热)。下列示意图中,能正确表示总反应过程中能量变化的是___________ 。
A.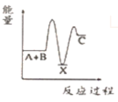 B.
B.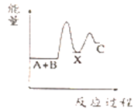
C.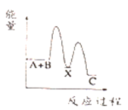 D.
D.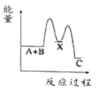
(2)合成氨工业中,合成塔中每产生 ,放出46.1kJ热量,已知(见图):则
,放出46.1kJ热量,已知(见图):则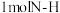 键断裂吸收的能量约等于
键断裂吸收的能量约等于___________ kJ。

Ⅱ.某温度时,在一个10L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
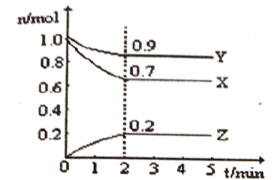
(1)该反应的化学方程式为___________ ;
(2)混合气体的平均相对分子质量比起始时___________ (填“大”,“小”或“相等”)平衡时容器内混合气体密度比起始时___________ (填“大”,“小”或“相等”)
(3)反应开始至2min,开始时的压强与此时体系内压强之比为___________ ;
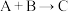 (吸热)分两步进行①
(吸热)分两步进行①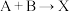 (放热);②
(放热);② (吸热)。下列示意图中,能正确表示总反应过程中能量变化的是
(吸热)。下列示意图中,能正确表示总反应过程中能量变化的是A.
 B.
B.
C.
 D.
D.
(2)合成氨工业中,合成塔中每产生
 ,放出46.1kJ热量,已知(见图):则
,放出46.1kJ热量,已知(见图):则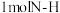 键断裂吸收的能量约等于
键断裂吸收的能量约等于
Ⅱ.某温度时,在一个10L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:

(1)该反应的化学方程式为
(2)混合气体的平均相对分子质量比起始时
(3)反应开始至2min,开始时的压强与此时体系内压强之比为
您最近一年使用:0次
解答题-实验探究题
|
适中(0.65)
名校
解题方法
19. 以下是关于原电池的装置图。请回答:
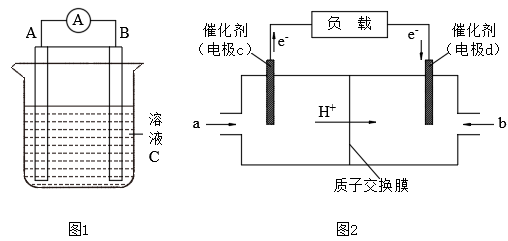
(1)图1中,若C为稀 ,电流表指针发生偏转,B电极材料为Zn且作负极,则A电极上发生的电极反应式为
,电流表指针发生偏转,B电极材料为Zn且作负极,则A电极上发生的电极反应式为___________ ;反应进行一段时间后溶液酸性将___________ (填“增强”“减弱”或“基本不变”)。
(2)若需将反应: 设计成如图1所示的原电池装置,则A(正极)极材料为
设计成如图1所示的原电池装置,则A(正极)极材料为___________ ,B(负极)极材料为___________ ,溶液C为___________ 。
(3) 可作为燃料使用,用
可作为燃料使用,用 和
和 组合形成的质子交换膜燃料电池的结构示意图如图2,电池总反应为
组合形成的质子交换膜燃料电池的结构示意图如图2,电池总反应为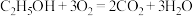 ,则d电极是
,则d电极是___________ (填“正极”或“负极”),c电极的电极反应式为___________ 。若线路中转移4mol电子,则上述 燃料电池消耗的
燃料电池消耗的 在标准状况下的体积为
在标准状况下的体积为___________ L。

(1)图1中,若C为稀
 ,电流表指针发生偏转,B电极材料为Zn且作负极,则A电极上发生的电极反应式为
,电流表指针发生偏转,B电极材料为Zn且作负极,则A电极上发生的电极反应式为(2)若需将反应:
 设计成如图1所示的原电池装置,则A(正极)极材料为
设计成如图1所示的原电池装置,则A(正极)极材料为(3)
 可作为燃料使用,用
可作为燃料使用,用 和
和 组合形成的质子交换膜燃料电池的结构示意图如图2,电池总反应为
组合形成的质子交换膜燃料电池的结构示意图如图2,电池总反应为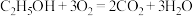 ,则d电极是
,则d电极是 燃料电池消耗的
燃料电池消耗的 在标准状况下的体积为
在标准状况下的体积为
您最近一年使用:0次
2021-04-25更新
|
295次组卷
|
2卷引用:江西省赣州市十六县(市)十七校2020-2021学年高一下学期期中联考化学试题
解答题-实验探究题
|
适中(0.65)
解题方法
20. 实验探究:探究碳、硅元素的非金属性的相对强弱,根据要求 完成下列各小题(D、E、F中溶液均为足量)
(1)实验装置:
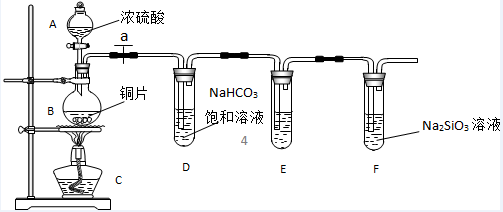
填写所示仪器名称A___________
(2)实验步骤:连接仪器、___________ 、加药品后,打开a、然后滴入浓硫酸,加热
(3)问题探究:(已知酸性强弱:亚硫酸>碳酸)
①铜与浓硫酸反应的化学方程式是___________ ,装置E中足量酸性KMnO4溶液的作用是___________
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是__________ ,相关的离子方程式为:___________
③依据试管D中的实验现象,能否证明硫元素的非金属性强于碳元素的非金属性___________ (填“能”或“否”),并说明理由___________
(1)实验装置:

填写所示仪器名称A
(2)实验步骤:连接仪器、
(3)问题探究:(已知酸性强弱:亚硫酸>碳酸)
①铜与浓硫酸反应的化学方程式是
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是
③依据试管D中的实验现象,能否证明硫元素的非金属性强于碳元素的非金属性
您最近一年使用:0次
解答题-无机推断题
|
适中(0.65)
21. X、Y、Z、Q、W、R是短周期元素,原子序数依次增大。X原子核外各层电子数之比为1∶2,Y原子和Q原子的核外电子数之和为20,Z是短周期中金属性最强的元素,W和R是同周期相邻元素,Y的氧化物和R的氧化物均能形成酸雨。请回答下列问题:
(1)元素X的最高价氧化物的电子式为___________ ;元素Y、Z、R的简单离子的半径由大到小顺序为___________ 。(用离子符号表示)
(2)元素R在周期表的位置为___________ ,其非金属性比W强,用原子结构的知识解释原因:___________ 。元素W和R的气态氢化物的稳定性从强到弱的顺序为:___________ (写出化学式)。
(3)足量X的最高价氧化物与Z的最高价氧化物对应水化物反应的离子方程式:___________ 。
(4)Y和Q组成的化合物QY,被大量用于制造电子元件。工业上用Q的氧化物、X单质和Y单质在高温下制备QY,其中Q的氧化物和X单质的物质的量之比为1∶3,则该反应的化学方程式为___________ 。
(1)元素X的最高价氧化物的电子式为
(2)元素R在周期表的位置为
(3)足量X的最高价氧化物与Z的最高价氧化物对应水化物反应的离子方程式:
(4)Y和Q组成的化合物QY,被大量用于制造电子元件。工业上用Q的氧化物、X单质和Y单质在高温下制备QY,其中Q的氧化物和X单质的物质的量之比为1∶3,则该反应的化学方程式为
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、化学与STSE、认识化学科学、化学反应原理、物质结构与性质、化学实验基础
试卷题型(共 21题)
题型
数量
单选题
16
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 二氧化硫与其他强氧化剂的反应 化学科学对人类文明发展的意义 光导纤维与硅芯片 | |
| 2 | 0.85 | 阿伏加德罗常数的求算 原电池原理的综合应用 离子键概念及判断 共价键概念及判断 | |
| 3 | 0.94 | 有机物的结构式、结构简式、比例模型、球棍模型、最简式 共价型分子结构式、电子式 原子、离子、原子团及其电子式的书写与判断 | |
| 4 | 0.65 | 离子反应的发生及书写 离子方程式的正误判断 | |
| 5 | 0.85 | 氯气的实验室制法 氨气的实验室制法 配制一定物质的量浓度的溶液的步骤、操作 化学实验方案的设计与评价 | |
| 6 | 0.65 | 二氧化硫的化学性质 | |
| 7 | 0.85 | 能量的相互转化 常见能量转化形式 吸热反应和放热反应 | |
| 8 | 0.85 | 原电池原理 原电池电子流向判断及应用 原电池正负极判断 原电池电极反应式书写 | |
| 9 | 0.65 | 原电池原理的应用 原电池电子流向判断及应用 | |
| 10 | 0.85 | 化学反应的速率 影响化学反应速率的外因 催化剂对化学反应速率的影响 | |
| 11 | 0.85 | 化学反应速率计算 转化率的相关计算及判断 | |
| 12 | 0.85 | 微粒半径大小的比较方法 根据原子结构进行元素种类推断 | |
| 13 | 0.85 | 预测元素的性质 元素周期律的应用 同主族元素性质递变规律理解及应用 类比预测在推断中的应用 | |
| 14 | 0.65 | 根据原子结构进行元素种类推断 | |
| 15 | 0.65 | 化学平衡状态的判断方法 | |
| 16 | 0.65 | 氧化还原反应定义、本质及特征 基于氧化还原反应守恒规律的计算 | |
| 二、解答题 | |||
| 17 | 0.65 | 元素周期律、元素周期表的推断 元素周期表提供的元素信息 “定位法”在推断中的应用 | 无机推断题 |
| 18 | 0.65 | 根据△H=生成物的总能量之和-反应物的总能量之和进行计算 化学平衡的有关计算 | 原理综合题 |
| 19 | 0.65 | 原电池原理的应用 燃料电池 | 实验探究题 |
| 20 | 0.65 | 浓硫酸的强氧化性 元素金属性、非金属性强弱探究实验 物质性质的探究 | 实验探究题 |
| 21 | 0.65 | 共价型分子结构式、电子式 同周期元素性质递变规律理解及应用 微粒半径大小的比较方法 根据物质性质进行元素种类推断 | 无机推断题 |

 与
与

