18. SO
2、NO
x是主要的空气污染源,需经过处理才能排放。回答下列问题:
(1)二氧化硫在V
2O
5作用下的催化氧化是工业上产生硫酸的主要反应。催化反应的机理是:
第一步:SO
2(g)+V
2O
5(s)=SO
3(g)+V
2O
4(s) ΔH=+akJ•mol
-1第二步:V
2O
4(s) +O
2(g)+2SO
2(g)=2VOSO
4(s) ΔH=-bkJ•mol
-1第三步:4VOSO
4(s)+O
2(g)=2V
2O
5(s)+4SO
3(g) ΔH=-ckJ•mol
-1请写出二氧化硫催化氧化的热化学方程式
___________。
(2)一定条件下,用Fe
2O
3作催化剂对燃煤烟气进行回收。反应为2CO(g)+SO
2(g)

2CO
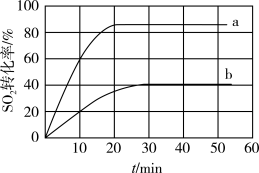
2(g)+S(l) ΔH<0.80℃时,在容积恒为1L的密闭容器中投入总物质的量为2mol的气体,按n(CO):n(SO
2)为1:1或3:1投料时SO
2转化率的变化情况如图。则图中表示n(CO):n(SO
2)=1:1的变化曲线为
___________(填字母),若曲线bSO
2的平衡转化率是42%,用SO
2表示30min内的平均反应速率是
___________。CO
2和SO
2的中心原子杂化方式分别为
______,
_____。
(3)一定温度下,在容积恒为1L的密闭容器中,充入0.3molNO与过量的金属Al,发生的反应存在如下平衡:Al(s)+2NO(g

N
2(g)+Al
2O
3(s) ΔH<0.已知在此条件下NO与N
2的消耗速率与各自的浓度有如下关系(k
1、k
2为速率常数):v(NO)=k
1•c
2(NO),v(N
2)=k
2•c(N
2)。
①在T
1温度下,k
1=0.004L•mol•min
-1,k
2=0.002min
-1,该温度下反应的平衡常数的值为
______。
②T
2温度下,NO的物质的量随时间的变化如图,其平衡常数的值为
___________;温度T
1___________T
2(填“小于”“等于”或“大于”),判断理由是
___________。
