10. 有效去除大气中的H
2S、SO
2以及废水中的硫化物是环境保护的重要课题。
(1)氨水可以脱除烟气中的SO
2.氨水脱硫的相关热化学方程式如下:
2NH
3(g) + H
2O(1) + SO
2(g)=(NH
4)
2SO
3(aq) ΔH=akJ/mol
2NH
4HSO
3(aq)=((NH
4)
2SO
3 (aq) + H
2O(l) + SO
2(g) ΔH =bkJ/mol
2(NH
4)
2SO
3(aq) + O
2(g)= 2(NH
4)
2SO
4 (aq) ΔH = ckJ/mol
反应2NH
3(g) + 2NH
4HSO
3(aq)+O
2(g)= 2(NH
4)
2SO
4+(aq)的 ΔH =
_______ kJ/mol(用含a、 b、c的代数式表示)。
(2)H
2S与CO
2在高温下发生反应: H
2S(g) + CO
2(g)

COS(g)+ H
2O(g)。在610K时,将。0.40 mol H
2S与0.20 mol CO
2充入5 L的空钢瓶中,反应达到平衡后水的物质的量分数为0.2。
①上述条件下H
2S的平衡转化事α
1=
_______ %。
②若在620 K重复实验,平衡后水的物质的量分数为0.3,该反应的ΔH
_______ 0(填“<” “>”“<或=”)。
③在610 K时反应H
2S(g) + CO
2(g)

COS(g) + H
2O(g)平衡建立的基础上,改变下列一种条件,能使H
2S平衡转化率增大的是
_______ (填标号)。
A.向容器中通入H
2S B.向容器中通入CO
2C.加入催化剂
D.缩小容器的体积
(3)在气体总压强分别为p
1和p
2时,反应2SO
3(g)

2SO
2 g) + O
2(g)在不同温度下达到平衡, 测得SO
3(g)及SO
2(g)的物质的量分数如图所示:
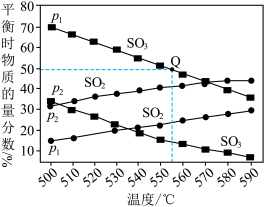
①压强: p
2_______ p
1(填:“>”或”<”) :判断的理由是
_______。
②若p
1=8.1MPa,起始时充入a mol的SO
3(g)发生反应,计算Q点对应温度下该反应的平衡常数K
p=
_______ MPa(用平衡分压代替平衡浓度计算,分压-总压×物质的量分数)。