17. 水合肼(N
2H
4·H
2O)可用作抗氧剂等,工业上常用尿素[CO(NH
2)
2]和NaClO 溶液反应制备水合肼。
已知:①NaClO受热易分解为NaCl和NaClO
3;②N
2H
4·H
2O沸点118℃,具有强还原性。
I.制备NaClO溶液(如图1)
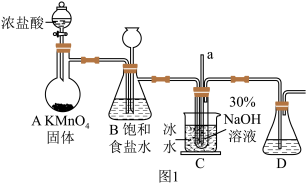
(1)将Cl
2通入过量NaOH溶液中制备NaClO,其离子方程式是
_____________。
(2)配制30%NaOH溶液时,所需玻璃仪器有烧杯、玻璃棒、胶头滴管和
_________。
(3)B中的长颈漏斗和C中的玻璃管a在实验中的作用相同,均为
_________。C中用冰水浴控制温度在25℃以下,其主要目的是
______________。
II.制取水合肼
(4)制备水合肼:将溶液X (NaClO 和过量NaOH溶液)滴入尿素水溶液中,控制一定温度,装置如图a (夹持及控温装置已略)。充分反应后,A中的溶液经蒸馏获得水合肼粗品后,剩余溶液再进一步处理还可获得副产品NaCl和Na
2CO
3·10H
2O。

①A中反应的化学方程式是
____________。
②若滴加NaClO溶液的速度较快时,水合肼的产率会下降,原因是
____________。
③NaCl和Na
2CO
3的溶解度曲线如图b。由蒸馏后的剩余溶液获得NaCl粗品的操作是
________。
(5)水合肼在溶液中可发生类似NH
3·H
2O的电离,呈弱碱性。水合肼和盐酸按物质的量之比1:1反应的离子方程式是
___________。