I.已知:乙二酸俗称草酸(结构简式为HOOC—COOH,可简写为H2C2O4)。25℃时,草酸的电离平衡常数为K1=5.0×10−2,K2=5.4×10−5;碳酸(H2CO3)的电离平衡常数为K1=4.5×10−7,K2=4.7×10−11。草酸钙的Ksp=4.0×10−8,碳酸钙的Ksp=2.5×10−9.回答下列问题:
(1)相同条件下等物质的量浓度的Na2C2O4溶液的pH比Na2CO3溶液的pH___________ (填“大”、“小”或“相等”);
(2)常温下将20mL 0.4mol/L的KOH溶液与20mL 0.2mol/L的草酸溶液混合,则混合后溶液中阴离子浓度的大小顺序为___________ 。
(3)25℃时向20mL碳酸钙的饱和溶液中逐滴加入8.0×10−4mol/L的草酸钾溶液20mL,能否产生沉淀___________ (填“能”或“不能”)。
II.已知:25 ℃时,0.1 mol·L-1的HA溶液中c(H+)/c(OH-)=1010。
①HA是___________ (填“强电解质”或“弱电解质”)。
②在加水稀释HA溶液的过程中,随着水量的增加而减小的是___________ (填字母)。
A.c(HA)/c(A-) B.c(H+)/c(HA)
C.c(H+)与c(OH-)的乘积 D.c(OH-)
(1)相同条件下等物质的量浓度的Na2C2O4溶液的pH比Na2CO3溶液的pH
(2)常温下将20mL 0.4mol/L的KOH溶液与20mL 0.2mol/L的草酸溶液混合,则混合后溶液中阴离子浓度的大小顺序为
(3)25℃时向20mL碳酸钙的饱和溶液中逐滴加入8.0×10−4mol/L的草酸钾溶液20mL,能否产生沉淀
II.已知:25 ℃时,0.1 mol·L-1的HA溶液中c(H+)/c(OH-)=1010。
①HA是
②在加水稀释HA溶液的过程中,随着水量的增加而减小的是
A.c(HA)/c(A-) B.c(H+)/c(HA)
C.c(H+)与c(OH-)的乘积 D.c(OH-)
更新时间:2021-01-09 12:47:04
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)常温下,将m mol·L-1的CH3COOH溶液和n mol·L-1NaOH溶液等体积混合后,溶液的pH=7,则m与n的大小关系是m____ n(填“>”、“<”或“=”,下同),原酸中c(H+)与碱中c(OH-)的大小关系是c(H+)____ c(OH-)。
(2)常温下,将浓度均为0.1mol·L-1的CH3COONa、CH3COOH溶液等体积混合后,溶液呈酸性。则混合溶液中各离子浓度由大到小排序为_____ 。关于该混合溶液的说法不正确的是___ (填代号)。
a.此溶液一定有c(Na+)+c(H+)=c(OH-)+c(CH3COO-)
b.此溶液一定有c(Na+)=c(CH3COOH)+c(CH3COO-)
c.此溶液中水的电离程度一定大于纯水的电离程度
d.向此溶液中加少量氢氧化钠或盐酸,溶液pH变化不大
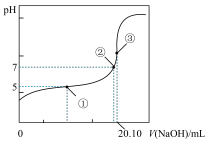
(3)用0.1000 mol·L-1NaOH溶液滴定20.00mL某浓度的CH3COOH溶液,滴定曲线如右图所示。其中点①所示溶液中c(CH3COO-)=1.7c(CH3COOH),点③所示溶液中c(CH3COO-)+c(CH3COOH)=c(Na+)。列式并计算醋酸的电离常数_____ ,CH3COOH的物质的量浓度为____ mol·L-1。
(1)常温下,将m mol·L-1的CH3COOH溶液和n mol·L-1NaOH溶液等体积混合后,溶液的pH=7,则m与n的大小关系是m
(2)常温下,将浓度均为0.1mol·L-1的CH3COONa、CH3COOH溶液等体积混合后,溶液呈酸性。则混合溶液中各离子浓度由大到小排序为
a.此溶液一定有c(Na+)+c(H+)=c(OH-)+c(CH3COO-)
b.此溶液一定有c(Na+)=c(CH3COOH)+c(CH3COO-)
c.此溶液中水的电离程度一定大于纯水的电离程度
d.向此溶液中加少量氢氧化钠或盐酸,溶液pH变化不大
(3)用0.1000 mol·L-1NaOH溶液滴定20.00mL某浓度的CH3COOH溶液,滴定曲线如右图所示。其中点①所示溶液中c(CH3COO-)=1.7c(CH3COOH),点③所示溶液中c(CH3COO-)+c(CH3COOH)=c(Na+)。列式并计算醋酸的电离常数

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】砷(As)与N、P是同主族元素,远古时期人们就开始开发利用砷的性质,现代技术中砷仍然起着非常重要的作用。请回答下列问题:
(1)砷只有一种稳定的同位素 ,其原子核内的中子数比核外电子数多
,其原子核内的中子数比核外电子数多_______ (填数值)。
(2)下列事实中,能说明As元素的非金属性弱于N元素的是_______(填标号)。
(3)Marsh试砷法和Gutzeit试砷法是法医学上鉴定砷的重要方法。其原理是先将 (剧毒)转化为
(剧毒)转化为 ,前者让:
,前者让: 分解产生黑亮的砷镜(As),后者让
分解产生黑亮的砷镜(As),后者让 被
被 溶液氧化为
溶液氧化为 ,同时还生成Ag单质。
,同时还生成Ag单质。
① 的电子式为
的电子式为_______ 。
②Gutzeit试砷法中 被氧化的离子方程式为
被氧化的离子方程式为_______ 。
(4)砷化镓(GaAs)是现代科技中制造芯片的一种原料,可用 溶液对其进行刻蚀,As元素的化合价变为+5价,则该反应中还原剂与氧化剂的物质的量之比为
溶液对其进行刻蚀,As元素的化合价变为+5价,则该反应中还原剂与氧化剂的物质的量之比为_______ ;砷化镓也可用于制造太阳能电池,该电池工作时的能量转化形式为_______ 。
(5)已知 的电离平衡常数分别为
的电离平衡常数分别为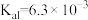 、
、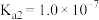 、
、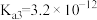 。
。
①25℃时,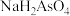 ,溶液中:
,溶液中: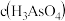
_______  (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
②25℃时,向 溶液中加入NaOH溶液至中性,此时溶液中
溶液中加入NaOH溶液至中性,此时溶液中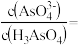
_______ 。
(1)砷只有一种稳定的同位素
 ,其原子核内的中子数比核外电子数多
,其原子核内的中子数比核外电子数多(2)下列事实中,能说明As元素的非金属性弱于N元素的是_______(填标号)。
A.沸点: |
B.等物质的量浓度溶液的酸性: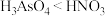 |
C.分解温度: |
D.相对分子质量: |
 (剧毒)转化为
(剧毒)转化为 ,前者让:
,前者让: 分解产生黑亮的砷镜(As),后者让
分解产生黑亮的砷镜(As),后者让 被
被 溶液氧化为
溶液氧化为 ,同时还生成Ag单质。
,同时还生成Ag单质。①
 的电子式为
的电子式为②Gutzeit试砷法中
 被氧化的离子方程式为
被氧化的离子方程式为(4)砷化镓(GaAs)是现代科技中制造芯片的一种原料,可用
 溶液对其进行刻蚀,As元素的化合价变为+5价,则该反应中还原剂与氧化剂的物质的量之比为
溶液对其进行刻蚀,As元素的化合价变为+5价,则该反应中还原剂与氧化剂的物质的量之比为(5)已知
 的电离平衡常数分别为
的电离平衡常数分别为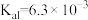 、
、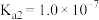 、
、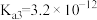 。
。①25℃时,
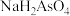 ,溶液中:
,溶液中: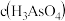
 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。②25℃时,向
 溶液中加入NaOH溶液至中性,此时溶液中
溶液中加入NaOH溶液至中性,此时溶液中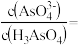
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】按要求填空:
(1)①将 溶液蒸干灼烧得到的物质是
溶液蒸干灼烧得到的物质是______ (填化学式);
②泡沫灭火器常用硫酸铝作为原料之一,其灭火原理为______ (用离子方程式表示);
③在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式______ 。
(2)已知25℃时有关弱酸的电离常数如下:
HCN: ,
, :
: ,
, ,则:
,则:
①相同物质的量浓度的 、
、 、NaCN溶液,pH
、NaCN溶液,pH由小到大 的顺序是:______ 。
②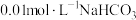 的溶液中
的溶液中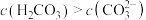 ,结合化学用语解释其原因:
,结合化学用语解释其原因:______ 。
(3)含 的废水毒性较大,某工厂废水中含
的废水毒性较大,某工厂废水中含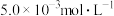 的
的 。为了使废水的排放达标,进行如下处理:(已知
。为了使废水的排放达标,进行如下处理:(已知 )
)

①绿矾为 ,反应(Ⅰ)中氧化剂与还原剂的物质的量之比为
,反应(Ⅰ)中氧化剂与还原剂的物质的量之比为______ ;
②常温下若处理后的废水中 ,则处理后的废水的
,则处理后的废水的
______ 。
(1)①将
 溶液蒸干灼烧得到的物质是
溶液蒸干灼烧得到的物质是②泡沫灭火器常用硫酸铝作为原料之一,其灭火原理为
③在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式
(2)已知25℃时有关弱酸的电离常数如下:
HCN:
 ,
, :
: ,
, ,则:
,则:①相同物质的量浓度的
 、
、 、NaCN溶液,pH
、NaCN溶液,pH②
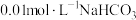 的溶液中
的溶液中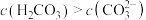 ,结合化学用语解释其原因:
,结合化学用语解释其原因:(3)含
 的废水毒性较大,某工厂废水中含
的废水毒性较大,某工厂废水中含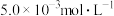 的
的 。为了使废水的排放达标,进行如下处理:(已知
。为了使废水的排放达标,进行如下处理:(已知 )
)
①绿矾为
 ,反应(Ⅰ)中氧化剂与还原剂的物质的量之比为
,反应(Ⅰ)中氧化剂与还原剂的物质的量之比为②常温下若处理后的废水中
 ,则处理后的废水的
,则处理后的废水的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】单一盐溶液中离子浓度比较
(1)NH4Cl溶液中存在的水解平衡是________ ,使c(H+)___ c(OH-)、c(Cl-)_____ c(NH4+),盐类的水解是很微弱的,所以溶液中剩余未水解的NH4+的浓度_______ 水解产生的OH-的浓度。所以溶液中离子浓度大小关系是________ 。
(2)Na2CO3溶液中存在的水解平衡是__________ 、_______ 离子浓度大小关系是_________ 。
(1)NH4Cl溶液中存在的水解平衡是
(2)Na2CO3溶液中存在的水解平衡是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列问题
(1)将Na2SO3溶液蒸干灼烧得到的物质是_______ (填化学式)。
(2)已知部分弱酸的电离常数如下表:(均为常温下的数据):
①同浓度的A-、B-、HC-、D-中结合H+的能力最强的是_______ 。
②pH相同的①NaA、②NaB、③NaD溶液,其物质的量浓度由大到小的顺序为_______ 。(填序号)
③25℃时,向NaD溶液中通入少量H2C,反应的离子方程式为_______ 。
④将浓度为0.02mol/L的HA与0.01mol/LNaOH溶液等体积混合,测得混合溶液中c(Na+)<c(A-),则c(H+)_______ c(OH-)(填“>”、“<”、“=”)
⑤下列反应不能发生的是:_______ (填编号)。
A.HA+NaB=HB+NaA B.HB+NaD=HD+NaB
C.H2C+NaB=HB+NaHC D.HD+A-=HA+D-
(1)将Na2SO3溶液蒸干灼烧得到的物质是
(2)已知部分弱酸的电离常数如下表:(均为常温下的数据):
| 酸 | 电离常数(Ka) |
| HA | 1.8×10-5 |
| HB | 3×10-8 |
| H2C | K1=4.4×10-7 K2=4.7×10-11 |
| HD | 6.2×10-10 |
②pH相同的①NaA、②NaB、③NaD溶液,其物质的量浓度由大到小的顺序为
③25℃时,向NaD溶液中通入少量H2C,反应的离子方程式为
④将浓度为0.02mol/L的HA与0.01mol/LNaOH溶液等体积混合,测得混合溶液中c(Na+)<c(A-),则c(H+)
⑤下列反应不能发生的是:
A.HA+NaB=HB+NaA B.HB+NaD=HD+NaB
C.H2C+NaB=HB+NaHC D.HD+A-=HA+D-
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】H2SO4是工业上常用的酸,NH4Al(SO4)2是一种食品加工业中常用的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)NH4Al(SO4)2可作净水剂,其原理是_____________ (用离子方程式说明)。
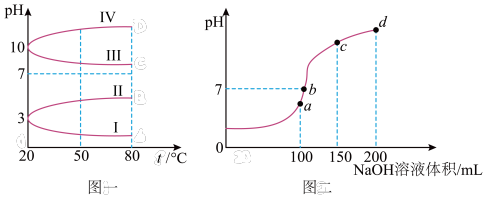
(2)20℃时,均为0.1mol L-1的几种电解质溶液的pH 随温度变化的曲线如图1 所示。
① 其中符合0.1mol·L-1 NH4Al(SO4)2溶液的pH随温度变化的曲线是_______ (填罗马数字)。
② 20℃ 时,0.1mol·L-1NH4Al(SO4)2溶液中,2c(SO42-)-c(NH4+)-3c(Al3+)=____ mol·L-1(填具体数字计算式,不必化简)
(3)室温时,向100mL0.1mol·L-1NH4HSO4溶液中滴加0.1mol L-1NaOH溶液,溶液pH 与NaOH溶液体积的关系曲线如图2所示。试分析图中a、b、c、d 四个点,水的电离程度最大的是__________ 点,在b点,溶液中各离子浓度由大到小的排列顺序是___________________ 。
(4)t℃时,pH=2的稀硫酸和pH=11的NaOH溶液等体积混合后溶液呈中性,则该温度下水的离子积常数Kw=________________ 。
(1)NH4Al(SO4)2可作净水剂,其原理是
(2)20℃时,均为0.1mol L-1的几种电解质溶液的pH 随温度变化的曲线如图1 所示。
① 其中符合0.1mol·L-1 NH4Al(SO4)2溶液的pH随温度变化的曲线是
② 20℃ 时,0.1mol·L-1NH4Al(SO4)2溶液中,2c(SO42-)-c(NH4+)-3c(Al3+)=
(3)室温时,向100mL0.1mol·L-1NH4HSO4溶液中滴加0.1mol L-1NaOH溶液,溶液pH 与NaOH溶液体积的关系曲线如图2所示。试分析图中a、b、c、d 四个点,水的电离程度最大的是
(4)t℃时,pH=2的稀硫酸和pH=11的NaOH溶液等体积混合后溶液呈中性,则该温度下水的离子积常数Kw=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】牙齿表面由一层坚硬的、组成为Ca5(PO4)3OH的物质保护着,它在唾液中存在着如下平衡:Ca5(PO4)3OH(固)⇌5Ca2++3PO +OH-。
+OH-。
(1)进食后,细菌和酶作用于食物,产生有机酸,此时,牙齿就会受到腐蚀,其原因是_______ 。
(2)已知Ca5(PO4)3F(s)的溶解度比上面的矿化产物更小,质地更坚固。请用离子方程式表示牙膏配有氟化物添加剂能防止龋齿的原因:___________ 。
(3)根据以上原理,请你提出一种其它促进矿化的方法:__________ 。
 +OH-。
+OH-。(1)进食后,细菌和酶作用于食物,产生有机酸,此时,牙齿就会受到腐蚀,其原因是
(2)已知Ca5(PO4)3F(s)的溶解度比上面的矿化产物更小,质地更坚固。请用离子方程式表示牙膏配有氟化物添加剂能防止龋齿的原因:
(3)根据以上原理,请你提出一种其它促进矿化的方法:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液的pH,达到分离金属离子的目的。难溶金属的氢氧化物在不同pH下的溶解度(S/mol/L)如图所示。
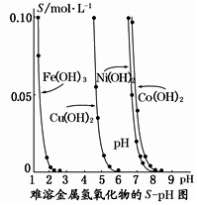
(1)当pH=3时,溶液中铜元素的主要存在形式是__________ 。
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH值为______ (填序号)。
A.<1 B.4左右 C.8>PH>6 D.>9
(3)在Ni(NO3)2溶液中含有少量的Co2+杂质,________ (填“能”或“不能”)通过调节溶液pH的方法来除去,理由是_____________________________________________ 。
(4)已知一些难溶电解质的溶度积常数如右下表:
为除去某工业废水中含有的Cu2+、Pb2+、Hg2+杂质,最适宜向此工业废水中加入过量的___________ (填序号)。
A.NaOH B.FeS C.Na2S D.NH4Cl

(1)当pH=3时,溶液中铜元素的主要存在形式是
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH值为
A.<1 B.4左右 C.8>PH>6 D.>9
(3)在Ni(NO3)2溶液中含有少量的Co2+杂质,
(4)已知一些难溶电解质的溶度积常数如右下表:
| 物质 | FeS | MnS | PbS | HgS | ZnS | CuS |
| Ksp | 6.3×10-18 | 2.5×10-13 | 3.4×10-28 | 6.4×10-33 | 1.6×10-24 | 1.3×10-35 |
为除去某工业废水中含有的Cu2+、Pb2+、Hg2+杂质,最适宜向此工业废水中加入过量的
A.NaOH B.FeS C.Na2S D.NH4Cl
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】废弃电池随意丢弃会对土壤或水产生污染,电池中含有的重金属离子对植物生长有毒害作用,摄入人体还会伤害人的脑细胞、神经、肝、肾、骨骼等等。某同学查阅一些难溶物常温下的溶度积常数如下表:
(1)该同学在含有相同浓度Mn2+和Cu2+的溶液中滴加Na2S的稀溶液,观察到先出现的沉淀颜色是______ ,该实验说明在相同条件下Ksp越小,物质的溶解度____ (填“越大”或“越小”)。
(2)已知室温下铁离子开始沉淀的pH为1.0,则此溶液中 Fe3+的物质的量浓度为______ ,若溶液中含有与Fe3+等浓度的 Al3+,调节 pH 使 Fe3+沉淀完全时,其中_____ Al(OH)3沉淀(填“含有”或“不含有”)。
(3)某工业废水中含有Cu2+、Pb2+、Hg2+杂质,利用沉淀转化原理最适宜加入过量的__________ (填序号)。写出加入该试剂除去Pb2+时发生的离子反应方程式_______ 。
A.FeS B.Fe2O3 C.Na2S D.ZnO
(4)由 FeCl3·6H2O晶体得到纯的无水FeCl3,需要进行的操作是_________ 。
| 物质 | FeS | CuS(黑色) | MnS(红色) | PbS | HgS | ZnS |
| Ksp |  |  |  |  |  |  |
| 物质 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 | Pb(OH)2 | Zn(OH)2 | |
| Ksp |  |  |  |  |  |
(2)已知室温下铁离子开始沉淀的pH为1.0,则此溶液中 Fe3+的物质的量浓度为
(3)某工业废水中含有Cu2+、Pb2+、Hg2+杂质,利用沉淀转化原理最适宜加入过量的
A.FeS B.Fe2O3 C.Na2S D.ZnO
(4)由 FeCl3·6H2O晶体得到纯的无水FeCl3,需要进行的操作是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.在0.1 mol·L-1的重铬酸钾(K2Cr2O7)溶液中存在如下平衡:
Cr2O +H2O
+H2O 2HCrO4
2HCrO4 2CrO
2CrO +2H+
+2H+
(1)在强碱溶液中,铬元素的主要存在形式为_______ (填离子符号),向重铬酸钾溶液中加入适量稀硫酸,溶液中c(Cr2O )/c(CrO
)/c(CrO )将
)将_______ (填“增大”、“减小”或“不变”)。
Ⅱ.已知某溶液中只存在OH-、H+、NH 、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:并按要求填写下列空白:
、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:并按要求填写下列空白:
①c(Cl-)>c(NH )>c(H+)>c(OH-) ②c(Cl-)>c(NH
)>c(H+)>c(OH-) ②c(Cl-)>c(NH )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
③c(NH )>c(Cl-)>c(OH-)>c(H+) ④c(Cl-)>c(H+)>c(NH
)>c(Cl-)>c(OH-)>c(H+) ④c(Cl-)>c(H+)>c(NH )>c(OH-)
)>c(OH-)
(2)若溶液中只溶解了一种溶质,则该溶质是_______ ,上述四种离子浓度的大小顺序为_______ (选填序号)。
(3)若上述关系中③是正确的,则溶液中的溶质为_______ ;
(4)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)_______ c(NH3·H2O) (填“大于”“小于”或“等于”)。
III.重金属离子对河流造成严重污染。某化工厂废水(pH=2.0,d≈1 g·mL-1)中含Ag+,Pb 2+等重金属离子,其浓度各约为0.0lmol·L-1.排放前拟用沉淀法除去这两种离子,查找有关数据如下:
(5)你认为往废水中投入_______(填字母序号),沉淀效果最好。
(6)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中c(Pb2+)=_______ 。
Cr2O
 +H2O
+H2O 2HCrO4
2HCrO4 2CrO
2CrO +2H+
+2H+(1)在强碱溶液中,铬元素的主要存在形式为
 )/c(CrO
)/c(CrO )将
)将Ⅱ.已知某溶液中只存在OH-、H+、NH
 、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:并按要求填写下列空白:
、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:并按要求填写下列空白:①c(Cl-)>c(NH
 )>c(H+)>c(OH-) ②c(Cl-)>c(NH
)>c(H+)>c(OH-) ②c(Cl-)>c(NH )>c(OH-)>c(H+)
)>c(OH-)>c(H+)③c(NH
 )>c(Cl-)>c(OH-)>c(H+) ④c(Cl-)>c(H+)>c(NH
)>c(Cl-)>c(OH-)>c(H+) ④c(Cl-)>c(H+)>c(NH )>c(OH-)
)>c(OH-)(2)若溶液中只溶解了一种溶质,则该溶质是
(3)若上述关系中③是正确的,则溶液中的溶质为
(4)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)
III.重金属离子对河流造成严重污染。某化工厂废水(pH=2.0,d≈1 g·mL-1)中含Ag+,Pb 2+等重金属离子,其浓度各约为0.0lmol·L-1.排放前拟用沉淀法除去这两种离子,查找有关数据如下:
| 难溶电解质 | AgI | AgOH | Ag2S | PbI2 | Pb(OH)2 | PbS |
| Ksp | 8.3×10-17 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
| A.NaOH | B.Na2S | C.KI | D.Ca(OH)2 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】 时,向
时,向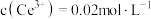 的溶液中加入氢氧化钠来调节溶液的
的溶液中加入氢氧化钠来调节溶液的 ,若反应后溶液
,若反应后溶液 ,此时
,此时 是否沉淀完全?
是否沉淀完全?__________ (填“是”或“否”),判断的理由是________ 。(要求列式计算,已知: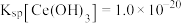 ,
,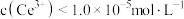 时视为沉淀完全)
时视为沉淀完全)
 时,向
时,向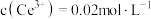 的溶液中加入氢氧化钠来调节溶液的
的溶液中加入氢氧化钠来调节溶液的 ,若反应后溶液
,若反应后溶液 ,此时
,此时 是否沉淀完全?
是否沉淀完全?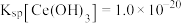 ,
,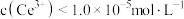 时视为沉淀完全)
时视为沉淀完全)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
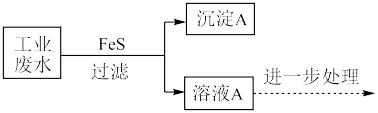
【推荐3】利用FeS作为沉淀剂除去某工业废水中Pb2+的部分流程如下:
(1)结合化学用语,从平衡移动角度解释可用FeS除去Pb2+的原因___________ 。
(2)可使(1)中平衡发生移动所需最小c(Pb2+)=___________ mol·L-1。(只写计算结果)
(3)处理1 L含Pb2+浓度为3.07 mg·L-1的该废水至合格(Pb2+浓度小于1 mg·L-1)最少所需FeS的质量是___________ mg。
| 溶度积(均为18~25℃数据) | |
| Ksp(FeS) | Ksp(PbS) |
| 约为10-18 | 约为10-28 |
(1)结合化学用语,从平衡移动角度解释可用FeS除去Pb2+的原因
(2)可使(1)中平衡发生移动所需最小c(Pb2+)=
(3)处理1 L含Pb2+浓度为3.07 mg·L-1的该废水至合格(Pb2+浓度小于1 mg·L-1)最少所需FeS的质量是
您最近一年使用:0次



