电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
(1)已知部分弱酸的电离常数如下表
①室温下,一定浓度的HCOONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是_______ 。
②0.1mol·L-1NaCN溶液和0.1mol·L-1NaHCO3溶液中,c(CN-)_______ c(HCO )(填“>”、“<”或“=”)。
)(填“>”、“<”或“=”)。
③常温下,pH相同的三种溶液a、HCOONab、NaCNc、Na2CO3,其物质的量浓度由大到小的顺序是_______ (填编号)。
④将少量CO2通入NaCN溶液,反应的离子方程式是_______ 。
(2)室温下,用0.100mol·L-1盐酸溶液滴定20.00mL0.100mol·L-1的某氨水溶液,滴定曲线如图所示:
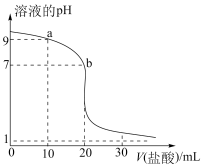
①b点液中离子浓度大小的关系式为_______ 。
②a点所示的溶液中电荷守恒式为_______ 。
(3)已知Ksp(BaCO3)=2.6×10-9,Ksp(BaSO4)=1.1×10-10
①现将浓度为2×10-4mol/LNa2CO3溶液与BaCl2溶液等体积混合,则生成BaCO3沉淀所需BaCl2溶液的最小浓度为_______ mol·L-1
②向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时,溶液中
_______ (保留三位有效数字)。
(1)已知部分弱酸的电离常数如下表
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离常数(25℃) | Ka=1.77×10-4 | Ka=4.3×10-10 | Ka1=5.0×10-7 Ka2=5.6×10-11 |
①室温下,一定浓度的HCOONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是
②0.1mol·L-1NaCN溶液和0.1mol·L-1NaHCO3溶液中,c(CN-)
 )(填“>”、“<”或“=”)。
)(填“>”、“<”或“=”)。③常温下,pH相同的三种溶液a、HCOONab、NaCNc、Na2CO3,其物质的量浓度由大到小的顺序是
④将少量CO2通入NaCN溶液,反应的离子方程式是
(2)室温下,用0.100mol·L-1盐酸溶液滴定20.00mL0.100mol·L-1的某氨水溶液,滴定曲线如图所示:

①b点液中离子浓度大小的关系式为
②a点所示的溶液中电荷守恒式为
(3)已知Ksp(BaCO3)=2.6×10-9,Ksp(BaSO4)=1.1×10-10
①现将浓度为2×10-4mol/LNa2CO3溶液与BaCl2溶液等体积混合,则生成BaCO3沉淀所需BaCl2溶液的最小浓度为
②向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时,溶液中

更新时间:2022-02-28 20:35:33
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】氮和硫的化合物在工农业生产、生活中具有重要应用。请回答下列问题:
(1)航天领域中常用肼 作为火箭发射的助燃剂。
作为火箭发射的助燃剂。
①已知各共价键键能如下表:
 ;
;
_______  。
。
② 与氨气相似,是一种碱性气体,易溶于水,生成弱碱
与氨气相似,是一种碱性气体,易溶于水,生成弱碱 。用电离方程式表示
。用电离方程式表示 显碱性的原因
显碱性的原因_______ 。
(2)查阅资料可知,常温下,部分弱电解质的电离平衡常数如表:
① 的电离平衡常数的表达式
的电离平衡常数的表达式
_______ ;
②常温下,等浓度的下列溶液a. 溶液;b.
溶液;b. 溶液;c.
溶液;c. 溶液,其
溶液,其 由大到小的顺序是
由大到小的顺序是_______ (用字母表示)。
(3)某同学设计一个肼 燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中
燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中 为阳离子交换膜。
为阳离子交换膜。_______ (填“正极”或“负极”),负极的电极反应式为_______ 。
②若甲中有 氧气(标准状况下)参加反应,乙中通过离子交换膜的阳离子个数为
氧气(标准状况下)参加反应,乙中通过离子交换膜的阳离子个数为____ ,丙中硫酸铜溶液的浓度_______ (填“变大”、“变小”或“不变”)。
(1)航天领域中常用肼
 作为火箭发射的助燃剂。
作为火箭发射的助燃剂。①已知各共价键键能如下表:
 |  |  |  |  | |
键能 | 946 | 497 | 193 | 391 | 463 |
 的结构如图
的结构如图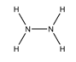
 ;
;
 。
。②
 与氨气相似,是一种碱性气体,易溶于水,生成弱碱
与氨气相似,是一种碱性气体,易溶于水,生成弱碱 。用电离方程式表示
。用电离方程式表示 显碱性的原因
显碱性的原因(2)查阅资料可知,常温下,部分弱电解质的电离平衡常数如表:
| 弱电解质 |  |  |  |
电离平衡常数 |  | 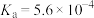 | 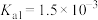 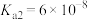 |
 的电离平衡常数的表达式
的电离平衡常数的表达式
②常温下,等浓度的下列溶液a.
 溶液;b.
溶液;b. 溶液;c.
溶液;c. 溶液,其
溶液,其 由大到小的顺序是
由大到小的顺序是(3)某同学设计一个肼
 燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中
燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中 为阳离子交换膜。
为阳离子交换膜。
②若甲中有
 氧气(标准状况下)参加反应,乙中通过离子交换膜的阳离子个数为
氧气(标准状况下)参加反应,乙中通过离子交换膜的阳离子个数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室模拟拉希法用氨和次氯酸钠反应制备肼(N2H4),并探究肼的性质,制备装置如图所示。
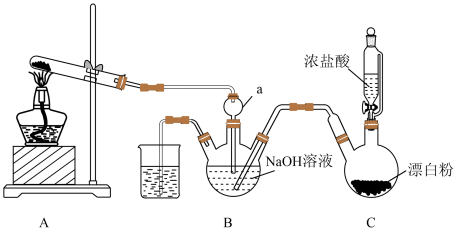
回答下列问题:
(1)肼的电子式为_______ 。
(2)装置A试管中的试剂为_______ 。
(3)装置B中制备肼的化学方程式为_______ 。
(4)上述装置中存在一处缺陷,会导致肼的产率降低,改进方法是_______ 。
(5)①探究性质。
已知N2H4是一种二元弱碱,在水中的电离与NH3相似,请写出肼的第二步电离的电离方程式:_______ ,室温下向N2H4水溶液中滴加某强酸,溶液的pH与 或
或 的变化关系如图所示,下列说法正确的是
的变化关系如图所示,下列说法正确的是_______ (填标号)。

A.N2H4在水溶液中第二步电离的平衡常数为10-1
B. 的平衡常数为109
的平衡常数为109
C. 的水解能力大于其电离能力
的水解能力大于其电离能力
D.N2H6Cl2溶液中: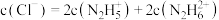
②测定产品中肼的质量分数。
称取装置B中溶液m g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH=6),加水配成100 mL溶液,移取25.00 mL置于锥形瓶中,并滴加2~3滴指示剂,用c mol/L的碘标准溶液滴定,滴定过程中有无色无味无毒气体产生,定终点时平均消耗标准溶液V mL,产品中肼的质量分数为_______ (用含m、c、V的式子表示)。

回答下列问题:
(1)肼的电子式为
(2)装置A试管中的试剂为
(3)装置B中制备肼的化学方程式为
(4)上述装置中存在一处缺陷,会导致肼的产率降低,改进方法是
(5)①探究性质。
已知N2H4是一种二元弱碱,在水中的电离与NH3相似,请写出肼的第二步电离的电离方程式:
 或
或 的变化关系如图所示,下列说法正确的是
的变化关系如图所示,下列说法正确的是
A.N2H4在水溶液中第二步电离的平衡常数为10-1
B.
 的平衡常数为109
的平衡常数为109C.
 的水解能力大于其电离能力
的水解能力大于其电离能力D.N2H6Cl2溶液中:
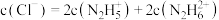
②测定产品中肼的质量分数。
称取装置B中溶液m g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH=6),加水配成100 mL溶液,移取25.00 mL置于锥形瓶中,并滴加2~3滴指示剂,用c mol/L的碘标准溶液滴定,滴定过程中有无色无味无毒气体产生,定终点时平均消耗标准溶液V mL,产品中肼的质量分数为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】水溶液广泛存在于生命体及其赖以生存的环境中,研究水溶液的性质及反应有重要意义,室温下,相关酸的电离平衡常数如下表所示:
回答下列问题。
(1) 电离方程式是
电离方程式是_________ 。
(2)物质的量浓度相同的 和
和 ,pH大小:
,pH大小:
_________  (填“<”“=”或“>”)。
(填“<”“=”或“>”)。
(3)物质的量浓度相同的 、
、 、
、 三种溶液,pH由大到小的顺序是
三种溶液,pH由大到小的顺序是_________ 。
(4)室温下,向未知浓度的 溶液中加入
溶液中加入 溶液。
溶液。
①溶液中的
_________ (填“增大”“减小”“不变”或“无法判断”)。
②当滴加 溶液至溶液中的
溶液至溶液中的 ,此时溶液中的pH
,此时溶液中的pH_________ 7(填“<”“=”或“>”),判断的依据_________ 。
(5)为测定某 溶液的浓度,取20.00
溶液的浓度,取20.00 待测溶液于锥形瓶中,滴加2滴酚酞溶液,用浓度为0.1000
待测溶液于锥形瓶中,滴加2滴酚酞溶液,用浓度为0.1000 的
的 标准溶液滴定。
标准溶液滴定。
①达到滴定终点的现象是_________ 。
②在滴定实验过程中,下列仪器中有蒸馏水,对实验结果没有影响的是_________ (填“滴定管”或“锥形瓶”)。
③经3次平行实验,达到滴定终点时,消耗 标准溶液体积的平均值为19.98
标准溶液体积的平均值为19.98 ,则此
,则此 溶液的浓度是
溶液的浓度是_________ 。
| 酸 |  | CH3COOH |  | HCl |
| 电离平衡常数 |  |  |  | —— |
(1)
 电离方程式是
电离方程式是(2)物质的量浓度相同的
 和
和 ,pH大小:
,pH大小:
 (填“<”“=”或“>”)。
(填“<”“=”或“>”)。(3)物质的量浓度相同的
 、
、 、
、 三种溶液,pH由大到小的顺序是
三种溶液,pH由大到小的顺序是(4)室温下,向未知浓度的
 溶液中加入
溶液中加入 溶液。
溶液。①溶液中的

②当滴加
 溶液至溶液中的
溶液至溶液中的 ,此时溶液中的pH
,此时溶液中的pH(5)为测定某
 溶液的浓度,取20.00
溶液的浓度,取20.00 待测溶液于锥形瓶中,滴加2滴酚酞溶液,用浓度为0.1000
待测溶液于锥形瓶中,滴加2滴酚酞溶液,用浓度为0.1000 的
的 标准溶液滴定。
标准溶液滴定。①达到滴定终点的现象是
②在滴定实验过程中,下列仪器中有蒸馏水,对实验结果没有影响的是
③经3次平行实验,达到滴定终点时,消耗
 标准溶液体积的平均值为19.98
标准溶液体积的平均值为19.98 ,则此
,则此 溶液的浓度是
溶液的浓度是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】 是重要的化工原料,某化学小组设计实验探究不同钠盐的阴离子对
是重要的化工原料,某化学小组设计实验探究不同钠盐的阴离子对 水解平衡的影响是否相同。
水解平衡的影响是否相同。
实验Ⅰ:配制100 mL 1 mol/L的 溶液,测得其pH为1.62。
溶液,测得其pH为1.62。
实验Ⅱ:常温下,用滴定管准确量取10.00 ml上述 溶液置于烧杯中,加入0.02 mol的NaCl固体,利用数字化仪器测得溶液pH与时间的关系如图1所示。
溶液置于烧杯中,加入0.02 mol的NaCl固体,利用数字化仪器测得溶液pH与时间的关系如图1所示。
实验Ⅲ:常温下,用滴定管准确量取10.00 mL上述 溶液置于烧杯中,加入0.01 mol的
溶液置于烧杯中,加入0.01 mol的 固体,利用数字化仪器测得溶液pH与时间的关系如图2所示。
固体,利用数字化仪器测得溶液pH与时间的关系如图2所示。

已知:①常温下, 的电离常数为
的电离常数为 ,
, 。
。
②在强酸弱碱盐溶液中加入强电解质,溶液中的离子总浓度增大,离子之间的相互牵制作用增强,易水解的阳离子的活性会增强或减弱。
回答下列问题:
(1)实验Ⅰ中配制的 溶液呈黄色,查阅资料得知是因为生成了少量的
溶液呈黄色,查阅资料得知是因为生成了少量的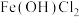 ,生成该物质的化学方程式为
,生成该物质的化学方程式为_______ 。
(2)实验Ⅱ和实验Ⅲ中量取 溶液时应选用
溶液时应选用_______ (填“酸式”或“碱式”)滴定管;该滴定管使用前必须进行的检查为_______ 写出其中一条即可)。
(3)常温下,对于 溶液,下列关系正确的是_______(填选项字母)。
溶液,下列关系正确的是_______(填选项字母)。
(4)图1中10s后溶液的pH下降的主要原因为_______ 。
(5)实验Ⅱ和实验Ⅰ中,加入NaCl固体和 固体的物质的量之比为2∶1的原因为
固体的物质的量之比为2∶1的原因为_______ 。
(6)图2中20s后溶液pH增大的主要原因为_______ 。结合图1和图2得出的实验结论:不同的钠盐对 溶液水解平衡的影响是不同的。
溶液水解平衡的影响是不同的。
 是重要的化工原料,某化学小组设计实验探究不同钠盐的阴离子对
是重要的化工原料,某化学小组设计实验探究不同钠盐的阴离子对 水解平衡的影响是否相同。
水解平衡的影响是否相同。实验Ⅰ:配制100 mL 1 mol/L的
 溶液,测得其pH为1.62。
溶液,测得其pH为1.62。实验Ⅱ:常温下,用滴定管准确量取10.00 ml上述
 溶液置于烧杯中,加入0.02 mol的NaCl固体,利用数字化仪器测得溶液pH与时间的关系如图1所示。
溶液置于烧杯中,加入0.02 mol的NaCl固体,利用数字化仪器测得溶液pH与时间的关系如图1所示。实验Ⅲ:常温下,用滴定管准确量取10.00 mL上述
 溶液置于烧杯中,加入0.01 mol的
溶液置于烧杯中,加入0.01 mol的 固体,利用数字化仪器测得溶液pH与时间的关系如图2所示。
固体,利用数字化仪器测得溶液pH与时间的关系如图2所示。
已知:①常温下,
 的电离常数为
的电离常数为 ,
, 。
。②在强酸弱碱盐溶液中加入强电解质,溶液中的离子总浓度增大,离子之间的相互牵制作用增强,易水解的阳离子的活性会增强或减弱。
回答下列问题:
(1)实验Ⅰ中配制的
 溶液呈黄色,查阅资料得知是因为生成了少量的
溶液呈黄色,查阅资料得知是因为生成了少量的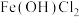 ,生成该物质的化学方程式为
,生成该物质的化学方程式为(2)实验Ⅱ和实验Ⅲ中量取
 溶液时应选用
溶液时应选用(3)常温下,对于
 溶液,下列关系正确的是_______(填选项字母)。
溶液,下列关系正确的是_______(填选项字母)。A. |
B. |
C. 的平衡常数 的平衡常数 |
D. |
(5)实验Ⅱ和实验Ⅰ中,加入NaCl固体和
 固体的物质的量之比为2∶1的原因为
固体的物质的量之比为2∶1的原因为(6)图2中20s后溶液pH增大的主要原因为
 溶液水解平衡的影响是不同的。
溶液水解平衡的影响是不同的。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。①~⑥表示元素在周期表中的位置,回答下列问题。
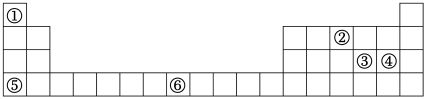
(1)①和④形成的化合物的化学式为_______ 。
(2)②的基态原子的轨道表示式为_______ ,其电子占据的最高能级的电子云轮廓是_______ 。
(3)⑤的基态原子占据的最高能层的符号是_______ ,其基态正一价离子占据的最高能级共有_______ 个原子轨道。
(4)⑥的基态正三价离子的价层电子排布式为_______ 。
(5)下列说法不正确 的是_______ 。
a.②的2px、2py、2pZ轨道互相垂直,但能量相等
b.④的p能级能量一定比s能级的能量高
c.⑥的2s、3s、4s能级的轨道数依次增多
(6)③和⑤形成的化合物的水溶液pH>7,结合离子方程式解释原因_______ 。

(1)①和④形成的化合物的化学式为
(2)②的基态原子的轨道表示式为
(3)⑤的基态原子占据的最高能层的符号是
(4)⑥的基态正三价离子的价层电子排布式为
(5)下列说法
a.②的2px、2py、2pZ轨道互相垂直,但能量相等
b.④的p能级能量一定比s能级的能量高
c.⑥的2s、3s、4s能级的轨道数依次增多
(6)③和⑤形成的化合物的水溶液pH>7,结合离子方程式解释原因
您最近一年使用:0次
【推荐3】某小组从反应速率和产物角度探究Mg与NaHCO3溶液反应。
实验I、25°C, 相同镁条分别与下列试剂反应
(1)已知: Mg(OH)2固体致密,易包裹在金属表面成膜。根据上述现象,推测在实验ii中。
①Mg可以提高 的电离程度,原因是
的电离程度,原因是___________ ;
②浑浊的主要原因是产生了___________ (填化学式) ;
③实验ii中产生气泡的速率快于实验i的原因可能是___________ 。
(2)补充实验II,证实(1)的推测:
①小组设计实验iii 的目的是___________ ; 甲同学结合实验iv的现象认为可以不必进行实验iii,他的理由是___________ ;
②实验ii生成气体的速率快于实验iv,原因可能是___________ ;
③查资料知 +Mg2+
+Mg2+  [Mg(HCO3)]+,请从平衡移动的角度解释实验ii产生气体速率更快的原因
[Mg(HCO3)]+,请从平衡移动的角度解释实验ii产生气体速率更快的原因___________ 。
实验I、25°C, 相同镁条分别与下列试剂反应
| 序号 | 试剂 | 浓度(mol·L-1) | 体积(mL) | pH | 现象 |
| i | H2O | —— | 7.5 | 7 | 镁条表面有微量气泡附着 |
| ii | NaHCO3溶液 | 1.0 | 7.5 | 8.4 | 镁条表面持续产生大量气泡,溶液略显浑浊,点燃气泡有爆鸣声 |
①Mg可以提高
 的电离程度,原因是
的电离程度,原因是②浑浊的主要原因是产生了
③实验ii中产生气泡的速率快于实验i的原因可能是
(2)补充实验II,证实(1)的推测:
| 序号 | 试剂 | 浓度(mol·L-1) | 体积(mL) | pH | 现象 |
| iii | NaNO3溶液 | 1.0 | 7.5 | 7 | 镁条表面有微量气泡附着 |
| iv | Na2CO3溶液 | 0.5 | 7.5 | 11.8 | 持续产生少量气泡,溶液显浑浊 |
②实验ii生成气体的速率快于实验iv,原因可能是
③查资料知
 +Mg2+
+Mg2+  [Mg(HCO3)]+,请从平衡移动的角度解释实验ii产生气体速率更快的原因
[Mg(HCO3)]+,请从平衡移动的角度解释实验ii产生气体速率更快的原因
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡,它们都可看作化学平衡。请根据所学知识回答:
(1)在0.1 mol·L-1的(NH4)2SO4溶液中,各种离子的浓度由大到小顺序为________ 。
(2)实验测得0.1 mol·L-1NaHCO3溶液的pH>7,请从电离和水解两方面分析导致NaHCO3溶液显碱性的原因:_____________________________________ 。(用化学用语及相关文字回答)
(3)①普通的泡沫灭火器内的塑料筒里盛放Al2(SO4)3溶液,铁筒中盛放NaHCO3溶液,其灭火的原理是__________________ 。(用化学用语及相关文字回答)
②不能把Al2(SO4)3溶液盛放在铁筒中的原因是___________ 。(用化学用语及相关文字回答)③不用溶解度较大的Na2CO3代替NaHCO3溶液的原因是___________________________ 。
(1)在0.1 mol·L-1的(NH4)2SO4溶液中,各种离子的浓度由大到小顺序为
(2)实验测得0.1 mol·L-1NaHCO3溶液的pH>7,请从电离和水解两方面分析导致NaHCO3溶液显碱性的原因:
(3)①普通的泡沫灭火器内的塑料筒里盛放Al2(SO4)3溶液,铁筒中盛放NaHCO3溶液,其灭火的原理是
②不能把Al2(SO4)3溶液盛放在铁筒中的原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】在工业合成尿素时常用 与
与 作原料进行生产.
作原料进行生产.
 如图为合成氨反应,氮气、氢气按体积比为1:3投料时不同温度和压强、使用相同催化剂条件下,平衡混合物中氨的体积分数图象.
如图为合成氨反应,氮气、氢气按体积比为1:3投料时不同温度和压强、使用相同催化剂条件下,平衡混合物中氨的体积分数图象.
 若分别用
若分别用 和
和 表示从反应开始至达平衡状态A、B时的化学反应速率,则
表示从反应开始至达平衡状态A、B时的化学反应速率,则
______  填“
填“ ”、“
”、“ ”或“
”或“ ”
” .
.
 在
在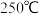 、
、 下,
下, 的转化率为
的转化率为
______  计算结果保留小数点后1位
计算结果保留小数点后1位 .
.
 将
将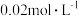 氨水与
氨水与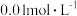 的盐酸等体积混合,若反应后混合溶液显碱性,则反应混合液中各离子浓度由大到小的顺序为
的盐酸等体积混合,若反应后混合溶液显碱性,则反应混合液中各离子浓度由大到小的顺序为 ______ .
 与
与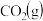 经过两步反应生成尿素,两步反应的能量变化示意图如下:
经过两步反应生成尿素,两步反应的能量变化示意图如下:
 与
与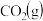 反应生成尿素的热化学方程式为
反应生成尿素的热化学方程式为 ______ .
 工业上合成尿素时,既能加快反应速率,又能提高原料利用率的措施有
工业上合成尿素时,既能加快反应速率,又能提高原料利用率的措施有 ______  填序号
填序号
A.升高温度 加入催化剂
加入催化剂 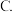 将尿素及时分离出去
将尿素及时分离出去  增大反应体系的压强
增大反应体系的压强
 某实验小组模拟工业上合成尿素的条件,在一体积为
某实验小组模拟工业上合成尿素的条件,在一体积为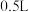 的密闭容器中投入4mol氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如图所示:
的密闭容器中投入4mol氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如图所示:

 已知总反应的速率通常由慢的一步反应决定,则合成尿素总反应的速率由第
已知总反应的速率通常由慢的一步反应决定,则合成尿素总反应的速率由第 ______ 步反应决定.
 反应进行到10min时测得
反应进行到10min时测得 的物质的量如图所示,则用
的物质的量如图所示,则用 表示的第一步反应的速率
表示的第一步反应的速率
______ .

 与
与 作原料进行生产.
作原料进行生产.  如图为合成氨反应,氮气、氢气按体积比为1:3投料时不同温度和压强、使用相同催化剂条件下,平衡混合物中氨的体积分数图象.
如图为合成氨反应,氮气、氢气按体积比为1:3投料时不同温度和压强、使用相同催化剂条件下,平衡混合物中氨的体积分数图象.  若分别用
若分别用 和
和 表示从反应开始至达平衡状态A、B时的化学反应速率,则
表示从反应开始至达平衡状态A、B时的化学反应速率,则
 填“
填“ ”、“
”、“ ”或“
”或“ ”
” .
. 在
在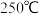 、
、 下,
下, 的转化率为
的转化率为  计算结果保留小数点后1位
计算结果保留小数点后1位 .
. 将
将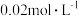 氨水与
氨水与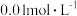 的盐酸等体积混合,若反应后混合溶液显碱性,则反应混合液中各离子浓度由大到小的顺序为
的盐酸等体积混合,若反应后混合溶液显碱性,则反应混合液中各离子浓度由大到小的顺序为  与
与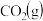 经过两步反应生成尿素,两步反应的能量变化示意图如下:
经过两步反应生成尿素,两步反应的能量变化示意图如下:
 与
与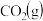 反应生成尿素的热化学方程式为
反应生成尿素的热化学方程式为  工业上合成尿素时,既能加快反应速率,又能提高原料利用率的措施有
工业上合成尿素时,既能加快反应速率,又能提高原料利用率的措施有  填序号
填序号
A.升高温度
 加入催化剂
加入催化剂 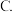 将尿素及时分离出去
将尿素及时分离出去  增大反应体系的压强
增大反应体系的压强  某实验小组模拟工业上合成尿素的条件,在一体积为
某实验小组模拟工业上合成尿素的条件,在一体积为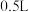 的密闭容器中投入4mol氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如图所示:
的密闭容器中投入4mol氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如图所示: 
 已知总反应的速率通常由慢的一步反应决定,则合成尿素总反应的速率由第
已知总反应的速率通常由慢的一步反应决定,则合成尿素总反应的速率由第  反应进行到10min时测得
反应进行到10min时测得 的物质的量如图所示,则用
的物质的量如图所示,则用 表示的第一步反应的速率
表示的第一步反应的速率

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】草酸 是一种还原性二元弱酸,存在于菠菜等植物中。
是一种还原性二元弱酸,存在于菠菜等植物中。
(1)常温下,将某浓度的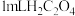 溶液加蒸馏水稀释,在稀释该溶液过程中,下列物理量始终增大的是
溶液加蒸馏水稀释,在稀释该溶液过程中,下列物理量始终增大的是_______ (填字母代号)
a. b.
b.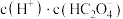
c. d.
d.
(2)已知 溶液呈酸性,则溶液中
溶液呈酸性,则溶液中
_______ 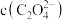 (填“>”“<”或“=”,下同);若
(填“>”“<”或“=”,下同);若 溶液中第二步电离出的
溶液中第二步电离出的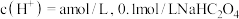 溶液中
溶液中 电离出的
电离出的
_______ a 。
。
某兴趣小组同学探究 溶液与草酸溶液反应速率的影响因素。配制
溶液与草酸溶液反应速率的影响因素。配制 溶液、
溶液、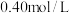 草酸溶液。将
草酸溶液。将 溶液与草酸溶液按如下比例混合。
溶液与草酸溶液按如下比例混合。
(3)上述实验中应控制 相同,可加入的试剂是
相同,可加入的试剂是_______ (填序号)。
a.盐酸 b.硫酸 c.草酸
小组同学将溶液 调至1并进行实验①和②,发现紫色并未直接褪去,而是分成两个阶段:
调至1并进行实验①和②,发现紫色并未直接褪去,而是分成两个阶段:
i,紫色溶液变为青色溶液,ii.青色溶液逐渐褪至无色溶液。
资料:(a) 在溶液中无色,在草酸中不能形成配合物;
在溶液中无色,在草酸中不能形成配合物;
(b) 无色,有强氧化性,发生反应
无色,有强氧化性,发生反应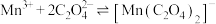 (青绿色)后氧化性减弱;
(青绿色)后氧化性减弱;
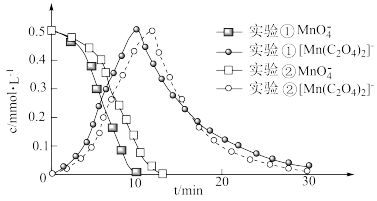
进一步实验证明溶液中含有 ,反应过程中
,反应过程中 和
和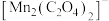 浓度随时间的变化如下图。
浓度随时间的变化如下图。
(4)第i阶段中检测到有 气体产生,反应的离子方程式为
气体产生,反应的离子方程式为_______ 。
(5)实验②在第ii阶段的反应速率较大,可能的原因是_______ 。
结论:反应可能是分阶段进行的。草酸浓度的改变对不同阶段反应速率的影响可能不同。
 是一种还原性二元弱酸,存在于菠菜等植物中。
是一种还原性二元弱酸,存在于菠菜等植物中。(1)常温下,将某浓度的
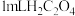 溶液加蒸馏水稀释,在稀释该溶液过程中,下列物理量始终增大的是
溶液加蒸馏水稀释,在稀释该溶液过程中,下列物理量始终增大的是a.
 b.
b.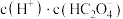
c.
 d.
d.
(2)已知
 溶液呈酸性,则溶液中
溶液呈酸性,则溶液中
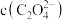 (填“>”“<”或“=”,下同);若
(填“>”“<”或“=”,下同);若 溶液中第二步电离出的
溶液中第二步电离出的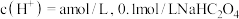 溶液中
溶液中 电离出的
电离出的
 。
。某兴趣小组同学探究
 溶液与草酸溶液反应速率的影响因素。配制
溶液与草酸溶液反应速率的影响因素。配制 溶液、
溶液、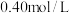 草酸溶液。将
草酸溶液。将 溶液与草酸溶液按如下比例混合。
溶液与草酸溶液按如下比例混合。| 序号 | 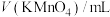 | 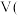 草酸 草酸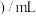 | 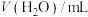 | 反应温度 |
| ① | 2.0 | 2.0 | 0 | 20 |
| ② | 2.0 | 1.0 | 1.0 | 20 |
(3)上述实验中应控制
 相同,可加入的试剂是
相同,可加入的试剂是a.盐酸 b.硫酸 c.草酸
小组同学将溶液
 调至1并进行实验①和②,发现紫色并未直接褪去,而是分成两个阶段:
调至1并进行实验①和②,发现紫色并未直接褪去,而是分成两个阶段:i,紫色溶液变为青色溶液,ii.青色溶液逐渐褪至无色溶液。
资料:(a)
 在溶液中无色,在草酸中不能形成配合物;
在溶液中无色,在草酸中不能形成配合物;(b)
 无色,有强氧化性,发生反应
无色,有强氧化性,发生反应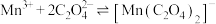 (青绿色)后氧化性减弱;
(青绿色)后氧化性减弱;进一步实验证明溶液中含有
 ,反应过程中
,反应过程中 和
和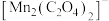 浓度随时间的变化如下图。
浓度随时间的变化如下图。
(4)第i阶段中检测到有
 气体产生,反应的离子方程式为
气体产生,反应的离子方程式为(5)实验②在第ii阶段的反应速率较大,可能的原因是
结论:反应可能是分阶段进行的。草酸浓度的改变对不同阶段反应速率的影响可能不同。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】我国是世界上最早制得和使用金属锌的国家。湿法炼锌产生的铜镉渣[主要含锌、铜、铁、镉(Cd)等单质]用于生产金属镉的工艺流程如图:
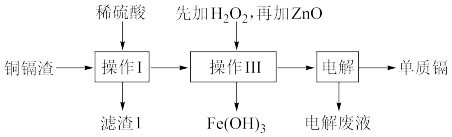
已知:相关金属离子生成氢氧化物沉淀的pH如下表(金属离子的起始浓度为0.1mol·L-1)
(1)操作I、III中都用到过滤操作,实验室中过滤操作适用于分离___________ 。
(2)操作I过程中,不采用通入空气的方法进行搅拌,原因是防止将Cu氧化浸出,若通入空气搅拌时,氧化浸出Cu2+的离子方程式为___________ 。
(3)①操作III中先加入适量H2O2,发生反应的离子方程式为___________ 。
②再加入ZnO控制反应液的pH,合适的pH范围为___________ 。
(4)净化后的溶液用惰性电极电解可获得镉单质,电解废液中含有Zn2+,电解废液中可循环利用的溶质是___________ ,说明活泼性Zn___________ Cd(填“>”或“<”)。
(5)该湿法炼锌废水中含有Zn2+,排放前需处理。向废水中加入CH3COOH和CH3COONa组成的缓冲溶液调节pH,通入H2S发生反应:Zn2++H2S⇌ZnS(s)+2H+。处理后的废水中部分微粒浓度如下表:
处理后的废水的c(Zn2+)=________ mol∙L-1,pH=________ [已知:Ksp(ZnS)=1.0×10-23,Ka(CH3COOH)=2.0×10-5]

已知:相关金属离子生成氢氧化物沉淀的pH如下表(金属离子的起始浓度为0.1mol·L-1)
| 开始沉淀时pH | 完全沉淀时pH | |
| Cd2+ | 7.0 | 9.4 |
| Fe2+ | 6.3 | 8.3 |
| Fe3+ | 1.5 | 3.2 |
(2)操作I过程中,不采用通入空气的方法进行搅拌,原因是防止将Cu氧化浸出,若通入空气搅拌时,氧化浸出Cu2+的离子方程式为
(3)①操作III中先加入适量H2O2,发生反应的离子方程式为
②再加入ZnO控制反应液的pH,合适的pH范围为
(4)净化后的溶液用惰性电极电解可获得镉单质,电解废液中含有Zn2+,电解废液中可循环利用的溶质是
(5)该湿法炼锌废水中含有Zn2+,排放前需处理。向废水中加入CH3COOH和CH3COONa组成的缓冲溶液调节pH,通入H2S发生反应:Zn2++H2S⇌ZnS(s)+2H+。处理后的废水中部分微粒浓度如下表:
| 微粒 | H2S | CH3COOH | CH3COO- | S2- |
| 浓度/mol•L-1 | 0.10 | 0.05 | 0.10 | 1.0×10-12 |
您最近一年使用:0次
【推荐2】某化学兴趣小组利用硫铁矿烧渣(主要成分为Fe3O4、Fe2O3、FeO、SiO2等)为原料来制取氧化铁。

请回答下列问题:(已知:ksp[Fe(OH)2]=4.9×10﹣17)
(1)步骤Ⅱ后得到的滤渣是:___________ 。
(2)为了提高酸浸时的速率,除了适当增大硫酸的浓度外,还可以采取的措施有:___________ (写出两条)。
(3)检验步骤Ⅲ反应后的溶液中金属阳离子的试剂是:___________ 。
(4)步骤V中,FeCO3达到沉淀溶解平衡时,室温下测得溶液的pH为8,c(Fe2+)为1.0×10﹣5mol/L,判断所得FeCO3中是否混有Fe(OH)2?___________ (填是或否)。
(5)步骤V反应成FeCO3的离子反应方程式:___________ 。

请回答下列问题:(已知:ksp[Fe(OH)2]=4.9×10﹣17)
(1)步骤Ⅱ后得到的滤渣是:
(2)为了提高酸浸时的速率,除了适当增大硫酸的浓度外,还可以采取的措施有:
(3)检验步骤Ⅲ反应后的溶液中金属阳离子的试剂是:
(4)步骤V中,FeCO3达到沉淀溶解平衡时,室温下测得溶液的pH为8,c(Fe2+)为1.0×10﹣5mol/L,判断所得FeCO3中是否混有Fe(OH)2?
(5)步骤V反应成FeCO3的离子反应方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】钼酸钠晶体(Na2MoO4·2H2O)是一种金属腐蚀抑制剂。如图是利用钼精矿(主要成分是MoS2,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图。
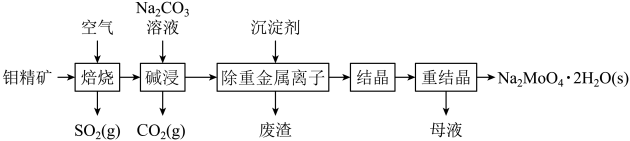
(1)在焙烧炉中,空气从炉底进入,矿石经粉碎后从炉顶加入,这样处理的目的是___ ,焙烧钼精矿所用的装置是多层焙烧炉,如图为各炉层固体物料的物质的量的百分数(φ)。
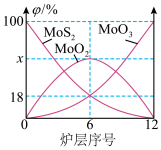
①x=___ 。
②“焙烧”时MoS2最终转化为MoO3,写出该反应的化学方程式:___ 。
(2)沉淀剂通常用Na2S,使用时若溶液pH较小,Pb2+沉淀不完全,原因是___ 。
(3)“结晶”前需向滤液中加入Ba(OH)2固体以除去CO 。若滤液中c(MoO
。若滤液中c(MoO )=0.40mol•L-1,c(CO
)=0.40mol•L-1,c(CO )=0.10mol•L-1,当BaMoO4开始沉淀时,CO
)=0.10mol•L-1,当BaMoO4开始沉淀时,CO 的去除率是
的去除率是___ %[已知:Ksp(BaCO3)=1×10-9,Ksp(BaMoO4)=4.0×10-8,溶液体积变化忽略不计]。
(4)在碱性条件下,将钼精矿加入NaClO溶液中也能制备Na2MoO4,同时生成硫酸盐,该反应的离子方程式是___ 。
(5)钼酸盐对碳钢的腐蚀具有缓蚀作用,其原理是:在空气中钼酸盐能在钢铁表面形成FeMoO4——Fe2O3保护膜。在密闭式循环冷却水系统中,为缓蚀碳钢管道,除加入钼酸盐外还需加入的物质是___ (填选项字母)。
A.NaNO2 B.通入适量N2 C.油脂 D.盐酸

(1)在焙烧炉中,空气从炉底进入,矿石经粉碎后从炉顶加入,这样处理的目的是

①x=
②“焙烧”时MoS2最终转化为MoO3,写出该反应的化学方程式:
(2)沉淀剂通常用Na2S,使用时若溶液pH较小,Pb2+沉淀不完全,原因是
(3)“结晶”前需向滤液中加入Ba(OH)2固体以除去CO
 。若滤液中c(MoO
。若滤液中c(MoO )=0.40mol•L-1,c(CO
)=0.40mol•L-1,c(CO )=0.10mol•L-1,当BaMoO4开始沉淀时,CO
)=0.10mol•L-1,当BaMoO4开始沉淀时,CO 的去除率是
的去除率是(4)在碱性条件下,将钼精矿加入NaClO溶液中也能制备Na2MoO4,同时生成硫酸盐,该反应的离子方程式是
(5)钼酸盐对碳钢的腐蚀具有缓蚀作用,其原理是:在空气中钼酸盐能在钢铁表面形成FeMoO4——Fe2O3保护膜。在密闭式循环冷却水系统中,为缓蚀碳钢管道,除加入钼酸盐外还需加入的物质是
A.NaNO2 B.通入适量N2 C.油脂 D.盐酸
您最近一年使用:0次



