已知2SO2(g)+O2(g) 2SO3(g),下图为不同温度(T1、T2)下SO2的转化率随时间的变化曲线。
2SO3(g),下图为不同温度(T1、T2)下SO2的转化率随时间的变化曲线。
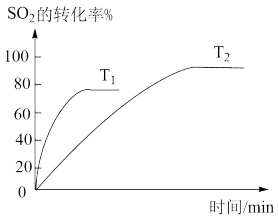
(1)T1___________ (选填“>”“<”或“=”)T2,判断依据是___________ ;该反应为___________ (选填“放”或“吸”)热反应,判断依据是___________ 。
(2)在相同温度下:2NO(g)+O2(g) 2NO2(g) K1=a;
2NO2(g) K1=a;
NO2(g)+SO2(g) SO3(g)+NO(g) K2=b;
SO3(g)+NO(g) K2=b;
则2SO2(g)+O2(g) 2SO3(g)的平衡常数K=
2SO3(g)的平衡常数K=___________ (用a、b表示)。
 2SO3(g),下图为不同温度(T1、T2)下SO2的转化率随时间的变化曲线。
2SO3(g),下图为不同温度(T1、T2)下SO2的转化率随时间的变化曲线。
(1)T1
(2)在相同温度下:2NO(g)+O2(g)
 2NO2(g) K1=a;
2NO2(g) K1=a;NO2(g)+SO2(g)
 SO3(g)+NO(g) K2=b;
SO3(g)+NO(g) K2=b;则2SO2(g)+O2(g)
 2SO3(g)的平衡常数K=
2SO3(g)的平衡常数K=
2022高二·上海·专题练习 查看更多[1]
(已下线)2.2.2 浓度商、温度对化学平衡的影响-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)
更新时间:2022/09/01 17:55:57
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】 是一种重要的化工原料,在生产和生活中应用十分广泛。地康法制取氯气的反应为:
是一种重要的化工原料,在生产和生活中应用十分广泛。地康法制取氯气的反应为: 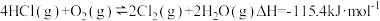 。该反应分两步进行,其基本原理如下图所示:
。该反应分两步进行,其基本原理如下图所示:
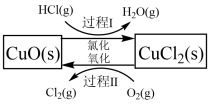
过程I的反应为,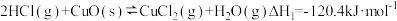
(])该原理中, 的作用是
的作用是_____________
(2)过程II反应的热化学方程式为____________
(3)压强为 时,地康法中
时,地康法中 的平衡转化率
的平衡转化率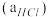 随温度变化曲线如图。
随温度变化曲线如图。
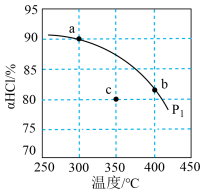
①平衡常数比较:K(a)____________ K(b)(填">“<"或“-").
②c点表示投料不变,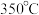 、压强为
、压强为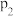 时,地康法中HCl的平衡转化率,则p2
时,地康法中HCl的平衡转化率,则p2_____________ p1(填“>”“<”或“=”),理由是___________ 。
 是一种重要的化工原料,在生产和生活中应用十分广泛。地康法制取氯气的反应为:
是一种重要的化工原料,在生产和生活中应用十分广泛。地康法制取氯气的反应为: 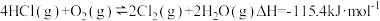 。该反应分两步进行,其基本原理如下图所示:
。该反应分两步进行,其基本原理如下图所示:
过程I的反应为,
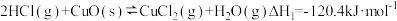
(])该原理中,
 的作用是
的作用是(2)过程II反应的热化学方程式为
(3)压强为
 时,地康法中
时,地康法中 的平衡转化率
的平衡转化率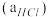 随温度变化曲线如图。
随温度变化曲线如图。
①平衡常数比较:K(a)
②c点表示投料不变,
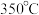 、压强为
、压强为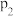 时,地康法中HCl的平衡转化率,则p2
时,地康法中HCl的平衡转化率,则p2
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】继金属储氢材料后,有机液态储氢技术(LOHC)由于其储氢密度高,脱氢效果好,倍受研究人员青睐。萘(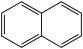 ,C10H8)与十氢萘(
,C10H8)与十氢萘( ,C10H18)的储氢脱氢就是其中重要的研究对象。
,C10H18)的储氢脱氢就是其中重要的研究对象。
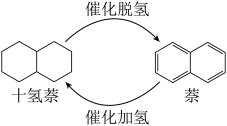
已知如下数据:
则十氢萘脱氢的热化学方程式为_____ 。
 ,C10H8)与十氢萘(
,C10H8)与十氢萘( ,C10H18)的储氢脱氢就是其中重要的研究对象。
,C10H18)的储氢脱氢就是其中重要的研究对象。
已知如下数据:
| 物质 | C10H18(十氢萘,l) | C10H8(萘,l) | H2(g) |
| 燃烧热ΔH/(kJ·mol-1) | -5896 | -5154 | -286 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】完成下列问题。
(1)研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如图:

反应I:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551kJ·mol-1
反应III:S(s)+O2(g)=SO2(g) ΔH3=-297kJ·mol-1
反应II的热化学方程式:___________ 。
(2)我国科学家实现了在铜催化剂条件下将(CH3)2NCHO转化为N(CH3)3。计算机模拟单个分子在铜催化剂表面的反应历程如图所示。

该反应的热化学方程式:___________ 。(用相对能量的变化来表示ΔH)
(1)研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如图:

反应I:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551kJ·mol-1
反应III:S(s)+O2(g)=SO2(g) ΔH3=-297kJ·mol-1
反应II的热化学方程式:
(2)我国科学家实现了在铜催化剂条件下将(CH3)2NCHO转化为N(CH3)3。计算机模拟单个分子在铜催化剂表面的反应历程如图所示。

该反应的热化学方程式:
您最近一年使用:0次
【推荐1】美国Bay工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如图所示:

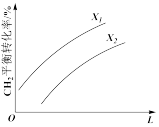
(1)该流程中第Ⅰ步反应为CH4(g)+H2O(g) CO(g)+3H2(g) △H>0。若如图表示在其他条件相同时,分别测定不同压强.不同温度下CH4的平衡转化率(纵坐标为CH4的平衡转化率),则图中L表示
CO(g)+3H2(g) △H>0。若如图表示在其他条件相同时,分别测定不同压强.不同温度下CH4的平衡转化率(纵坐标为CH4的平衡转化率),则图中L表示__ ,其中X1__ X2(填“>”或“<”)。
(2)该流程的第Ⅱ步反应为CO(g)+H2O(g) H2(g)+CO2(g),该反应的化学平衡常数表达式为K=
H2(g)+CO2(g),该反应的化学平衡常数表达式为K=__ ;反应的平衡常数随温度的变化如表所示。
①从表可以推断:此反应的正反应是__ (填“吸”或“放”)热反应。
②在500℃下,若开始时向恒容密闭容器中充入CO与H2O均为3mol,则达到平衡后CO的转化率为__ 。
③在830℃时,以表格的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向逆反应方向进行的有__ (填实验编号)。
④在一个不传热的固定容积的容器中,判断该反应达到平衡的标志是__ (填字母)。
A.各组分的物质的量浓度不再改变
B.v(CO2)正=v(H2O)逆
C.混合气体的密度不变
D.混合气体的平均相对分子质量不变
E.体系的压强不再发生变化
F.体系的温度不再发生变化
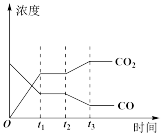
⑤如图表示该反应在t1时刻达到平衡,在t2时刻分别因改变某个条件而发生变化的情况:图中t2时刻发生改变的条件可能是__ (写出两种)。

(1)该流程中第Ⅰ步反应为CH4(g)+H2O(g)
 CO(g)+3H2(g) △H>0。若如图表示在其他条件相同时,分别测定不同压强.不同温度下CH4的平衡转化率(纵坐标为CH4的平衡转化率),则图中L表示
CO(g)+3H2(g) △H>0。若如图表示在其他条件相同时,分别测定不同压强.不同温度下CH4的平衡转化率(纵坐标为CH4的平衡转化率),则图中L表示
(2)该流程的第Ⅱ步反应为CO(g)+H2O(g)
 H2(g)+CO2(g),该反应的化学平衡常数表达式为K=
H2(g)+CO2(g),该反应的化学平衡常数表达式为K=| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
①从表可以推断:此反应的正反应是
②在500℃下,若开始时向恒容密闭容器中充入CO与H2O均为3mol,则达到平衡后CO的转化率为
| 实验编号 | n(CO) | n(H2O) | n(H2) | n(CO2) |
| 甲 | 2 | 5 | 4 | 3 |
| 乙 | 3 | 3 | 2 | 2 |
| 丙 | 0.25 | 4 | 2 | 1 |
③在830℃时,以表格的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向逆反应方向进行的有
④在一个不传热的固定容积的容器中,判断该反应达到平衡的标志是
A.各组分的物质的量浓度不再改变
B.v(CO2)正=v(H2O)逆
C.混合气体的密度不变
D.混合气体的平均相对分子质量不变
E.体系的压强不再发生变化
F.体系的温度不再发生变化
⑤如图表示该反应在t1时刻达到平衡,在t2时刻分别因改变某个条件而发生变化的情况:图中t2时刻发生改变的条件可能是

您最近一年使用:0次
【推荐2】合成氨技术的创立开辟了人工固氮的重要途径。回答下列问题:
(1)德国化学家F.Haber从1902年开始研究N2和H2直接合成NH3。在1.01×105Pa、250℃时,将1 molN2和1 molH2加入aL刚性容器中充分反应,测得NH3体积分数为0.04;其他条件不变,温度升高至450℃,测得NH3体积分数为0.025,则可判断合成氨反应为____ 填“吸热”或“放热”)反应。
(2)在1.01×105Pa、250℃时,将2 molN2和2 molH2加入aL密闭容器中充分反应,H2平衡转化率可能为___ (填标号)。
A =4% B <4% C 4%~7% D >11.5%
(3)我国科学家结合实验与计算机模拟结果,研究了在铁掺杂W18049纳米反应器催化剂表面上实现常温低电位合成氨,获得较高的氨产量和法拉第效率。反应历程如图所示,其中吸附在催化剂表面的物种用*标注。

需要吸收能量最大的能垒(活化能)E=____ ev,该步骤的化学方程式为____ ,若通入H2体积分数过大,可能造成 ___ 。
(4)T℃时,在恒温恒容的密闭条件下发生反应: 反应过程中各物质浓度的变化曲线如图所示:
反应过程中各物质浓度的变化曲线如图所示:
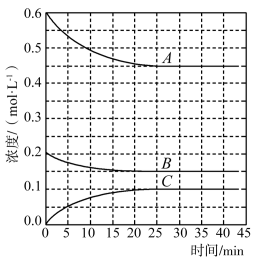
①表示N2浓度变化的曲线是____ (填“A”、“B”或“C’,)。与(1)中的实验条件(1.01×105Pa、450℃)相比,改变的条件可能是_____ 。
②在0~25min内H2的平均反应速率为____ 。在该条件下反应的平衡常数为 ___ mol-2.L2(保留两位有效数字)。
(1)德国化学家F.Haber从1902年开始研究N2和H2直接合成NH3。在1.01×105Pa、250℃时,将1 molN2和1 molH2加入aL刚性容器中充分反应,测得NH3体积分数为0.04;其他条件不变,温度升高至450℃,测得NH3体积分数为0.025,则可判断合成氨反应为
(2)在1.01×105Pa、250℃时,将2 molN2和2 molH2加入aL密闭容器中充分反应,H2平衡转化率可能为
A =4% B <4% C 4%~7% D >11.5%
(3)我国科学家结合实验与计算机模拟结果,研究了在铁掺杂W18049纳米反应器催化剂表面上实现常温低电位合成氨,获得较高的氨产量和法拉第效率。反应历程如图所示,其中吸附在催化剂表面的物种用*标注。

需要吸收能量最大的能垒(活化能)E=
(4)T℃时,在恒温恒容的密闭条件下发生反应:
 反应过程中各物质浓度的变化曲线如图所示:
反应过程中各物质浓度的变化曲线如图所示:
①表示N2浓度变化的曲线是
②在0~25min内H2的平均反应速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ 当温度高于500 K时,科学家成功利用二氧化碳和氢气合成了乙醇,这在节能减排、降低碳排放方面具有重大意义。回答下列问题:
(1)该反应的化学方程式为________________________ ;
(2)在恒容密闭容器中,判断上述反应达到平衡状态的依据是________ 。
a.CO2与乙醇的浓度之比不再改变
b.单位时间内消耗H2和CO2的物质的量之比为3∶1
c.H2的体积分数保持不变
d.混合气体的平均相对分子质量不再改变
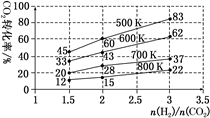
(3)在一定压强下,测得由CO2制取乙醇的实验数据中,起始投料比、温度与CO2的转化率的关系如图。根据图中数据分析:
①升高温度,平衡向________ (正或逆)反应方向移动。
②在700 K、起始投料比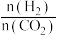 =1.5时,H2的体积分数为
=1.5时,H2的体积分数为________ (保留小数点后一位)。
③在500 K、起始投料比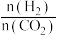 =2时,达到平衡后乙醇的浓度为a mol·L-1,则达到平衡时H2的浓度为
=2时,达到平衡后乙醇的浓度为a mol·L-1,则达到平衡时H2的浓度为________ (保留小数点后两位)。
Ⅱ 汽车尾气中含有NO、CO和碳颗粒等有害物质,已成为某些大城市空气的主要污染源。
(1)汽车燃料中一般不含氮元素,汽缸中生成NO的原因为(可逆反应,用化学方程式表示)________________________________ ,且汽缸内温度越高,单位时间内NO排放量越大,试分析其原因____________________ 。
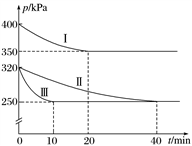
(2)治理汽车尾气中NO和CO污染的一种方法是将其转化为无害的CO2和N2,反应原理:2NO(g)+2CO(g) 2CO2(g)+N2(g) ΔH<0。某研究小组在三个容积均为5L的恒容密闭容器中,分别充入0.2molNO和0.2molCO,在三种不同实验条件下进行上述反应(体系各自保持温度不变),反应体系总压强随时间的变化如图所示。
2CO2(g)+N2(g) ΔH<0。某研究小组在三个容积均为5L的恒容密闭容器中,分别充入0.2molNO和0.2molCO,在三种不同实验条件下进行上述反应(体系各自保持温度不变),反应体系总压强随时间的变化如图所示。
①计算实验Ⅱ从开始至达到平衡时的反应速率v(NO)=________________ 。
②图中三组实验从开始至达到平衡时的反应速率v(NO)由小到大的顺序为________ (填序号)。
③与实验Ⅱ相比,实验Ⅰ和实验Ⅲ分别仅改变一种反应条件,所改变的条件为:实验Ⅰ_______________________________ ;实验Ⅲ_______________________ 。
④三组实验中CO的平衡转化率αⅠ(CO)、αⅡ(CO)、αⅢ(CO)的大小关系为______________ 。判断依据为__________________________________________ 。
(1)该反应的化学方程式为
(2)在恒容密闭容器中,判断上述反应达到平衡状态的依据是
a.CO2与乙醇的浓度之比不再改变
b.单位时间内消耗H2和CO2的物质的量之比为3∶1
c.H2的体积分数保持不变
d.混合气体的平均相对分子质量不再改变

(3)在一定压强下,测得由CO2制取乙醇的实验数据中,起始投料比、温度与CO2的转化率的关系如图。根据图中数据分析:
①升高温度,平衡向
②在700 K、起始投料比
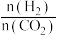 =1.5时,H2的体积分数为
=1.5时,H2的体积分数为③在500 K、起始投料比
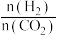 =2时,达到平衡后乙醇的浓度为a mol·L-1,则达到平衡时H2的浓度为
=2时,达到平衡后乙醇的浓度为a mol·L-1,则达到平衡时H2的浓度为Ⅱ 汽车尾气中含有NO、CO和碳颗粒等有害物质,已成为某些大城市空气的主要污染源。
(1)汽车燃料中一般不含氮元素,汽缸中生成NO的原因为(可逆反应,用化学方程式表示)

(2)治理汽车尾气中NO和CO污染的一种方法是将其转化为无害的CO2和N2,反应原理:2NO(g)+2CO(g)
 2CO2(g)+N2(g) ΔH<0。某研究小组在三个容积均为5L的恒容密闭容器中,分别充入0.2molNO和0.2molCO,在三种不同实验条件下进行上述反应(体系各自保持温度不变),反应体系总压强随时间的变化如图所示。
2CO2(g)+N2(g) ΔH<0。某研究小组在三个容积均为5L的恒容密闭容器中,分别充入0.2molNO和0.2molCO,在三种不同实验条件下进行上述反应(体系各自保持温度不变),反应体系总压强随时间的变化如图所示。①计算实验Ⅱ从开始至达到平衡时的反应速率v(NO)=
②图中三组实验从开始至达到平衡时的反应速率v(NO)由小到大的顺序为
③与实验Ⅱ相比,实验Ⅰ和实验Ⅲ分别仅改变一种反应条件,所改变的条件为:实验Ⅰ
④三组实验中CO的平衡转化率αⅠ(CO)、αⅡ(CO)、αⅢ(CO)的大小关系为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】目前城市空气质量恶化的原因之一是机动车尾气和燃煤产生的烟气。NO和CO均为汽车尾气的成分这两种气体在催化转换器中发生如下反应:2NO(g)+2CO(g) 2CO2(g)+N2(g) △H=-a kJ/mol,在一定温度下,将
2CO2(g)+N2(g) △H=-a kJ/mol,在一定温度下,将 ,
,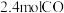 气体通入固定容积为2L的密闭容器中,发应过程中部分物质的浓度变化如图1所示
气体通入固定容积为2L的密闭容器中,发应过程中部分物质的浓度变化如图1所示 计算结果保留三位有效数字
计算结果保留三位有效数字 。
。
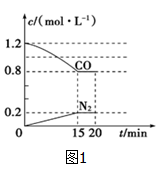
(1)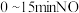 的平均速率
的平均速率
______ ,CO的转化率为______ 。
(2)15 min后反应达到平衡,若将此时得到的 气体用含有
气体用含有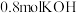 的溶液吸收,则电解质溶液中各种离子的物质的量浓度由大到小的顺序是
的溶液吸收,则电解质溶液中各种离子的物质的量浓度由大到小的顺序是______ 。
(3)20 min时,若改变某一反应条件,导致CO浓度增大,则改变的条件可能是______  填序号
填序号 。
。
 缩小容器体积
缩小容器体积  扩大容器体积
扩大容器体积  增加 NO的量
增加 NO的量
 降低温度
降低温度  增加CO的量
增加CO的量  使用催化剂
使用催化剂
(4)若保持反应体系的温度不变,20min时再向容器中充入CO、 各
各 ,化学平衡将
,化学平衡将______  填“向左”、“向右”或“不”
填“向左”、“向右”或“不” 移动,重新达到平衡后,该反应的化学平衡常数为
移动,重新达到平衡后,该反应的化学平衡常数为______ 。
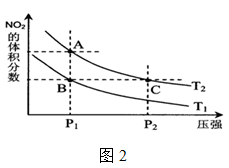
(5)对于反应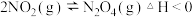 ,在温度为
,在温度为 ,
, 时,平衡体系中
时,平衡体系中 的体积分数随压强变化曲线如图所2示。则下列说法正确的是
的体积分数随压强变化曲线如图所2示。则下列说法正确的是______ 。
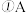 、C两点的反应速率:
、C两点的反应速率:
 、C两点气体的颜色:A深、C浅
、C两点气体的颜色:A深、C浅
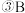 、C两点的气体的平均相对分子质量:
、C两点的气体的平均相对分子质量:
 由状态B到状态A,可以用加热的方法
由状态B到状态A,可以用加热的方法
 2CO2(g)+N2(g) △H=-a kJ/mol,在一定温度下,将
2CO2(g)+N2(g) △H=-a kJ/mol,在一定温度下,将 ,
,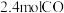 气体通入固定容积为2L的密闭容器中,发应过程中部分物质的浓度变化如图1所示
气体通入固定容积为2L的密闭容器中,发应过程中部分物质的浓度变化如图1所示 计算结果保留三位有效数字
计算结果保留三位有效数字 。
。

(1)
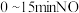 的平均速率
的平均速率
(2)15 min后反应达到平衡,若将此时得到的
 气体用含有
气体用含有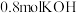 的溶液吸收,则电解质溶液中各种离子的物质的量浓度由大到小的顺序是
的溶液吸收,则电解质溶液中各种离子的物质的量浓度由大到小的顺序是(3)20 min时,若改变某一反应条件,导致CO浓度增大,则改变的条件可能是
 填序号
填序号 。
。 缩小容器体积
缩小容器体积  扩大容器体积
扩大容器体积  增加 NO的量
增加 NO的量 降低温度
降低温度  增加CO的量
增加CO的量  使用催化剂
使用催化剂(4)若保持反应体系的温度不变,20min时再向容器中充入CO、
 各
各 ,化学平衡将
,化学平衡将 填“向左”、“向右”或“不”
填“向左”、“向右”或“不” 移动,重新达到平衡后,该反应的化学平衡常数为
移动,重新达到平衡后,该反应的化学平衡常数为(5)对于反应
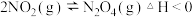 ,在温度为
,在温度为 ,
, 时,平衡体系中
时,平衡体系中 的体积分数随压强变化曲线如图所2示。则下列说法正确的是
的体积分数随压强变化曲线如图所2示。则下列说法正确的是 、C两点的反应速率:
、C两点的反应速率:
 、C两点气体的颜色:A深、C浅
、C两点气体的颜色:A深、C浅 、C两点的气体的平均相对分子质量:
、C两点的气体的平均相对分子质量:
 由状态B到状态A,可以用加热的方法
由状态B到状态A,可以用加热的方法
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氨催化氧化是硝酸工业的基础,氨气在Pt催化剂作用下发生主反应I和副反应II:
I.4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g) ∆H1=-905 kJ/mol
II.4NH3(g)+3O2(g)⇌2N2(g)+6H2O(g) ∆H2=-1265KJ/mol
(1)2NO(g)⇌N2(g) + O2(g) ∆H3=____ 。
(2)以Pt为催化剂,在1L密闭容器中充入1mol NH3和2mol O2, 测得有关物质的量与温度的关系如图:
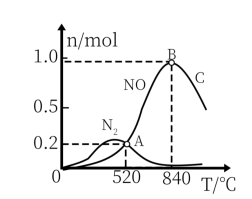
①该催化剂在高温时对反应___ 更有利(填“I”或“II”)。
②520℃时,NH3的转化率为___ 。(提示:多平衡问题一定以多平衡后最终结果计算)
③520℃时,反应II的平衡常数K=___ (写出平衡常数数字表达式,不用计算结果)。
④下列说法正确的是__ (填标号)。
A.工业上氨催化氧化生成NO时,最佳温度应控制在840℃左右
B.增大NH3与O2的初始投料比,可以提高NH3生成NO的平衡转化率
C.投料比不变,增加反应物的浓度,可以提高NH3生成NO的平衡转化率
D.使用催化剂时,可降低反应的活化能,加快其反应速率
⑤温度高于840℃时,NO的物质的量减少的原因可能是___ (回答任意一条)
(3)在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2。
①NH3与NO2生成N2的反应中,当生成1mol N2时,转移的电子数用分数表示为___ mol。
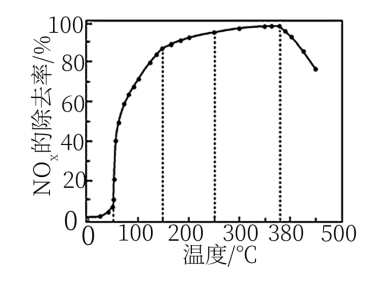
②将一定比例的O2、NH3和NOx的混合气体,匀速通入装有催化剂的反应器中反应。反应相同时间NOx的去除率随反应温度的变化曲线如下图所示,在50-250℃范围内随着温度的升高,NOx的去除率先迅速上升后上升缓慢,先迅速上升的主要原因是___ 。
I.4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g) ∆H1=-905 kJ/mol
II.4NH3(g)+3O2(g)⇌2N2(g)+6H2O(g) ∆H2=-1265KJ/mol
(1)2NO(g)⇌N2(g) + O2(g) ∆H3=
(2)以Pt为催化剂,在1L密闭容器中充入1mol NH3和2mol O2, 测得有关物质的量与温度的关系如图:

①该催化剂在高温时对反应
②520℃时,NH3的转化率为
③520℃时,反应II的平衡常数K=
④下列说法正确的是
A.工业上氨催化氧化生成NO时,最佳温度应控制在840℃左右
B.增大NH3与O2的初始投料比,可以提高NH3生成NO的平衡转化率
C.投料比不变,增加反应物的浓度,可以提高NH3生成NO的平衡转化率
D.使用催化剂时,可降低反应的活化能,加快其反应速率
⑤温度高于840℃时,NO的物质的量减少的原因可能是
(3)在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2。
①NH3与NO2生成N2的反应中,当生成1mol N2时,转移的电子数用分数表示为
②将一定比例的O2、NH3和NOx的混合气体,匀速通入装有催化剂的反应器中反应。反应相同时间NOx的去除率随反应温度的变化曲线如下图所示,在50-250℃范围内随着温度的升高,NOx的去除率先迅速上升后上升缓慢,先迅速上升的主要原因是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】基本知识填空
(1)在一定条件下,当一个可逆反应的_____ 与____ 相等时,反应物的浓度与生成物的浓度不再改变,即达到化学平衡状态。
(2)化学平衡状态的特征:_____ 、____ 、_____ 、_____ 、_____ 。
(3)对于可逆化学反应 mA+nB⇋pC+qD在一定温度下达到化学平衡时,其平衡常数表达式为:______ 。
(4)强电解质包括的范围:____ 、____ 、____ 。弱电解质包括的范围:____ 、_____ 、____ 、_____ 。
(1)在一定条件下,当一个可逆反应的
(2)化学平衡状态的特征:
(3)对于可逆化学反应 mA+nB⇋pC+qD在一定温度下达到化学平衡时,其平衡常数表达式为:
(4)强电解质包括的范围:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】I.已知2A2(g)+B2(g) 2C(g) ΔH=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为w mol/L,放出热量b kJ。
2C(g) ΔH=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为w mol/L,放出热量b kJ。
(1)a________ b(填“>”“=”或“<”)。
(2)若将反应温度升高到700 ℃,该反应的平衡常数将________ (填“增大”“减小”或“不变”)。
(3)若在原来的容器中,只加入2 mol C,500 ℃时充分反应达到平衡后, C的浓度________ w mol/L(填“>”“=”或“<”)
(4)使该反应的反应速率增大,且平衡向正反应方向移动的操作是________ 。
a.及时分离出C气体 b.适当升高温度
c.增大B2的浓度 d.选择高效的催化剂
II.氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+ 2N2(g) Si3N4(s)+ 6CO(g) △H>0 。
Si3N4(s)+ 6CO(g) △H>0 。
(1)该反应的平衡常数表达式为__________ 。
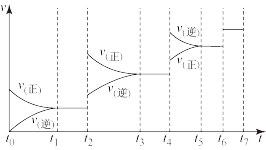
(2)达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率 与时间t的关系如下图。图中t3时引起平衡移动的条件可以是
与时间t的关系如下图。图中t3时引起平衡移动的条件可以是____________________ ;t4时引起平衡移动的条件可以是____________________ ;图中表示平衡混合物中CO的含量最高的一段时间是_________ 。
 2C(g) ΔH=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为w mol/L,放出热量b kJ。
2C(g) ΔH=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为w mol/L,放出热量b kJ。(1)a
(2)若将反应温度升高到700 ℃,该反应的平衡常数将
(3)若在原来的容器中,只加入2 mol C,500 ℃时充分反应达到平衡后, C的浓度
(4)使该反应的反应速率增大,且平衡向正反应方向移动的操作是
a.及时分离出C气体 b.适当升高温度
c.增大B2的浓度 d.选择高效的催化剂
II.氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+ 2N2(g)
 Si3N4(s)+ 6CO(g) △H>0 。
Si3N4(s)+ 6CO(g) △H>0 。(1)该反应的平衡常数表达式为
(2)达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率
 与时间t的关系如下图。图中t3时引起平衡移动的条件可以是
与时间t的关系如下图。图中t3时引起平衡移动的条件可以是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】煤气中主要的含硫杂质有H2S以及COS(有机硫),煤气燃烧后含硫杂质会转化成SO2从而引起大气污染。煤气中H2S的脱除程度已成为其洁净度的一个重要指标。回答下列问题:
(1)将H2S通入FeCl3溶液中,该反应的还原产物为___________ 。
(2)脱除煤气中COS的方法有Br2的KOH溶液氧化法、H2还原法以及水解法等。
①COS的分子结构与CO2相似,COS的电子式为_____________ 。
②Br2的KOH溶液将COS氧化为硫酸盐和碳酸盐的离子方程式为_____________ 。
③已知断裂1mol化学键所需的能量如下:
H2还原COS发生的反应为H2(g)+COS(g) ═H2S(g)+CO(g),该反应的ΔH=________ kJ·mol-1。
④用活性α—Al2O3催化COS水解的反应为COS(g)+ H2 O(g) CO2(g)+ H2S (g) ΔH<0,相同投料比、相同流量且在催化剂表面停留相同时间时,不同温度下COS的转化率(未达到平衡)如图1所示;某温度下,COS的平衡转化率与
CO2(g)+ H2S (g) ΔH<0,相同投料比、相同流量且在催化剂表面停留相同时间时,不同温度下COS的转化率(未达到平衡)如图1所示;某温度下,COS的平衡转化率与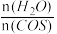 的关系如图2所示。
的关系如图2所示。
由图1可知,催化剂活性最大时对应的温度约为____________ ;由图2可知,P点时平衡常数K=_____
(保留2位有效数字)。
(3)常温下可发生反应:ZnS(s)+2H+(aq) Zn2+(aq)+H2S(aq),达到平衡时,该反应的平衡常数K=
Zn2+(aq)+H2S(aq),达到平衡时,该反应的平衡常数K=_______ [已知:Ksp(ZnS)=2.93×10-25;H2S电离常数;Ka1=9.5×10-8,Ka2=1.3×10-14]。
(1)将H2S通入FeCl3溶液中,该反应的还原产物为
(2)脱除煤气中COS的方法有Br2的KOH溶液氧化法、H2还原法以及水解法等。
①COS的分子结构与CO2相似,COS的电子式为
②Br2的KOH溶液将COS氧化为硫酸盐和碳酸盐的离子方程式为
③已知断裂1mol化学键所需的能量如下:
| 化学键 | H—H | C═O | C═S | H—S | C≡O |
| E/kJ•mol-1 | 436 | 745 | 577 | 339 | 1072 |
H2还原COS发生的反应为H2(g)+COS(g) ═H2S(g)+CO(g),该反应的ΔH=
④用活性α—Al2O3催化COS水解的反应为COS(g)+ H2 O(g)
 CO2(g)+ H2S (g) ΔH<0,相同投料比、相同流量且在催化剂表面停留相同时间时,不同温度下COS的转化率(未达到平衡)如图1所示;某温度下,COS的平衡转化率与
CO2(g)+ H2S (g) ΔH<0,相同投料比、相同流量且在催化剂表面停留相同时间时,不同温度下COS的转化率(未达到平衡)如图1所示;某温度下,COS的平衡转化率与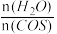 的关系如图2所示。
的关系如图2所示。

由图1可知,催化剂活性最大时对应的温度约为
(保留2位有效数字)。
(3)常温下可发生反应:ZnS(s)+2H+(aq)
 Zn2+(aq)+H2S(aq),达到平衡时,该反应的平衡常数K=
Zn2+(aq)+H2S(aq),达到平衡时,该反应的平衡常数K=
您最近一年使用:0次

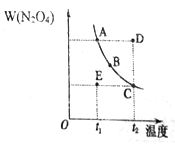
 N2O4(g) 的反应体系,在压强一定时,平衡体系中N2O4的质量分数w(N2O4) 随温度的变化情况如图所示(实线上的任何一点为对应温度下的平衡状态)。
N2O4(g) 的反应体系,在压强一定时,平衡体系中N2O4的质量分数w(N2O4) 随温度的变化情况如图所示(实线上的任何一点为对应温度下的平衡状态)。