I.已知2A2(g)+B2(g) 2C(g) ΔH=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为w mol/L,放出热量b kJ。
2C(g) ΔH=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为w mol/L,放出热量b kJ。
(1)a________ b(填“>”“=”或“<”)。
(2)若将反应温度升高到700 ℃,该反应的平衡常数将________ (填“增大”“减小”或“不变”)。
(3)若在原来的容器中,只加入2 mol C,500 ℃时充分反应达到平衡后, C的浓度________ w mol/L(填“>”“=”或“<”)
(4)使该反应的反应速率增大,且平衡向正反应方向移动的操作是________ 。
a.及时分离出C气体 b.适当升高温度
c.增大B2的浓度 d.选择高效的催化剂
II.氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+ 2N2(g) Si3N4(s)+ 6CO(g) △H>0 。
Si3N4(s)+ 6CO(g) △H>0 。
(1)该反应的平衡常数表达式为__________ 。
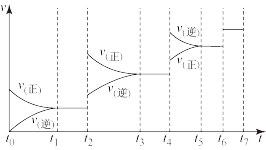
(2)达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率 与时间t的关系如下图。图中t3时引起平衡移动的条件可以是
与时间t的关系如下图。图中t3时引起平衡移动的条件可以是____________________ ;t4时引起平衡移动的条件可以是____________________ ;图中表示平衡混合物中CO的含量最高的一段时间是_________ 。
 2C(g) ΔH=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为w mol/L,放出热量b kJ。
2C(g) ΔH=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为w mol/L,放出热量b kJ。(1)a
(2)若将反应温度升高到700 ℃,该反应的平衡常数将
(3)若在原来的容器中,只加入2 mol C,500 ℃时充分反应达到平衡后, C的浓度
(4)使该反应的反应速率增大,且平衡向正反应方向移动的操作是
a.及时分离出C气体 b.适当升高温度
c.增大B2的浓度 d.选择高效的催化剂
II.氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+ 2N2(g)
 Si3N4(s)+ 6CO(g) △H>0 。
Si3N4(s)+ 6CO(g) △H>0 。(1)该反应的平衡常数表达式为
(2)达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率
 与时间t的关系如下图。图中t3时引起平衡移动的条件可以是
与时间t的关系如下图。图中t3时引起平衡移动的条件可以是
更新时间:2020-03-20 12:39:37
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】某同学在用锌与稀硫酸反应制氢气的实验中,发现加入少量硫酸铜溶液可以加快氢气的生成速率,请回答问题:
(1)上述实验中,发生反应的离子方程式是:_______________ ;________________________ 。
(2)少量硫酸铜溶液可以加快氢气的生成速率的原因是_______ 。
(3)实验室有Na2SO4、MgSO4、Ag2SO4等三种溶液,可与实验中的硫酸铜溶液起相似作用的是___________ 。
(4)为进一步研究硫酸铜的量对锌与硫酸反应生成氢气速率的影响,该同学设计了如下一系列的实验,将表中混合溶液加到6个盛有过量锌粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需要的时间:
请完成此实验设计:V2 =_________ V5=_________
(5)要加快锌与氢气的生成速率还可以采取的措施是________ (至少写两点)。
(1)上述实验中,发生反应的离子方程式是:
(2)少量硫酸铜溶液可以加快氢气的生成速率的原因是
(3)实验室有Na2SO4、MgSO4、Ag2SO4等三种溶液,可与实验中的硫酸铜溶液起相似作用的是
(4)为进一步研究硫酸铜的量对锌与硫酸反应生成氢气速率的影响,该同学设计了如下一系列的实验,将表中混合溶液加到6个盛有过量锌粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需要的时间:
| 混合溶液 | A | B | C | D | E | F |
| 4mol/LH2SO4/mL | 40 | 40 | V1 | 40 | 40 | V2 |
| 饱和CuSO4溶液/mL | 0 | 1 | 5 | V5 | V6 | 25 |
| H2O/mL | V3 | V4 | 20 | 15 | 5 | 0 |
请完成此实验设计:V2 =
(5)要加快锌与氢气的生成速率还可以采取的措施是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在恒温2L密闭容器中通入气体X并发生反应:2X(g)  Y(g) ΔH<0,X的物质的量n(x)随时间t变化的曲线如下图所示(图中两曲线分别代表有无催化剂的情形)
Y(g) ΔH<0,X的物质的量n(x)随时间t变化的曲线如下图所示(图中两曲线分别代表有无催化剂的情形)
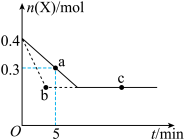
(1)下列措施不能提高反应速率的是____ 。
A 升高温度 B 加入适量X C 增大压强 D 及时分离出Y
(2)反应从开始到a点的平均反应速率可表示为v(Y)=_____ ,X的转化率为____ ;
(3)____ 线表示使用催化剂的情形(填“实”或“虚”);
(4)图中c点对应的速率关系是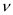 (正)
(正)____  (逆) (填“大于”“小于”或“等于”);
(逆) (填“大于”“小于”或“等于”);
(5)反应进行到a点时放出的热量_______ 反应进行到b点时放出的热量(填“大于”“小于”或“等于”)。
 Y(g) ΔH<0,X的物质的量n(x)随时间t变化的曲线如下图所示(图中两曲线分别代表有无催化剂的情形)
Y(g) ΔH<0,X的物质的量n(x)随时间t变化的曲线如下图所示(图中两曲线分别代表有无催化剂的情形)
(1)下列措施不能提高反应速率的是
A 升高温度 B 加入适量X C 增大压强 D 及时分离出Y
(2)反应从开始到a点的平均反应速率可表示为v(Y)=
(3)
(4)图中c点对应的速率关系是
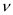 (正)
(正) (逆) (填“大于”“小于”或“等于”);
(逆) (填“大于”“小于”或“等于”);(5)反应进行到a点时放出的热量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I. 800℃时在2L密闭容器内反应:2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
(1)达平衡时NO的转化率_________________ 。
(2)下图中表示NO2的变化的曲线是________ ,用O2表示从0~2s内该反应的平均速率v(O2)=____________ 。

(3)能增大该反应的反应速率的是___________________ 。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)下图中表示NO2的变化的曲线是

(3)能增大该反应的反应速率的是
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在一定条件下,
 的可逆反应达到平衡,当分别改变下列条件时,
的可逆反应达到平衡,当分别改变下列条件时, 百分含量与原百分含量的比较情况(填“增大”、“减小”或“不变”)。
百分含量与原百分含量的比较情况(填“增大”、“减小”或“不变”)。
(1)保持容器容积不变,通入一定量 ,则达到平衡时
,则达到平衡时 百分含量
百分含量________ ;保持容器容积不变,通入一定量 ,则达到平衡时
,则达到平衡时 百分含量
百分含量________________ 。
(2)保持压强不变,通入一定量 则达到平衡时
则达到平衡时 百分含量
百分含量________ ;保持压强不变,通入一定量 ,则达到平衡时
,则达到平衡时 百分含量
百分含量____________ 。
(3)保持容器容积不变,通入一定量氖气,则达到平衡时 转化率
转化率________ ;保持压强不变,通入氖气使体系的容积增大一倍,则达到平衡时 转化率
转化率___________ 。

 的可逆反应达到平衡,当分别改变下列条件时,
的可逆反应达到平衡,当分别改变下列条件时, 百分含量与原百分含量的比较情况(填“增大”、“减小”或“不变”)。
百分含量与原百分含量的比较情况(填“增大”、“减小”或“不变”)。(1)保持容器容积不变,通入一定量
 ,则达到平衡时
,则达到平衡时 百分含量
百分含量 ,则达到平衡时
,则达到平衡时 百分含量
百分含量(2)保持压强不变,通入一定量
 则达到平衡时
则达到平衡时 百分含量
百分含量 ,则达到平衡时
,则达到平衡时 百分含量
百分含量(3)保持容器容积不变,通入一定量氖气,则达到平衡时
 转化率
转化率 转化率
转化率
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】检验Fe3+的存在,可向溶液中加入KSCN溶液,发生反应如下:FeCl3(棕黄色)+3KSCN(无色) 3KCl(无色)+Fe(SCN)3(红色),能使该可逆反应发生平衡移动的是
3KCl(无色)+Fe(SCN)3(红色),能使该可逆反应发生平衡移动的是_____ 。
①加入KCl固体 ②加入Fe粉 ③加入FeCl3固体
若有不能使平衡发生移动的,请解释原因_____ 。
 3KCl(无色)+Fe(SCN)3(红色),能使该可逆反应发生平衡移动的是
3KCl(无色)+Fe(SCN)3(红色),能使该可逆反应发生平衡移动的是①加入KCl固体 ②加入Fe粉 ③加入FeCl3固体
若有不能使平衡发生移动的,请解释原因
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)若反应2NO(g)+O2(g) 2NO2的平衡常数为K1,2NO2(g)
2NO2的平衡常数为K1,2NO2(g) N2O4(g)的平衡常数为K2,则反应2NO(g)+O2(g)
N2O4(g)的平衡常数为K2,则反应2NO(g)+O2(g) N2O4(g)的平衡常数K=
N2O4(g)的平衡常数K=___ 。
(2)25℃、101KPa时,1kg乙醇充分燃烧后放出的热量为29714kJ,则乙醇的燃烧热△H=__ 。
(3)反应mA+nB pC在某温度下达到平衡。
pC在某温度下达到平衡。
①若A、B、C都是气体,减压后正反应速率小于逆反应速率,则m、n、p的关是___ 。
②若C为气体,且m+n=p,在加压时化学平衡发生移动,则平衡必定向___ 方向移动。
③如果在体系中增加或减少B的量,平衡均不发生移动,则B肯定不能为__ 态。
 2NO2的平衡常数为K1,2NO2(g)
2NO2的平衡常数为K1,2NO2(g) N2O4(g)的平衡常数为K2,则反应2NO(g)+O2(g)
N2O4(g)的平衡常数为K2,则反应2NO(g)+O2(g) N2O4(g)的平衡常数K=
N2O4(g)的平衡常数K=(2)25℃、101KPa时,1kg乙醇充分燃烧后放出的热量为29714kJ,则乙醇的燃烧热△H=
(3)反应mA+nB
 pC在某温度下达到平衡。
pC在某温度下达到平衡。①若A、B、C都是气体,减压后正反应速率小于逆反应速率,则m、n、p的关是
②若C为气体,且m+n=p,在加压时化学平衡发生移动,则平衡必定向
③如果在体系中增加或减少B的量,平衡均不发生移动,则B肯定不能为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】已知2SO2(g)+O2(g) 2SO3(g),下图为不同温度(T1、T2)下SO2的转化率随时间的变化曲线。
2SO3(g),下图为不同温度(T1、T2)下SO2的转化率随时间的变化曲线。
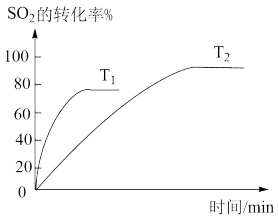
(1)T1___________ (选填“>”“<”或“=”)T2,判断依据是___________ ;该反应为___________ (选填“放”或“吸”)热反应,判断依据是___________ 。
(2)在相同温度下:2NO(g)+O2(g) 2NO2(g) K1=a;
2NO2(g) K1=a;
NO2(g)+SO2(g) SO3(g)+NO(g) K2=b;
SO3(g)+NO(g) K2=b;
则2SO2(g)+O2(g) 2SO3(g)的平衡常数K=
2SO3(g)的平衡常数K=___________ (用a、b表示)。
 2SO3(g),下图为不同温度(T1、T2)下SO2的转化率随时间的变化曲线。
2SO3(g),下图为不同温度(T1、T2)下SO2的转化率随时间的变化曲线。
(1)T1
(2)在相同温度下:2NO(g)+O2(g)
 2NO2(g) K1=a;
2NO2(g) K1=a;NO2(g)+SO2(g)
 SO3(g)+NO(g) K2=b;
SO3(g)+NO(g) K2=b;则2SO2(g)+O2(g)
 2SO3(g)的平衡常数K=
2SO3(g)的平衡常数K=
您最近一年使用:0次
【推荐2】已知2X2(g)+Y2(g) 2Z(g) ΔH1=-akJ·mol-1(a>0),在一个容积固定的容器中加入2molX2和lmolY2,在500℃时充分反应达平衡后Z的浓度为Wmol·L-1,放出热量bkJ。
2Z(g) ΔH1=-akJ·mol-1(a>0),在一个容积固定的容器中加入2molX2和lmolY2,在500℃时充分反应达平衡后Z的浓度为Wmol·L-1,放出热量bkJ。
(1)此反应平衡常数表达式为___ ;若将温度降低到300℃,则反应平衡常数将___ (填增大、减少或不变)。
(2)能说明反应已达平衡状态的是___
A.浓度c(Z)=2c(Y2) B.容器内压强保持不变
C.v逆(X2)=2v正(Y2) D.容器内的密度保持不变
(3)若将上述容器改为恒压容器 反应器开始体积相同
反应器开始体积相同 ,相同温度下起始加入2molX2和lmolY2达到平衡后,Y2的转化率将
,相同温度下起始加入2molX2和lmolY2达到平衡后,Y2的转化率将____ (填变大、变小或不变)。
 2Z(g) ΔH1=-akJ·mol-1(a>0),在一个容积固定的容器中加入2molX2和lmolY2,在500℃时充分反应达平衡后Z的浓度为Wmol·L-1,放出热量bkJ。
2Z(g) ΔH1=-akJ·mol-1(a>0),在一个容积固定的容器中加入2molX2和lmolY2,在500℃时充分反应达平衡后Z的浓度为Wmol·L-1,放出热量bkJ。(1)此反应平衡常数表达式为
(2)能说明反应已达平衡状态的是
A.浓度c(Z)=2c(Y2) B.容器内压强保持不变
C.v逆(X2)=2v正(Y2) D.容器内的密度保持不变
(3)若将上述容器改为恒压容器
 反应器开始体积相同
反应器开始体积相同 ,相同温度下起始加入2molX2和lmolY2达到平衡后,Y2的转化率将
,相同温度下起始加入2molX2和lmolY2达到平衡后,Y2的转化率将
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】CO还原脱硝技术可有效降低烟气中的NOx的排放量。
(1)汽车在行驶过程中会产生有害气体CO、NO,在催化剂作用下发生如下脱硝反应: ,该反应平衡常数的表达式K=
,该反应平衡常数的表达式K=______________ ,在570 K时,K值极大,为1×1059,但汽车上仍需装备尾气处理装置,其可能原因是________________ 。
(2)以Mn3O4为脱硝反应的催化剂,研究者提出如下反应历程,将历程补充完整。
第一步:___________________________________ ;
第二步:
(3)T℃、2L密闭容器中,充入各1mol的CO和NO混合气体,加入Mn3O4发生脱硝反应,t0 时达到平衡,测得反应过程中CO2的体积分数与时间的关系如下图所示:

①比较大小:a处v正______ b处v逆(填“>”、“<”或“=”)
②若t0 =10min,反应从开始到达平衡CO气体的平均反应速率v( CO) =_____ 。
③NO的平衡转化率为______ ,T℃时反应的化学平衡常数K=_________ 。
④T℃时,某时刻测得体系中各物质的量如下:n(CO)=0.2mol,n(NO)=0.2mol,n(N2)=0.1mol,n(CO2)=0.2mol,则此时该反应_______ 进行(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)。
(1)汽车在行驶过程中会产生有害气体CO、NO,在催化剂作用下发生如下脱硝反应:
 ,该反应平衡常数的表达式K=
,该反应平衡常数的表达式K=(2)以Mn3O4为脱硝反应的催化剂,研究者提出如下反应历程,将历程补充完整。
第一步:
第二步:

(3)T℃、2L密闭容器中,充入各1mol的CO和NO混合气体,加入Mn3O4发生脱硝反应,t0 时达到平衡,测得反应过程中CO2的体积分数与时间的关系如下图所示:

①比较大小:a处v正
②若t0 =10min,反应从开始到达平衡CO气体的平均反应速率v( CO) =
③NO的平衡转化率为
④T℃时,某时刻测得体系中各物质的量如下:n(CO)=0.2mol,n(NO)=0.2mol,n(N2)=0.1mol,n(CO2)=0.2mol,则此时该反应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】在一固定容积的密闭容器中,充入2 mol CO2和1 mol H2发生如下化学反应:CO2(g)+H2(g)⇌CO(g)+H2O(g),其化学平衡常数与温度(T)的关系如表:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=__________ 。
(2)若反应在830℃下达到平衡,则CO2气体的转化率为_________ 。
(3)若绝热时(容器内外没有热量交换),平衡发生移动的结果是使容器内CO的浓度增大,则容器内气体温度_________ (填“升高”、“降低”或“不能确定”)。
(4)在830℃达平衡后在其容器中分别又充入1 mol CO2 和1 molCO后,该反应的v正__ v逆(填“大于”“小于”“等于”)。
| T/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=
(2)若反应在830℃下达到平衡,则CO2气体的转化率为
(3)若绝热时(容器内外没有热量交换),平衡发生移动的结果是使容器内CO的浓度增大,则容器内气体温度
(4)在830℃达平衡后在其容器中分别又充入1 mol CO2 和1 molCO后,该反应的v正
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】I.一密封体系中发生下列反应:N2+3H2 2NH3 ΔH<0,下图是某一时间段中反应速率与反应进程的曲线关系图:
2NH3 ΔH<0,下图是某一时间段中反应速率与反应进程的曲线关系图:
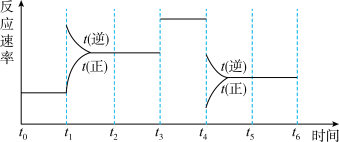
回答下列问题:
(1)处于平衡状态的时间段是___________ 、___________ 、___________ 。
(2)t1、t3、t4时刻体系中分别是什么条件发生了变化:____________ 、___________ 、___________ 。
(3)下列各时间段时,氨的百分含量最高的是___________ (填序号)。
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6
II.830K时,在密闭容器中发生下列可逆反应:CO(g)+H2O(g) CO2(g)+H2(g)△H<0。试回答下列问题:
CO2(g)+H2(g)△H<0。试回答下列问题:
(4)若起始时c(CO)=2 mol·L-1,c(H2O)=3 mol·L-1,达到平衡时CO的转化率为60%,则在该温度下,该反应的平衡常数K=____________ 。
(5)在相同温度下,若起始时c(CO)=1mol·L-1,c(H2O)=2mol·L-1,反应进行一段时间后,测得H2的浓度为0.5mol·L-1,则此时该反应是否达到平衡状态______ (填“是”与“否”),此时v(正)____ v(逆)(填“大于”“小于”或“等于”)。
 2NH3 ΔH<0,下图是某一时间段中反应速率与反应进程的曲线关系图:
2NH3 ΔH<0,下图是某一时间段中反应速率与反应进程的曲线关系图:
回答下列问题:
(1)处于平衡状态的时间段是
(2)t1、t3、t4时刻体系中分别是什么条件发生了变化:
(3)下列各时间段时,氨的百分含量最高的是
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6
II.830K时,在密闭容器中发生下列可逆反应:CO(g)+H2O(g)
 CO2(g)+H2(g)△H<0。试回答下列问题:
CO2(g)+H2(g)△H<0。试回答下列问题:(4)若起始时c(CO)=2 mol·L-1,c(H2O)=3 mol·L-1,达到平衡时CO的转化率为60%,则在该温度下,该反应的平衡常数K=
(5)在相同温度下,若起始时c(CO)=1mol·L-1,c(H2O)=2mol·L-1,反应进行一段时间后,测得H2的浓度为0.5mol·L-1,则此时该反应是否达到平衡状态
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】一定条件下,水气变换反应CO+H2O⇌CO2+H2的中间产物是HCOOH。为探究该反应过程,研究 水溶液在密封石英管中的分子反应:
水溶液在密封石英管中的分子反应:
I.HCOOH⇌CO+H2O (快)
Ⅱ.HCOOH⇌CO2+H2 (慢)
(1) 温度下,在密封石英管内完全充满1.0mol·L-1HCOOH水溶液,使
温度下,在密封石英管内完全充满1.0mol·L-1HCOOH水溶液,使 分解,分解产物均完全溶于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。
分解,分解产物均完全溶于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。 时刻测得CO、CO2的浓度分别为0.70mol·L-1、0.16mol·L-1,反应Ⅱ达平衡时,测得H2的浓度为ymol·L-1。体系达平衡后
时刻测得CO、CO2的浓度分别为0.70mol·L-1、0.16mol·L-1,反应Ⅱ达平衡时,测得H2的浓度为ymol·L-1。体系达平衡后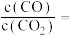
_______ (用含y的代数式表示,下同),反应Ⅱ的平衡常数为_______ 。
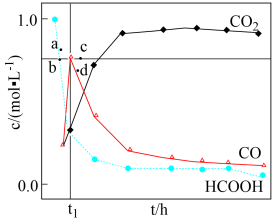
(2)相同条件下,若反应起始时溶液中同时还含有0.10mol·L-1盐酸,则图示点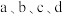 中,CO的浓度峰值点可能是
中,CO的浓度峰值点可能是_______ (填标号)。与不同盐酸相比,CO达浓度峰值时,CO2浓度_______ (填“增大”“减小”或“不变”), 的反应
的反应_______ (填“增大”“减小”或“不变”)。
 水溶液在密封石英管中的分子反应:
水溶液在密封石英管中的分子反应:I.HCOOH⇌CO+H2O (快)
Ⅱ.HCOOH⇌CO2+H2 (慢)
(1)
 温度下,在密封石英管内完全充满1.0mol·L-1HCOOH水溶液,使
温度下,在密封石英管内完全充满1.0mol·L-1HCOOH水溶液,使 分解,分解产物均完全溶于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。
分解,分解产物均完全溶于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。 时刻测得CO、CO2的浓度分别为0.70mol·L-1、0.16mol·L-1,反应Ⅱ达平衡时,测得H2的浓度为ymol·L-1。体系达平衡后
时刻测得CO、CO2的浓度分别为0.70mol·L-1、0.16mol·L-1,反应Ⅱ达平衡时,测得H2的浓度为ymol·L-1。体系达平衡后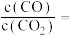

(2)相同条件下,若反应起始时溶液中同时还含有0.10mol·L-1盐酸,则图示点
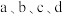 中,CO的浓度峰值点可能是
中,CO的浓度峰值点可能是 的反应
的反应
您最近一年使用:0次



