次鳞酸 )是一种精细化工产品。
)是一种精细化工产品。
(1) 溶液中的含鳞微粒只有
溶液中的含鳞微粒只有 和
和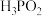 ,则该溶液量
,则该溶液量_______ 性(填“酸”“碱”或“中”),原因是_______ (用离子方程式解释); 为
为_______ (填“正盐”或“酸式盐”),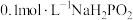 溶液中离子浓度由大到小的顺序为
溶液中离子浓度由大到小的顺序为_______ 。
(2) 时,将相同物质的量浓度的
时,将相同物质的量浓度的 溶液和盐酸分别加水稀释至相同的倍数,此时
溶液和盐酸分别加水稀释至相同的倍数,此时 溶液的
溶液的
_______ (填“大于”“小于”或“等于”)盐酸的 。
。
(3)常温下, 溶液中
溶液中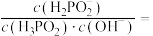
_______ [用含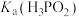 和
和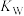 的代数式表示]。
的代数式表示]。
 )是一种精细化工产品。
)是一种精细化工产品。(1)
 溶液中的含鳞微粒只有
溶液中的含鳞微粒只有 和
和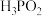 ,则该溶液量
,则该溶液量 为
为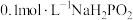 溶液中离子浓度由大到小的顺序为
溶液中离子浓度由大到小的顺序为(2)
 时,将相同物质的量浓度的
时,将相同物质的量浓度的 溶液和盐酸分别加水稀释至相同的倍数,此时
溶液和盐酸分别加水稀释至相同的倍数,此时 溶液的
溶液的
 。
。(3)常温下,
 溶液中
溶液中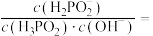
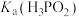 和
和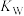 的代数式表示]。
的代数式表示]。
更新时间:2022-09-02 16:29:32
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某学习小组用0.1000mol/LNaOH标准溶液来测定未知物质的量浓度的盐酸时,选择酚酞作指示剂。请回答下列问题:
(1)若滴定开始和结束时,该仪器中溶液读数如图所示,所用NaOH标准溶液的体积为_______ mL。
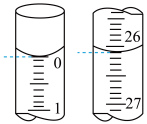
(2)某学生根据3次实验分别记录有关数据如表所示:
依据表中数据计算该盐酸的物质的量浓度为_______ mol/L。
(3)下列操作会使所测结果偏高的是_______ (填字母)。
A.滴定前用蒸馏水冲洗锥形瓶
B.滴定过程中振荡锥形瓶时不慎将瓶内溶液溅出
C.滴定过程中不慎将数滴碱液滴在锥形瓶外
D.碱式滴定管在滴定前有气泡,滴定后气泡消失
E.读取NaOH体积时,开始仰视读数,滴定结束时俯视读数
(4)用0.1mol/LNaOH溶液分别滴定体积均为20.00mL、浓度均为0.1mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。
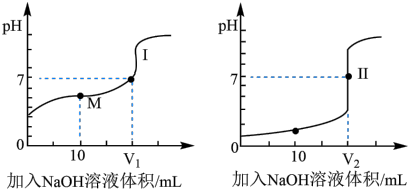
①滴定醋酸的曲线是_______ (填“Ⅰ”或“Ⅱ”)。
②V1和V2的关系:V1_______ V2(填“>”、“=”或“<”)。
③M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是_______ 。
(5)氧化还原滴定法是氧化还原反应为基础的一种滴定分析方法,某同学用0.1000mol/L的酸性KMnO4标准溶液滴定某试样中过氧化氢的含量。
①反应原理为(用离子方程式表示):_______ 。
②到达滴定终点时的现象为_______ 。
(1)若滴定开始和结束时,该仪器中溶液读数如图所示,所用NaOH标准溶液的体积为

(2)某学生根据3次实验分别记录有关数据如表所示:
| 滴定次数 | 待测盐酸的体积/mL | 标准NaOH溶液体积 | |
| 滴定前的刻度/mL | 滴定后的刻度/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 |
| 第三次 | 25.00 | 0.22 | 26.31 |
(3)下列操作会使所测结果偏高的是
A.滴定前用蒸馏水冲洗锥形瓶
B.滴定过程中振荡锥形瓶时不慎将瓶内溶液溅出
C.滴定过程中不慎将数滴碱液滴在锥形瓶外
D.碱式滴定管在滴定前有气泡,滴定后气泡消失
E.读取NaOH体积时,开始仰视读数,滴定结束时俯视读数
(4)用0.1mol/LNaOH溶液分别滴定体积均为20.00mL、浓度均为0.1mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。

①滴定醋酸的曲线是
②V1和V2的关系:V1
③M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是
(5)氧化还原滴定法是氧化还原反应为基础的一种滴定分析方法,某同学用0.1000mol/L的酸性KMnO4标准溶液滴定某试样中过氧化氢的含量。
①反应原理为(用离子方程式表示):
②到达滴定终点时的现象为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ. 溶液与
溶液与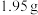 锌粉在量热计中充分反应。测得反应前温度为20.1℃,反应后最高温度为30.1℃。已知:反应前后,溶液的比热容均近似为
锌粉在量热计中充分反应。测得反应前温度为20.1℃,反应后最高温度为30.1℃。已知:反应前后,溶液的比热容均近似为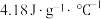 、溶液的密度均近似为
、溶液的密度均近似为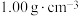 ,忽略溶液体积、质量变化和金属吸收的热量。请计算:
,忽略溶液体积、质量变化和金属吸收的热量。请计算:
(1)反应放出的热量Q=_______  。
。
(2)反应 的
的
_______  。
。
(3)可以证明乙酸是弱酸的事实是_______(填序号)
(4)有下列物质的溶液:a. b.
b. c.
c. d.
d. 。若四种溶液的物质的量浓度相同,其
。若四种溶液的物质的量浓度相同,其 由大到小顺序为
由大到小顺序为_______ (用字母序号表示,下同)。若四种溶液的 相同,其物质的量浓度由大到小顺序为
相同,其物质的量浓度由大到小顺序为_______ 。
(5)常温下,有 相同、体积相同的醋酸和盐酸两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
相同、体积相同的醋酸和盐酸两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是_______ (填字母)。(①表示盐酸,②表示醋酸)

Ⅱ.纯过氧化氢( )是淡蓝色的黏稠液体,可与水以任意比混合,水溶液俗称双氧水,为无色透明液体,用途广泛。回答下列问题:
)是淡蓝色的黏稠液体,可与水以任意比混合,水溶液俗称双氧水,为无色透明液体,用途广泛。回答下列问题:
(6)该兴趣小组的同学查阅资料后发现 为二元弱酸,其酸性比碳酸弱。写出
为二元弱酸,其酸性比碳酸弱。写出 在水溶液中的电离方程式:
在水溶液中的电离方程式:_______ 。
(7)同学们用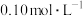 的
的 标准溶液(硫酸酸化)滴定某试样中过氧化氢的含量,反应原理为
标准溶液(硫酸酸化)滴定某试样中过氧化氢的含量,反应原理为 。
。
①在该反应中, 被
被_______ (填“氧化”或“还原”)。
②用移液管吸取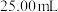 试样置于锥形瓶中,重复滴定四次,每次消耗的酸性
试样置于锥形瓶中,重复滴定四次,每次消耗的酸性 标准溶液体积如下表所示:
标准溶液体积如下表所示:
则试样中过氧化氢的浓度为_______  。
。
③若滴定前尖嘴中有气泡,滴定后消失,则测定结果_______ (填“偏低”“偏高”或“不变”)。
(8)同学们发现向滴加了酚酞的NaOH溶液中加入 后,溶液中红色消失。关于褪色原因,甲同学认为
后,溶液中红色消失。关于褪色原因,甲同学认为 是二元弱酸,消耗了
是二元弱酸,消耗了 使红色消失;乙同学认为
使红色消失;乙同学认为 具有漂白性使溶液褪色(酚酞生成了其他物质)。请设计一个简单的实验方案判断甲、乙同学的说法是否正确:
具有漂白性使溶液褪色(酚酞生成了其他物质)。请设计一个简单的实验方案判断甲、乙同学的说法是否正确:_______ 。
 溶液与
溶液与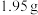 锌粉在量热计中充分反应。测得反应前温度为20.1℃,反应后最高温度为30.1℃。已知:反应前后,溶液的比热容均近似为
锌粉在量热计中充分反应。测得反应前温度为20.1℃,反应后最高温度为30.1℃。已知:反应前后,溶液的比热容均近似为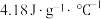 、溶液的密度均近似为
、溶液的密度均近似为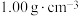 ,忽略溶液体积、质量变化和金属吸收的热量。请计算:
,忽略溶液体积、质量变化和金属吸收的热量。请计算:(1)反应放出的热量Q=
 。
。(2)反应
 的
的
 。
。(3)可以证明乙酸是弱酸的事实是_______(填序号)
| A.乙酸钠水溶液显碱性 | B.在乙酸水溶液中含有未电离的乙酸分子 |
C.乙酸与 溶液反应放出 溶液反应放出 气体 气体 | D.常温下, 的乙酸水溶液pH为3 的乙酸水溶液pH为3 |
 b.
b. c.
c. d.
d. 。若四种溶液的物质的量浓度相同,其
。若四种溶液的物质的量浓度相同,其 由大到小顺序为
由大到小顺序为 相同,其物质的量浓度由大到小顺序为
相同,其物质的量浓度由大到小顺序为(5)常温下,有
 相同、体积相同的醋酸和盐酸两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
相同、体积相同的醋酸和盐酸两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
Ⅱ.纯过氧化氢(
 )是淡蓝色的黏稠液体,可与水以任意比混合,水溶液俗称双氧水,为无色透明液体,用途广泛。回答下列问题:
)是淡蓝色的黏稠液体,可与水以任意比混合,水溶液俗称双氧水,为无色透明液体,用途广泛。回答下列问题:(6)该兴趣小组的同学查阅资料后发现
 为二元弱酸,其酸性比碳酸弱。写出
为二元弱酸,其酸性比碳酸弱。写出 在水溶液中的电离方程式:
在水溶液中的电离方程式:(7)同学们用
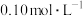 的
的 标准溶液(硫酸酸化)滴定某试样中过氧化氢的含量,反应原理为
标准溶液(硫酸酸化)滴定某试样中过氧化氢的含量,反应原理为 。
。①在该反应中,
 被
被②用移液管吸取
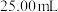 试样置于锥形瓶中,重复滴定四次,每次消耗的酸性
试样置于锥形瓶中,重复滴定四次,每次消耗的酸性 标准溶液体积如下表所示:
标准溶液体积如下表所示:| 第一次 | 第二次 | 第三次 | 第四次 | |
| 体积(mL) | 17.10 | 18.10 | 18.00 | 17.90 |
则试样中过氧化氢的浓度为
 。
。③若滴定前尖嘴中有气泡,滴定后消失,则测定结果
(8)同学们发现向滴加了酚酞的NaOH溶液中加入
 后,溶液中红色消失。关于褪色原因,甲同学认为
后,溶液中红色消失。关于褪色原因,甲同学认为 是二元弱酸,消耗了
是二元弱酸,消耗了 使红色消失;乙同学认为
使红色消失;乙同学认为 具有漂白性使溶液褪色(酚酞生成了其他物质)。请设计一个简单的实验方案判断甲、乙同学的说法是否正确:
具有漂白性使溶液褪色(酚酞生成了其他物质)。请设计一个简单的实验方案判断甲、乙同学的说法是否正确:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某探究小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验。查阅资料,有关信息如下:
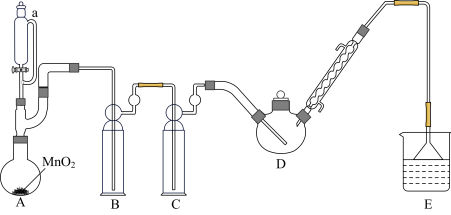
①制备反应原理:C2H5OH + 4Cl2 → CCl3CHO+5HCl
可能发生的副反应:
C2H5OH + HCl → C2H5Cl+H2O
CCl3CHO+HClO→CCl3COOH(三氯乙酸)+HCl
②相关物质的部分物理性质:
(1)仪器a中盛放的试剂是_______ ;仪器a中侧管的作用_______ ;装置B的作用是_______ 。
(2)若撤去装置C,可能导致装置D中副产物_______ (填化学式)的量增加;装置D可采用_______ 加热的方法以控制反应温度在70℃左右。
(3)装置E中可能发生的无机反应的离子方程式有_______ 。
(4)反应结束后,有人提出先将D中的混合物冷却到室温,再用过滤的方法分离出CCl3COOH。你认为此方案是否可行,为什么?_______
(5)测定产品纯度:称取产品0.30 g配成待测溶液,加入0.1000 mol·L-1碘标准溶液20.00 mL,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,立即用0.02000 mol·L-1 Na2S2O3溶液滴定至终点。进行平行实验后,测得消耗Na2S2O3溶液20.00 mL。则产品的纯度为_______ 。滴定的反应原理:CCl3CHO +OH- → CHCl3 + HCOO-、 HCOO-+ I2 =H+ + 2I- + CO2↑、 I2 + 2S2O = 2I-+ S4O
= 2I-+ S4O
(6)请设计实验证明三氯乙酸的酸性比乙酸强。_______

①制备反应原理:C2H5OH + 4Cl2 → CCl3CHO+5HCl
可能发生的副反应:
C2H5OH + HCl → C2H5Cl+H2O
CCl3CHO+HClO→CCl3COOH(三氯乙酸)+HCl
②相关物质的部分物理性质:
| C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
| 熔点/℃ | -114.1 | -57.5 | 58 | -138.7 |
| 沸点/℃ | 78.3 | 97.8 | 198 | 12.3 |
| 溶解性 | 与水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇 | 微溶于水,可溶于乙醇 |
(2)若撤去装置C,可能导致装置D中副产物
(3)装置E中可能发生的无机反应的离子方程式有
(4)反应结束后,有人提出先将D中的混合物冷却到室温,再用过滤的方法分离出CCl3COOH。你认为此方案是否可行,为什么?
(5)测定产品纯度:称取产品0.30 g配成待测溶液,加入0.1000 mol·L-1碘标准溶液20.00 mL,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,立即用0.02000 mol·L-1 Na2S2O3溶液滴定至终点。进行平行实验后,测得消耗Na2S2O3溶液20.00 mL。则产品的纯度为
 = 2I-+ S4O
= 2I-+ S4O
(6)请设计实验证明三氯乙酸的酸性比乙酸强。
您最近一年使用:0次
【推荐1】工业上用方铅矿(主要成分为PbS,含有少量FeS等杂质)和软锰矿(主要成分为 ,含有少量
,含有少量 、
、 、
、 等杂质)制备
等杂质)制备 和
和 ,工艺流程如图所示。
,工艺流程如图所示。
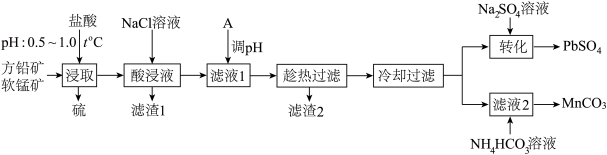
已知:① 难溶于冷水,不溶于乙醇,易溶于热水;
难溶于冷水,不溶于乙醇,易溶于热水;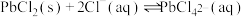
 ;
;
②部分金属离子开始沉淀和沉淀完全的pH如下表:
③25℃时,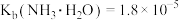 ,
,
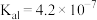 ,
, ;
;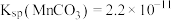 。
。
回答下列问题:
(1)为提高方铅矿的浸出率,结合下图信息,选择“浸取”的合适条件_______ 。“浸取”过程中发生的主要反应的化学方程式为_______ ,“酸浸液”中含有的金属阳离子有 、
、_______ 。
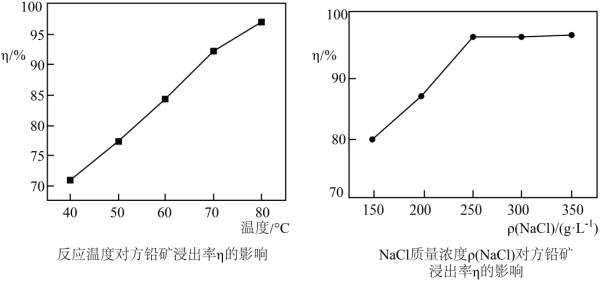
(2)加入NaCl溶液的目的是_______ ;“调pH”前检验滤液1中是否含 所用的试剂是
所用的试剂是_______ ,物质A调节pH的范围是_______ 。
(3)“滤液2”中加入的 溶液显
溶液显_______ (填“酸性”、“碱性”或“中性”),发生反应的离子方程式为_______ 。
 ,含有少量
,含有少量 、
、 、
、 等杂质)制备
等杂质)制备 和
和 ,工艺流程如图所示。
,工艺流程如图所示。
已知:①
 难溶于冷水,不溶于乙醇,易溶于热水;
难溶于冷水,不溶于乙醇,易溶于热水;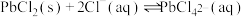
 ;
;②部分金属离子开始沉淀和沉淀完全的pH如下表:
| 金属离子 |  |  |  |  |  |
| 开始沉淀的pH | 7.0 | 1.7 | 3.7 | 7.6 | 7.0 |
| 沉淀完全的pH | 9.6 | 3.2 | 4.7 | 9.8 | 9.0 |
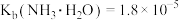 ,
,
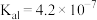 ,
, ;
;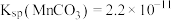 。
。回答下列问题:
(1)为提高方铅矿的浸出率,结合下图信息,选择“浸取”的合适条件
 、
、
(2)加入NaCl溶液的目的是
 所用的试剂是
所用的试剂是(3)“滤液2”中加入的
 溶液显
溶液显
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】下表数据是高三拓展教材P43页对应物质的熔点:
请根据上表中的信息回答下列问题:
(1)上述涉及到的元素中最活泼非金属原子核外电子排布式是___________ ,其核外有___________ 种不同运动状态的电子,能量最高且相同的电子有___________ 个。能形成简单离子的半径由大到小(用离子符号表示)___________ 。
(2)物质①的电子式___________ ,⑤的分子空间构型___________ ,⑧的晶体类型___________ 。
(3)④溶于水溶液呈酸性,用离子方程式表示其原因___________ ,若把其溶于加热蒸干并灼烧,得到的固体是___________ 。
(4)不能用于比较Na与Al金属性相对强弱的事实是___________。
(5)③比④熔点高出很多,其原因是:___________ 。①和②都属于离子晶体,但①比②的熔点高,请解释原因___________ 。
| 编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 物质 | Na2O | NaCl | AlF3 | AlCl3 | BCl3 | Al2O3 | CO2 | SiO2 |
| 熔点℃ | 920 | 801 | 1291 | 160 | -107 | 2072 | -57 | 1723 |
请根据上表中的信息回答下列问题:
(1)上述涉及到的元素中最活泼非金属原子核外电子排布式是
(2)物质①的电子式
(3)④溶于水溶液呈酸性,用离子方程式表示其原因
(4)不能用于比较Na与Al金属性相对强弱的事实是___________。
| A.最高价氧化物对应水化物的碱性 |
| B.Na最外层1个电子,Al最外层3个电子 |
| C.单质与H2O反应的难易程度 |
| D.比较同温浓度NaCl和AlCl3的pH值 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】I:乙二酸俗称草酸,是一种二元弱酸(结构简式为HOOC—COOH,可简写为H2C2O4),它是一种重要的化工原料。(常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如表所示)填空:
(1)KHC2O4溶液显酸性的原因是___________
(2)向0.1mol/L的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是________
A.c(K+)═ c(HC2O4-)+c(H2C2O4)+c(C2O42-)
B.c(Na+)═ c(H2C2O4)+c(C2O42-)
C.c(K+)+c(Na+)═ c(HC2O4-)+c(C2O42-)
D.c(K+)>c(Na+)
II:电离平衡常数是衡量弱电解质电离程度的量。已知如下表数据(25 ℃):
(1)25 ℃时,等浓度的三种溶液(A.NaCN溶液、B.Na2CO3溶液、C.CH3COONa溶液)的pH由大到小的顺序为______ (填写序号)
(2)25℃时,向NaCN溶液中通入少量CO2,所发生反应的离子方程式为__________ ;
(3)现有浓度为0.02 mol/L的HCN与0.01mol/L NaOH等体积混合后,测得c(Na+)>c(CN-),下列关系正确的是____ (填标号)。
A.c(H+)>c(OH-) B.c(H+)<c(OH-)
C.c(H+)+c(HCN) = c(OH-) D.c(HCN)+ c(CN-)=0.01mol/L
(4)写出NaHCO3溶液中的质子守恒式:______________________ 。
| H2C2O4 | KHC2O4 | K2C2O4 | |
| pH | 2.1 | 3.1 | 8.1 |
(1)KHC2O4溶液显酸性的原因是
(2)向0.1mol/L的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是
A.c(K+)═ c(HC2O4-)+c(H2C2O4)+c(C2O42-)
B.c(Na+)═ c(H2C2O4)+c(C2O42-)
C.c(K+)+c(Na+)═ c(HC2O4-)+c(C2O42-)
D.c(K+)>c(Na+)
II:电离平衡常数是衡量弱电解质电离程度的量。已知如下表数据(25 ℃):
| 化学式 | 电离平衡常数 |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.4×10-7,K2=4.7×10-11 |
(1)25 ℃时,等浓度的三种溶液(A.NaCN溶液、B.Na2CO3溶液、C.CH3COONa溶液)的pH由大到小的顺序为
(2)25℃时,向NaCN溶液中通入少量CO2,所发生反应的离子方程式为
(3)现有浓度为0.02 mol/L的HCN与0.01mol/L NaOH等体积混合后,测得c(Na+)>c(CN-),下列关系正确的是
A.c(H+)>c(OH-) B.c(H+)<c(OH-)
C.c(H+)+c(HCN) = c(OH-) D.c(HCN)+ c(CN-)=0.01mol/L
(4)写出NaHCO3溶液中的质子守恒式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。 时,部分物质的相关平衡常数如表所示,按要求回答下列问题:
时,部分物质的相关平衡常数如表所示,按要求回答下列问题:
(1)相同温度下,相等物质的量浓度溶液中,判断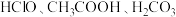 的酸性由强到弱的顺序为
的酸性由强到弱的顺序为_______ 。
(2)将少量 气体通入
气体通入 溶液中,发生的离子方程式为
溶液中,发生的离子方程式为_______ 。
(3)相同温度下,判断 溶液显
溶液显_______ (填“酸性”、“中性”、“碱性”),物质的量浓度相等的下列溶液① ②
② ③
③ ④
④ ,溶液中的
,溶液中的 浓度由大到小的顺序为
浓度由大到小的顺序为_______ (用序号表示)。
(4)下列事实可以证明 是弱碱的有
是弱碱的有_______ (填序号)。
①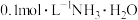 溶液能使酚酞溶液变红
溶液能使酚酞溶液变红
②常温下,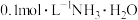 溶液的
溶液的
③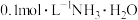 溶液的导电性比
溶液的导电性比 溶液弱
溶液弱
④等体积的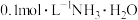 溶液与
溶液与 溶液恰好完全反应
溶液恰好完全反应
⑤ 的
的 溶液稀释至100倍,
溶液稀释至100倍, 约为10
约为10
(5) 的
的 溶液与
溶液与 的
的 溶液等体积混合后,溶液中四种离子物质的量浓度由大到小的顺序为
溶液等体积混合后,溶液中四种离子物质的量浓度由大到小的顺序为_______ 。
(6)已知不同 条件下,水溶液中碳元素的存在形态如图所示。
条件下,水溶液中碳元素的存在形态如图所示。
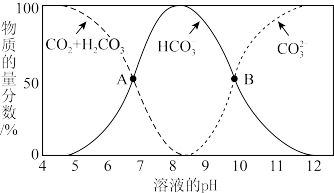
下列说法不正确的是_______ 。
a. 时,溶液中含碳元素的微粒主要是
时,溶液中含碳元素的微粒主要是
b.A点,溶液中 和
和 浓度相同
浓度相同
c.当 时,
时,
(7)水垢中的 可用
可用 溶液处理。当两种沉淀共存于溶液中,此时
溶液处理。当两种沉淀共存于溶液中,此时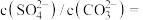
_______ 。
 时,部分物质的相关平衡常数如表所示,按要求回答下列问题:
时,部分物质的相关平衡常数如表所示,按要求回答下列问题:| 化学式 | 相关平衡常数 | 化学式 | 相关平衡常数 |
 | 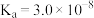 |  |  |
 |  |  | 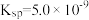 |
 | 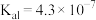  |  | 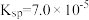 |
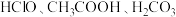 的酸性由强到弱的顺序为
的酸性由强到弱的顺序为(2)将少量
 气体通入
气体通入 溶液中,发生的离子方程式为
溶液中,发生的离子方程式为(3)相同温度下,判断
 溶液显
溶液显 ②
② ③
③ ④
④ ,溶液中的
,溶液中的 浓度由大到小的顺序为
浓度由大到小的顺序为(4)下列事实可以证明
 是弱碱的有
是弱碱的有①
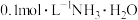 溶液能使酚酞溶液变红
溶液能使酚酞溶液变红②常温下,
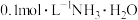 溶液的
溶液的
③
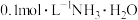 溶液的导电性比
溶液的导电性比 溶液弱
溶液弱④等体积的
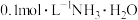 溶液与
溶液与 溶液恰好完全反应
溶液恰好完全反应⑤
 的
的 溶液稀释至100倍,
溶液稀释至100倍, 约为10
约为10(5)
 的
的 溶液与
溶液与 的
的 溶液等体积混合后,溶液中四种离子物质的量浓度由大到小的顺序为
溶液等体积混合后,溶液中四种离子物质的量浓度由大到小的顺序为(6)已知不同
 条件下,水溶液中碳元素的存在形态如图所示。
条件下,水溶液中碳元素的存在形态如图所示。
下列说法不正确的是
a.
 时,溶液中含碳元素的微粒主要是
时,溶液中含碳元素的微粒主要是
b.A点,溶液中
 和
和 浓度相同
浓度相同c.当
 时,
时,
(7)水垢中的
 可用
可用 溶液处理。当两种沉淀共存于溶液中,此时
溶液处理。当两种沉淀共存于溶液中,此时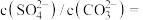
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】硫及其化合物在生产、生活中有广泛应用。
(1)硫原子最外层有_______ 种不同运动状态的电子,其中能量最高的电子所占电子亚层符号为_______ 。
(2)硫与同主族的氧元素相比,两者各自形成气态氢化物稳定性
_______  (选填“>”、“<”或“=”下同),分别与氢元素形成化学键键能大小关系为
(选填“>”、“<”或“=”下同),分别与氢元素形成化学键键能大小关系为
_______  。
。
(3)正交硫和单斜硫是硫常见的两种单质,它们互为_____ 。
已知: (正交)
(正交) (单斜)
(单斜) 。正交硫与单斜硫相比,相对比较稳定的是
。正交硫与单斜硫相比,相对比较稳定的是_______ 。已知通常状况下4g硫粉完全燃烧放出37 的热量,写出该反应的燃烧热的热化学方程式
的热量,写出该反应的燃烧热的热化学方程式_______ 。
(4)同温同浓度的 、
、 、
、 三种溶液,
三种溶液, 最大的是
最大的是_______ ;
(5) 溶液中
溶液中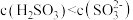 ,则
,则 溶液呈
溶液呈_______ (填“酸”或“碱”)性;
(6)等物质的量浓度的下列四种溶液:① ②
② ③
③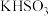 ④
④ ,溶液中水的电离程度由大到小排列顺序为
,溶液中水的电离程度由大到小排列顺序为_______ 。
(1)硫原子最外层有
(2)硫与同主族的氧元素相比,两者各自形成气态氢化物稳定性

 (选填“>”、“<”或“=”下同),分别与氢元素形成化学键键能大小关系为
(选填“>”、“<”或“=”下同),分别与氢元素形成化学键键能大小关系为
 。
。(3)正交硫和单斜硫是硫常见的两种单质,它们互为
已知:
 (正交)
(正交) (单斜)
(单斜) 。正交硫与单斜硫相比,相对比较稳定的是
。正交硫与单斜硫相比,相对比较稳定的是 的热量,写出该反应的燃烧热的热化学方程式
的热量,写出该反应的燃烧热的热化学方程式(4)同温同浓度的
 、
、 、
、 三种溶液,
三种溶液, 最大的是
最大的是(5)
 溶液中
溶液中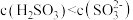 ,则
,则 溶液呈
溶液呈(6)等物质的量浓度的下列四种溶液:①
 ②
② ③
③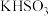 ④
④ ,溶液中水的电离程度由大到小排列顺序为
,溶液中水的电离程度由大到小排列顺序为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】CO、NH3、NO2、SO2处理不当易造成环境污染,如果对这些气体加以利用就可以变废为宝。回答下列问题:
(1)硝酸厂常用催化还原法处理尾气。CH4在催化条件下可以将NO2还原为N2。
已知:I.CH4(g)+ 2O2(g)=CO2(g) +2H2O(l) ΔH1=-890.3kJ·mol-1;
II.N2(g)+ 2O2(g)=2NO2(g) ΔH2= +67.7 kJ·mol-1
则CH4(g) +2NO2(g)=CO2(g) +N2(g)+ 2H2O(l) ΔH=_______ 。
(2)工业上利用NH3生产氢氰酸(HCN)的反应为CH4(g)+NH3(g) ⇌HCN(g)+3H2(g) ΔH>0。
①该反应在_______ (填“较高”或“较低”)温度下能自发进行。
②一定温度下,向2L恒容密闭容器中充入2 mol CH4(g)和2 mol NH3(g),发生上述反应,10 min末达到平衡状态,测得NH3的体积分数为30%。则0~10 min内,用HCN的浓度变化表示的平均反应速率为_______ ;CH4的平衡转化率为_______ ;该温度下,该反应的平衡常数K=_______ ( mol/L)2
(3)在催化剂作用下,CO还原NO2进行汽车尾气处理:2NO2(g) + 4CO(g) ⇌4CO2(g)+ N2(g) ΔH<0。
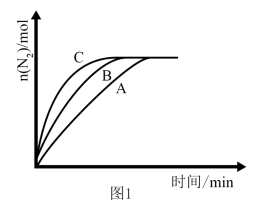
①相同条件下,选用A、B、C三种催化剂进行反应,生成N2的物质的量随时间的变化如图1所示。活化能最小的是_______ [填“E(A)” “E(B)”或“E(C)”]。
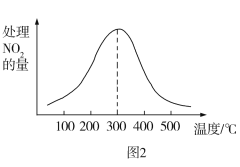
②在催化剂B作用下,测得相同时间内,处理NO2的量与温度的关系如图2所示。温度高于300℃,处理NO2的量随温度升高而减小的原因为(假设该温度范围内催化效率相同)_______ 。
(4)煤燃烧产生的SO2可用足量NaOH溶液吸收生成Na2SO3,Na2SO3溶液中各离子浓度由大到小的顺序为_______ 。
(1)硝酸厂常用催化还原法处理尾气。CH4在催化条件下可以将NO2还原为N2。
已知:I.CH4(g)+ 2O2(g)=CO2(g) +2H2O(l) ΔH1=-890.3kJ·mol-1;
II.N2(g)+ 2O2(g)=2NO2(g) ΔH2= +67.7 kJ·mol-1
则CH4(g) +2NO2(g)=CO2(g) +N2(g)+ 2H2O(l) ΔH=
(2)工业上利用NH3生产氢氰酸(HCN)的反应为CH4(g)+NH3(g) ⇌HCN(g)+3H2(g) ΔH>0。
①该反应在
②一定温度下,向2L恒容密闭容器中充入2 mol CH4(g)和2 mol NH3(g),发生上述反应,10 min末达到平衡状态,测得NH3的体积分数为30%。则0~10 min内,用HCN的浓度变化表示的平均反应速率为
(3)在催化剂作用下,CO还原NO2进行汽车尾气处理:2NO2(g) + 4CO(g) ⇌4CO2(g)+ N2(g) ΔH<0。
①相同条件下,选用A、B、C三种催化剂进行反应,生成N2的物质的量随时间的变化如图1所示。活化能最小的是

②在催化剂B作用下,测得相同时间内,处理NO2的量与温度的关系如图2所示。温度高于300℃,处理NO2的量随温度升高而减小的原因为(假设该温度范围内催化效率相同)

(4)煤燃烧产生的SO2可用足量NaOH溶液吸收生成Na2SO3,Na2SO3溶液中各离子浓度由大到小的顺序为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】氨水和 均可用于脱除烟气中
均可用于脱除烟气中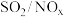 。
。
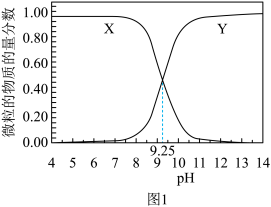
(1)以氨水作为吸收剂吸收 。25℃时,氨水中
。25℃时,氨水中 、
、 的物质的量分数随pH的分布如图所示。
的物质的量分数随pH的分布如图所示。
①氨水与 反应生成
反应生成 的离子方程式为
的离子方程式为___________ 。
②25℃时,氨水的电离常数
___________ 。(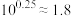 )
)
(2)查阅资料获得25℃时部分弱电解质的电离平衡常数数据:
① 溶液的水解平衡常数
溶液的水解平衡常数
___________ 。
②现有25℃时等浓度的5种溶液:A. ;B.
;B. ;C.
;C. ;D.
;D. ; E.
; E. ;F.(NH4)2CO3,这6种溶液中
;F.(NH4)2CO3,这6种溶液中 浓度由大到小的顺序排列是:
浓度由大到小的顺序排列是:___________ (填字母)。
(3) 可对烟气中NOx、
可对烟气中NOx、 进行协同脱除。
进行协同脱除。
①电解 溶液制备
溶液制备 气体的装置如图2所示。
气体的装置如图2所示。 通过阳离子交换膜向阴极室迁移,电解时阴极的电极反应为
通过阳离子交换膜向阴极室迁移,电解时阴极的电极反应为___________ 。

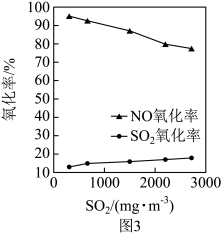
②保持其他条件不变,调节烟气中SO2初始浓度,将烟气按一定流速通入反应器与 反应,测得NO、SO2氧化率随SO2初始浓度的变化如图3所示。SO2氧化率始终低于NO氧化率的原因可能是
反应,测得NO、SO2氧化率随SO2初始浓度的变化如图3所示。SO2氧化率始终低于NO氧化率的原因可能是___________ 。
 均可用于脱除烟气中
均可用于脱除烟气中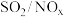 。
。(1)以氨水作为吸收剂吸收
 。25℃时,氨水中
。25℃时,氨水中 、
、 的物质的量分数随pH的分布如图所示。
的物质的量分数随pH的分布如图所示。
①氨水与
 反应生成
反应生成 的离子方程式为
的离子方程式为②25℃时,氨水的电离常数

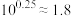 )
)(2)查阅资料获得25℃时部分弱电解质的电离平衡常数数据:
| 化学式 |  |  | HSCN |
| 电离平衡常数 |  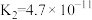 | 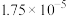 | 0.13 |
 溶液的水解平衡常数
溶液的水解平衡常数
②现有25℃时等浓度的5种溶液:A.
 ;B.
;B. ;C.
;C. ;D.
;D. ; E.
; E. ;F.(NH4)2CO3,这6种溶液中
;F.(NH4)2CO3,这6种溶液中 浓度由大到小的顺序排列是:
浓度由大到小的顺序排列是:(3)
 可对烟气中NOx、
可对烟气中NOx、 进行协同脱除。
进行协同脱除。①电解
 溶液制备
溶液制备 气体的装置如图2所示。
气体的装置如图2所示。 通过阳离子交换膜向阴极室迁移,电解时阴极的电极反应为
通过阳离子交换膜向阴极室迁移,电解时阴极的电极反应为
②保持其他条件不变,调节烟气中SO2初始浓度,将烟气按一定流速通入反应器与
 反应,测得NO、SO2氧化率随SO2初始浓度的变化如图3所示。SO2氧化率始终低于NO氧化率的原因可能是
反应,测得NO、SO2氧化率随SO2初始浓度的变化如图3所示。SO2氧化率始终低于NO氧化率的原因可能是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】已知 是常见的弱酸,现有常温下
是常见的弱酸,现有常温下 的
的 溶液。
溶液。
(1)取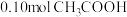 作导电性实验,测得其导电率随加入的水量变化如图所示。
作导电性实验,测得其导电率随加入的水量变化如图所示。

① :a
:a___________ b(填“>”、“<”或“=”,下同);
② :a
:a___________ b;
③完全中和时消耗NaOH的物质的量:a___________ b。
(2)温度不变,加水稀释过程中,下列表达式的数据一定变小的是___________(填字母,下同);若该溶液升高温度,下列表达式的数据增大的是___________。
(3)25℃时,部分物质的电离平衡常数如下表所示:
① 、
、 、HCN的酸性由强到弱的顺序为
、HCN的酸性由强到弱的顺序为___________ 。
②焦炉煤气中一般含有 和HCN气体,有的工厂在真空条件下,使用
和HCN气体,有的工厂在真空条件下,使用 溶液吸收煤气中的
溶液吸收煤气中的 和HCN气体,实现脱硫脱氰。根据上述数据,从理论上推测同为
和HCN气体,实现脱硫脱氰。根据上述数据,从理论上推测同为 的
的 溶液和HCN混合后,最可能发生反应的离子方程式为
溶液和HCN混合后,最可能发生反应的离子方程式为___________ 。
 是常见的弱酸,现有常温下
是常见的弱酸,现有常温下 的
的 溶液。
溶液。(1)取
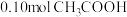 作导电性实验,测得其导电率随加入的水量变化如图所示。
作导电性实验,测得其导电率随加入的水量变化如图所示。
①
 :a
:a②
 :a
:a③完全中和时消耗NaOH的物质的量:a
(2)温度不变,加水稀释过程中,下列表达式的数据一定变小的是___________(填字母,下同);若该溶液升高温度,下列表达式的数据增大的是___________。
A. | B.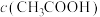 |
C. | D.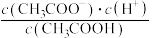 |
 |  | HCN |
 |  、 、 |  |
 、
、 、HCN的酸性由强到弱的顺序为
、HCN的酸性由强到弱的顺序为②焦炉煤气中一般含有
 和HCN气体,有的工厂在真空条件下,使用
和HCN气体,有的工厂在真空条件下,使用 溶液吸收煤气中的
溶液吸收煤气中的 和HCN气体,实现脱硫脱氰。根据上述数据,从理论上推测同为
和HCN气体,实现脱硫脱氰。根据上述数据,从理论上推测同为 的
的 溶液和HCN混合后,最可能发生反应的离子方程式为
溶液和HCN混合后,最可能发生反应的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】乙酸制氢具有重要意义:
热裂解反应:CH3COOH(g)=2CO(g)+2H2(g) ∆H=+213.7kJ·mol-1
脱羧基反应:CH3COOH(g)=CH4(g)+CO2(g) ∆H=−33.5kJ·mol-1
(1)2CO(g)+2H2(g)=CH4(g)+CO2(g) ∆H=____ kJ·mol-1。
(2)在密闭容器中,利用乙酸制氢,选择的压强为_____ (填“高压”或“常压”)。其中温度与气体产率的关系如图:

①约650℃之前,脱羧基反应活化能低,反应速率快,很快达到平衡,故氢气产率低于甲烷;650℃之后氢气产率高于甲烷,理由是____ 。
②保持其他条件不变,在乙酸气中掺杂一定量的水,氢气产率显著提高而CO的产率下降,请用化学方程式表示____ 。
(3)保持温度为T℃,压强为pkPa不变的条件下,在密闭容器中投入一定量的醋酸发生上述两个反应,达到平衡时热裂解反应消耗乙酸20%,脱羧基反应消耗乙酸60%,则平衡时乙酸体积分数为____ (结果保留1位小数);脱羧基反应的平衡常数Kp为____ kPa(结果保留1位小数)。
(4)光催化反应技术使用CH4和____ (填化学式)直接合成乙酸,且符合“绿色化学”的要求(原子利用率100%)。
(5)若室温下将amol/L的CH3COOH溶液和bmol/LBa(OH)2溶液等体积混合,恢复室温后有2c(Ba2+)=c(CH3COO-),则乙酸的电离平衡常数Ka=____ (用含a和b的代数式表示)。
热裂解反应:CH3COOH(g)=2CO(g)+2H2(g) ∆H=+213.7kJ·mol-1
脱羧基反应:CH3COOH(g)=CH4(g)+CO2(g) ∆H=−33.5kJ·mol-1
(1)2CO(g)+2H2(g)=CH4(g)+CO2(g) ∆H=
(2)在密闭容器中,利用乙酸制氢,选择的压强为

①约650℃之前,脱羧基反应活化能低,反应速率快,很快达到平衡,故氢气产率低于甲烷;650℃之后氢气产率高于甲烷,理由是
②保持其他条件不变,在乙酸气中掺杂一定量的水,氢气产率显著提高而CO的产率下降,请用化学方程式表示
(3)保持温度为T℃,压强为pkPa不变的条件下,在密闭容器中投入一定量的醋酸发生上述两个反应,达到平衡时热裂解反应消耗乙酸20%,脱羧基反应消耗乙酸60%,则平衡时乙酸体积分数为
(4)光催化反应技术使用CH4和
(5)若室温下将amol/L的CH3COOH溶液和bmol/LBa(OH)2溶液等体积混合,恢复室温后有2c(Ba2+)=c(CH3COO-),则乙酸的电离平衡常数Ka=
您最近一年使用:0次



