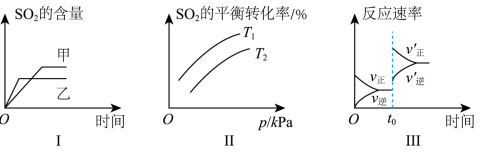
下列方案设计、现象和结论都正确的是
实验 | 目的 | 方案设计 | 现象和结论 |
| A | 探究压强对 (红棕色)与 (红棕色)与 (无色)平衡的影响 (无色)平衡的影响 | 快速压缩装有 、 、 平衡混合气体的针筒 平衡混合气体的针筒 | 如果气体颜色变深,则增大压强,平衡向生成 的方向移动 的方向移动 |
| B | 探究温度对  平衡产生的影响 平衡产生的影响 | 先加热装有 溶液的试管,后置于冷水中,观察溶液颜色变化 溶液的试管,后置于冷水中,观察溶液颜色变化 | 溶液变为黄绿色,后溶液由黄绿色变为蓝绿色,证明温度降低,平衡向生成 的方向移动 的方向移动 |
| C | 验证 溶液中存在水解平衡 溶液中存在水解平衡 | 取2mL 溶液于试管中,加2滴酚酞,再加入少量 溶液于试管中,加2滴酚酞,再加入少量 溶液 溶液 | 如果溶液红色变浅,则 溶液中存在水解平衡 溶液中存在水解平衡 |
| D | 相同温度下,比较 与 与 的酸性强弱 的酸性强弱 | 向等体积的水中分别通入 、 、 至饱和,再用pH计测定两种溶液的pH 至饱和,再用pH计测定两种溶液的pH | 如果通 后所得溶液的pH小,则 后所得溶液的pH小,则 的酸性比 的酸性比 强 强 |
| A.A | B.B | C.C | D.D |
更新时间:2024-01-09 17:58:40
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】拥有中国自主知识产权的全球首套煤制乙醇工业化项目投产成功。某煤制乙醇过程表示如下:
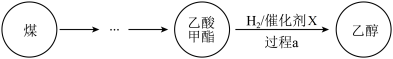
过程a包括以下3个主要反应:
I.

Ⅱ.

Ⅲ.

相同时间内,测得乙酸甲酯转化率随温度的变化如图1所示,乙醇和乙酸乙酯的选择性[乙醇选择性 ]随温度的变化如图2所示。
]随温度的变化如图2所示。

下列说法不正确的是

过程a包括以下3个主要反应:
I.


Ⅱ.


Ⅲ.


相同时间内,测得乙酸甲酯转化率随温度的变化如图1所示,乙醇和乙酸乙酯的选择性[乙醇选择性
 ]随温度的变化如图2所示。
]随温度的变化如图2所示。
下列说法不正确的是
| A.205℃后反应Ⅲ开始发生反应 |
| B.225~235℃,反应I处于平衡状态 |
| C.温度可影响催化剂的选择性,从而影响目标产物乙醇的选择性 |
| D.205℃时,CH3COOCH3起始物质的量为5mol,转化率为30%,则最终生成乙醇0.6mol |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】在2L恒容密闭容器中充入2mol X和1mol Y发生反应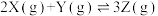
 ,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断错误的是
,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断错误的是

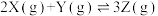
 ,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断错误的是
,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断错误的是
| A.Q点时,Y的转化率最大 |
| B.W点X的正反应速率小于M点X的正反应速率 |
| C.升高温度,平衡向左移动,平衡常数减小 |
| D.平衡时充入Y,达到新平衡时Y的转化率比原平衡时大 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在碳中性循环的模式下,通过 制备甲醇能减少或避免向大气中排放
制备甲醇能减少或避免向大气中排放 ,具有重要的应用价值。使用铜基催化剂时,体系内发生如下反应:
,具有重要的应用价值。使用铜基催化剂时,体系内发生如下反应:
①
 kJ⋅mol
kJ⋅mol
②
 2kJ⋅mol
2kJ⋅mol
③

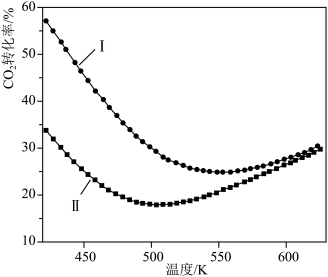
在两个相同容器内以1∶3的比例分别充入 和
和 ,其压强分别为2 MPa和5 MPa,测得
,其压强分别为2 MPa和5 MPa,测得 转化率随反应温度的变化如图,下列说法不正确的是
转化率随反应温度的变化如图,下列说法不正确的是
 制备甲醇能减少或避免向大气中排放
制备甲醇能减少或避免向大气中排放 ,具有重要的应用价值。使用铜基催化剂时,体系内发生如下反应:
,具有重要的应用价值。使用铜基催化剂时,体系内发生如下反应:①

 kJ⋅mol
kJ⋅mol
②

 2kJ⋅mol
2kJ⋅mol
③


在两个相同容器内以1∶3的比例分别充入
 和
和 ,其压强分别为2 MPa和5 MPa,测得
,其压强分别为2 MPa和5 MPa,测得 转化率随反应温度的变化如图,下列说法不正确的是
转化率随反应温度的变化如图,下列说法不正确的是
A. kJ⋅mol kJ⋅mol |
| B.曲线Ⅰ压强为5 MPa,曲线Ⅱ压强为2 MPa |
C.随温度升高 转化率先减小后增大,其原因是低温下主要发生反应①,高温主要发生反应② 转化率先减小后增大,其原因是低温下主要发生反应①,高温主要发生反应② |
D.若将纵坐标改为 产率,则图像变化趋势与原图一致 产率,则图像变化趋势与原图一致 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】A、B的混合气体在密闭容器中发生如下反应:xA(g)+yB(g) zC(g) △H<0。达到化学平衡后测得A的浓度为0.5 mol·L-1;在恒温下,将密闭容器的容积压缩至原来的二分之一,再次达到平衡时,测得A的浓度为0.9 mol·L-1。则下列叙述中正确的是
zC(g) △H<0。达到化学平衡后测得A的浓度为0.5 mol·L-1;在恒温下,将密闭容器的容积压缩至原来的二分之一,再次达到平衡时,测得A的浓度为0.9 mol·L-1。则下列叙述中正确的是
 zC(g) △H<0。达到化学平衡后测得A的浓度为0.5 mol·L-1;在恒温下,将密闭容器的容积压缩至原来的二分之一,再次达到平衡时,测得A的浓度为0.9 mol·L-1。则下列叙述中正确的是
zC(g) △H<0。达到化学平衡后测得A的浓度为0.5 mol·L-1;在恒温下,将密闭容器的容积压缩至原来的二分之一,再次达到平衡时,测得A的浓度为0.9 mol·L-1。则下列叙述中正确的是 | A.x+y<z | B.平衡向正反应方向移动了 |
| C.B的转化率下降 | D.C的体积分数减小 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
下列说法错误的是
| 物质 | X | Y | Z |
| 初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
| A.反应达到平衡时,X的转化率为50% |
| B.增大压强使平衡向生成Z的方向移动 |
| C.在25℃下,反应的平衡常数为1600,改变温度可以改变此反应的平衡常数 |
| D.在25℃下,测得c(X)=0.04mol·L-1,c(Y)=0.1mol·L-1,c(Z)=0.08mol·L-1,则此时v正<v逆 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】在氨水中存在电离平衡: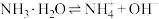 ,下列情况能使电离平衡向左移动的是
,下列情况能使电离平衡向左移动的是
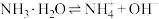 ,下列情况能使电离平衡向左移动的是
,下列情况能使电离平衡向左移动的是| A.加水 | B.通HCl | C.加NH4Cl固体 | D.加CH3COOH |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】pH=2的A、B两种酸溶液各1mL,分别加水稀释到1000mL, 其pH值与溶液体积V的关系如图所示。下列说法正确的是:
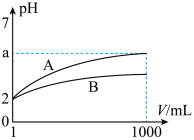

| A.A、B两酸溶液的物质的量浓度一定相等 |
| B.稀释后,A溶液的酸性比B溶液强 |
| C.a=5时,A是强酸,B是弱酸 |
| D.若A、B都是弱酸,则酸性:A<B |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】俗名为“臭碱”的硫化钠广泛应用于冶金、染料、皮革、电镀等工业。硫化钠的一种制备方法是Na2SO4+2C Na2S+2CO2↑。设NA为阿伏加 德罗常数的值,下列有关说法正确的是
Na2S+2CO2↑。设NA为阿伏加 德罗常数的值,下列有关说法正确的是
 Na2S+2CO2↑。设NA为阿伏加 德罗常数的值,下列有关说法正确的是
Na2S+2CO2↑。设NA为阿伏加 德罗常数的值,下列有关说法正确的是| A.1L0.25mol/LNa2SO4溶液中含有的氧原子数目为NA |
| B.1L0.1mol/LNa2S溶液中含有的阴离子数目小于0.1NA |
| C.12g金刚石中含有的碳碳单键数为4NA |
| D.标准状况下,11.2LCO2中含有的共用电子对数目为2NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法不正确 的是
A. 时,中和 时,中和 和体积均相等的乙酸和盐酸溶液,乙酸消耗 和体积均相等的乙酸和盐酸溶液,乙酸消耗 的物质的量多 的物质的量多 |
B. 时, 时, 的氯化铵溶液中滴入氨水至 的氯化铵溶液中滴入氨水至 , , 数目大于 数目大于 数目 数目 |
C. 时, 时, 的 的 溶液浓度小于 溶液浓度小于 的 的 溶液浓度的10倍 溶液浓度的10倍 |
D. 时,某溶液水电离出的 时,某溶液水电离出的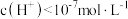 ,则该溶液的溶质可能是酸、碱或盐 ,则该溶液的溶质可能是酸、碱或盐 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐3】设NA为阿伏加德罗常数的值,下列说法不正确的是
A.25℃时,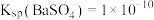 ,则1 L饱和BaSO4溶液中Ba2+数目为10-5NA ,则1 L饱和BaSO4溶液中Ba2+数目为10-5NA |
| B.25℃时,1 LpH=13的Ba(OH)2溶液中含有OH-数目为0.1NA |
C.25℃时,1 L0.1 mol/L的NH4Cl溶液中 数目为0.1NA 数目为0.1NA |
| D.H2和N2充分反应生成0.2 mol NH3时,转移电子数为0.6NA |
您最近半年使用:0次