砷是生命的第七元素,可形成多种重要化合物,如雌黄(As2S3)、雄黄(As4S4)、砷酸(H3AsO4)和亚砷酸(H3AsO3)等。
(1)雄黄可入药。若0.5mol雄黄与O2反应生成As2O3,转移14mol电子,则另一种产物为______________ (填化学式)。
(2)砷酸(H3AsO4)是一种重要化工产品,可与足量NaOH溶液反应生成Na3AsO4。NaH2AsO4溶液水解反应的Kh=_________ ,该溶液显______ (填“酸”或“碱”)性。若向该溶液中加入少量NaOH固体,则溶液中 将
将_______ (填“增大”、“减小”或“不变”)。(已知:25℃,砷酸的Ka1=5×10-3,Ka2=1.7×10-7)
(3)亚砷酸(H3AsO3)可以用于治疗白血病,其在溶液中存在多种微粒形态。常温下,用NaOH溶液滴定H3AsO3时,各种微粒的物质的量分数随pH的变化如图所示。
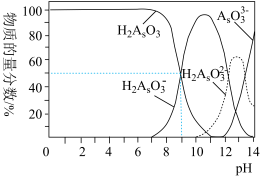
以酚酞为指示剂,将NaOH溶液逐滴加入到H3AsO3溶液中,当溶液由无色变为红色时停止滴加。该过程中主要反应的离子方程式为_______________ ,pH=8时,溶液中,c(Na+)________ c(H2AsO3-)(填“>”、“<”或“=”)。
(1)雄黄可入药。若0.5mol雄黄与O2反应生成As2O3,转移14mol电子,则另一种产物为
(2)砷酸(H3AsO4)是一种重要化工产品,可与足量NaOH溶液反应生成Na3AsO4。NaH2AsO4溶液水解反应的Kh=
 将
将(3)亚砷酸(H3AsO3)可以用于治疗白血病,其在溶液中存在多种微粒形态。常温下,用NaOH溶液滴定H3AsO3时,各种微粒的物质的量分数随pH的变化如图所示。

以酚酞为指示剂,将NaOH溶液逐滴加入到H3AsO3溶液中,当溶液由无色变为红色时停止滴加。该过程中主要反应的离子方程式为
19-20高三·山东泰安·期末 查看更多[3]
河南省开封市五县2020-2021学年高二上学期期末考试化学试题(已下线)考点11 弱电解质的电离及溶液pH-2020年高考化学命题预测与模拟试题分类精编山东省泰安市2020届高三上学期期末考试化学试题
更新时间:2020-01-15 09:44:44
|
相似题推荐
【推荐1】氧化锌在工业和生活中的运用非常广泛,以闪锌矿(主要成分为ZnS,含有少量FeS和SiO2)为原料制备活性氧化锌的工艺流程如下,请回答下列问题:
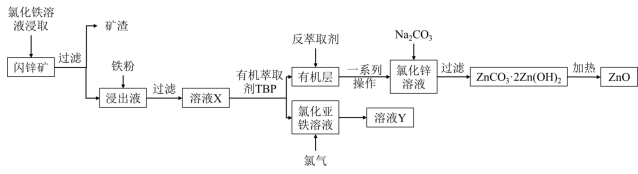
(1)浸取前,将闪锌矿粉碎的目的是_________ 。
(2)矿渣中除了有淡黄色的物质,还有_________ (填化学式);浸取时FeS发生反应的离子方程式为_________ 。
(3)加入铁粉的目的是_________ ,能循环利用的无机物是_________ (填化学式)。
(4)生成ZnCO3·2Zn(OH)2的离子方程式为_________ 。
(5)有机萃取剂TBP能将氯化亚铁和氯化锌分离的原因是_________ 。

(1)浸取前,将闪锌矿粉碎的目的是
(2)矿渣中除了有淡黄色的物质,还有
(3)加入铁粉的目的是
(4)生成ZnCO3·2Zn(OH)2的离子方程式为
(5)有机萃取剂TBP能将氯化亚铁和氯化锌分离的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】物质的大小会对其性质有极大影响。
(1)纳米金:具有高电子密度、介电特性和催化作用。纳米金的制法:将0.01%的 溶液煮沸,迅速加入1%的柠檬酸钠(
溶液煮沸,迅速加入1%的柠檬酸钠( )溶液,持续煮沸7~10分钟。制备时溶液会因为加入的柠檬酸钠的量不同而产生不同的颜色,如下表所示。
)溶液,持续煮沸7~10分钟。制备时溶液会因为加入的柠檬酸钠的量不同而产生不同的颜色,如下表所示。
资料: 的溶液呈黄色,其酸性比柠檬酸强。
的溶液呈黄色,其酸性比柠檬酸强。
①在制备过程中,存在如下反应,已知产物 是柠檬酸脱去一个羧基得到的,核磁共振氢谱显示其有4组峰。请补全并配平下面的反应方程式(要写出
是柠檬酸脱去一个羧基得到的,核磁共振氢谱显示其有4组峰。请补全并配平下面的反应方程式(要写出 的结构简式)
的结构简式) _______ 。
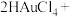 □
□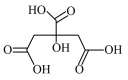 →□_______+□_______(
→□_______+□_______( )+□
)+□ +□HCl
+□HCl
②柠檬酸钠的作用是_______ ,如果一段时间后的液体仍为黄色,则可以_______ (填操作)来检验是否生成纳米金。
(2)微米水:可以高效诱导分子的还原反应,且不需要任何的外加还原剂或外加电荷。科学家使用上述方法制取纳米金时,引入了不加柠檬酸的对照组。令人惊奇的是对照组也发生了反应,他经过猜想与论证,最终将目光锁定在水身上,用如下装置(如图1所示)进行验证。

①使用丙酮酸( )来验证,通过检验由丙酮酸生成的产物
)来验证,通过检验由丙酮酸生成的产物_______ ,证明猜想成立。
②发现随着丙酮酸浓度的增加,还原效率会迅速降低,图2与图3中丙酮酸浓度均为10mol/L。

还原效率会随着雾化气体压强的增大而增大的原因是_______ 。
③为探究还原反应的具体过程,继续设计实验:向水中加入一种指示剂R,这种指示剂正常状态下不显色,R在遇到一定浓度的 与还原剂后会显示红色荧光,过程可以表示为:R(无色)
与还原剂后会显示红色荧光,过程可以表示为:R(无色) (红色荧光)。加入R后观测到的现象如图4所示。
(红色荧光)。加入R后观测到的现象如图4所示。

结合图4和上述实验,你可以得出什么推论?_______ 。
(3)综合上述内容,你对物质有了哪些更深入的认识?_______ 。
(1)纳米金:具有高电子密度、介电特性和催化作用。纳米金的制法:将0.01%的
 溶液煮沸,迅速加入1%的柠檬酸钠(
溶液煮沸,迅速加入1%的柠檬酸钠( )溶液,持续煮沸7~10分钟。制备时溶液会因为加入的柠檬酸钠的量不同而产生不同的颜色,如下表所示。
)溶液,持续煮沸7~10分钟。制备时溶液会因为加入的柠檬酸钠的量不同而产生不同的颜色,如下表所示。| 纳米金颗粒大小(nm) | 颜色 |
| 2~5 | 黄 |
| 10~20 | 红 |
| 30~80 | 紫 |
 的溶液呈黄色,其酸性比柠檬酸强。
的溶液呈黄色,其酸性比柠檬酸强。①在制备过程中,存在如下反应,已知产物
 是柠檬酸脱去一个羧基得到的,核磁共振氢谱显示其有4组峰。请补全并配平下面的反应方程式(要写出
是柠檬酸脱去一个羧基得到的,核磁共振氢谱显示其有4组峰。请补全并配平下面的反应方程式(要写出 的结构简式)
的结构简式) 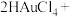 □
□ →□_______+□_______(
→□_______+□_______( )+□
)+□ +□HCl
+□HCl②柠檬酸钠的作用是
(2)微米水:可以高效诱导分子的还原反应,且不需要任何的外加还原剂或外加电荷。科学家使用上述方法制取纳米金时,引入了不加柠檬酸的对照组。令人惊奇的是对照组也发生了反应,他经过猜想与论证,最终将目光锁定在水身上,用如下装置(如图1所示)进行验证。

①使用丙酮酸(
 )来验证,通过检验由丙酮酸生成的产物
)来验证,通过检验由丙酮酸生成的产物②发现随着丙酮酸浓度的增加,还原效率会迅速降低,图2与图3中丙酮酸浓度均为10mol/L。

还原效率会随着雾化气体压强的增大而增大的原因是
③为探究还原反应的具体过程,继续设计实验:向水中加入一种指示剂R,这种指示剂正常状态下不显色,R在遇到一定浓度的
 与还原剂后会显示红色荧光,过程可以表示为:R(无色)
与还原剂后会显示红色荧光,过程可以表示为:R(无色) (红色荧光)。加入R后观测到的现象如图4所示。
(红色荧光)。加入R后观测到的现象如图4所示。
结合图4和上述实验,你可以得出什么推论?
(3)综合上述内容,你对物质有了哪些更深入的认识?
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】 是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:

回答下列问题:
(1)写出“反应”步骤生成 的离子方程式
的离子方程式___________ 。
(2)“电解”所用食盐水由粗盐水精制而成,精制时,为除去 和
和 ,要加入的试剂分别为
,要加入的试剂分别为___________ 。
(3)已知“尾气吸收”中发生的化学反应如下。
①X中氯的化合价为___________
②氧化剂是___________ (填写化学式)氧化产物是___________ (填写名称)
③此吸收反应中,消耗17g还原剂,生成氧化产物的质量为___________
 是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
回答下列问题:
(1)写出“反应”步骤生成
 的离子方程式
的离子方程式(2)“电解”所用食盐水由粗盐水精制而成,精制时,为除去
 和
和 ,要加入的试剂分别为
,要加入的试剂分别为(3)已知“尾气吸收”中发生的化学反应如下。

①X中氯的化合价为
②氧化剂是
③此吸收反应中,消耗17g还原剂,生成氧化产物的质量为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动。实验方案如下:
甲:①准确配制0.1mol·L-1的HA、HCl溶液各100mL;
②取纯度相同、质量、大小相等的锌粒放入两支试管中,同时加入0.1mol·L-1的HA、HCl溶液各100mL,按下图装好,观察现象。
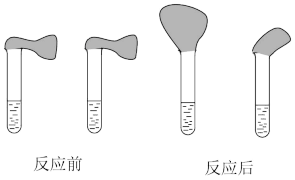
乙:①用pH计测定物质的量浓度均为0.1mol·L-1的HA和HCl溶液的pH;
②再取0.1mol·L-1的HA和HCl溶液各2滴(1滴约为0.05mL)分别稀释至100mL,再用pH计测其pH变化。
(1)乙方案中说明HA是弱电解质的理由是,测得0.1mol·L-1的HA溶液的pH___________ 1(填“>”“<”或“=”);甲方案中,说明HA是弱电解质的实验现象是___________ 。
A. 装HCl的试管中放出的氢气速率大
B.装HA溶液的试管中放出氢气的速率大
C.两个试管中产生气体速率一样大
(2)乙同学设计的实验第②步,能证明改变条件,弱电解质平衡发生移动。加水稀释,弱酸HA的电离程度___________ (填“增大、减小、不变”)。
(3)甲同学为了进一步证明弱电解质电离平衡移动的情况,设计如下实验:使HA的电离程度和c(H+)都减小,c(A)增大,可在0.1mol·L -1的HA溶液中,选择加入___________试剂。
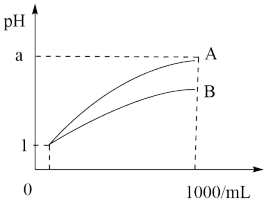
(4)pH=1的两种酸溶液A、B各1mL,分别加水稀释到1000mL,其pH与溶液体积V的关系如图所示,则下列说法不正确的有___________。
甲:①准确配制0.1mol·L-1的HA、HCl溶液各100mL;
②取纯度相同、质量、大小相等的锌粒放入两支试管中,同时加入0.1mol·L-1的HA、HCl溶液各100mL,按下图装好,观察现象。

乙:①用pH计测定物质的量浓度均为0.1mol·L-1的HA和HCl溶液的pH;
②再取0.1mol·L-1的HA和HCl溶液各2滴(1滴约为0.05mL)分别稀释至100mL,再用pH计测其pH变化。
(1)乙方案中说明HA是弱电解质的理由是,测得0.1mol·L-1的HA溶液的pH
A. 装HCl的试管中放出的氢气速率大
B.装HA溶液的试管中放出氢气的速率大
C.两个试管中产生气体速率一样大
(2)乙同学设计的实验第②步,能证明改变条件,弱电解质平衡发生移动。加水稀释,弱酸HA的电离程度
(3)甲同学为了进一步证明弱电解质电离平衡移动的情况,设计如下实验:使HA的电离程度和c(H+)都减小,c(A)增大,可在0.1mol·L -1的HA溶液中,选择加入___________试剂。
| A.NaA固体(可完全溶于水) | B.1mol·L-1 NaOH溶液 |
| C.1mol·L-1 H2SO4 | D.2mol·L-1 HA |

| A.若a=4,则A是强酸,B是弱酸 |
| B.若1<a<4,则A、B都是弱酸 |
| C.两种酸溶液的物质的量浓度一定相等 |
| D.稀释后,A溶液的酸性比B溶液弱 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】弱电解质的电离平衡与日常生活、工农业生产等息息相关。回答下列问题:
Ⅰ.部分弱酸的电离平衡常数如下表:
(1)H2S的二级电离平衡常数的表达式为___________ 。
(2)c(H+)浓度相同的HCOOH和HClO溶液中:c(HCOOH)___________ c(HClO)。
(3)根据上述电离常数及物质的特性判断下列化学反应方程式错误的是___________ (填序号)。
①次氯酸与NaHCO3溶液的反应:HClO+CO =ClO﹣+HCO
=ClO﹣+HCO
②少量CO2通入NaClO溶液中:CO2+H2O+ClO﹣=HCO +HClO
+HClO
③硫化氢气体通入NaClO溶液中:H2S+ClO﹣=HS﹣+HClO
④碳酸钠滴入足量甲酸溶液中:2HCOOH+CO =2HCOO﹣+CO2↑+H2O
=2HCOO﹣+CO2↑+H2O
⑤碳酸钠溶液通入少量H2S: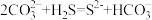
Ⅱ.常压下,某化学兴趣小组取不同浓度、不同温度的醋酸进行各项内容的测定,得到下表实验数据。
已知:电离度= ×100%
×100%
(4)温度升高,CH3COOH的电离平衡向___________ (填“左”或“右”)移动,能支持该结论的表中数据是___________ (填字母)。
a.c(H+) b.电离度 c.电离常数 d.c(CH3COOH)
(5)表中c(H+)基本不变的原因是___________ 。
(6)常温下,在醋酸溶液中加入纯醋酸,醋酸的电离度___________ (填“增大”“减小”或“不变”下同);在醋酸溶液中加入一定量的醋酸钠晶体,醋酸的电离度___________ 。
Ⅰ.部分弱酸的电离平衡常数如下表:
| 弱酸 | HCOOH | H2S | H2CO3 | HClO |
| 电离平衡常数(25℃) | K=1.77×10﹣4 | K1=1.3×10﹣7 K2=7.1×10﹣15 | K1=4.4×10﹣7K2=4.7×10﹣11 | K=3.0×10﹣8 |
(2)c(H+)浓度相同的HCOOH和HClO溶液中:c(HCOOH)
(3)根据上述电离常数及物质的特性判断下列化学反应方程式错误的是
①次氯酸与NaHCO3溶液的反应:HClO+CO
 =ClO﹣+HCO
=ClO﹣+HCO
②少量CO2通入NaClO溶液中:CO2+H2O+ClO﹣=HCO
 +HClO
+HClO③硫化氢气体通入NaClO溶液中:H2S+ClO﹣=HS﹣+HClO
④碳酸钠滴入足量甲酸溶液中:2HCOOH+CO
 =2HCOO﹣+CO2↑+H2O
=2HCOO﹣+CO2↑+H2O⑤碳酸钠溶液通入少量H2S:
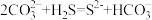
Ⅱ.常压下,某化学兴趣小组取不同浓度、不同温度的醋酸进行各项内容的测定,得到下表实验数据。
| 温度/℃ | c(CH3COOH)/mol⋅L﹣1 | 电离常数 | 电离度/% | c(H+)/mol⋅L﹣1 |
| 0 | 16.06 | 1.37×10﹣1 | 9.098 | 1.507×10﹣2 |
| 10 | 15.16 | 1.57×10﹣1 | 10.18 | 1.543×10﹣2 |
| 20 | 13.63 | 1.71×10﹣1 | 11.2 | 1.527×10﹣2 |
 ×100%
×100%(4)温度升高,CH3COOH的电离平衡向
a.c(H+) b.电离度 c.电离常数 d.c(CH3COOH)
(5)表中c(H+)基本不变的原因是
(6)常温下,在醋酸溶液中加入纯醋酸,醋酸的电离度
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】今有①CH3COOH ②HCl ③H2SO4 三种溶液。根据要求回答下列问题:
(1)当它们pH相同时,其物质的量浓度最大的是________________ (填序号)。
(2)当它们的物质的量浓度相同时,其pH最小的是____________ (填序号)。
(3)将c(H+)相同的三种酸均加水稀释至原来的10倍,c(H+)由大到小的顺序为_________ 。(填序号)
(4)体积和物质的量浓度均相同的①②③三种酸溶液,分别与相同浓度的烧碱溶液恰好完全反应,所需烧碱的体积比为_____________ ;此时所得到的三种溶液的pH大小关系为_______________ (填序号)。
(5)若酸性FeCl2溶液中c(Fe2+)=2.0×10-2mol·L-1,c(Fe3+)=1.0×10-3mol·L-1,c(Cl-)=5.3×10-2mol·L-1,则该溶液的pH约为__________ 。
(1)当它们pH相同时,其物质的量浓度最大的是
(2)当它们的物质的量浓度相同时,其pH最小的是
(3)将c(H+)相同的三种酸均加水稀释至原来的10倍,c(H+)由大到小的顺序为
(4)体积和物质的量浓度均相同的①②③三种酸溶液,分别与相同浓度的烧碱溶液恰好完全反应,所需烧碱的体积比为
(5)若酸性FeCl2溶液中c(Fe2+)=2.0×10-2mol·L-1,c(Fe3+)=1.0×10-3mol·L-1,c(Cl-)=5.3×10-2mol·L-1,则该溶液的pH约为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】I.研究电解质在水溶液中的离子反应与平衡有重要的意义。
(1) 下,将
下,将 的
的 溶液
溶液 与
与 的
的 溶液
溶液 混合,若所得溶液
混合,若所得溶液 ,则
,则
_______ 。
(2)已知 时,
时, 的溶度积常数
的溶度积常数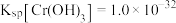 。则使
。则使 恰好完全沉淀,即溶液中
恰好完全沉淀,即溶液中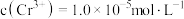 时,应调节
时,应调节 为
为_______ 。
(3)已知: 下
下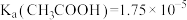 。
。
 下将
下将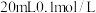 的
的 溶液与
溶液与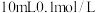 的
的 溶液混合后,所得混合溶液中离子浓度由大到小的顺序为
溶液混合后,所得混合溶液中离子浓度由大到小的顺序为_______ 。
II.2022年11月29日23时08分,我国在酒泉卫星发射中心使用长征二号F遥十五火箭,成功将神舟十五号载人飞船发射升空,是空间站建造阶段最后一次载人飞行任务。
(4)火箭发射时可以用肼( ,液态)作燃料,
,液态)作燃料, 作氧化剂,二者反应生成
作氧化剂,二者反应生成 和水蒸气。已知:
和水蒸气。已知:
①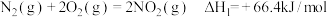
②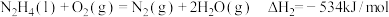
请写出 与
与 反应的热化学方程式:
反应的热化学方程式:_______ 。
(5)二甲醚 是一种新型能源,被誉为“21世纪的清洁燃料”。
是一种新型能源,被誉为“21世纪的清洁燃料”。
用 和
和 合成二甲醚的主反应为:
合成二甲醚的主反应为: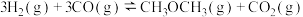
制备过程中还会发生副反应:
①在恒温恒容体系中,下列能判断主反应达到平衡状态的是_______ (填字母)。
A.气体的平均相对分子质量不变
B.气体的密度不再发生变化
C.每断裂 键的同时断裂
键的同时断裂 的
的 键
键
D.二甲醚的体积分数不再变化
②在实验室模拟进行二甲醚制备实验,在 刚性容器中,起始加入
刚性容器中,起始加入 和
和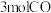 ,体系起始总压为
,体系起始总压为 ,体系温度保持恒温(在该温度下甲醇为气态)。经实验测定,平衡时
,体系温度保持恒温(在该温度下甲醇为气态)。经实验测定,平衡时 且
且 的体积分数为
的体积分数为 ,则
,则 的平衡转化率为
的平衡转化率为_______ (写成百分数形式,保留一位小数),该温度下主反应的
_______ 。
(1)
 下,将
下,将 的
的 溶液
溶液 与
与 的
的 溶液
溶液 混合,若所得溶液
混合,若所得溶液 ,则
,则
(2)已知
 时,
时, 的溶度积常数
的溶度积常数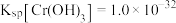 。则使
。则使 恰好完全沉淀,即溶液中
恰好完全沉淀,即溶液中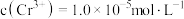 时,应调节
时,应调节 为
为(3)已知:
 下
下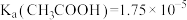 。
。 下将
下将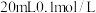 的
的 溶液与
溶液与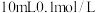 的
的 溶液混合后,所得混合溶液中离子浓度由大到小的顺序为
溶液混合后,所得混合溶液中离子浓度由大到小的顺序为II.2022年11月29日23时08分,我国在酒泉卫星发射中心使用长征二号F遥十五火箭,成功将神舟十五号载人飞船发射升空,是空间站建造阶段最后一次载人飞行任务。
(4)火箭发射时可以用肼(
 ,液态)作燃料,
,液态)作燃料, 作氧化剂,二者反应生成
作氧化剂,二者反应生成 和水蒸气。已知:
和水蒸气。已知:①
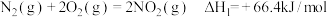
②
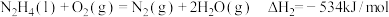
请写出
 与
与 反应的热化学方程式:
反应的热化学方程式:(5)二甲醚
 是一种新型能源,被誉为“21世纪的清洁燃料”。
是一种新型能源,被誉为“21世纪的清洁燃料”。用
 和
和 合成二甲醚的主反应为:
合成二甲醚的主反应为: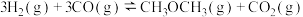
制备过程中还会发生副反应:

①在恒温恒容体系中,下列能判断主反应达到平衡状态的是
A.气体的平均相对分子质量不变
B.气体的密度不再发生变化
C.每断裂
 键的同时断裂
键的同时断裂 的
的 键
键D.二甲醚的体积分数不再变化
②在实验室模拟进行二甲醚制备实验,在
 刚性容器中,起始加入
刚性容器中,起始加入 和
和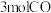 ,体系起始总压为
,体系起始总压为 ,体系温度保持恒温(在该温度下甲醇为气态)。经实验测定,平衡时
,体系温度保持恒温(在该温度下甲醇为气态)。经实验测定,平衡时 且
且 的体积分数为
的体积分数为 ,则
,则 的平衡转化率为
的平衡转化率为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)根据分类标准,将有关物质的序号填写在表格中:①金属Fe ②熔融KNO3 ③干冰④NH3 ⑤液态HCl ⑥硫酸 ⑦AgNO3固体 ⑧酒精 ⑨碳酸氢钠溶液 ⑩澄清石灰水。
(2)某温度下,纯水的 为
为 ,则此时
,则此时 为
为_______  ,若温度不变,滴入稀H2SO4使
,若温度不变,滴入稀H2SO4使 ,则由水电离出的c(H+)为
,则由水电离出的c(H+)为_______  。
。
(3)常温下,0.1mon/L的CH3COONa溶液pH值大于7,请用离子方程式表示原因:_______ ,加热蒸干FeCl3溶液并灼烧固体,最后得到的物质是_______ 。
(4)常温下,向10mL氨水中加入蒸馏水,将其稀释到1L,下列说法中不正确的是_______。
(5)常温下,将 0.2 mol·L-1 的某一元酸HA溶液和 0.1 mol·L-1NaOH 溶液等体积混合后溶液pH大于7,若混合液体积等于两溶液体积之和,则混合液中下列关系正确的是_______ (填字母)。
(1)根据分类标准,将有关物质的序号填写在表格中:①金属Fe ②熔融KNO3 ③干冰④NH3 ⑤液态HCl ⑥硫酸 ⑦AgNO3固体 ⑧酒精 ⑨碳酸氢钠溶液 ⑩澄清石灰水。
| 分类标准 | 能导电 | 电解质 | 非电解质 |
| 属于该类的物质 |
 为
为 ,则此时
,则此时 为
为 ,若温度不变,滴入稀H2SO4使
,若温度不变,滴入稀H2SO4使 ,则由水电离出的c(H+)为
,则由水电离出的c(H+)为 。
。(3)常温下,0.1mon/L的CH3COONa溶液pH值大于7,请用离子方程式表示原因:
(4)常温下,向10mL氨水中加入蒸馏水,将其稀释到1L,下列说法中不正确的是_______。
A. 的电离程度减小 的电离程度减小 | B.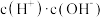 不变 不变 |
C.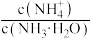 减小 减小 | D. 数目增多 数目增多 |
| A.c(HA)<c(A-) | B.c(HA)一定大于 0.05 mol·L-1 |
| C.c(Na+)=c(HA)+c(A-) | D.2c(OH-)=2c(H+)+[c(HA)-c(A-)] |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】科学家积极探索新技术对CO2进行综合利用。
Ⅰ.CO2可用FeO 吸收获得H2。
i. 6FeO(s) +CO2(g)=2Fe3O4(s) +C(s) △Hl =-76.0 kJ·mol-1
ⅱ. C(s) +2H2O(g)=CO2(g) +2H2(g) △H2 = +113.4 kJ·mol-1
(1)3FeO(s) +H2O(g)= Fe3O4(s) +H2(g) △H3 =_________ 。
(2)在反应i中,每放出38.0 kJ热量,有______ g FeO被氧化。
Ⅱ.CO2可用来生产燃料甲醇。
CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。在体积为1L的恒容密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应;测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。在体积为1L的恒容密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应;测得CO2和CH3OH(g)的浓度随时间变化如图所示。

(3)从反应开始到平衡,氢气的平均反应速率v(H2)=___________________ mol·(L·min) -1。
(4)氢气的转化率=________________________ 。
(5)该反应的平衡常数为__________________________ (保留小数点后2位)。
(6)下列措施中能使平衡体系中n(CH3OH)/n(CO2)增大的是_____________________ 。
A.升高温度 B.充入He(g),使体系压强增大
C.再充入1 mol H2 D.将H2O(g)从体系中分离出去
(7)当反应达到平衡时,H2的物质的量浓度为c1,然后向容器中再加入一定量H2,待反应再一次达到平衡后,H2的物质的量浓度为c2,则c1________ c2的关系(填“>”、“<”或“=”)。
III.CO2可用碱溶液吸收获得相应的原料。
利用100 mL 3 mol·L-1NaOH溶液吸收4.48 LCO2(标准状况),得到吸收液。
(8)该吸收液中离子浓度的大小排序为___________________ 。将该吸收液蒸干,灼烧至恒重,所得固体的成分是_________ (填化学式)。
Ⅰ.CO2可用FeO 吸收获得H2。
i. 6FeO(s) +CO2(g)=2Fe3O4(s) +C(s) △Hl =-76.0 kJ·mol-1
ⅱ. C(s) +2H2O(g)=CO2(g) +2H2(g) △H2 = +113.4 kJ·mol-1
(1)3FeO(s) +H2O(g)= Fe3O4(s) +H2(g) △H3 =
(2)在反应i中,每放出38.0 kJ热量,有
Ⅱ.CO2可用来生产燃料甲醇。
CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。在体积为1L的恒容密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应;测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。在体积为1L的恒容密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应;测得CO2和CH3OH(g)的浓度随时间变化如图所示。
(3)从反应开始到平衡,氢气的平均反应速率v(H2)=
(4)氢气的转化率=
(5)该反应的平衡常数为
(6)下列措施中能使平衡体系中n(CH3OH)/n(CO2)增大的是
A.升高温度 B.充入He(g),使体系压强增大
C.再充入1 mol H2 D.将H2O(g)从体系中分离出去
(7)当反应达到平衡时,H2的物质的量浓度为c1,然后向容器中再加入一定量H2,待反应再一次达到平衡后,H2的物质的量浓度为c2,则c1
III.CO2可用碱溶液吸收获得相应的原料。
利用100 mL 3 mol·L-1NaOH溶液吸收4.48 LCO2(标准状况),得到吸收液。
(8)该吸收液中离子浓度的大小排序为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】研究大气中含硫化合物(主要是SO2和H2S)的转化具有重要意义。回答下列问题:
(1)高温条件下,利用催化剂可将大气样品中的含硫化合物(SO2和H2S的含量分别为0.16 mg·m-3和0.34mg·m-3)完全转化为单质硫,该过程为_______ (用一个化学方程式表示)。
(2)土壤中的微生物可将大气中的H2S经两步反应氧化成SO ,能量变化如图:
,能量变化如图:

1 mol SO (aq)全部转化为H2S(g)的热化学方程式为
(aq)全部转化为H2S(g)的热化学方程式为_______ 。
(3)二氧化硫-空气质子交换膜燃料电池可以利用大气所含SO2快速启动,原理如图所示:

①放电时消耗SO2和O2的物质的量之比为_______ 。
②负极的电极反应式为_______ 。
(4)燃煤烟气的脱硫减排是减少大气中含硫化合物的关键,用纯碱溶液吸收SO2生成CO2和HSO ,反应的离子方程式为
,反应的离子方程式为_______ ;已知H2SO3的电离常数Ka1=1×10-2,Ka2=6×10-8,则HSO 的水解常数Kh=
的水解常数Kh=_______ 。
(1)高温条件下,利用催化剂可将大气样品中的含硫化合物(SO2和H2S的含量分别为0.16 mg·m-3和0.34mg·m-3)完全转化为单质硫,该过程为
(2)土壤中的微生物可将大气中的H2S经两步反应氧化成SO
 ,能量变化如图:
,能量变化如图:
1 mol SO
 (aq)全部转化为H2S(g)的热化学方程式为
(aq)全部转化为H2S(g)的热化学方程式为(3)二氧化硫-空气质子交换膜燃料电池可以利用大气所含SO2快速启动,原理如图所示:

①放电时消耗SO2和O2的物质的量之比为
②负极的电极反应式为
(4)燃煤烟气的脱硫减排是减少大气中含硫化合物的关键,用纯碱溶液吸收SO2生成CO2和HSO
 ,反应的离子方程式为
,反应的离子方程式为 的水解常数Kh=
的水解常数Kh=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)C元素是组成化合物种类最多的元素,含C元素的酸有也多种,其中氢氰酸(HCN)有剧毒,25℃时,该酸的电离常数为Ka=6.2×10—10。
①25℃时KCN溶液中CN—的水解常数Kh= =
=___________ (保留一位小数)。
②0.2mol•L-1的KOH溶液与0.4mol•L-1的HCN溶液等体积混合后,恢复到25℃,混合溶液中c(K+)和c(HCN)浓度大小关系是c(K+)___________ c(HCN)(填“>”、“<”或“=”)。
(2)为测定某草酸晶体产品中H2C2O4·2H2O的质量分数,称取14.00g产品溶于水,配制成500mL溶液,用浓度为0.1000mol•L-1的酸性高锰酸钾溶液滴定,每次所取待测液体积均为25.00mL,实验结果记录如表。已知2MnO +5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,杂质不与高锰酸钾反应,H2C2O4·2H2O相对分子质量为126。
+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,杂质不与高锰酸钾反应,H2C2O4·2H2O相对分子质量为126。
①滴定终点的现象是:当最后半滴KMnO4溶液滴入时,___________ 。
②通过实验数据,计算该产品中H2C2O4·2H2O的质量分数为___________ 。
③下列操作会导致测定结果偏低的是___________ 。
A.锥形瓶用待测液润洗
B.装酸性高锰酸钾溶液的滴定管没有润洗
C.滴定前滴定管尖嘴处有气泡,滴定结束后气泡消失
D.滴定前平视,滴定结束时俯视
(3)一种3D打印机的柔性电池以碳纳米管作电极材料,以吸收ZnSO4溶液的有机高聚物为固态电解质,工作原理示意图如图,电池总反应为6MnO2+3Zn+(6+x)H2O+ZnSO4 6MnOOH(不溶于水)+ZnSO4·3Zn(OH)2·xH2O,请回答下列问题。
6MnOOH(不溶于水)+ZnSO4·3Zn(OH)2·xH2O,请回答下列问题。

①放电时负极为___________ (填“锌膜”或“MnO2膜”),正极质量___________ (填“增大”、“减小”或“不变”)。
②充电时,SO 向
向___________ (填“锌膜”或“MnO2膜”)移动。
(1)C元素是组成化合物种类最多的元素,含C元素的酸有也多种,其中氢氰酸(HCN)有剧毒,25℃时,该酸的电离常数为Ka=6.2×10—10。
①25℃时KCN溶液中CN—的水解常数Kh=
 =
=②0.2mol•L-1的KOH溶液与0.4mol•L-1的HCN溶液等体积混合后,恢复到25℃,混合溶液中c(K+)和c(HCN)浓度大小关系是c(K+)
(2)为测定某草酸晶体产品中H2C2O4·2H2O的质量分数,称取14.00g产品溶于水,配制成500mL溶液,用浓度为0.1000mol•L-1的酸性高锰酸钾溶液滴定,每次所取待测液体积均为25.00mL,实验结果记录如表。已知2MnO
 +5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,杂质不与高锰酸钾反应,H2C2O4·2H2O相对分子质量为126。
+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,杂质不与高锰酸钾反应,H2C2O4·2H2O相对分子质量为126。| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗KMnO4溶液体积/mL | 20.05 | 19.95 | 24.36 |
②通过实验数据,计算该产品中H2C2O4·2H2O的质量分数为
③下列操作会导致测定结果偏低的是
A.锥形瓶用待测液润洗
B.装酸性高锰酸钾溶液的滴定管没有润洗
C.滴定前滴定管尖嘴处有气泡,滴定结束后气泡消失
D.滴定前平视,滴定结束时俯视
(3)一种3D打印机的柔性电池以碳纳米管作电极材料,以吸收ZnSO4溶液的有机高聚物为固态电解质,工作原理示意图如图,电池总反应为6MnO2+3Zn+(6+x)H2O+ZnSO4
 6MnOOH(不溶于水)+ZnSO4·3Zn(OH)2·xH2O,请回答下列问题。
6MnOOH(不溶于水)+ZnSO4·3Zn(OH)2·xH2O,请回答下列问题。
①放电时负极为
②充电时,SO
 向
向
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】氰化钠化学式为NaCN(C元素+2价,N元素-3价),氰化钠是一种白色结晶颗粒,剧毒,易溶于水,水溶液呈碱性,易水解生成氰化氢。
(1)NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,该反应的离子方程式是____________________________________________ 。
(2)氰化钠与硫代硫酸钠的反应为:NaCN+Na2S2O3═NaSCN+Na2SO3;已知:NaSCN中S为-2价,写出SCN-的电子式___________ 。
(3)CN-中C元素显+2价,N元素显-3价,说明非金属性N>C,请设计实验证明:_____________ 。
(4)同时HCN又能与水互溶,造成水污染。已知部分弱酸的电离平衡常数如表:
①向NaCN溶液中通入少量CO2,发生的离子反应为_______________________________ 。
②等体积、等物质的量浓度的HCOONa和NaCN溶液中所含离子总数的关系是:HCOONa______ NaCN。(填“>”、“<”或“=”)
(5)常温下,用0.10mol·L-1NaOH溶液分别滴定20.00 mL浓度均为0.10 mol·L-1CH3COOH溶液和HCN溶液所得滴定曲线如下图。

①常温时醋酸的电离常数为1.96×10-5,0.10 mol·L-1CH3COOH溶液中c(H+)=__________ mol·L-1。
②在①所示的溶液中溶质为_____
③在①和②所示溶液中c(CH3COO-)-c(CN-)_______ (填“>”、“<”或“=”)c(HCN)-c(CH3COOH)。
(1)NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,该反应的离子方程式是
(2)氰化钠与硫代硫酸钠的反应为:NaCN+Na2S2O3═NaSCN+Na2SO3;已知:NaSCN中S为-2价,写出SCN-的电子式
(3)CN-中C元素显+2价,N元素显-3价,说明非金属性N>C,请设计实验证明:
(4)同时HCN又能与水互溶,造成水污染。已知部分弱酸的电离平衡常数如表:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | Ka=1.77×10-4 | Ka=5.0×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
②等体积、等物质的量浓度的HCOONa和NaCN溶液中所含离子总数的关系是:HCOONa
(5)常温下,用0.10mol·L-1NaOH溶液分别滴定20.00 mL浓度均为0.10 mol·L-1CH3COOH溶液和HCN溶液所得滴定曲线如下图。

①常温时醋酸的电离常数为1.96×10-5,0.10 mol·L-1CH3COOH溶液中c(H+)=
②在①所示的溶液中溶质为
③在①和②所示溶液中c(CH3COO-)-c(CN-)
您最近一年使用:0次



