解题方法
1 . 根据下列图示所得出的结论不正确的是
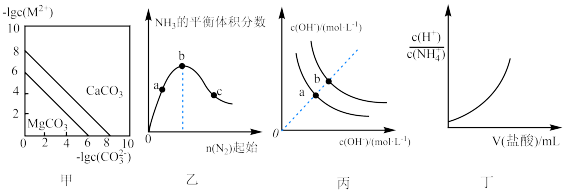
A.图甲表示一定温度下,MCO3(M:Mg2+、Ca2+)的沉淀溶解平衡曲线,则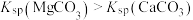 |
B.图乙是H2的起始量一定时恒温密闭容器中发生:N2(g)+3H2(g) 2NH3(g)反应,达到平衡时NH3的体积分数随N2的起始物质的量的变化曲线,则H2的转化率:b>c>a 2NH3(g)反应,达到平衡时NH3的体积分数随N2的起始物质的量的变化曲线,则H2的转化率:b>c>a |
| C.图丙表示不同温度下溶液中H+和OH-的浓度变化曲线,图中a点对应温度低于b点 |
D.图丁投示向0.lmol/L的NH4Cl溶液中滴加0.1mol/L的盐酸,溶液中 随盐酸的体积变化关系 随盐酸的体积变化关系 |
您最近一年使用:0次
名校
解题方法
2 . 推动 的综合利用实现碳中和是党中央作出的重大战略决策。
的综合利用实现碳中和是党中央作出的重大战略决策。
Ⅰ. 催化加氢法:以下是
催化加氢法:以下是 催化加氢合成二甲醚发生的两个主要反应:
催化加氢合成二甲醚发生的两个主要反应:
反应Ⅰ:
反应Ⅱ:
(1)反应
___________ 。
(2)在恒压、 和
和 起始量一定的条件下,
起始量一定的条件下, 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度的变化如图。其中:
的选择性随温度的变化如图。其中: 的选择性
的选择性
 平衡转化率随温度升高而上升的原因是
平衡转化率随温度升高而上升的原因是___________ 。
②220℃时,在催化剂作用下 与
与 反应一段时间后,测得
反应一段时间后,测得 的选择性为:
的选择性为: (图中
(图中 点)。不改变反应时间和温度,一定能提高
点)。不改变反应时间和温度,一定能提高 选择性的措施有:
选择性的措施有:___________ 。(答1点即可)
Ⅱ. 催化加氢法:高炉气中捕集
催化加氢法:高炉气中捕集 制
制 的综合利用示意图如图所示。
的综合利用示意图如图所示。 。
。
(3)T℃时,当吸收池中溶液的 时,此时该溶液中
时,此时该溶液中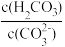 =
=___________ 。
(4)电解池中 电催化还原为
电催化还原为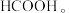
① 在铂电极反应方程式为
在铂电极反应方程式为___________ 。
②铂电极上的副反应除析氢外,没有其它放电过程。若生成 的电解效率
的电解效率 ,当电路中转移
,当电路中转移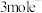 时,阴极室溶液的质量增加
时,阴极室溶液的质量增加___________  。定义:
。定义: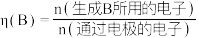
 的综合利用实现碳中和是党中央作出的重大战略决策。
的综合利用实现碳中和是党中央作出的重大战略决策。Ⅰ.
 催化加氢法:以下是
催化加氢法:以下是 催化加氢合成二甲醚发生的两个主要反应:
催化加氢合成二甲醚发生的两个主要反应:反应Ⅰ:

反应Ⅱ:

(1)反应

(2)在恒压、
 和
和 起始量一定的条件下,
起始量一定的条件下, 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度的变化如图。其中:
的选择性随温度的变化如图。其中: 的选择性
的选择性
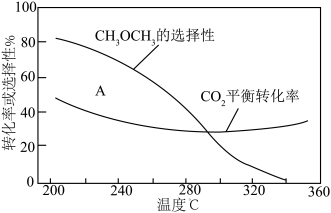
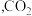 平衡转化率随温度升高而上升的原因是
平衡转化率随温度升高而上升的原因是②220℃时,在催化剂作用下
 与
与 反应一段时间后,测得
反应一段时间后,测得 的选择性为:
的选择性为: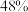 (图中
(图中 点)。不改变反应时间和温度,一定能提高
点)。不改变反应时间和温度,一定能提高 选择性的措施有:
选择性的措施有:Ⅱ.
 催化加氢法:高炉气中捕集
催化加氢法:高炉气中捕集 制
制 的综合利用示意图如图所示。
的综合利用示意图如图所示。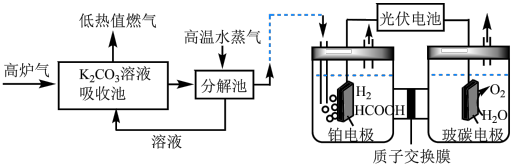
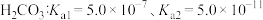 。
。(3)T℃时,当吸收池中溶液的
 时,此时该溶液中
时,此时该溶液中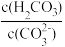 =
=(4)电解池中
 电催化还原为
电催化还原为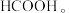
①
 在铂电极反应方程式为
在铂电极反应方程式为②铂电极上的副反应除析氢外,没有其它放电过程。若生成
 的电解效率
的电解效率 ,当电路中转移
,当电路中转移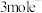 时,阴极室溶液的质量增加
时,阴极室溶液的质量增加 。定义:
。定义: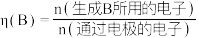
您最近一年使用:0次
3 . 根据下列各图曲线表征的信息,得出的结论不正确的是

A.图1表示常温下向体积为 的 的 溶液中逐滴加入 溶液中逐滴加入  溶液的 溶液的 变化曲线,则 变化曲线,则 点处有 点处有 |
B.图2曲线表示冰醋酸稀释过程中溶液导电能力变化,a、b、c三点对应的溶液中,醋酸电离程度最大的是 |
C.图3曲线表示 溶解度随温度变化情况,则 溶解度随温度变化情况,则 点存在 点存在  |
D.结合图4分析可知,向 含 含 均为 均为 的混合溶液中逐滴加入 的混合溶液中逐滴加入 溶液, 溶液, 先沉淀 先沉淀 |
您最近一年使用:0次
名校
解题方法
4 . 对下列事实的解释不正确 的是
| 事实 | 解释 | |
| A | NaCl溶液呈中性 | c平(H+)=c平 (OH-) |
| B | 相对分子质量相近的一元醇和烷烃相比,醇的沸点远远高于烷烃 | 醇分子中羟基的氧原子与另一醇分子羟基的氢原子间存在着氢键 |
| C | CuS的溶解程度远比ZnS的溶解程度小 | Ksp(CuS)<Ksp(ZnS) |
| D | 氮分子中的氮原子是以共价三键结合的 | 当形成氮分子的两个氮原子相互接近时,一个氮原子的2s轨道和另一个氮原子的2s轨道重叠形成一个共价键,同时它们的2px和2py轨道也会分别两两重叠形成两个共价键,进而形成共价三键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
5 . 可用解除法制硫酸产生的废钒催化剂( )制备钒(Ⅳ)。
)制备钒(Ⅳ)。
已知:钒(Ⅳ)在水溶液中存在形态与pH的关系如下。 催化
催化 和
和 反应时,反应机理如下:
反应时,反应机理如下:

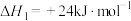
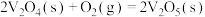
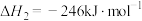
则

______ 。
(2)废钒催化剂 的一种处理方法为
的一种处理方法为 ,“还原”过程“
,“还原”过程“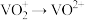 ”的离子方程式为
”的离子方程式为______ 。
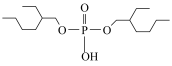
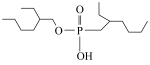
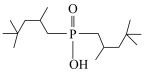
(3)三种常见的金属离子萃取剂(简写为HR)结构如下表。
①HR在煤油中以二聚体形式( )与金属离子络合,HR通过
)与金属离子络合,HR通过______ 形成 (填微粒间相互作用名称)。
(填微粒间相互作用名称)。
②在水中电离出 能力最强的是
能力最强的是______ (填“A”“B”或“C”)。
(4)25℃时, 萃取钒(Ⅳ)过程示意图如下。
萃取钒(Ⅳ)过程示意图如下。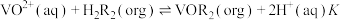 ,其中org表示有机相。
,其中org表示有机相。
已知:有机相和水相的分配比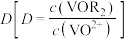 ;钒萃取率
;钒萃取率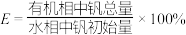 。
。
①萃取达到平衡的标志是______ (填标号)。
A.水相pH不再变化 B.水相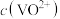 不再变化
不再变化
C.有机相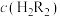 不再变化 D.分配比D不再变化
不再变化 D.分配比D不再变化
②利用NaOH溶液调节水相初始pH,pH从1调至4的过程中,E先增大后减小。结合平衡移动原理进行解释______ 。
③维持水相 ,分别测得萃取剂A、B、C的
,分别测得萃取剂A、B、C的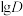 随
随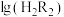 变化曲线如图。
变化曲线如图。
 )制备钒(Ⅳ)。
)制备钒(Ⅳ)。已知:钒(Ⅳ)在水溶液中存在形态与pH的关系如下。
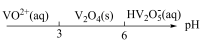
 催化
催化 和
和 反应时,反应机理如下:
反应时,反应机理如下:
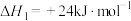
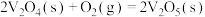
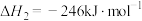
则


(2)废钒催化剂
 的一种处理方法为
的一种处理方法为 ,“还原”过程“
,“还原”过程“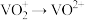 ”的离子方程式为
”的离子方程式为(3)三种常见的金属离子萃取剂(简写为HR)结构如下表。
萃取剂 | A | B | C |
结构 |
|
|
|
 )与金属离子络合,HR通过
)与金属离子络合,HR通过 (填微粒间相互作用名称)。
(填微粒间相互作用名称)。②在水中电离出
 能力最强的是
能力最强的是(4)25℃时,
 萃取钒(Ⅳ)过程示意图如下。
萃取钒(Ⅳ)过程示意图如下。
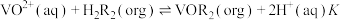 ,其中org表示有机相。
,其中org表示有机相。已知:有机相和水相的分配比
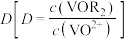 ;钒萃取率
;钒萃取率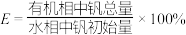 。
。①萃取达到平衡的标志是
A.水相pH不再变化 B.水相
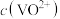 不再变化
不再变化C.有机相
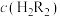 不再变化 D.分配比D不再变化
不再变化 D.分配比D不再变化②利用NaOH溶液调节水相初始pH,pH从1调至4的过程中,E先增大后减小。结合平衡移动原理进行解释
③维持水相
 ,分别测得萃取剂A、B、C的
,分别测得萃取剂A、B、C的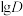 随
随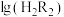 变化曲线如图。
变化曲线如图。
 代表的是萃取剂
代表的是萃取剂
您最近一年使用:0次
解题方法
6 . I 碱法脱硫。用K2CO3溶液吸收H2S。
已知:常温下,氢硫酸和碳酸的电离常数如表。
1.K2CO3溶液中微粒浓度关系正确的是___________。
2.常温下,比较等物质的量浓度的NaHS与NaHCO3溶液的pH___________ 。
A.前者大 B.后者大 C.无法比较
向某FeCl2溶液中加入一定浓度的NaHS溶液,采用分光光度法测得
[Fe2+]=8.88×10-5mol•L-1.(常温下,Ksp(FeS)=6.3×10-18)
3.计算溶液中的 =
=___________ 。
II. 热分解法脱硫。在2 L恒容密闭容器中发生反应2H2S(g) S2(g) + 2H2(g)。
S2(g) + 2H2(g)。
4.985℃时,若加入1mol H2S,经过5s达到平衡,此时H2S的转化率为40%。
则v(S2) =___________ ,该温度下K=___________ (计算结果保留两位有效数字)。
III. Fe2(SO4)3脱硫。
吸收液[Fe2(SO4)3]作用原理如下:
① H2S(g)⇌H2S(aq) ②H2S(aq) ⇌H++HS- ③HS-+2Fe3+=S↓+2Fe2++H+
一定条件下测得脱硫率与Fe3+浓度以及溶液起始pH的关系如图所示。___________ 。原因是___________ 。
6.吸收液过滤出S后,可通入空气再生,写出该反应的离子方程式并标出电子转移方向和数目。___________ 。
IV. 电化学法脱硫(如图)___________ 经负载流向电极___________ 。(均选填“A”或“B”) A极发生的电极反应式为___________ 。
已知:常温下,氢硫酸和碳酸的电离常数如表。
| 二元酸 | Ka1 | Ka2 |
| H2S | 1.1×10-7 | 7.1×10-15 |
| H2CO3 | 4.5×10-7 | 4.7×10-11 |
1.K2CO3溶液中微粒浓度关系正确的是___________。
A.[K+]= [ ]+ 2[ ]+ 2[ ] +[OH-] ] +[OH-] | B.[K+]= [ ]+[ ]+[ ] +[OH-] ] +[OH-] |
C.[K+]= 2[ ]+ 2[ ]+ 2[ ] +2[H2CO3] ] +2[H2CO3] | D.[K+]= [ ]+ [ ]+ [ ] +[H2CO3] ] +[H2CO3] |
A.前者大 B.后者大 C.无法比较
向某FeCl2溶液中加入一定浓度的NaHS溶液,采用分光光度法测得
[Fe2+]=8.88×10-5mol•L-1.(常温下,Ksp(FeS)=6.3×10-18)
3.计算溶液中的
 =
=II. 热分解法脱硫。在2 L恒容密闭容器中发生反应2H2S(g)
 S2(g) + 2H2(g)。
S2(g) + 2H2(g)。4.985℃时,若加入1mol H2S,经过5s达到平衡,此时H2S的转化率为40%。
则v(S2) =
III. Fe2(SO4)3脱硫。
吸收液[Fe2(SO4)3]作用原理如下:
① H2S(g)⇌H2S(aq) ②H2S(aq) ⇌H++HS- ③HS-+2Fe3+=S↓+2Fe2++H+
一定条件下测得脱硫率与Fe3+浓度以及溶液起始pH的关系如图所示。

6.吸收液过滤出S后,可通入空气再生,写出该反应的离子方程式并标出电子转移方向和数目。
IV. 电化学法脱硫(如图)
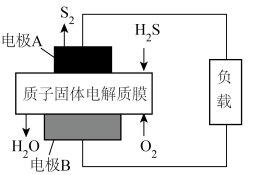
您最近一年使用:0次
名校
解题方法
7 . 下列不能用勒夏特列原理解释的事实是
| A.红棕色的NO2加压后颜色先变深后变浅 |
| B.黄绿色的氯水光照后颜色变浅 |
| C.盐碱地(含较多NaCl、Na2CO3)通过施加适量的石膏(CaSO4•H2O),可以降低土壤碱性 |
| D.500 ℃左右比室温更有利于合成氨反应 |
您最近一年使用:0次
解题方法
8 . 分银渣是从阳极泥中提取贵金属后的尾渣,含有PbSO4、BaSO4、SnO2及Au、Ag等,有较高的综合利用价值。一种从分银渣中提取有用产品流程的如下: [PbCl4]2-(aq);ⅳ中生成[AuCl4]-和[AgCl3]2-;PbSO4、PbCO3、BaSO4、BaCO3的Ksp依次为2.8×10-8、7.4×10-14、1.1×10-10、2.6×10-9。下列说法
[PbCl4]2-(aq);ⅳ中生成[AuCl4]-和[AgCl3]2-;PbSO4、PbCO3、BaSO4、BaCO3的Ksp依次为2.8×10-8、7.4×10-14、1.1×10-10、2.6×10-9。下列说法不正确 的是

 [PbCl4]2-(aq);ⅳ中生成[AuCl4]-和[AgCl3]2-;PbSO4、PbCO3、BaSO4、BaCO3的Ksp依次为2.8×10-8、7.4×10-14、1.1×10-10、2.6×10-9。下列说法
[PbCl4]2-(aq);ⅳ中生成[AuCl4]-和[AgCl3]2-;PbSO4、PbCO3、BaSO4、BaCO3的Ksp依次为2.8×10-8、7.4×10-14、1.1×10-10、2.6×10-9。下列说法A.步骤ⅰ中一定发生反应:PbSO4(s)+ (aq) (aq) PbCO3(s)+ PbCO3(s)+ (aq) (aq) |
| B.步骤ⅰ、ⅲ后需先过滤再加盐酸 |
| C.步骤ⅱ、ⅳ提取Pb(Ⅱ)、Ba2+时,均有H+和Cl-参加反应 |
| D.试剂a可为NaCl,促进Au、Ag的浸出 |
您最近一年使用:0次
2024-04-13更新
|
403次组卷
|
2卷引用:2023-2024学年海淀区第二学期期中考试高三化学试卷
名校
解题方法
9 . 劳动有利于“知行合一”。下列劳动项目与所述的化学知识没有关联的是
| 选项 | 劳动项目 | 化学知识 |
| A | 食品加工:添加维生素C做防腐剂 | 维生素C具有还原性 |
| B | 工厂实践:用饱和碳酸钠除去锅炉水垢 | 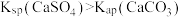 |
| C | 家务劳动:用四氯乙烯对衣物进行干洗 | 四氯乙烯属于烃的衍生物 |
| D | 学农活动:撒草木灰改良酸性土壤 | 草木灰溶液显碱性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-12更新
|
397次组卷
|
2卷引用:广东省茂名市2024届高三下学期第二次综合测试化学试卷
解题方法
10 . 探究同浓度的 与
与 溶液和不同盐溶液间的反应,①中产生白色沉淀和无色气体,②中只产生白色沉淀。(已知:碳酸铝在水溶液中不能稳定存在)
溶液和不同盐溶液间的反应,①中产生白色沉淀和无色气体,②中只产生白色沉淀。(已知:碳酸铝在水溶液中不能稳定存在)
 与
与 溶液和不同盐溶液间的反应,①中产生白色沉淀和无色气体,②中只产生白色沉淀。(已知:碳酸铝在水溶液中不能稳定存在)
溶液和不同盐溶液间的反应,①中产生白色沉淀和无色气体,②中只产生白色沉淀。(已知:碳酸铝在水溶液中不能稳定存在)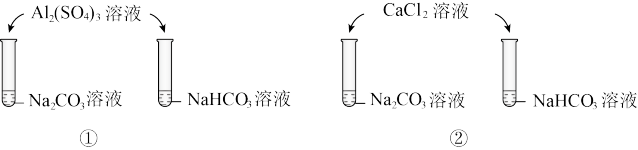
A. 能促进 能促进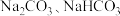 的水解 的水解 |
| B.①中沉淀可能是氢氧化铝和碱式碳酸铝中的一种或二者的混合物 |
C.同浓度的 与 与 溶液分别加入酚酞, 溶液分别加入酚酞, 溶液的红色深 溶液的红色深 |
D.②中 溶液滴入后, 溶液滴入后, 溶液的 溶液的 不变, 不变, 溶液的 溶液的 降低 降低 |
您最近一年使用:0次