解题方法
1 . 请填空:
(1)A元素L能层p电子数比s电子数多2个,A的元素符号为______ ;B元素M能层p电子数为s电子数的一半,B的元素名称为______ 。
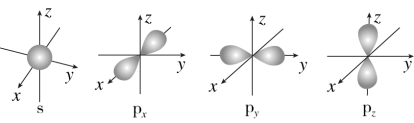
(2)下图是s能级和p能级的原子轨道图。____ 形,每个s能级有____ 个原子轨道;p电子的原子轨道呈____ 形,每个p能级有____ 个原子轨道。
(3)C元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,C的元素符号为____ ,其基态原子的核外电子排布式为______ 。
(4)常温下,向100 mL 0.01 mol⋅L HA溶液中逐滴加入0.02 mol⋅L
HA溶液中逐滴加入0.02 mol⋅L MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题。
MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题。_____ (填“强”或“弱”)酸。常温下一定浓度的MA稀溶液的 ,则a
,则a_____ (填“>”“<”或“=”)7,用离子方程式表示其原因:______ 。
(1)A元素L能层p电子数比s电子数多2个,A的元素符号为
(2)下图是s能级和p能级的原子轨道图。
(3)C元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,C的元素符号为
(4)常温下,向100 mL 0.01 mol⋅L
 HA溶液中逐滴加入0.02 mol⋅L
HA溶液中逐滴加入0.02 mol⋅L MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题。
MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题。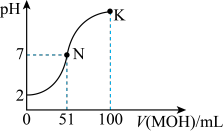
 ,则a
,则a
您最近一年使用:0次
2 . 水中存在电离平衡:H2O H++OH-。若在水中分别加入下列各物质:
H++OH-。若在水中分别加入下列各物质:
①NaOH(s) ②NH4Cl(s) ③Na2CO3(s) ④CH3COOH(l) ⑤K2SO4(s),试回答下列问题:
(1)能使水的电离平衡向左移动的是___________ ,不发生移动的是___________ 。(用序号填空)
(2)溶液呈酸性的是___________ ,溶液呈碱性的是___________ 。(用序号填空)
(3)能促进水的电离,且溶液pH>7的是___________ 。(用序号填空)
(4)将0.1mol CH3COOH溶于水制成1L溶液,此溶液的物质的量浓度为0.1mol/L,经测定溶液中c(CH3COO-)为1.4×10-3mol∙L-1,此温度下醋酸的电离常数Ka=___________ ,温度升高,Ka将___________ (填“变大”、“不变”或“变小”)。
(5)向 溶液中滴入酚酞试液,观察到的现象是
溶液中滴入酚酞试液,观察到的现象是___________ ,若微热溶液,观察到的现象是___________ ,由此证明碳酸钠的水解是___________ (填“吸热”或“放热”)反应。 溶液中
溶液中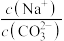
___________ 2(填“大于”或“小于”),能使其比值接近2的措施是___________ (填序号)。
①加入适量盐酸 ②加入适量NaOH固体 ③加入适量KOH固体 ④加热
 H++OH-。若在水中分别加入下列各物质:
H++OH-。若在水中分别加入下列各物质:①NaOH(s) ②NH4Cl(s) ③Na2CO3(s) ④CH3COOH(l) ⑤K2SO4(s),试回答下列问题:
(1)能使水的电离平衡向左移动的是
(2)溶液呈酸性的是
(3)能促进水的电离,且溶液pH>7的是
(4)将0.1mol CH3COOH溶于水制成1L溶液,此溶液的物质的量浓度为0.1mol/L,经测定溶液中c(CH3COO-)为1.4×10-3mol∙L-1,此温度下醋酸的电离常数Ka=
(5)向
 溶液中滴入酚酞试液,观察到的现象是
溶液中滴入酚酞试液,观察到的现象是 溶液中
溶液中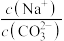
①加入适量盐酸 ②加入适量NaOH固体 ③加入适量KOH固体 ④加热
您最近一年使用:0次
3 . 图为某学生进行粗盐提纯实验时过滤操作的示意图。试回答:
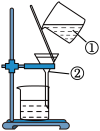
(1)写出标号仪器的名称:
①___________ ;②___________ 。
(2)漏斗中液体的液面应该___________ (填“高”或“低”)于滤纸的边缘。

(1)写出标号仪器的名称:
①
(2)漏斗中液体的液面应该
您最近一年使用:0次
4 . 关于燃烧与灭火,下列说法正确的是
| A.热油锅着火用锅盖盖灭,隔绝了氧气 | B.纸箱着火用水浇灭,降低了可燃物着火点 |
| C.室内起火,迅速打开门窗通风 | D.煤不充分燃烧有利于节约燃料 |
您最近一年使用:0次
名校
解题方法
5 . 下列说法正确的是
A.基态 原子的轨道表示式 原子的轨道表示式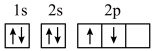 |
B.基态 原子 原子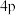 能级上有一个未成对电子 能级上有一个未成对电子 |
C.基态 原子核外电子 原子核外电子 轨道不是半充满状态 轨道不是半充满状态 |
| D.第四周期中,未成对电子数最多元素的基态原子电子填充了4个能层,7个能级 |
您最近一年使用:0次
名校
解题方法
6 . 第十九届亚运会在杭州召开,会中处处可见与化学有关的事例,下列说法正确的是
| A.亚运会吉祥物“琮踪”的设计灵感来自良渚古城遗址,古城遗址同时出土了大量陶器,陶器原料黏土的主要成分是硅酸盐 |
| B.杭州为亚运会特别推出了可充电座椅,电能属于一次能源 |
| C.本次亚运会的一个理念是节能减排,汽车尾气中含有的氮氧化物,是汽油不完全燃烧造成的 |
| D.地铁让大家的出行变得更加便利,地铁的轨道大规模应用到了金属铝 |
您最近一年使用:0次
名校
解题方法
7 . 磷的含氧酸具有重要的性质和应用。
(1) 是二元弱酸,某温度下,
是二元弱酸,某温度下, 的
的 溶液
溶液 ,即溶液中
,即溶液中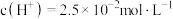 。求该温度下
。求该温度下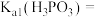
_______ 。( 的第二步电离忽略不计,结果用科学记数法表示,保留两位有效数字)
的第二步电离忽略不计,结果用科学记数法表示,保留两位有效数字)
(2) 是三元中强酸,
是三元中强酸, 时,
时, 与
与 溶液反应,反应混合物中含磷各微粒的分布分数(平衡时某微粒的浓度占微粒浓度之和的分数)与
溶液反应,反应混合物中含磷各微粒的分布分数(平衡时某微粒的浓度占微粒浓度之和的分数)与 的关系如图所示:
的关系如图所示:
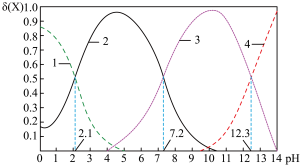
① 溶液显碱性,原因是
溶液显碱性,原因是________ ,若向溶液中加入足量的 溶液,溶液则显酸性,其原因是
溶液,溶液则显酸性,其原因是________ (用离子方程式表示)。
② 时,溶液中的
时,溶液中的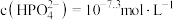 ,则
,则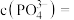
______  。
。
③ 时,溶液中由水电离出的
时,溶液中由水电离出的
______  。
。
④已知: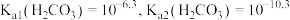 ,写出足量碳酸钠与
,写出足量碳酸钠与 反应的化学方程式:
反应的化学方程式:_______ 。
⑤以酚䣭为指示剂,当溶液由无色变为浅红色时,写出发生主要反应的离子方程:______ 。
⑥ 时,溶液中的电荷守恒关系为
时,溶液中的电荷守恒关系为_________ 。
(1)
 是二元弱酸,某温度下,
是二元弱酸,某温度下, 的
的 溶液
溶液 ,即溶液中
,即溶液中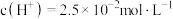 。求该温度下
。求该温度下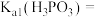
 的第二步电离忽略不计,结果用科学记数法表示,保留两位有效数字)
的第二步电离忽略不计,结果用科学记数法表示,保留两位有效数字)(2)
 是三元中强酸,
是三元中强酸, 时,
时, 与
与 溶液反应,反应混合物中含磷各微粒的分布分数(平衡时某微粒的浓度占微粒浓度之和的分数)与
溶液反应,反应混合物中含磷各微粒的分布分数(平衡时某微粒的浓度占微粒浓度之和的分数)与 的关系如图所示:
的关系如图所示:
①
 溶液显碱性,原因是
溶液显碱性,原因是 溶液,溶液则显酸性,其原因是
溶液,溶液则显酸性,其原因是②
 时,溶液中的
时,溶液中的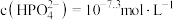 ,则
,则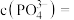
 。
。③
 时,溶液中由水电离出的
时,溶液中由水电离出的
 。
。④已知:
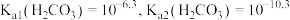 ,写出足量碳酸钠与
,写出足量碳酸钠与 反应的化学方程式:
反应的化学方程式:⑤以酚䣭为指示剂,当溶液由无色变为浅红色时,写出发生主要反应的离子方程:
⑥
 时,溶液中的电荷守恒关系为
时,溶液中的电荷守恒关系为
您最近一年使用:0次
解题方法
8 . 氢氧燃料电池(构造示意图如图)单位质量输出电能较高,可以用于载人航天工程,反应生成的水可作为航天员的饮用水,氧气可以作为备用氧源供给航天员呼吸。
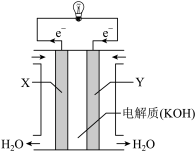
(1)判断Y极为电池的_______ 极,发生_______ 反应。
(2)X电极的电极反应式为_______ 。
(3)若电解质更换为以稀硫酸为电解质,则X电极的电极反应式为_______ 。
(4)Y电极的电极反应式为_______ 。

(1)判断Y极为电池的
(2)X电极的电极反应式为
(3)若电解质更换为以稀硫酸为电解质,则X电极的电极反应式为
(4)Y电极的电极反应式为
您最近一年使用:0次
解题方法
9 . 如图所示装置是二甲醚( )燃料电池,已知该装置工作时电子从b极流出,a极流入。
)燃料电池,已知该装置工作时电子从b极流出,a极流入。_______ 极(填“正”或“负”)。
(2)A池中a电极反应式为_______ 。
(3)A池中b电极反应式为_______ 。
(4)当装置A中消耗0.25mol二甲醚时,此时转移的电子的物质的量为_______ ;
(5)装置A中溶液的pH会_______ (填写“增大”“减小”或“不变”)。
 )燃料电池,已知该装置工作时电子从b极流出,a极流入。
)燃料电池,已知该装置工作时电子从b极流出,a极流入。
(2)A池中a电极反应式为
(3)A池中b电极反应式为
(4)当装置A中消耗0.25mol二甲醚时,此时转移的电子的物质的量为
(5)装置A中溶液的pH会
您最近一年使用:0次
2024-01-03更新
|
118次组卷
|
2卷引用:内蒙古呼伦贝尔市满洲里远方中学2023-2024学年高三上学期期末考试化学试卷
10 . 已知有机物A由C、H、O三种元素组成,取1mol充分燃烧生成4molCO2和54gH2O,A的相对分子质量为86,回答下列问题:
(1)A物质的分子式是___________ 。
(2)A物质符合下列条件:
①能与溴的四氯化碳溶液发生反应使其褪色 ②能与NaHCO3溶液反应放出CO2气体
③分子中没有支链,且有一个-CH3
则A分子中含氧官能团的名称是___________ ,A分子的结构简式是___________ 。
(3)写出下列反应方程式与反应类型:
①A与NaOH反应___________
②A与乙醇和浓硫酸混合加热___________ ,反应类型___________ 。
(4)A在一定条件下反应生成B,与B互为同分异构体,且与乙酸互为同系物的D的结构简式为___________ 。
(5)1mol D与足量NaHCO3溶液反应,生成的气体在标况下的体积是___________ 。
(1)A物质的分子式是
(2)A物质符合下列条件:
①能与溴的四氯化碳溶液发生反应使其褪色 ②能与NaHCO3溶液反应放出CO2气体
③分子中没有支链,且有一个-CH3
则A分子中含氧官能团的名称是
(3)写出下列反应方程式与反应类型:
①A与NaOH反应
②A与乙醇和浓硫酸混合加热
(4)A在一定条件下反应生成B,与B互为同分异构体,且与乙酸互为同系物的D的结构简式为
(5)1mol D与足量NaHCO3溶液反应,生成的气体在标况下的体积是
您最近一年使用:0次



