解题方法
1 . 下列除去物质中的少量杂质(括号内为杂质),选用的试剂正确的是
| 选项 | 物质 | 除杂试剂 |
| A | N2(O2) | 灼热的CuO |
| B | CO2(HCl) | 足量Na2CO3溶液 |
| C | FeCl2溶液(FeCl3) | 足量铁屑 |
| D | KCl溶液(MgCl2) | 适量NaOH溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 下列离子在溶液中因发生氧化还原反应而不能大量共存的是
A.H+、 、Fe2+、Na+ 、Fe2+、Na+ | B.Ag+、 、Cl-、K+ 、Cl-、K+ |
C.K+、Ba2+、OH-、 | D.Cu2+、 、Br-、OH- 、Br-、OH- |
您最近一年使用:0次
3 . 反应 可用于捕捉废气中的CO2,下列有关说法错误的是
可用于捕捉废气中的CO2,下列有关说法错误的是
 可用于捕捉废气中的CO2,下列有关说法错误的是
可用于捕捉废气中的CO2,下列有关说法错误的是A.中子数为8的氧原子: | B.Na2CO3不能一步制备NaOH |
| C.CO2的空间结构为直线形 | D.H2O中不含有非极性键 |
您最近一年使用:0次
4 . 将表面已完全钝化的铝条,插入下列溶液中,不会发生反应的是
| A.稀硫酸 | B.稀盐酸 | C.硫酸铜 | D.氢氧化钠 |
您最近一年使用:0次
5 . 下列各组物质熔化或升华时,所克服的粒子间作用力不属于同种类型的是
| A.冰和金刚石的熔化 | B.碘和干冰升华 |
C. 和 和 (苯)的熔化 (苯)的熔化 | D.碳化硅与单晶硅的熔化 |
您最近一年使用:0次
2024-05-09更新
|
41次组卷
|
2卷引用:黑龙江省绥化市绥棱县第一中学2023-2024学年高二下学期开学化学试题
6 . 砷化镓(GaAs)是一种重要的半导体材料。回答下列问题:
(1)基态砷原子的电子排布式为___________ ,电子的自旋有顺时针、逆时针两种方向,分别用自旋量子数 、
、 表示,则该原子中两种自旋量子数的代数和为
表示,则该原子中两种自旋量子数的代数和为___________ 。
(2)砷、镓与硒位于同一周期,三者电负性由大到小的顺序为___________ (用元素符号表示)。
(3)如图,a、b、c、d、e分别代表与镓同周期第一电离能较大的前五种元素(Kr元素除外),则c对应的原子序数为___________ ,d对应的元素是___________ (填元素符号),镓的电离能 、
、 、
、 、
、 …前四个电离能中,相邻两电离能之差最大的是
…前四个电离能中,相邻两电离能之差最大的是___________ 。上述五种元素中原子序数较大的两种元素形成的氢化物稳定性较强的是___________ (填分子式)。
(1)基态砷原子的电子排布式为
 、
、 表示,则该原子中两种自旋量子数的代数和为
表示,则该原子中两种自旋量子数的代数和为(2)砷、镓与硒位于同一周期,三者电负性由大到小的顺序为
(3)如图,a、b、c、d、e分别代表与镓同周期第一电离能较大的前五种元素(Kr元素除外),则c对应的原子序数为
 、
、 、
、 、
、 …前四个电离能中,相邻两电离能之差最大的是
…前四个电离能中,相邻两电离能之差最大的是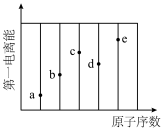
您最近一年使用:0次
解题方法
7 . 磷的单质及其化合物在生产、生活中具有广泛应用。回答下列问题:
(1)基态磷原子价电子排布式为___________ ,核外电子占据的最高能级的电子云轮廓图为___________ 形。
(2)第三周期元素中第一电离能介于硅和磷之间的元素为___________ (填元素符号),离子半径:
___________ (填“>”“<”或“=”) 。
。
(3) 固体属于
固体属于___________ 晶体,键能: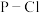
___________ (填“>”“<”或“=”) ,
, 、
、 中键角较大的是
中键角较大的是___________ 。
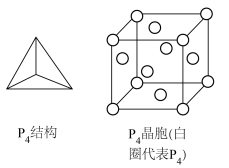
(4)白磷的分子结构及其晶胞结构如图所示,晶胞参数为 。
。 中磷原子的杂化方式为
中磷原子的杂化方式为___________ 。
②白磷晶体中,距离一个 最近的
最近的 个数为
个数为___________ 。
③该晶体的密度=___________  (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(1)基态磷原子价电子排布式为
(2)第三周期元素中第一电离能介于硅和磷之间的元素为

 。
。(3)
 固体属于
固体属于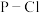
 ,
, 、
、 中键角较大的是
中键角较大的是(4)白磷的分子结构及其晶胞结构如图所示,晶胞参数为
 。
。
 中磷原子的杂化方式为
中磷原子的杂化方式为②白磷晶体中,距离一个
 最近的
最近的 个数为
个数为③该晶体的密度=
 (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
8 . 下表中列出几种常见元素的电负性数值,根据表中数据推断下列结论正确的是
| 元素 | Na | Mg | Al | Si | P | S | Cl |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.8 | 2.1 | 2.5 | 3.0 |
A. 的电负性小于 的电负性小于 的 的 |
B. 的电负性数值大于 的电负性数值大于 |
| C.同周期元素电负性越大,金属性越强 |
| D.电负性数值在1.8左右的元素既有金属性又有非金属性 |
您最近一年使用:0次
9 . 下列有关说法中正确的是
A.电子易从 跃迁到 跃迁到 上 上 |
| B.电子只有获得能量后才能发生跃迁 |
C.核外电子排布式为 的碳原子能产生发射光谱 的碳原子能产生发射光谱 |
| D.灼烧含钠元素物质时,产生黄光过程中相应电子的能量会升高 |
您最近一年使用:0次
名校
解题方法
10 . 科学研究表明: 存储能量的能力是
存储能量的能力是 的12000倍左右,在大气中的寿命可达740年,如表所示是几种化学键的键能(断裂或形成1mol化学键时吸收或释放的热量)
的12000倍左右,在大气中的寿命可达740年,如表所示是几种化学键的键能(断裂或形成1mol化学键时吸收或释放的热量)
回答下列问题:
(1)①过程
___________ (填“吸收”或“放出”)能量。
②反应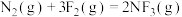
 =
=___________ 。
(2)已知:
①
 ;
;
②
 。
。
现有2mol由炭粉和氢气组成的悬浮气,在足量氧气中完全燃烧生成 (g)和
(g)和 (l),共放出679.0kJ的热量,则2mol悬浮气中C与
(l),共放出679.0kJ的热量,则2mol悬浮气中C与 的物质的量之比为
的物质的量之比为___________ 。
(3)电石( )可通过下列反应制备:
)可通过下列反应制备:
①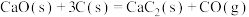
 ;
;
②
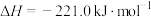 。
。
若不考虑热量损耗,物料转化率均为100%,最终炉中出来的气体只有CO。则为了维持热量平衡,每生产64g ,投料的量为56g CaO及
,投料的量为56g CaO及___________ mol C、___________ mol  。
。
 存储能量的能力是
存储能量的能力是 的12000倍左右,在大气中的寿命可达740年,如表所示是几种化学键的键能(断裂或形成1mol化学键时吸收或释放的热量)
的12000倍左右,在大气中的寿命可达740年,如表所示是几种化学键的键能(断裂或形成1mol化学键时吸收或释放的热量)| 化学键 | N≡N | F—F | N—F |
键能( ) ) | 946 | 154 | 283 |
(1)①过程

②反应
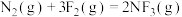
 =
=(2)已知:
①

 ;
;②

 。
。现有2mol由炭粉和氢气组成的悬浮气,在足量氧气中完全燃烧生成
 (g)和
(g)和 (l),共放出679.0kJ的热量,则2mol悬浮气中C与
(l),共放出679.0kJ的热量,则2mol悬浮气中C与 的物质的量之比为
的物质的量之比为(3)电石(
 )可通过下列反应制备:
)可通过下列反应制备:①
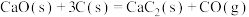
 ;
;②

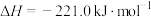 。
。若不考虑热量损耗,物料转化率均为100%,最终炉中出来的气体只有CO。则为了维持热量平衡,每生产64g
 ,投料的量为56g CaO及
,投料的量为56g CaO及 。
。
您最近一年使用:0次
2024-05-07更新
|
184次组卷
|
2卷引用:黑龙江省绥化市绥棱县第一中学2023-2024学年高一下学期4月月考化学试题



