1 . 某化学实验室需要240ml0.5mol·L-1的稀硫酸,现欲用 的浓硫酸配制,填空并回答下列问题:
的浓硫酸配制,填空并回答下列问题:
(1)通过计算确定量取_______ mL浓硫酸。可以选用下列哪种规格量筒_______ 。
A. B.
B. C.
C. D.
D.
(2)在配制的过程中一定不需要使用到的仪器是_______ (填序号),还缺少的仪器有_______
A.烧杯 B.托盘天平 C.玻璃棒 D.量筒 E.胶头滴管
(3)下列关于容量瓶的使用方法中,正确的是_______。
(4)在横线上填写下列各种情况对所配制溶液浓度的影响(偏高、偏低、无影响)。
①定容时俯视刻度线_______ ;
②容量瓶用蒸馏水洗涤后残留有少量的水_______ 。
 的浓硫酸配制,填空并回答下列问题:
的浓硫酸配制,填空并回答下列问题:(1)通过计算确定量取
A.
 B.
B. C.
C. D.
D.
(2)在配制的过程中一定不需要使用到的仪器是
A.烧杯 B.托盘天平 C.玻璃棒 D.量筒 E.胶头滴管
(3)下列关于容量瓶的使用方法中,正确的是_______。
| A.使用前要检验是否漏水 | B.在容量瓶中直接溶解固体或稀释液体 |
| C.溶液未经冷却即注入容量瓶中 | D.向容量瓶中转移溶液要用玻璃棒引流 |
①定容时俯视刻度线
②容量瓶用蒸馏水洗涤后残留有少量的水
您最近一年使用:0次
解题方法
2 . 水的电离过程为H2O OH++OH-。在25℃、35℃时水的离子积常数分别为1.0×10-14、2.1×10-14。下列叙述正确的是
OH++OH-。在25℃、35℃时水的离子积常数分别为1.0×10-14、2.1×10-14。下列叙述正确的是
 OH++OH-。在25℃、35℃时水的离子积常数分别为1.0×10-14、2.1×10-14。下列叙述正确的是
OH++OH-。在25℃、35℃时水的离子积常数分别为1.0×10-14、2.1×10-14。下列叙述正确的是| A.水的电离是放热过程 | B.水的电离度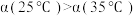 |
C.在35℃时,纯水中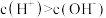 | D.纯水中 随着温度的升高而增大 随着温度的升高而增大 |
您最近一年使用:0次
2024-03-20更新
|
62次组卷
|
4卷引用:黑龙江省哈尔滨师范大学青冈实验中学2023-2024学年高二上学期期中考试化学试题
3 . 某化学兴趣小组为制取较为纯净、干燥的氯气设计了如下实验装置:其中A是氯气发生仪器,B、C为气体净化装置(B中装有饱和食盐水,C中装有浓硫酸),D为干燥的空广口瓶,烧杯E中装有氢氧化钠溶液。
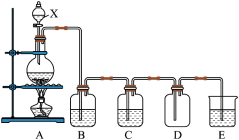
请回答下列问题:
(1)装置D中收集到的氯气在通常情况下呈_______ 色的有毒气体。
(2)B装置的作用是_______ ;C装置的作用是_______ ;E装置中发生反应的化学方程式_______ 。
(3)实验室制氯气的反应原理的方程式为_______ 请指出反应中的氧化剂_______ ,还原剂_______ 。

请回答下列问题:
(1)装置D中收集到的氯气在通常情况下呈
(2)B装置的作用是
(3)实验室制氯气的反应原理的方程式为
您最近一年使用:0次
4 . 离子反应是中学化学中重要的反应类型,回答下列问题:
(1)某工业废水中存在大量的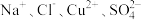 ,欲除去其中的
,欲除去其中的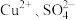 ,设计提纯流程如图所示:
,设计提纯流程如图所示:
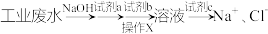
①试剂b溶液为_______ (化学式),试剂c溶液为_______ (化学式)。
②操作X为_______ 。
(2)将两种盐混合后溶于水得到一种无色透明溶液,溶液中含有下列离子中的某些离子:H+、Na+、Mg2+、Cu2+、Ba2+、SO 、CO
、CO 和Cl-,取该溶液进行如下实验:
和Cl-,取该溶液进行如下实验:
I.取少量溶液滴入紫色石蕊溶液,溶液呈红色。
Ⅱ.取少许溶液滴入过量的Ba(OH)2溶液,有白色沉淀产生。过滤,向沉淀中加入足量稀硝酸,沉淀不溶解。
Ⅲ.取步骤Ⅱ中滤液少许,先滴加硝酸酸化,再滴加AgNO3溶液,产生白色沉淀。
①根据以上现象判断,两种盐的混合溶液中肯定不存在的离子是_____ ;两种盐分别是______ 。
②写出反应的离子方程式:
实验Ⅱ中滴入过量的Ba(OH)2溶液:_______ ;
实验Ⅲ中:_______ 。
(1)某工业废水中存在大量的
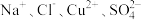 ,欲除去其中的
,欲除去其中的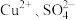 ,设计提纯流程如图所示:
,设计提纯流程如图所示: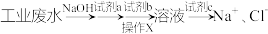
①试剂b溶液为
②操作X为
(2)将两种盐混合后溶于水得到一种无色透明溶液,溶液中含有下列离子中的某些离子:H+、Na+、Mg2+、Cu2+、Ba2+、SO
 、CO
、CO 和Cl-,取该溶液进行如下实验:
和Cl-,取该溶液进行如下实验:I.取少量溶液滴入紫色石蕊溶液,溶液呈红色。
Ⅱ.取少许溶液滴入过量的Ba(OH)2溶液,有白色沉淀产生。过滤,向沉淀中加入足量稀硝酸,沉淀不溶解。
Ⅲ.取步骤Ⅱ中滤液少许,先滴加硝酸酸化,再滴加AgNO3溶液,产生白色沉淀。
①根据以上现象判断,两种盐的混合溶液中肯定不存在的离子是
②写出反应的离子方程式:
实验Ⅱ中滴入过量的Ba(OH)2溶液:
实验Ⅲ中:
您最近一年使用:0次
5 . I.现有9种物质:①Na;②盐酸;③ ;④
;④ ;⑤空气;⑥
;⑤空气;⑥ ;⑦
;⑦ 胶体;⑧Na2O2;⑨CO
胶体;⑧Na2O2;⑨CO
(1)属于电解质的是_______ (用序号填空,下同);属于酸性氧化物的是_______ 。
(2)实验室中少量①通常保存在_____ 中;④在工业上大量用于_____ (写出一种用途即可)。
(3)⑧与⑥反应的化学方程式_______
(4)③是一种白色晶体,因受热易分解并产生气体适宜作膨松剂,请写出此物质受热分解的化学方程式_______ 。
Ⅱ.某种飞船以联氨 和
和 为动力源,发生反应:
为动力源,发生反应: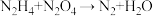 ,反应温度可高达
,反应温度可高达 ,回答下列问题。
,回答下列问题。
(5)①配平该方程式_______ 。
②该反应中,氧化产物与还原产物的质量之比为_______ 。
 ;④
;④ ;⑤空气;⑥
;⑤空气;⑥ ;⑦
;⑦ 胶体;⑧Na2O2;⑨CO
胶体;⑧Na2O2;⑨CO(1)属于电解质的是
(2)实验室中少量①通常保存在
(3)⑧与⑥反应的化学方程式
(4)③是一种白色晶体,因受热易分解并产生气体适宜作膨松剂,请写出此物质受热分解的化学方程式
Ⅱ.某种飞船以联氨
 和
和 为动力源,发生反应:
为动力源,发生反应: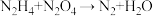 ,反应温度可高达
,反应温度可高达 ,回答下列问题。
,回答下列问题。(5)①配平该方程式
②该反应中,氧化产物与还原产物的质量之比为
您最近一年使用:0次
6 . 下列离子方程式正确的是
A.碳酸钙和盐酸反应:CO +2H+=H2O+CO2↑ +2H+=H2O+CO2↑ |
B.向氢氧化钡溶液中加硫酸:Ba2++SO =BaSO4↓ =BaSO4↓ |
| C.向稀盐酸中加铁:3Fe+6H+=3Fe3++3H2↑ |
D.用小苏打治疗胃酸过多: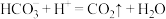 |
您最近一年使用:0次
解题方法
7 . 下列各组离子在无色透明水溶液中能大量共存的是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次
8 . 下列说法不正确的是
| A.过氧化钠可在呼吸面具或潜水艇中作为氧气的来源 |
| B.漂白粉既可作漂白棉、麻、纸张的漂白剂,又可用作游泳池等场所的消毒剂 |
| C.金属钠着火时,可用干燥的细沙覆盖灭火 |
| D.钠切开后,光亮的表面迅速变暗,是因为生成了Na2O2 |
您最近一年使用:0次
9 . Ⅰ.某温度时,在一个容积为2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图1所示。根据图中数据,填写下列空白。

(1)该反应的化学方程式为________________________________________ 。
(2)反应开始至2 min,气体Z的平均反应速率v(Z)=________ 。
(3)若X、Y、Z均为气体,反应达到平衡时:
①压强是开始时的________ 倍。
②若此时将容器的体积缩小为原来的 ,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为
,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为________ (填“放热”或“吸热”)反应。
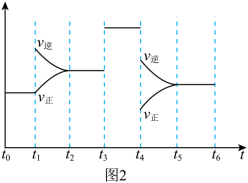
(4)上述反应在t1~t6内反应速率与时间图象如图2所示,在每一时刻均改变一个影响反应速率的因素,则下列说法正确的是 (填字母)。
Ⅱ.已知水溶液中c(H+)和c(OH-)的关系如图所示:
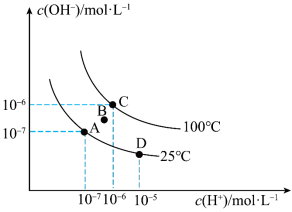
(5)图中B点水的离子积常数___________ 10-12(填“>”、“=”或“<”)。
(6)从A点到D点,可采取的措施是___________ 。
a.升温 b.加入少量盐酸 c.降温 d.加入少量NaOH
(7)100℃时,pH=2的盐酸中水电离产生的H+浓度为___________ mol/L。
(8)25℃时,将pH=12的NaOH溶液与pH=3的H2SO4溶液混合,若所得混合溶液pH=7,则NaOH溶液与H2SO4溶液的体积比为___________ 。

(1)该反应的化学方程式为
(2)反应开始至2 min,气体Z的平均反应速率v(Z)=
(3)若X、Y、Z均为气体,反应达到平衡时:
①压强是开始时的
②若此时将容器的体积缩小为原来的
 ,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为
,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为(4)上述反应在t1~t6内反应速率与时间图象如图2所示,在每一时刻均改变一个影响反应速率的因素,则下列说法正确的是 (填字母)。

| A.在t1时增大了压强 | B.B.在t3时加入催化剂 |
| C.在t4时降低了温度 | D.t2~t3时X的转化率最高 |
Ⅱ.已知水溶液中c(H+)和c(OH-)的关系如图所示:

(5)图中B点水的离子积常数
(6)从A点到D点,可采取的措施是
a.升温 b.加入少量盐酸 c.降温 d.加入少量NaOH
(7)100℃时,pH=2的盐酸中水电离产生的H+浓度为
(8)25℃时,将pH=12的NaOH溶液与pH=3的H2SO4溶液混合,若所得混合溶液pH=7,则NaOH溶液与H2SO4溶液的体积比为
您最近一年使用:0次
10 . Ⅰ.下列物质① 、 ②
、 ② 、③NaOH、④
、③NaOH、④ 、⑤
、⑤ 、⑥
、⑥ 、⑦
、⑦ 、⑧
、⑧ 、⑨Fe、⑩氯化钠溶液
、⑨Fe、⑩氯化钠溶液
(1)向⑦的溶液中滴加几滴浓盐酸,平衡______ 移动(填“正向”、“逆向”或“不移动”),平衡时溶液中c(H+)______ (填“增大”、“减小”或者“不变”),
______ (填“增大”、“减小”或者“不变”)。
(2)将 的①溶液和
的①溶液和 的③溶液等体积混合后溶液显酸性,原因是
的③溶液等体积混合后溶液显酸性,原因是_____________ (结合有关离子方程式说明)。
(3)将标准状况下2.24L⑥缓慢通入1L0.15mol/L的③的溶液中,气体被充分吸收,离子浓度大小关系____________ 。
(4)将足量⑥缓慢通入1L0.15mol/L的③的溶液中,所得溶液显碱性,则溶液中水电离出的氢氧根离子浓度_________ 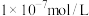 (填“大于”、“小于”、或“等于”),加水稀释后pH
(填“大于”、“小于”、或“等于”),加水稀释后pH_________ 填“增大”、“减小”、或“不变”)。
Ⅱ.常温下,向20mL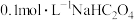 溶液中缓慢滴加pH=13的NaOH溶液,混合溶液的温度与滴加NaOH溶液体积的关系如图2所示。
溶液中缓慢滴加pH=13的NaOH溶液,混合溶液的温度与滴加NaOH溶液体积的关系如图2所示。
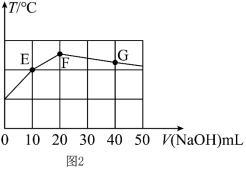
(5)试分析图中E、F、G三点,水的电离程度最大的是_________ 点。
(6)下列关系式正确的是_________ (填字母)。
a.E点存在: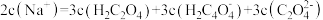
b.F点存在:
c.G点对应的溶液中:
 、 ②
、 ② 、③NaOH、④
、③NaOH、④ 、⑤
、⑤ 、⑥
、⑥ 、⑦
、⑦ 、⑧
、⑧ 、⑨Fe、⑩氯化钠溶液
、⑨Fe、⑩氯化钠溶液(1)向⑦的溶液中滴加几滴浓盐酸,平衡

(2)将
 的①溶液和
的①溶液和 的③溶液等体积混合后溶液显酸性,原因是
的③溶液等体积混合后溶液显酸性,原因是(3)将标准状况下2.24L⑥缓慢通入1L0.15mol/L的③的溶液中,气体被充分吸收,离子浓度大小关系
(4)将足量⑥缓慢通入1L0.15mol/L的③的溶液中,所得溶液显碱性,则溶液中水电离出的氢氧根离子浓度
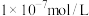 (填“大于”、“小于”、或“等于”),加水稀释后pH
(填“大于”、“小于”、或“等于”),加水稀释后pHⅡ.常温下,向20mL
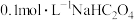 溶液中缓慢滴加pH=13的NaOH溶液,混合溶液的温度与滴加NaOH溶液体积的关系如图2所示。
溶液中缓慢滴加pH=13的NaOH溶液,混合溶液的温度与滴加NaOH溶液体积的关系如图2所示。
(5)试分析图中E、F、G三点,水的电离程度最大的是
(6)下列关系式正确的是
a.E点存在:
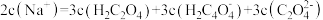
b.F点存在:

c.G点对应的溶液中:

您最近一年使用:0次



