名校
1 . 用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A:4HCl(g)+O2(g)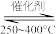 2Cl2(g)+2H2O(g) △H=-115.6kJ/mol,可实现氯的循环利用。
2Cl2(g)+2H2O(g) △H=-115.6kJ/mol,可实现氯的循环利用。
(1)HCl的电子式是_______ 。
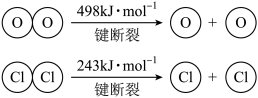
(2)已知:_______ kJ。
(3)4HCl(g)+O2(g)⇌2Cl2(g)+2H2O(g)在不同条件下的化学反应速率如下,请比较上述4种情况下反应速率的大小_______。(由大到小的顺序)
(4)Cl2可用氯碱工业(电解精制饱和食盐水)的方法制得。为提高原料的利用率,节能降耗。设计如图所示工艺流程,其中氯碱工业装置中的电极未标出。 及泥沙,得到纯净的NaCl,可将粗盐溶于水,正确的操作步骤的顺序是
及泥沙,得到纯净的NaCl,可将粗盐溶于水,正确的操作步骤的顺序是_______ (填序号)。
a.过滤;b.加过量NaOH溶液;c.加适量盐酸;d.加过量Na2CO3溶液;e.加过量BaCl2溶液
A.adabec B.abedac C.abdec D.dbe
②电解饱和食盐水的化学方程式为_______ 。
③下列生产措施有利于提高氯碱工业中的Cl2产量、降低阳极O2含量的是_______ 。
A.定期检查并更换阳离子交换膜
B.向阳极区加入适量盐酸
C.使用精制饱和食盐水提高c(Cl-)
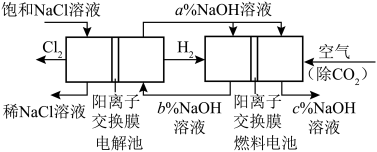
④流程中NaOH溶液的质量分数a%、b%、c%,由大到小的顺序为_______ 。
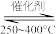 2Cl2(g)+2H2O(g) △H=-115.6kJ/mol,可实现氯的循环利用。
2Cl2(g)+2H2O(g) △H=-115.6kJ/mol,可实现氯的循环利用。(1)HCl的电子式是
(2)已知:
(3)4HCl(g)+O2(g)⇌2Cl2(g)+2H2O(g)在不同条件下的化学反应速率如下,请比较上述4种情况下反应速率的大小_______。(由大到小的顺序)
| A.v(HCl)=1.0mol·L-1·min-1 | B.v(O2)=0.1mol·L-1·s-1 |
| C.v(Cl2)=1.8mol·L-1·min-1 | D.v(H2O)=0.6mol·L-1·min-1 |
(4)Cl2可用氯碱工业(电解精制饱和食盐水)的方法制得。为提高原料的利用率,节能降耗。设计如图所示工艺流程,其中氯碱工业装置中的电极未标出。
 及泥沙,得到纯净的NaCl,可将粗盐溶于水,正确的操作步骤的顺序是
及泥沙,得到纯净的NaCl,可将粗盐溶于水,正确的操作步骤的顺序是a.过滤;b.加过量NaOH溶液;c.加适量盐酸;d.加过量Na2CO3溶液;e.加过量BaCl2溶液
A.adabec B.abedac C.abdec D.dbe
②电解饱和食盐水的化学方程式为
③下列生产措施有利于提高氯碱工业中的Cl2产量、降低阳极O2含量的是
A.定期检查并更换阳离子交换膜
B.向阳极区加入适量盐酸
C.使用精制饱和食盐水提高c(Cl-)
④流程中NaOH溶液的质量分数a%、b%、c%,由大到小的顺序为
您最近一年使用:0次
名校
解题方法
2 . 某处工厂排出的烟道气中含氮氧化物(主要为NO、 )、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图:
)、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图: 混合气体按一定比例被
混合气体按一定比例被 溶液完全吸收生成
溶液完全吸收生成 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式______________ ;若反应后尾气无残留,则参加反应的 、NO物质的量比值为
、NO物质的量比值为_____ (填字母)。
a.≥1 b.≤1 c.任意值
(2)可使用适量酸性 溶液,将溶液中的
溶液,将溶液中的 全部氧化为
全部氧化为 ,发生反应的离子方程式是
,发生反应的离子方程式是_______________ 。
(3)气囊用来储存处理后气体,其中可能含少量NO气体,可用酸性 溶液来处理。
溶液来处理。 氧化NO生成
氧化NO生成 和
和 ,发生反应的离子方程式是
,发生反应的离子方程式是_______________ 。
(4)有氧条件下,NO在催化剂作用下可被 还原为
还原为 。在钒基催化剂
。在钒基催化剂 作用下的脱硝反应机理如图所示:
作用下的脱硝反应机理如图所示: 在有氧条件下的总化学方程式是
在有氧条件下的总化学方程式是___________ 。
(5)羟基自由基( )也可以用于脱硫脱硝。如图表示光催化氧化技术可生成
)也可以用于脱硫脱硝。如图表示光催化氧化技术可生成 ﹔光照时,价带失去电子产生有强氧化性的空穴,价带上
﹔光照时,价带失去电子产生有强氧化性的空穴,价带上 直接转化为
直接转化为 ;描述产生
;描述产生 的另一种过程:
的另一种过程:______________ 。 等杂质,可以采用
等杂质,可以采用 测定含量。称取
测定含量。称取 该亚硝酸钠产品溶于水配制成
该亚硝酸钠产品溶于水配制成 的样品溶液。取
的样品溶液。取 该样品溶液于锥形瓶中,用稀
该样品溶液于锥形瓶中,用稀 酸化后,再向锥形瓶中滴加
酸化后,再向锥形瓶中滴加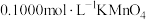 溶液,至恰好完全反应时,消耗
溶液,至恰好完全反应时,消耗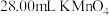 溶液。计算该产品中
溶液。计算该产品中 的质量分数
的质量分数__________ 。(写出计算过程)
 )、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图:
)、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图: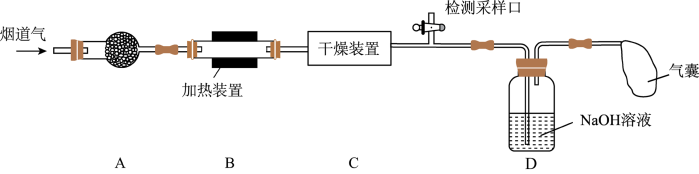
 混合气体按一定比例被
混合气体按一定比例被 溶液完全吸收生成
溶液完全吸收生成 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式 、NO物质的量比值为
、NO物质的量比值为a.≥1 b.≤1 c.任意值
(2)可使用适量酸性
 溶液,将溶液中的
溶液,将溶液中的 全部氧化为
全部氧化为 ,发生反应的离子方程式是
,发生反应的离子方程式是(3)气囊用来储存处理后气体,其中可能含少量NO气体,可用酸性
 溶液来处理。
溶液来处理。 氧化NO生成
氧化NO生成 和
和 ,发生反应的离子方程式是
,发生反应的离子方程式是(4)有氧条件下,NO在催化剂作用下可被
 还原为
还原为 。在钒基催化剂
。在钒基催化剂 作用下的脱硝反应机理如图所示:
作用下的脱硝反应机理如图所示: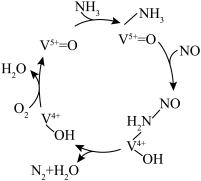
 在有氧条件下的总化学方程式是
在有氧条件下的总化学方程式是(5)羟基自由基(
 )也可以用于脱硫脱硝。如图表示光催化氧化技术可生成
)也可以用于脱硫脱硝。如图表示光催化氧化技术可生成 ﹔光照时,价带失去电子产生有强氧化性的空穴,价带上
﹔光照时,价带失去电子产生有强氧化性的空穴,价带上 直接转化为
直接转化为 ;描述产生
;描述产生 的另一种过程:
的另一种过程: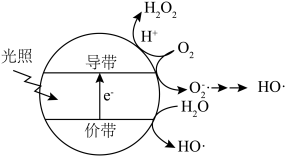
 等杂质,可以采用
等杂质,可以采用 测定含量。称取
测定含量。称取 该亚硝酸钠产品溶于水配制成
该亚硝酸钠产品溶于水配制成 的样品溶液。取
的样品溶液。取 该样品溶液于锥形瓶中,用稀
该样品溶液于锥形瓶中,用稀 酸化后,再向锥形瓶中滴加
酸化后,再向锥形瓶中滴加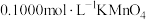 溶液,至恰好完全反应时,消耗
溶液,至恰好完全反应时,消耗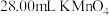 溶液。计算该产品中
溶液。计算该产品中 的质量分数
的质量分数
您最近一年使用:0次
2024-05-03更新
|
256次组卷
|
3卷引用:03 2024年苏州昆山中学高一3月月考
解题方法
3 . 废弃物的综合利用有利于节约资源、保护环境。实验室利用废旧电池的铜帽(Cu、Zn总含量约为99%)制备 和
和 的部分实验步骤如下:
的部分实验步骤如下: ”步骤中,为加快溶解速率,可采取的措施是
”步骤中,为加快溶解速率,可采取的措施是___________ 。(任写一种方法)。
(2)从“滤液 ”中提取
”中提取 的实验步骤依次为
的实验步骤依次为___________ 、过滤、冰水洗涤、低温干燥,其中冰水洗涤晶体的目的是___________ 。
(3)在“溶解 ”步骤中,发生反应的化学方程式为
”步骤中,发生反应的化学方程式为___________ 。
(4)为测定产品中 的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000
的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000
 溶液至刚好完全反应,消耗
溶液至刚好完全反应,消耗 溶液25.00mL。
溶液25.00mL。
已知: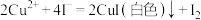 ,
, 。请依据实验数据计算样品中
。请依据实验数据计算样品中 的质量分数
的质量分数___________ (写出计算过程,结果保留2位小数)。
 和
和 的部分实验步骤如下:
的部分实验步骤如下: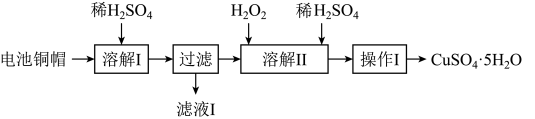
 ”步骤中,为加快溶解速率,可采取的措施是
”步骤中,为加快溶解速率,可采取的措施是(2)从“滤液
 ”中提取
”中提取 的实验步骤依次为
的实验步骤依次为(3)在“溶解
 ”步骤中,发生反应的化学方程式为
”步骤中,发生反应的化学方程式为(4)为测定产品中
 的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000
的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000
 溶液至刚好完全反应,消耗
溶液至刚好完全反应,消耗 溶液25.00mL。
溶液25.00mL。已知:
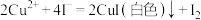 ,
, 。请依据实验数据计算样品中
。请依据实验数据计算样品中 的质量分数
的质量分数
您最近一年使用:0次
名校
4 . 硫化物含硫量的测定、脱硫是极具价值的重要课题。
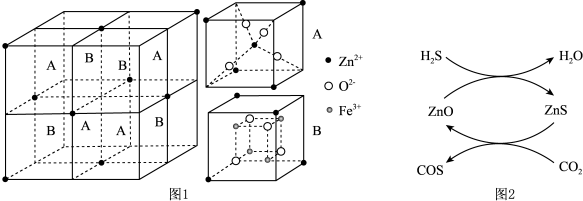
(1)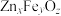 是一种复合脱硫剂,可用于脱除煤气中的
是一种复合脱硫剂,可用于脱除煤气中的 。
。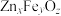 晶胞结构如图1所示(A、B交替排列,且A、B分别为晶胞的
晶胞结构如图1所示(A、B交替排列,且A、B分别为晶胞的 的结构),其化学式为
的结构),其化学式为__________ 。
②一定温度下将一定比例 和
和 的混合气体以一定流速通过装有上述脱硫剂的反应器,一段时间后,出口处检测到
的混合气体以一定流速通过装有上述脱硫剂的反应器,一段时间后,出口处检测到 。研究表明
。研究表明 参与了
参与了 与
与 生成
生成 的反应,反应机理如图2所示,反应前后
的反应,反应机理如图2所示,反应前后 的质量不变,该反应过程可描述为
的质量不变,该反应过程可描述为__________ 。
(2)稀土硫化物中硫含量的测定对其生产和质量控制具有重要意义。用如下方法对稀土硫化物中具有代表性的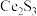 (
( 基态原子核外电子排布式为
基态原子核外电子排布式为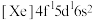 )样品硫含量进行测定。实验检测原理为
)样品硫含量进行测定。实验检测原理为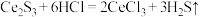
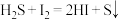

步骤1:称取0.1600g样品于反应瓶中,再准确滴加20.00mL 碘溶液;
碘溶液;
步骤2:缓慢滴加稍过量的稀盐酸(边滴加边摇动反应瓶),盖上瓶塞,剧烈摇动2min;
步骤3:滴入
 溶液至恰好完全反应,消耗
溶液至恰好完全反应,消耗 溶液20.00mL。
溶液20.00mL。
① 元素最高正化合价为
元素最高正化合价为__________ 。
②步骤1中不能使用稀硝酸的原因是__________ 。
③该样品中硫的质量分数为__________ (写出计算过程)。
(1)
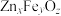 是一种复合脱硫剂,可用于脱除煤气中的
是一种复合脱硫剂,可用于脱除煤气中的 。
。 
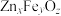 晶胞结构如图1所示(A、B交替排列,且A、B分别为晶胞的
晶胞结构如图1所示(A、B交替排列,且A、B分别为晶胞的 的结构),其化学式为
的结构),其化学式为②一定温度下将一定比例
 和
和 的混合气体以一定流速通过装有上述脱硫剂的反应器,一段时间后,出口处检测到
的混合气体以一定流速通过装有上述脱硫剂的反应器,一段时间后,出口处检测到 。研究表明
。研究表明 参与了
参与了 与
与 生成
生成 的反应,反应机理如图2所示,反应前后
的反应,反应机理如图2所示,反应前后 的质量不变,该反应过程可描述为
的质量不变,该反应过程可描述为(2)稀土硫化物中硫含量的测定对其生产和质量控制具有重要意义。用如下方法对稀土硫化物中具有代表性的
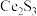 (
( 基态原子核外电子排布式为
基态原子核外电子排布式为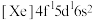 )样品硫含量进行测定。实验检测原理为
)样品硫含量进行测定。实验检测原理为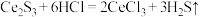
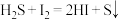

步骤1:称取0.1600g样品于反应瓶中,再准确滴加20.00mL
 碘溶液;
碘溶液;步骤2:缓慢滴加稍过量的稀盐酸(边滴加边摇动反应瓶),盖上瓶塞,剧烈摇动2min;
步骤3:滴入

 溶液至恰好完全反应,消耗
溶液至恰好完全反应,消耗 溶液20.00mL。
溶液20.00mL。①
 元素最高正化合价为
元素最高正化合价为②步骤1中不能使用稀硝酸的原因是
③该样品中硫的质量分数为
您最近一年使用:0次
解题方法
5 . 废弃物的综合利用有利于节约资源、保护环境。实验室利用废旧电池的铜帽(Cu、Zn总含量约为99%)制备ZnSO4·7H2O和CuSO4·5H2O的部分实验步骤如下:
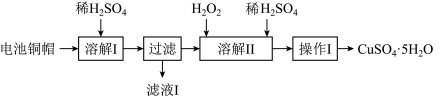
(1)在“溶解I”步骤中,为加快溶解速率,可采取的措施是_______ (任写一种方法)。
(2)从“滤液I”中提取ZnSO4·7H2O的实验步骤依次为_______ 、_______ 、过滤、冰水洗涤、低温干燥。
(3)仔细分析流程,在“溶解II”步骤中,发生反应的化学方程式为_______ (用双线桥标出电子转移的方向和数目)。
(4)为测定产品中CuSO4·5H2O的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000mol/LNa2S2O3标准溶液至滴定终点,消耗Na2S2O3溶液25.00mL。
已知:2CuSO4+4KI=2CuI(白色)+I2+2K2SO4;2Na2S2O3+I2=2NaI+Na2S4O6
请依据实验数据计算样品中CuSO4·5H2O的质量分数_______ (写出计算过程,结果用百分数表示,小数点后保留1位有效数字)。

(1)在“溶解I”步骤中,为加快溶解速率,可采取的措施是
(2)从“滤液I”中提取ZnSO4·7H2O的实验步骤依次为
(3)仔细分析流程,在“溶解II”步骤中,发生反应的化学方程式为
(4)为测定产品中CuSO4·5H2O的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000mol/LNa2S2O3标准溶液至滴定终点,消耗Na2S2O3溶液25.00mL。
已知:2CuSO4+4KI=2CuI(白色)+I2+2K2SO4;2Na2S2O3+I2=2NaI+Na2S4O6
请依据实验数据计算样品中CuSO4·5H2O的质量分数
您最近一年使用:0次
解题方法
6 . 碱式次氯酸镁[化学式为Mg2ClO(OH)3·H2O]是一种白色粉末,难溶于水,也是新一代无机抗菌剂。可由Cl2、NaOH及MgCl2为原料制取。
(1)甲同学拟利用如图装置制备质量分数约为5%的次氯酸钠溶液。
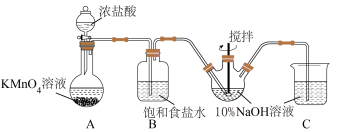
①B装置中饱和食盐水的作用为___________ 。
②Cl2和NaOH在较高的温度下反应生成NaClO3,写出该反应的离子反应方程式___________ ,因此控制反应在0~5℃范围内进行,实验中适宜的措施是___________ 。
(2)乙同学拟利用甲同学制得的NaClO溶液制取碱式次氯酸镁,步骤如下:
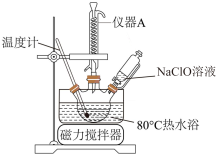
步骤1:往烧瓶中加入氯化镁,开动搅拌器并升温到80℃;
步骤2:逐滴滴入NaClO溶液;
步骤3:调节溶液pH=10,回流反应4h;
步骤4:过滤,烘干。
①上图中,冷凝水从仪器A___________ (填"上口"或“下口"”) 进入。
②过滤时,需用到的玻璃仪器除烧杯外,还需___________ 。
③写出MgCl2、NaOH、Cl2反应制取Mg2ClO(OH)3·H2O的化学方程式:___________ 。
④通过测定Mg2ClO(OH)3·H2O产品有效氯的含量来衡量产品品质。次氯酸盐的有效氯含量可用次氯酸盐与盐酸反应所生成的氯气的含量来表示,有效氯含量=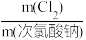 ×100%。实测值的测量方法:称取1.775g所制得的碱式次氯酸镁,放置于带塞的磨口瓶中,加入稍过量KI溶液和稀硫酸(ClO-+2I-+2H+=I2+Cl-+H2O),滴入20.00mL1mol/LNa2S2O3溶液(I2+2
×100%。实测值的测量方法:称取1.775g所制得的碱式次氯酸镁,放置于带塞的磨口瓶中,加入稍过量KI溶液和稀硫酸(ClO-+2I-+2H+=I2+Cl-+H2O),滴入20.00mL1mol/LNa2S2O3溶液(I2+2 =2I-+
=2I-+ )恰好完全反应,测得有效氯含量为
)恰好完全反应,测得有效氯含量为___________ 。(写出计算过程)
(1)甲同学拟利用如图装置制备质量分数约为5%的次氯酸钠溶液。

①B装置中饱和食盐水的作用为
②Cl2和NaOH在较高的温度下反应生成NaClO3,写出该反应的离子反应方程式
(2)乙同学拟利用甲同学制得的NaClO溶液制取碱式次氯酸镁,步骤如下:

步骤1:往烧瓶中加入氯化镁,开动搅拌器并升温到80℃;
步骤2:逐滴滴入NaClO溶液;
步骤3:调节溶液pH=10,回流反应4h;
步骤4:过滤,烘干。
①上图中,冷凝水从仪器A
②过滤时,需用到的玻璃仪器除烧杯外,还需
③写出MgCl2、NaOH、Cl2反应制取Mg2ClO(OH)3·H2O的化学方程式:
④通过测定Mg2ClO(OH)3·H2O产品有效氯的含量来衡量产品品质。次氯酸盐的有效氯含量可用次氯酸盐与盐酸反应所生成的氯气的含量来表示,有效氯含量=
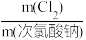 ×100%。实测值的测量方法:称取1.775g所制得的碱式次氯酸镁,放置于带塞的磨口瓶中,加入稍过量KI溶液和稀硫酸(ClO-+2I-+2H+=I2+Cl-+H2O),滴入20.00mL1mol/LNa2S2O3溶液(I2+2
×100%。实测值的测量方法:称取1.775g所制得的碱式次氯酸镁,放置于带塞的磨口瓶中,加入稍过量KI溶液和稀硫酸(ClO-+2I-+2H+=I2+Cl-+H2O),滴入20.00mL1mol/LNa2S2O3溶液(I2+2 =2I-+
=2I-+ )恰好完全反应,测得有效氯含量为
)恰好完全反应,测得有效氯含量为
您最近一年使用:0次
名校
7 . 某种胃药的有效成分为碳酸钙.某实验小组为测定其中碳酸钙的含量.取10粒药片(0.1g/粒)研碎后溶解.加入25.00mL NaOH溶液中和过量的盐酸,测定所消耗的NaOH的溶液体积如下:
NaOH溶液中和过量的盐酸,测定所消耗的NaOH的溶液体积如下:
(1)配制500mL 的NaOH溶液,需要NaOH的质量是
的NaOH溶液,需要NaOH的质量是____________ 。
(2)药片中碳酸钙的质量分数_________ 。(写出计算过程)
 NaOH溶液中和过量的盐酸,测定所消耗的NaOH的溶液体积如下:
NaOH溶液中和过量的盐酸,测定所消耗的NaOH的溶液体积如下:测定次数 | 第1次 | 第2次 | 第3次 | 第4次 |
V(NaOH)/mL | 13.00 | 12.90 | 11.40 | 13.10 |
 的NaOH溶液,需要NaOH的质量是
的NaOH溶液,需要NaOH的质量是(2)药片中碳酸钙的质量分数
您最近一年使用:0次
名校
解题方法
8 . I.现有一定量含有Na2O杂质的Na2O2试样,用如图所示的实验装置测定Na2O2试样的纯度(通过CO2与样品反应后生成O2的量测定Na2O2的含量。可供选用的反应物:CaCO3固体、盐酸、硫酸溶液和蒸馏水)。回答下列问题:
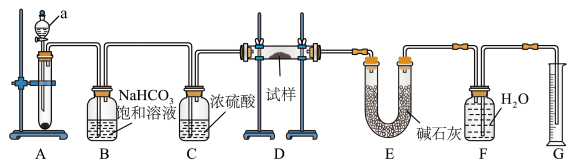
(1)装置a的名称为_____ 。
(2)装置B中除杂反应的离子方程式为_________ 。
(3)装置D中反应的化学方程式为_______ 。
(4)装置E中碱石灰的主要作用是________ 。
(5)已知装置D中试样质量为19.5g,装置G中所得O2体积为1120mL(已折算成标准状况下体积,且O2全部逸出)。求试样中Na2O2的质量分数___________ 。
Ⅱ.现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:
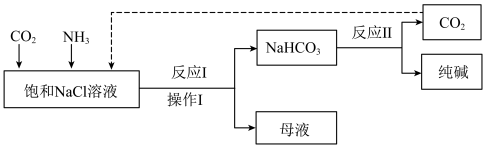
(6)为提高NaHCO3的产量,CO2和NH3通入饱和NaCl溶液的先后顺序为_____ 。
A.先通CO2再通NH3 B.先通NH3再通CO2

(1)装置a的名称为
(2)装置B中除杂反应的离子方程式为
(3)装置D中反应的化学方程式为
(4)装置E中碱石灰的主要作用是
(5)已知装置D中试样质量为19.5g,装置G中所得O2体积为1120mL(已折算成标准状况下体积,且O2全部逸出)。求试样中Na2O2的质量分数
Ⅱ.现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:

(6)为提高NaHCO3的产量,CO2和NH3通入饱和NaCl溶液的先后顺序为
A.先通CO2再通NH3 B.先通NH3再通CO2
您最近一年使用:0次
名校
解题方法
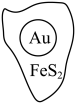
9 . 抗原检测盒中T线处使用的是胶体金(Au)标记物。一种从被 包裹的含金矿物(如图)中提取金单质的过程为:将金矿进行预处理,可除去
包裹的含金矿物(如图)中提取金单质的过程为:将金矿进行预处理,可除去 而露出金矿物,再加入
而露出金矿物,再加入 溶液和
溶液和 溶液对金矿物进行浸取,得到含金的溶液,然后加入
溶液对金矿物进行浸取,得到含金的溶液,然后加入 置换出
置换出 。其工艺流程如下:
。其工艺流程如下:
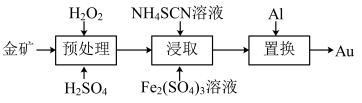
(1)①“预处理”时,用 将
将 直接氧化为
直接氧化为 和硫酸,写出该反应的化学方程式
和硫酸,写出该反应的化学方程式______ 。
②研究发现:在 的催化作用下,
的催化作用下, 产生具有强氧化能力的中间体
产生具有强氧化能力的中间体 ,
, 将金表面的
将金表面的 氧化溶出,
氧化溶出, 越多,
越多, 溶出率越高.
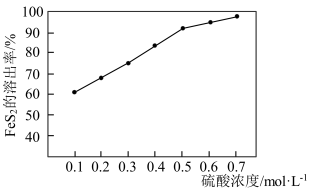
溶出率越高. 溶出率与硫酸初始浓度的关系如图所示,随着硫酸初始浓度的增大,
溶出率与硫酸初始浓度的关系如图所示,随着硫酸初始浓度的增大, 溶出率逐渐提高的主要原因是
溶出率逐渐提高的主要原因是________ 。
(2)“置换”时需维持无氧环境,其主要原因是_________ 。
(3)测定样品中 的含量:准确称取
的含量:准确称取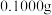 试样,加入王水,将样品中的
试样,加入王水,将样品中的 完全转化成具有强氧化性的氯金酸
完全转化成具有强氧化性的氯金酸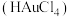 ,在除去硝酸根后的溶液中,边不断搅拌,边向溶液中加入过量
,在除去硝酸根后的溶液中,边不断搅拌,边向溶液中加入过量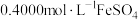 溶液
溶液 ,将
,将 完全还原为
完全还原为 ,滴加二苯胺磺酸钠作指示剂,用
,滴加二苯胺磺酸钠作指示剂,用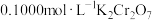 标准溶液滴定至终点(将剩余的
标准溶液滴定至终点(将剩余的 恰好完全氧化),消耗
恰好完全氧化),消耗 溶液
溶液 。
。
已知: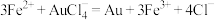

计算样品中金的质量分数(写出计算过程)_____________ 。
 包裹的含金矿物(如图)中提取金单质的过程为:将金矿进行预处理,可除去
包裹的含金矿物(如图)中提取金单质的过程为:将金矿进行预处理,可除去 而露出金矿物,再加入
而露出金矿物,再加入 溶液和
溶液和 溶液对金矿物进行浸取,得到含金的溶液,然后加入
溶液对金矿物进行浸取,得到含金的溶液,然后加入 置换出
置换出 。其工艺流程如下:
。其工艺流程如下:

(1)①“预处理”时,用
 将
将 直接氧化为
直接氧化为 和硫酸,写出该反应的化学方程式
和硫酸,写出该反应的化学方程式②研究发现:在
 的催化作用下,
的催化作用下, 产生具有强氧化能力的中间体
产生具有强氧化能力的中间体 ,
, 将金表面的
将金表面的 氧化溶出,
氧化溶出, 越多,
越多, 溶出率越高.
溶出率越高. 溶出率与硫酸初始浓度的关系如图所示,随着硫酸初始浓度的增大,
溶出率与硫酸初始浓度的关系如图所示,随着硫酸初始浓度的增大, 溶出率逐渐提高的主要原因是
溶出率逐渐提高的主要原因是
(2)“置换”时需维持无氧环境,其主要原因是
(3)测定样品中
 的含量:准确称取
的含量:准确称取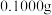 试样,加入王水,将样品中的
试样,加入王水,将样品中的 完全转化成具有强氧化性的氯金酸
完全转化成具有强氧化性的氯金酸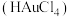 ,在除去硝酸根后的溶液中,边不断搅拌,边向溶液中加入过量
,在除去硝酸根后的溶液中,边不断搅拌,边向溶液中加入过量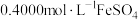 溶液
溶液 ,将
,将 完全还原为
完全还原为 ,滴加二苯胺磺酸钠作指示剂,用
,滴加二苯胺磺酸钠作指示剂,用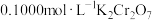 标准溶液滴定至终点(将剩余的
标准溶液滴定至终点(将剩余的 恰好完全氧化),消耗
恰好完全氧化),消耗 溶液
溶液 。
。已知:
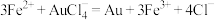

计算样品中金的质量分数(写出计算过程)
您最近一年使用:0次
2023-04-25更新
|
977次组卷
|
2卷引用:江苏省泰州中学2022-2023学年高一上学期期末考试化学试题
名校
10 . 某兴趣小组利用废旧电池的铜帽(铜锌总含量约99%)制备了 样品,制备流程如下:
样品,制备流程如下:
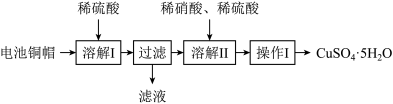
(1)“滤液”中主要含有的阳离子是______ 。
(2)“溶解II”过程中,发生反应的离子方程式为______ 。
(3)“溶解II”过程中应控制反应温度不能过高的原因是______ 。
(4)操作I的具体操作是______ 。
(5)为测定所得 样品的纯度,兴趣小组进行了如下实验:称取2.570 g样品,配制成250 mL溶液,取25.00 mL溶液于锥形瓶中,加入过量KI并充分振荡后,滴加几滴淀粉溶液,再滴入
样品的纯度,兴趣小组进行了如下实验:称取2.570 g样品,配制成250 mL溶液,取25.00 mL溶液于锥形瓶中,加入过量KI并充分振荡后,滴加几滴淀粉溶液,再滴入 的
的 溶液至刚好完全反应,恰好完全反应时消耗
溶液至刚好完全反应,恰好完全反应时消耗 溶液的体积为25.00 mL。实验过程中发生的反应如下:
溶液的体积为25.00 mL。实验过程中发生的反应如下:
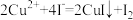 ;
; 。
。
①配制250 mL溶液所需的玻璃仪器除烧杯、玻璃棒外还有______ 。
②计算出样品中 的质量分数
的质量分数______ 。(写出计算过程,保留三位有效数字)
 样品,制备流程如下:
样品,制备流程如下:
(1)“滤液”中主要含有的阳离子是
(2)“溶解II”过程中,发生反应的离子方程式为
(3)“溶解II”过程中应控制反应温度不能过高的原因是
(4)操作I的具体操作是
(5)为测定所得
 样品的纯度,兴趣小组进行了如下实验:称取2.570 g样品,配制成250 mL溶液,取25.00 mL溶液于锥形瓶中,加入过量KI并充分振荡后,滴加几滴淀粉溶液,再滴入
样品的纯度,兴趣小组进行了如下实验:称取2.570 g样品,配制成250 mL溶液,取25.00 mL溶液于锥形瓶中,加入过量KI并充分振荡后,滴加几滴淀粉溶液,再滴入 的
的 溶液至刚好完全反应,恰好完全反应时消耗
溶液至刚好完全反应,恰好完全反应时消耗 溶液的体积为25.00 mL。实验过程中发生的反应如下:
溶液的体积为25.00 mL。实验过程中发生的反应如下: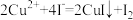 ;
; 。
。①配制250 mL溶液所需的玻璃仪器除烧杯、玻璃棒外还有
②计算出样品中
 的质量分数
的质量分数
您最近一年使用:0次
2023-04-23更新
|
258次组卷
|
2卷引用:江苏省徐州市2022-2023学年高一下学期期中考试化学试题



