1 . 硝酸是重要的化工原料,工业上制硝酸的历程及硝酸性质如下:
(1)A的化学式___________ 。
(2)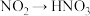 的化学反应方程式
的化学反应方程式___________ 。
(3)浓硝酸常温能与 反应,体现
反应,体现 具有
具有___________ 性。
(4)下列说法正确的是___________。

(1)A的化学式
(2)
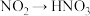 的化学反应方程式
的化学反应方程式(3)浓硝酸常温能与
 反应,体现
反应,体现 具有
具有(4)下列说法正确的是___________。
| A.工业合成A,需要高温高压,催化剂 |
B. 、 、 在潮湿大气中不会形成酸雨 在潮湿大气中不会形成酸雨 |
C.浓 与 与 反应后的溶液呈绿色,是由于溶有 反应后的溶液呈绿色,是由于溶有 ,加入水稀释后变蓝色 ,加入水稀释后变蓝色 |
| D.工业上可用铁或铝制容器装运稀硝酸 |
您最近一年使用:0次
解题方法
2 . 高能氢氧燃烧电池,以 为电解质溶液,以
为电解质溶液,以 为电极材料,下列说法
为电极材料,下列说法不正确 的是
 为电解质溶液,以
为电解质溶液,以 为电极材料,下列说法
为电极材料,下列说法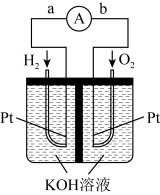
A.电池总反应式为: |
B.通 的 的 极为负极 极为负极 |
C.正极的电极反应式: |
| D.电子从氧电极经外电路流向氢电极 |
您最近一年使用:0次
名校
解题方法
3 . 低碳烯烃(乙烯、丙烯等)作为化学工业重要基本有机化工原料,在现代石油和化学工业中起着举足轻重的作用。碘甲烷 热裂解制低碳烯烃的主要反应有:
热裂解制低碳烯烃的主要反应有:
反应Ⅰ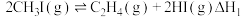
反应Ⅱ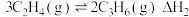
反应Ⅲ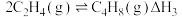
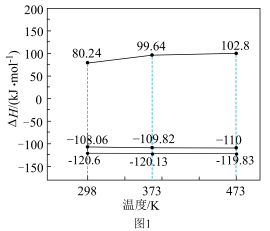
(1)反应Ⅰ、Ⅱ、Ⅲ的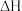 随温度的变化如图1所示。
随温度的变化如图1所示。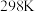 下,
下,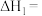
_______ kJ/mol。
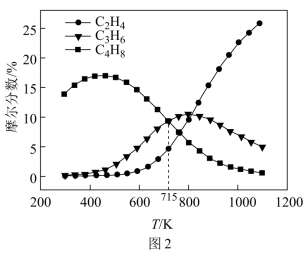
(3)利用计算机模拟反应过程。一定压强条件下,测定反应温度对碘甲烷热裂解制低碳烯烃平衡体系中乙烯、丙烯和丁烯组成的影响如图2所示。结合图1、图2,回答下列问题:_______ 。
A.同一个反应,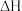 会随温度的变化而变,但变化程度不大
会随温度的变化而变,但变化程度不大
B.若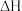 随温度的上升而增大,则
随温度的上升而增大,则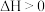
C.随温度升高,反应Ⅱ的化学平衡先正向移动后逆向移动
D.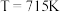 时,反应Ⅱ的平衡常数小于反应Ⅲ
时,反应Ⅱ的平衡常数小于反应Ⅲ
②从图2中可看出,当体系温度高于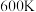 时,乙烯的摩尔分数随温度升高而显著增加,可能的原因是:
时,乙烯的摩尔分数随温度升高而显著增加,可能的原因是:_______ 。
(4)维持温度为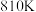 ,压强为
,压强为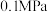 ,起始投料
,起始投料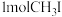 ,测得平衡体系中
,测得平衡体系中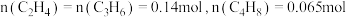 。
。
①平衡时 的物质的量分数
的物质的量分数 为
为_______ 。
②已知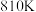 条件下,存在等式
条件下,存在等式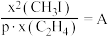 (常数)
(常数)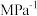 (对于气相反应,用某组分B的平衡压强
(对于气相反应,用某组分B的平衡压强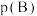 可代替物质的量浓度
可代替物质的量浓度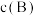 ,如
,如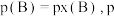 为平衡总压强,
为平衡总压强,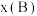 为平衡系统中B的物质的量分数)。保持其它条件不变,请在图3中画出
为平衡系统中B的物质的量分数)。保持其它条件不变,请在图3中画出 与压强
与压强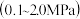 关系的曲线示意图
关系的曲线示意图_______ 。
 热裂解制低碳烯烃的主要反应有:
热裂解制低碳烯烃的主要反应有:反应Ⅰ
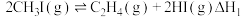
反应Ⅱ
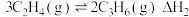
反应Ⅲ
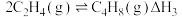
(1)反应Ⅰ、Ⅱ、Ⅲ的
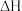 随温度的变化如图1所示。
随温度的变化如图1所示。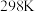 下,
下,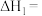
| A.高压 | B.高温 | C.移去 | D.催化剂 |
(3)利用计算机模拟反应过程。一定压强条件下,测定反应温度对碘甲烷热裂解制低碳烯烃平衡体系中乙烯、丙烯和丁烯组成的影响如图2所示。结合图1、图2,回答下列问题:
A.同一个反应,
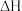 会随温度的变化而变,但变化程度不大
会随温度的变化而变,但变化程度不大B.若
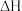 随温度的上升而增大,则
随温度的上升而增大,则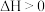
C.随温度升高,反应Ⅱ的化学平衡先正向移动后逆向移动
D.
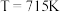 时,反应Ⅱ的平衡常数小于反应Ⅲ
时,反应Ⅱ的平衡常数小于反应Ⅲ②从图2中可看出,当体系温度高于
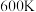 时,乙烯的摩尔分数随温度升高而显著增加,可能的原因是:
时,乙烯的摩尔分数随温度升高而显著增加,可能的原因是:(4)维持温度为
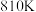 ,压强为
,压强为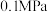 ,起始投料
,起始投料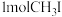 ,测得平衡体系中
,测得平衡体系中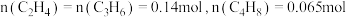 。
。①平衡时
 的物质的量分数
的物质的量分数 为
为②已知
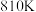 条件下,存在等式
条件下,存在等式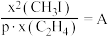 (常数)
(常数)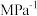 (对于气相反应,用某组分B的平衡压强
(对于气相反应,用某组分B的平衡压强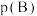 可代替物质的量浓度
可代替物质的量浓度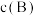 ,如
,如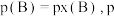 为平衡总压强,
为平衡总压强,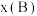 为平衡系统中B的物质的量分数)。保持其它条件不变,请在图3中画出
为平衡系统中B的物质的量分数)。保持其它条件不变,请在图3中画出 与压强
与压强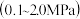 关系的曲线示意图
关系的曲线示意图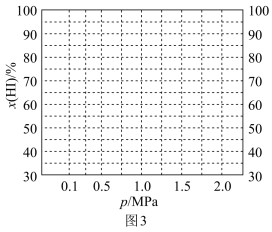
您最近一年使用:0次
名校
解题方法
4 . 下列化学用语正确的是
A.基态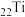 原子的轨道表示式: 原子的轨道表示式: |
B.用电子云轮廓图表示 中的 中的 键形成的示意图: 键形成的示意图: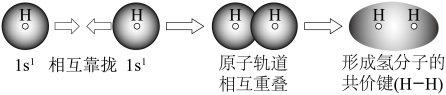 |
C. 的空间结构为三角锥形 的空间结构为三角锥形 |
D.2-甲基-1-丁醇的键线式: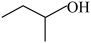 |
您最近一年使用:0次
解题方法
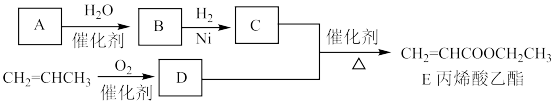
5 . 丙烯酸乙酯在于菠萝等水果中,合成路线如下: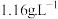 ,B能发生银镜反应,请回答:
,B能发生银镜反应,请回答:
(1)A的结构式为;___________ 。
(2)E的官能团的名称是___________ 。
(3)B→C的反应类型为___________ 。
(4)写出 在催化剂作用下与
在催化剂作用下与 反应生成D的化学反应方程式
反应生成D的化学反应方程式___________ 。
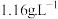 ,B能发生银镜反应,请回答:
,B能发生银镜反应,请回答:(1)A的结构式为;
(2)E的官能团的名称是
(3)B→C的反应类型为
(4)写出
 在催化剂作用下与
在催化剂作用下与 反应生成D的化学反应方程式
反应生成D的化学反应方程式
您最近一年使用:0次
6 . 土豆丝入水浸泡得到A,A遇碘变蓝色,一系列转化关系如下:不正确 的是

| A.A是淀粉,属于多糖 |
B.用 溶液可鉴别C、D、E 溶液可鉴别C、D、E |
| C.B→C的转化被广泛用于酿酒和利用生物质生产燃料 |
D.有机物D能与新制 悬浊液加热反应生成砖红色沉淀 悬浊液加热反应生成砖红色沉淀 |
您最近一年使用:0次
解题方法
7 . 在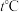
 容器中发生A、B两种气体间的转化反应,A为红棕色,B为无色,A、B的物质的量随时间变化曲线如图所示,下列说法
容器中发生A、B两种气体间的转化反应,A为红棕色,B为无色,A、B的物质的量随时间变化曲线如图所示,下列说法不正确 是
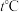
 容器中发生A、B两种气体间的转化反应,A为红棕色,B为无色,A、B的物质的量随时间变化曲线如图所示,下列说法
容器中发生A、B两种气体间的转化反应,A为红棕色,B为无色,A、B的物质的量随时间变化曲线如图所示,下列说法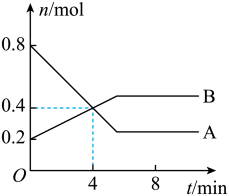
A.该反应的方程式为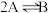 |
B.反应开始至 ,B的平均反应速率为 ,B的平均反应速率为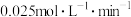 |
C. 时,正逆反应速率相等 时,正逆反应速率相等 |
D.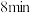 时,反应已达到平衡状态,容器内压强不变,气体的颜色不变 时,反应已达到平衡状态,容器内压强不变,气体的颜色不变 |
您最近一年使用:0次
名校
解题方法
8 . 工业上高炉炼铁产生的CO和CO2可以按如下流程脱除或利用。___________ 。
(2)煅烧产生的尾气可通过途径Ⅱ转化为CO2.。2分子氨和1分子CO2生产A,最终转化为尿素[CO(NH2)2];可通过途径Ⅲ转为b。
①下列说法正确的是___________ 。
A.黄铁(FeS2)可作为高炉炼铁的铁源
B.途径Ⅱ可实现反应转化MnO2+CO→CO2+Mn2O3
C.化合物A是一种盐
D.化合物B为CH3COONa
②尿素[CO(NH2)2]在较高温度下可以聚合成环状化合物三聚氰胺(C3H6N6),写出该反应的化学方程式___________ 。
(3)设计实验验证化合物A中含有N元素___________ ;写出实验过程中涉及的反应方程式___________ 。

已知: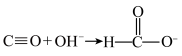 。请回答:
。请回答:
(2)煅烧产生的尾气可通过途径Ⅱ转化为CO2.。2分子氨和1分子CO2生产A,最终转化为尿素[CO(NH2)2];可通过途径Ⅲ转为b。
①下列说法正确的是
A.黄铁(FeS2)可作为高炉炼铁的铁源
B.途径Ⅱ可实现反应转化MnO2+CO→CO2+Mn2O3
C.化合物A是一种盐
D.化合物B为CH3COONa
②尿素[CO(NH2)2]在较高温度下可以聚合成环状化合物三聚氰胺(C3H6N6),写出该反应的化学方程式
(3)设计实验验证化合物A中含有N元素
您最近一年使用:0次
解题方法
9 . 仪器名称为“蒸发皿”的是
A.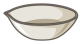 | B.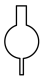 | C. | D. |
您最近一年使用:0次
解题方法
10 . 从 的
的 废液中回收
废液中回收 ,流程如下:
,流程如下:不正确 的是
 的
的 废液中回收
废液中回收 ,流程如下:
,流程如下: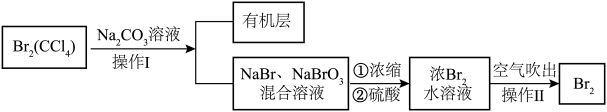
| A.操作I是萃取分液,有机层在上层 |
B.加 溶液反应的离子方程式为 溶液反应的离子方程式为 |
C.加 溶液的目的是将 溶液的目的是将 转化成盐溶液,然后浓缩,加入硫酸后生成浓度较大的含 转化成盐溶液,然后浓缩,加入硫酸后生成浓度较大的含 溶液 溶液 |
D.操作Ⅱ通入热空气降低 的溶解度,并利用了 的溶解度,并利用了 的挥发性 的挥发性 |
您最近一年使用:0次



