名校
1 . 利用下列装置进行实验,能达到实验目的的是
| 选项 | A | B | C | D |
| 实验装置 | 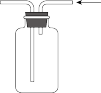 | 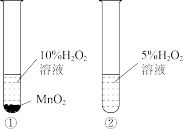 | 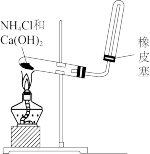 | 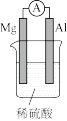 |
| 实验目的 | 收集NO | 探究催化剂对反应速率的影响 | 制备并收集 | 验证Mg比Al活泼 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-07-08更新
|
135次组卷
|
2卷引用:安徽省池州市2021-2022学年高一下学期期末联考化学试题
名校
解题方法
2 . 下列装置用于进行指定实验时,能达到实验目的的是

| A.用装置甲制备氨气 | B.用装置乙除去氨气中的水蒸气 |
| C.用装置丙收集氨气 | D.用装置丁吸收多余的氨气 |
您最近一年使用:0次
2022-05-15更新
|
1132次组卷
|
21卷引用:安徽省池州市贵池区2021-2022学年高一下学期期中考试化学试题
安徽省池州市贵池区2021-2022学年高一下学期期中考试化学试题广东省深圳市光明区高级中学2021-2022学年高一下学期期中考试化学试题广西河池市八校2021-2022学年高一下学期第二次联考化学试题广东省佛山市第一中学2021-2022学年高一下学期期中考试化学试题河南省洛阳市洛阳格致学校2021-2022学年高一下学期三月月考化学试题黑龙江省肇东市第四中学2021-2022学年高一下学期期中考试化学试题山东省菏泽市单县第二中学2021-2022学年高一上学期1月段考(实验班)化学试题湖南省常德市第二中学2020-2021学年高一下学期期中考试化学试题上海市第四中学2022-2023学年高一上学期期末考试化学试题福建省福州屏东中学2022-2023学年高一下学期期中考试化学试题河南省濮阳市第一高级中学2022-2023学年高一下学期4月期中化学试题江苏省南京市协同体七校2022-2023学年高一下学期期中联合考试化学试题北京市中国人民大学附属中学2018-2019学年高一上学期期末考试化学试题广东省揭阳市揭东第一中学等三校2022-2023学年高一下学期期中联考化学试题广东省广州市第二中学2022-2023学年高一下学期期中考试化学试题广东省深圳市罗湖高级中学2022-2023学年高一下学期4月期中考试化学试题广东省江门市培英高级中学2022-2023学年高一下学期期中考试化学试题广东省湛江市第二十一中学2022-2023学年高一下学期期中考试(选考)化学试题广东省佛山市三水中学2022-2023学年高一下学期3月第一次统测化学试题江苏省扬州市邗江中学2023-2024学年高一下学期期中考试化学试题广东省惠州市第一中学2023-2024学年高一下学期4月月考化学试卷
3 . 用下列实验装置进行相应实验,能达到实验目的的是
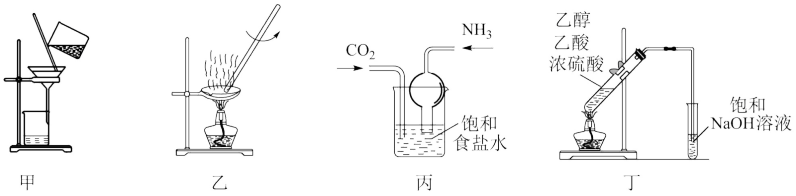

| A.用装置甲分离氢氧化铁胶体和蔗糖溶液 |
| B.用装置乙蒸干氯化铝饱和溶液制备纯净的无水氯化铝 |
| C.用装置丙制取碳酸氢钠 |
| D.用装置丁制备乙酸乙酯 |
您最近一年使用:0次
2021-04-04更新
|
150次组卷
|
2卷引用:安徽省池州市2021届高三下学期4月普通高中教学质量统一监测(二模)理综化学试题
名校
4 . 苯甲酸(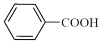 )具有广泛的用途,可用作食品防腐剂及有机合成的原料,实验室利用高锰酸钾溶液氧化甲苯制备苯甲酸,实验装置如图(部分装置省略):
)具有广泛的用途,可用作食品防腐剂及有机合成的原料,实验室利用高锰酸钾溶液氧化甲苯制备苯甲酸,实验装置如图(部分装置省略):
(1)仪器甲的名称是_______ ;仪器乙的进水口是_______ 。
(2)“反应混合物”是由9.20g甲苯和稍过量的KMnO4溶液组成的。反应混合物配制好后,溶液出现分层现象,上层为_______ (填“油状液体”或“紫红色溶液”)。
(3)“反应”在90℃、电动搅拌器作用下进行,并加热回流至分水器不再出现油珠。
①“反应”需在较高温度下进行并搅拌,其目的为_______ 。
②当分水器不再出现油珠时,这说明_______ 。
(4)用浓盐酸酸化时的相关化学方程式为_______ 。
(5)采用“减压过滤”的优点是_______ 。
(6)粗苯甲酸提纯后获得11.53g晶体,则苯甲酸的产率为_______ %(计算结果保留三位有效数字)。
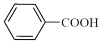 )具有广泛的用途,可用作食品防腐剂及有机合成的原料,实验室利用高锰酸钾溶液氧化甲苯制备苯甲酸,实验装置如图(部分装置省略):
)具有广泛的用途,可用作食品防腐剂及有机合成的原料,实验室利用高锰酸钾溶液氧化甲苯制备苯甲酸,实验装置如图(部分装置省略):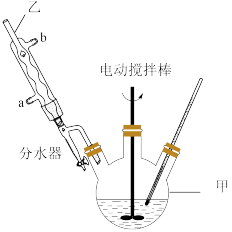

流程图中“反应”为: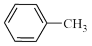 +2KMnO4
+2KMnO4
 +KOH+2MnO2↓+H2O。
+KOH+2MnO2↓+H2O。
(1)仪器甲的名称是
(2)“反应混合物”是由9.20g甲苯和稍过量的KMnO4溶液组成的。反应混合物配制好后,溶液出现分层现象,上层为
(3)“反应”在90℃、电动搅拌器作用下进行,并加热回流至分水器不再出现油珠。
①“反应”需在较高温度下进行并搅拌,其目的为
②当分水器不再出现油珠时,这说明
(4)用浓盐酸酸化时的相关化学方程式为
(5)采用“减压过滤”的优点是
(6)粗苯甲酸提纯后获得11.53g晶体,则苯甲酸的产率为
您最近一年使用:0次
2023-06-11更新
|
152次组卷
|
4卷引用:安徽省池州市第一中学(A10联盟)2022-2023学年高二下学期6月月考化学试题
名校
5 . 硫代硫酸钠( )俗称大苏打,可用作分析试剂及还原剂,受热、遇酸易分解。某化学兴趣小组用如图装置模拟古法制硫酸,同时利用生成的
)俗称大苏打,可用作分析试剂及还原剂,受热、遇酸易分解。某化学兴趣小组用如图装置模拟古法制硫酸,同时利用生成的 气体制备
气体制备

已知:
①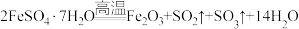 ;
;
② 的沸点为44.8℃;
的沸点为44.8℃;
③ 中S元素的化合价分别为
中S元素的化合价分别为 价和+6价。
价和+6价。
回答下列问题:
(1)检查装置气密性,加入药品。 和
和 混合溶液用煮沸过的蒸馏水配制且溶液上方设计油封,目的是
混合溶液用煮沸过的蒸馏水配制且溶液上方设计油封,目的是___________ ,D装置中所盛试剂为___________ 。
(2)B中为何要使用冰水浴,请说明理由___________ ,使用pH传感器始终观测混合溶液pH原因是___________ 。
(3)学习小组探究 的性质;取
的性质;取 晶体,溶解配成0.2mol/L的溶液:取4mL溶液。向其中加入1mL饱和氯水(pH=2.4),溶液立即出现浑浊。对溶液变浑浊的原因,提出假设:
晶体,溶解配成0.2mol/L的溶液:取4mL溶液。向其中加入1mL饱和氯水(pH=2.4),溶液立即出现浑浊。对溶液变浑浊的原因,提出假设:
假设1:氯水氧化了 价硫元素;
价硫元素;
假设2:酸性条件下 分解产生S。
分解产生S。
实验验证:a、b试管均盛有4mL0.2mol/L 溶液。
溶液。

①用胶头滴管向试管b中加入的试剂为___________ 。
②依据现象,S产生的主要原因是___________ (用化学方程式表示)。
 )俗称大苏打,可用作分析试剂及还原剂,受热、遇酸易分解。某化学兴趣小组用如图装置模拟古法制硫酸,同时利用生成的
)俗称大苏打,可用作分析试剂及还原剂,受热、遇酸易分解。某化学兴趣小组用如图装置模拟古法制硫酸,同时利用生成的 气体制备
气体制备

已知:
①
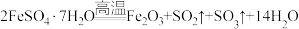 ;
;②
 的沸点为44.8℃;
的沸点为44.8℃;③
 中S元素的化合价分别为
中S元素的化合价分别为 价和+6价。
价和+6价。回答下列问题:
(1)检查装置气密性,加入药品。
 和
和 混合溶液用煮沸过的蒸馏水配制且溶液上方设计油封,目的是
混合溶液用煮沸过的蒸馏水配制且溶液上方设计油封,目的是(2)B中为何要使用冰水浴,请说明理由
(3)学习小组探究
 的性质;取
的性质;取 晶体,溶解配成0.2mol/L的溶液:取4mL溶液。向其中加入1mL饱和氯水(pH=2.4),溶液立即出现浑浊。对溶液变浑浊的原因,提出假设:
晶体,溶解配成0.2mol/L的溶液:取4mL溶液。向其中加入1mL饱和氯水(pH=2.4),溶液立即出现浑浊。对溶液变浑浊的原因,提出假设:假设1:氯水氧化了
 价硫元素;
价硫元素;假设2:酸性条件下
 分解产生S。
分解产生S。实验验证:a、b试管均盛有4mL0.2mol/L
 溶液。
溶液。
①用胶头滴管向试管b中加入的试剂为
②依据现象,S产生的主要原因是
您最近一年使用:0次
6 . 某学习小组用下图所示装置制备氯水,设计实验方案探究氯水的成分。请回答下列问题:
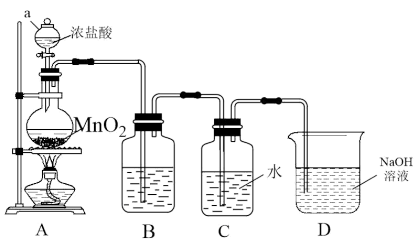
I.制备氯水:
(1)仪器 的名称是
的名称是_______ 。
(2)装置 中反应的化学方程式为
中反应的化学方程式为_______ 。
(3)装置 中的试剂是
中的试剂是_______ 。
(4)装置 的作用是
的作用是_______ 。
Ⅱ.探究氯水的性质:
取试剂 少量于试管中,分别滴加装置
少量于试管中,分别滴加装置 中的液体进行下列实验,完成表格并回答下列问题:
中的液体进行下列实验,完成表格并回答下列问题:
(5)实验①的实验现象为_______ 。
(6)实验②反应的离子方程式为_______ 。
(7)实验③中滴有酚酞的 溶液褪色的原因:
溶液褪色的原因:
i.氯水显酸性,与 发生中和反应,使溶液显中性;
发生中和反应,使溶液显中性;
ii.氯水具有漂白性,其漂白作用使溶液褪色;
请设计一个简单的实验,证明哪一个是正确的:_______ 。
(8)实验④反应的离子方程式为_______ 。

I.制备氯水:
(1)仪器
 的名称是
的名称是(2)装置
 中反应的化学方程式为
中反应的化学方程式为(3)装置
 中的试剂是
中的试剂是(4)装置
 的作用是
的作用是Ⅱ.探究氯水的性质:
取试剂
 少量于试管中,分别滴加装置
少量于试管中,分别滴加装置 中的液体进行下列实验,完成表格并回答下列问题:
中的液体进行下列实验,完成表格并回答下列问题: | 实验序号 | 试剂 | 实验现象 |
| ① | 紫色石蕊 | 溶液颜色 | |
| ② | 淀粉 溶液 溶液 | 溶液变蓝 | |
| ③ | 滴有酚酞的 溶液 溶液 | 溶液褪色 | |
| ④ |  溶液 溶液 | 产生无色无味的气体 |
(6)实验②反应的离子方程式为
(7)实验③中滴有酚酞的
 溶液褪色的原因:
溶液褪色的原因:i.氯水显酸性,与
 发生中和反应,使溶液显中性;
发生中和反应,使溶液显中性;ii.氯水具有漂白性,其漂白作用使溶液褪色;
请设计一个简单的实验,证明哪一个是正确的:
(8)实验④反应的离子方程式为
您最近一年使用:0次
解题方法
7 . 某化学兴趣小组欲探究含硫物质的性质及制备。
(探究一)选用下面的装置和药品探究亚硫酸与次氯酸的酸性强弱:
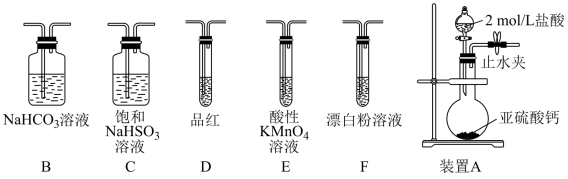
(1)装置连接顺序为A、___________ ,其中装置C的作用是___________ ,通过现象___________ ,即可证明亚硫酸的酸性强于次氯酸。
(探究二)硫代硫酸钠晶体( ,
,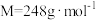 )可用作定影剂、还原剂。
)可用作定影剂、还原剂。
(2)已知: ,
,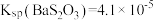 ,
,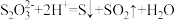 。
。
市售硫代硫酸钠中常含有硫酸根杂质,选用下列试剂设计实验方案进行检验:
限选试剂:稀盐酸、稀 、
、 溶液、
溶液、 溶液、
溶液、 溶液
溶液
(探究一)选用下面的装置和药品探究亚硫酸与次氯酸的酸性强弱:

(1)装置连接顺序为A、
(探究二)硫代硫酸钠晶体(
 ,
,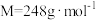 )可用作定影剂、还原剂。
)可用作定影剂、还原剂。(2)已知:
 ,
,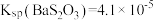 ,
,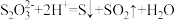 。
。市售硫代硫酸钠中常含有硫酸根杂质,选用下列试剂设计实验方案进行检验:
限选试剂:稀盐酸、稀
 、
、 溶液、
溶液、 溶液、
溶液、 溶液
溶液| 实验步骤 | 现象 |
| ①取少量样品,加入除氧蒸馏水 | ②固体完全溶解得无色澄清溶液 |
| ③ | ④ |
| ⑤静置, | ⑥ |
您最近一年使用:0次
8 . 某化学兴趣小组在实验室中制取氯气,并探究Cl2与Na2S的反应。回答下列问题:
(1)实验室制备纯净的氯气
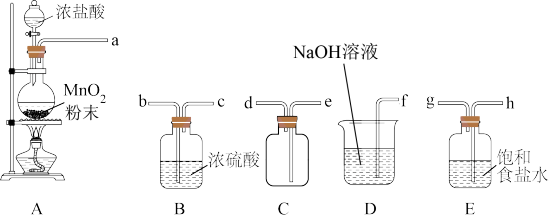
①装置A中反应的化学方程式为____ 。
②欲收集纯净的氯气,选择图中的装置,其连接顺序为a→____ (按气流方向,用小写字母表示)。
③装置D中NaOH溶液的作用是____ 。
(2)探究Cl2与Na2S的反应。将上述收集到的Cl2通入如图所示装置中充分反应,装置I中的溶液变为淡黄色浑浊。一段时间后,将装置Ⅰ中的浑浊物过滤,取其滤液进行下列实验,探究装置I中反应产物。
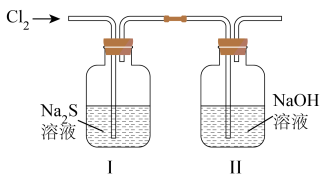
③写出Cl2与Na2S反应生成黄色沉淀的离子方程式为____ 。
(1)实验室制备纯净的氯气
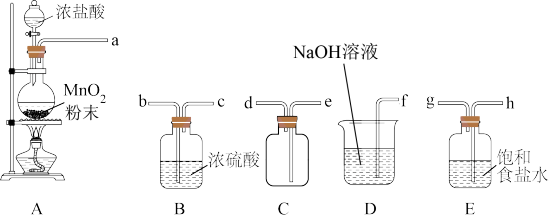
①装置A中反应的化学方程式为
②欲收集纯净的氯气,选择图中的装置,其连接顺序为a→
③装置D中NaOH溶液的作用是
(2)探究Cl2与Na2S的反应。将上述收集到的Cl2通入如图所示装置中充分反应,装置I中的溶液变为淡黄色浑浊。一段时间后,将装置Ⅰ中的浑浊物过滤,取其滤液进行下列实验,探究装置I中反应产物。

| 操作步骤 | 实验现象 | 结论 |
| 取少量滤液于试管甲中,加入Ba(OH)2溶液,振荡 | ① | 有 生成 生成 |
| 另取少量滤液于试管乙中,滴加品红溶液和过量盐酸 | 品红溶液不褪色 | ②无 |
③写出Cl2与Na2S反应生成黄色沉淀的离子方程式为
您最近一年使用:0次
解题方法
9 . 兴趣小组探究实验室中制备Cl2的过程,为证明过程中有水蒸气和HCl挥发出来,同时证明Cl2的某些性质,甲同学设计了如图所示的实验装置,按要求回答问题:
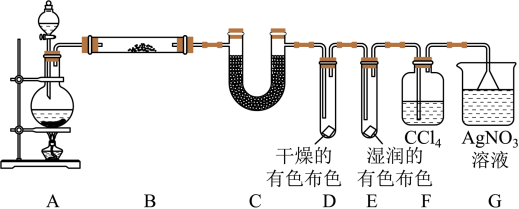
(1)若用浓盐酸与足量的MnO2反应制Cl2。MnO2+4HCl(浓)△MnCl2+Cl2↑+2H2O。
①用双线桥表示该反应的电子转移___ 。
②___ 作氧化剂 ,___ 作还原产物。
(2)①装置B中盛放的试剂名称为___ ,作用是___ 。
②装置D和E中出现的不同现象说明的问题是___ 。
③写出装置G中发生反应的离子方程式:___ 。

(1)若用浓盐酸与足量的MnO2反应制Cl2。MnO2+4HCl(浓)△MnCl2+Cl2↑+2H2O。
①用双线桥表示该反应的电子转移
②
(2)①装置B中盛放的试剂名称为
②装置D和E中出现的不同现象说明的问题是
③写出装置G中发生反应的离子方程式:
您最近一年使用:0次
2020-01-09更新
|
135次组卷
|
3卷引用:安徽省池州市江南中学2021届高三12月月考(三调)化学试题
10 . 某校化学实验兴趣小组探究实验室中制备 Cl2的过程,为证明过程中有水蒸气和 HCl 挥发出来,同时证明Cl2的某些性质,甲同学设计了如下图所示的实验装置,按要求回答问题。

(1)用浓盐酸与足量的 MnO2反应制Cl2的化学反应方程式_____ 。
(2)①装置 B 中盛放的试剂名称为_____ ,作用是_____ ,现象是_____ 。
②装置 D 和E 中出现的不同现象说明的问题是_________ 。
③装置 F 的作用是_____ 。
④写出装置G 中发生反应的离子方程式_____ 。

(1)用浓盐酸与足量的 MnO2反应制Cl2的化学反应方程式
(2)①装置 B 中盛放的试剂名称为
②装置 D 和E 中出现的不同现象说明的问题是
③装置 F 的作用是
④写出装置G 中发生反应的离子方程式
您最近一年使用:0次
2020-05-02更新
|
492次组卷
|
3卷引用:安徽省池州市江南教育集团2021届高三上学期1月月考化学试题
安徽省池州市江南教育集团2021届高三上学期1月月考化学试题北京市人大附中朝阳学校2019~2020年度第二学期高一年级阶段练习化学化学试题(合格班)(已下线)单科化学-2021年秋季高三开学摸底考试卷02(课标全国专用)



