1 . 用下列实验装置进行相应实验,能达到实验目的的是
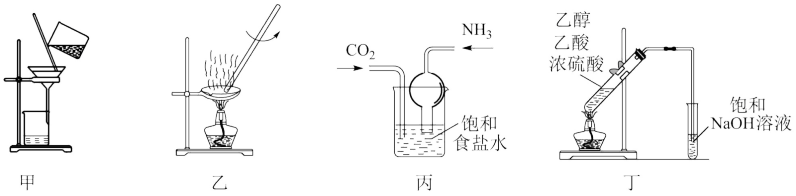

| A.用装置甲分离氢氧化铁胶体和蔗糖溶液 |
| B.用装置乙蒸干氯化铝饱和溶液制备纯净的无水氯化铝 |
| C.用装置丙制取碳酸氢钠 |
| D.用装置丁制备乙酸乙酯 |
您最近一年使用:0次
2021-04-04更新
|
150次组卷
|
2卷引用:安徽省宿州市萧县鹏程中学2021-2022学年高二下学期第一次质量检测化学试题
2 . 用下列装置进行相应实验,能达到实验目的的是
| 选项 | A | B | C | D |
| 装置 |  | 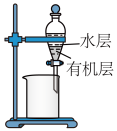 | 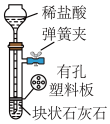 |  |
| 目的 | 蒸干NH4Cl饱和溶液制备NH4Cl晶体 | 分离CCl4萃取碘水后已分层的有机层和水层 | 制取少量纯净的CO2气体 | 除去Cl2中含有的少量HCl |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-05-01更新
|
165次组卷
|
2卷引用:安徽省泗县第一中学2022届高三上学期开学考试化学试题
解题方法
3 . 下列图中的实验方案,不能达到实验目的的是:
A | B | C | D | |
| 实验方案 |  | 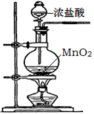 | 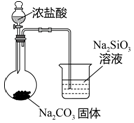 | 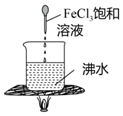 |
| 实验目的 | 验证化学能可以转化成电能 | 实验室利用该装置制备少量氯气 | 验证非金属性: Cl>C>Si | 加热至混合液呈红褐色,停止加热,制备Fe(OH)3胶体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-07-14更新
|
149次组卷
|
3卷引用:安徽省宿州市十三所省重点中学2019-2020学年高一下学期期末联考化学试题
名校
解题方法
4 . 为检验浓硫酸与木炭在加热条件下反应产生SO2和CO2气体,设计了如下图所示实验装置,a、b、c为止水夹,B是用于储气的气囊,D中放有用I2和淀粉的蓝色溶液浸湿的脱脂棉。
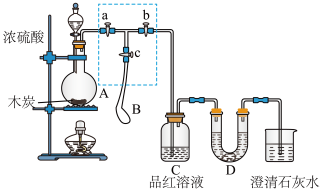
请回答下列问题:
(1)实验前欲检查装置A的气密性,可以采取的操作是_____________ 。
(2)此实验成败的关键在于控制反应产生气体的速率不能过快,由此设计了虚框部分的装置,则正确的操作顺序是_______________ (用操作编号填写);
①向A装置中加入浓硫酸,加热,使A中产生的气体进入气囊B,当气囊中充入一定量气体时,停止加热;
②待装置A冷却,且气囊B的体积不再变化后,关闭止水夹a,打开止水夹b,慢慢挤压气囊,使气囊B中气体慢慢进入装置C中,待达到实验目的后,关闭止水夹b;
③打开止水夹a和c,关闭止水夹b;
(3)实验时,装置C中的现象为____________________________________ 。
(4)当D中产生_____________ (多选不得分)现象时,可以说明使E中澄清石灰水变浑的是CO2,而不是SO2;A进气口一端脱脂棉蓝色变浅,出气口一端脱脂棉蓝色不变 B脱脂棉上蓝色均变浅 C脱脂棉上蓝色褪去。
则装置D的作用为_____________ 。

请回答下列问题:
(1)实验前欲检查装置A的气密性,可以采取的操作是
(2)此实验成败的关键在于控制反应产生气体的速率不能过快,由此设计了虚框部分的装置,则正确的操作顺序是
①向A装置中加入浓硫酸,加热,使A中产生的气体进入气囊B,当气囊中充入一定量气体时,停止加热;
②待装置A冷却,且气囊B的体积不再变化后,关闭止水夹a,打开止水夹b,慢慢挤压气囊,使气囊B中气体慢慢进入装置C中,待达到实验目的后,关闭止水夹b;
③打开止水夹a和c,关闭止水夹b;
(3)实验时,装置C中的现象为
(4)当D中产生
则装置D的作用为
您最近一年使用:0次
2017-02-17更新
|
1122次组卷
|
2卷引用:安徽省宿州市第二中学2022-2023学年高一上学期第一次月考化学试题
名校
5 . 苯甲酸(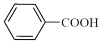 )具有广泛的用途,可用作食品防腐剂及有机合成的原料,实验室利用高锰酸钾溶液氧化甲苯制备苯甲酸,实验装置如图(部分装置省略):
)具有广泛的用途,可用作食品防腐剂及有机合成的原料,实验室利用高锰酸钾溶液氧化甲苯制备苯甲酸,实验装置如图(部分装置省略):
(1)仪器甲的名称是_______ ;仪器乙的进水口是_______ 。
(2)“反应混合物”是由9.20g甲苯和稍过量的KMnO4溶液组成的。反应混合物配制好后,溶液出现分层现象,上层为_______ (填“油状液体”或“紫红色溶液”)。
(3)“反应”在90℃、电动搅拌器作用下进行,并加热回流至分水器不再出现油珠。
①“反应”需在较高温度下进行并搅拌,其目的为_______ 。
②当分水器不再出现油珠时,这说明_______ 。
(4)用浓盐酸酸化时的相关化学方程式为_______ 。
(5)采用“减压过滤”的优点是_______ 。
(6)粗苯甲酸提纯后获得11.53g晶体,则苯甲酸的产率为_______ %(计算结果保留三位有效数字)。
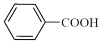 )具有广泛的用途,可用作食品防腐剂及有机合成的原料,实验室利用高锰酸钾溶液氧化甲苯制备苯甲酸,实验装置如图(部分装置省略):
)具有广泛的用途,可用作食品防腐剂及有机合成的原料,实验室利用高锰酸钾溶液氧化甲苯制备苯甲酸,实验装置如图(部分装置省略):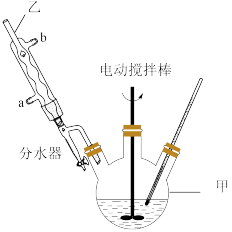

流程图中“反应”为: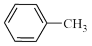 +2KMnO4
+2KMnO4
 +KOH+2MnO2↓+H2O。
+KOH+2MnO2↓+H2O。
(1)仪器甲的名称是
(2)“反应混合物”是由9.20g甲苯和稍过量的KMnO4溶液组成的。反应混合物配制好后,溶液出现分层现象,上层为
(3)“反应”在90℃、电动搅拌器作用下进行,并加热回流至分水器不再出现油珠。
①“反应”需在较高温度下进行并搅拌,其目的为
②当分水器不再出现油珠时,这说明
(4)用浓盐酸酸化时的相关化学方程式为
(5)采用“减压过滤”的优点是
(6)粗苯甲酸提纯后获得11.53g晶体,则苯甲酸的产率为
您最近一年使用:0次
2023-06-11更新
|
152次组卷
|
4卷引用:安徽省灵璧县第一中学2022-2023学年高二下学期6月学情调研考试化学试题
名校
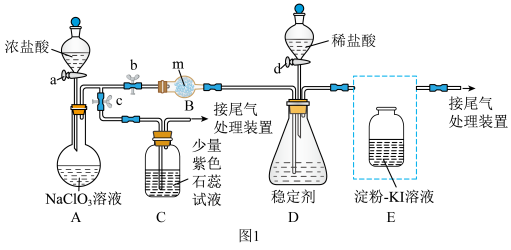
6 . ClO2与Cl2的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过如图所示装置对其制备、吸收、释放和应用进行了探究(夹持装置已省略)。
已知:
ⅰ.装置A中发生反应的化学方程式为 ;
;
ⅱ.淀粉遇 会呈现蓝色;
会呈现蓝色;
ⅲ.ClO2能溶于水但不与水反应。
回答下列问题:
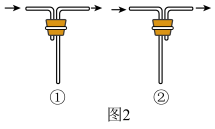
(1)仪器m的名称为___________ ;安装装置E中导管,应选用图2中的___________ (填“①”或“②”)。
(2)开始进行实验,打开a、c,关闭b,装置C中出现的实验现象为___________________ 。
(3)一段时间后,打开b,关闭c,ClO2在装置D中被稳定剂完全吸收生成NaClO2,此时装置E中溶液的颜色不变,则装置B的作用为___________ ;为保证ClO2气体被充分吸收,可以采取的措施为___________ (填字母)。
A.装置A中滴加浓盐酸的速率减慢 B.装置A中滴加浓盐酸的速率加快
C.装置D进气导管末端加一个多孔球泡 D.加热装置D,提升稳定剂的温度
(4)做ClO2释放实验时,关闭a、b,打开d,在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为___________ ;此时装置E的作用是___________ 。
(5)自来水用ClO2处理后,可用碘量法检测水中ClO2浓度,反应为 ,若1L水样消耗16.6g KI,则水样中ClO2的物质的量浓度为
,若1L水样消耗16.6g KI,则水样中ClO2的物质的量浓度为___________ mol·L-1。

已知:
ⅰ.装置A中发生反应的化学方程式为
 ;
;ⅱ.淀粉遇
 会呈现蓝色;
会呈现蓝色;ⅲ.ClO2能溶于水但不与水反应。
回答下列问题:
(1)仪器m的名称为

(2)开始进行实验,打开a、c,关闭b,装置C中出现的实验现象为
(3)一段时间后,打开b,关闭c,ClO2在装置D中被稳定剂完全吸收生成NaClO2,此时装置E中溶液的颜色不变,则装置B的作用为
A.装置A中滴加浓盐酸的速率减慢 B.装置A中滴加浓盐酸的速率加快
C.装置D进气导管末端加一个多孔球泡 D.加热装置D,提升稳定剂的温度
(4)做ClO2释放实验时,关闭a、b,打开d,在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为
(5)自来水用ClO2处理后,可用碘量法检测水中ClO2浓度,反应为
 ,若1L水样消耗16.6g KI,则水样中ClO2的物质的量浓度为
,若1L水样消耗16.6g KI,则水样中ClO2的物质的量浓度为
您最近一年使用:0次
2024-01-08更新
|
147次组卷
|
4卷引用:安徽省灵璧中学名校联考2023-2024学年高一上学期1月阶段性考试化学试题
7 . 已知氯气与碱反应时,产物受温度的影响。实验室中利用如图装置(部分装置省略)制备KClO3和NaClO,并探究其氧化还原性质。
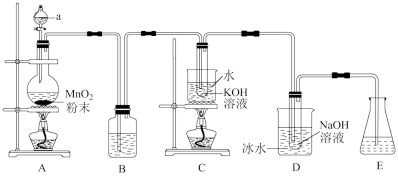
回答下列问题:
(1)仪器a的名称是___________ ;
(2)装置A产生氯气的化学方程式为___________ ;
(3)装置B中的试剂为___________ ;
(4)装置C采用的加热方式是___________ ;
(5)装置E选用试剂___________ (填标号);
A.NaCl溶液 B.NaOH溶液 C.澄清石灰水 D.稀硫酸
(6)探究KClO3、NaClO的氧化能力
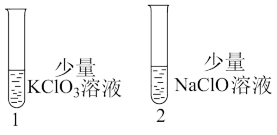
操作:向1号(KClO3)和2号(NaClO)试管中,滴加中性KI溶液。
现象:1号试管溶液颜色不变,2号试管溶液变为棕色。
结论:该条件下氧化能力KClO3___________ NaClO(填“大于”或“小于”)。

回答下列问题:
(1)仪器a的名称是
(2)装置A产生氯气的化学方程式为
(3)装置B中的试剂为
(4)装置C采用的加热方式是
(5)装置E选用试剂
A.NaCl溶液 B.NaOH溶液 C.澄清石灰水 D.稀硫酸
(6)探究KClO3、NaClO的氧化能力

操作:向1号(KClO3)和2号(NaClO)试管中,滴加中性KI溶液。
现象:1号试管溶液颜色不变,2号试管溶液变为棕色。
结论:该条件下氧化能力KClO3
您最近一年使用:0次
解题方法
8 . 84消毒液(有效成分NaClO)和医用酒精(75%的乙醇水溶液)都能用于杀菌消毒。
Ⅰ.84消毒液的制备:
(1)在实验室利用如图装置(电极材料为惰性电极)制备少量84消毒液,则a为电源的___________ 极(填“正”或“负”)。为提高NaClO的稳定性并抑制其水解,可向其溶液中加入少量___________ (填化学式)。
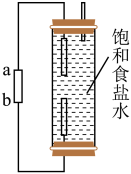
Ⅱ.对于网传的“84消毒液与酒精混用会产生氯气”的说法,某小组进行了如下活动。
查阅资料:
①乙醇能与NaClO发生一系列的复杂反应,可能生成氯气、乙醛、乙酸、氯仿等;
②乙醛具有强还原性,可以被NaClO、新制Cu(OH)2悬浊液等氧化。
实验探究:
采用某品牌的84消毒液和乙醇溶液按如图装置进行实验(加热及加持仪器略)。

(2)仪器A的作用是___________ ,为使C中乙醛(CH3CHO)含量较高,B中盛放的试剂为___________ 。实验室稀释84消毒液需要的玻璃仪器有___________ 。
(3)实验①和②中,仪器D中不变色的原因可能是:___________ 。
(4)有同学认为实验④产生的大量气泡中除Cl2外,还可能含有O2,产生的原因是___________ 。(用化学方程式表示)。
(5)试写出NaClO与C2H5OH反应生成CH3CHO的化学方程式___________ 。
Ⅰ.84消毒液的制备:
(1)在实验室利用如图装置(电极材料为惰性电极)制备少量84消毒液,则a为电源的

Ⅱ.对于网传的“84消毒液与酒精混用会产生氯气”的说法,某小组进行了如下活动。
查阅资料:
①乙醇能与NaClO发生一系列的复杂反应,可能生成氯气、乙醛、乙酸、氯仿等;
②乙醛具有强还原性,可以被NaClO、新制Cu(OH)2悬浊液等氧化。
实验探究:
采用某品牌的84消毒液和乙醇溶液按如图装置进行实验(加热及加持仪器略)。

| 编号. | ① | ② | ③ | ④ |
| 实验 | 75%乙醇与稀释100倍84消毒液,不加热 | 75%乙醇与稀释100倍84消毒液, 加热 | 95%乙醇与不稀释84消毒液,不加热 | 95% 乙醇与不稀释84消毒液,加热 |
| 仪器C中 | 无明显现象 | 无明显现象 | 少量气泡生成 | 大量气泡生成 |
| 仪器D中 | 不变色 | 不变色 | 变浅 | 变浅 |
(3)实验①和②中,仪器D中不变色的原因可能是:
(4)有同学认为实验④产生的大量气泡中除Cl2外,还可能含有O2,产生的原因是
(5)试写出NaClO与C2H5OH反应生成CH3CHO的化学方程式
您最近一年使用:0次
名校
解题方法
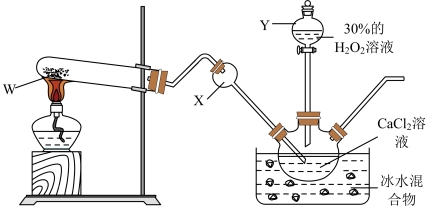
9 . 过氧化钙(CaO2)是一种白色的固体,微溶于水,且不溶于乙醇、乙醚和碱性溶液,溶于酸。利用反应Ca2++H2O2+2NH3+8H2O=CaO2∙8H2O+2 制备过氧化钙的装置如图所示。下列说法正确的是
制备过氧化钙的装置如图所示。下列说法正确的是
 制备过氧化钙的装置如图所示。下列说法正确的是
制备过氧化钙的装置如图所示。下列说法正确的是
| A.仪器Y的名称为长颈漏斗 |
| B.仪器X的作用是导气,并防止发生倒吸现象 |
| C.W可以是NH4Cl,通过加热W提供反应所需的NH3 |
| D.为加快反应速率和提高产率,可将冰水混合物改为温水浴加热 |
您最近一年使用:0次
2021-05-25更新
|
520次组卷
|
4卷引用:安徽省萧城一中2023届高三上学期期末考试化学试题
名校
解题方法
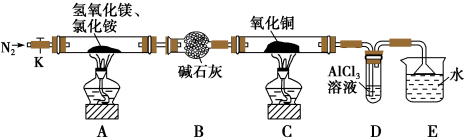
10 . 碱式氯化镁(MgOHCl)常用作塑料添加剂,工业上制备方法较多,其中利用氢氧化镁热分解氯化铵制氨气并得到碱式氯化镁的工艺属于我国首创。某中学科研小组根据该原理设计如下装置图进行相关实验,装置C中CuO的质量为8.0g。
请回答下列问题:
(1)装置A中发生反应生成碱式氯化镁的化学方程式为:______________ 。
(2)装置D中生成沉淀,发生反应的离子方程式为___________________ 。
(3)反应过程中持续通入N2的作用有两点:一是:将装置A中产生的氨气完全导出,二是:_______________________ 。
(4)反应完毕,装置C中的氧化铜全部由黑色变为红色,称其质量为6.8g,且生成的气体可直接排放到大气中,该反应中转移电子的物质的量为_______ mol。
(5)请你设计一个实验方案证明装置C中的氧化铜反应完全后得到的红色固体中含有氧化亚铜。已知:①Cu2O+2H+=Cu2++Cu+H2O
②限选试剂:2 mol·L-1H2SO4溶液、浓硫酸、2 mol·L-1HNO3溶液、10 mol·L-1 HNO3溶液

请回答下列问题:
(1)装置A中发生反应生成碱式氯化镁的化学方程式为:
(2)装置D中生成沉淀,发生反应的离子方程式为
(3)反应过程中持续通入N2的作用有两点:一是:将装置A中产生的氨气完全导出,二是:
(4)反应完毕,装置C中的氧化铜全部由黑色变为红色,称其质量为6.8g,且生成的气体可直接排放到大气中,该反应中转移电子的物质的量为
(5)请你设计一个实验方案证明装置C中的氧化铜反应完全后得到的红色固体中含有氧化亚铜。已知:①Cu2O+2H+=Cu2++Cu+H2O
②限选试剂:2 mol·L-1H2SO4溶液、浓硫酸、2 mol·L-1HNO3溶液、10 mol·L-1 HNO3溶液
| 实验步骤 | 预期现象和结论 |
| 步骤1:取反应后装置C中的少许固体于试管中 | |
| 步骤2: |
您最近一年使用:0次



