名校
1 . 某含铜样品的主要成分为aCuCO3·bCu(OH)2(a、b均为最简正整数),为测定其化学组成和Cu元素的质量分数,甲、乙两个实验小组经查阅资料,设计了两种不同的实验方案(假定杂质对实验无干扰)。
Ⅰ.甲组同学利用以下方法测定:
①在一定质量的样品中加入过量的稀硫酸,过滤,测量产生气体的体积(忽略水蒸气的体积);
②在滤液中加过量的NaOH稀溶液,过滤;
③灼烧②中所得滤渣,直至残留固体恒重。
(1)为了除去滤渣中的可溶性杂质,需要对滤渣进行的操作是_______ 。滤渣应在_________________________ (填仪器名称)中进行灼烧。
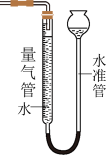
(2)利用如图装置测量气体体积时,读数时应注意:①恢复至室温;②________ ;③平视且视线与凹液面最低处相切。若操作无误,但气体体积测量结果仍然明显偏低,合理的改进措施是__________ 。
(3)甲组同学在处理实验数据时,将常温常压下测得的气体体积VL换算成V/22.4 mol进行计算,则计算所得的a将_______ (填“偏大”“偏小”或“无影响”)。
Ⅱ.乙组同学利用如图装置进行测定(夹持及加热装置略去):

(4)装置B中的药品是_______ ,装置D的作用是__________________________ 。
(5)若样品的质量为20 g,充分反应后测得装置B中固体质量增加了0.9 g,装置C中固体质量增加了4.4 g,则样品中主要成分的化学式为__________ ,样品中铜元素的质量分数为______________________ 。
Ⅰ.甲组同学利用以下方法测定:
①在一定质量的样品中加入过量的稀硫酸,过滤,测量产生气体的体积(忽略水蒸气的体积);
②在滤液中加过量的NaOH稀溶液,过滤;
③灼烧②中所得滤渣,直至残留固体恒重。

(1)为了除去滤渣中的可溶性杂质,需要对滤渣进行的操作是
(2)利用如图装置测量气体体积时,读数时应注意:①恢复至室温;②
(3)甲组同学在处理实验数据时,将常温常压下测得的气体体积VL换算成V/22.4 mol进行计算,则计算所得的a将
Ⅱ.乙组同学利用如图装置进行测定(夹持及加热装置略去):

(4)装置B中的药品是
(5)若样品的质量为20 g,充分反应后测得装置B中固体质量增加了0.9 g,装置C中固体质量增加了4.4 g,则样品中主要成分的化学式为
您最近一年使用:0次
名校
2 . 人教版高中化学选修4实验2-3中用到了硫代硫酸钠,某化学兴趣小组对这一物质展开了如下探究。

实验一.制备Na2S2O3·5H2O
通过查阅资料,该化学兴趣小组设计了如下的装置(略去部分夹持仪器)来制取Na2S2O3·5H2O晶体。
已知烧瓶C中发生如下三个反应:
Na2S(aq)+H2O(l)+SO2(g) = Na2SO3(aq)+H2S(aq)
2H2S(aq)+SO2(g) =3S(s)+2H2O(l);S(s)+Na2SO3(aq) Na2S2O3(aq)
Na2S2O3(aq)
(1)写出A中的化学反应方程式___________________________________ 。
(2)装置B的作用之一是观察SO2的生成速率。控制SO2生成速率可以采取的措施有_________________________ (写一条)。
(3)装置E的作用是____________________ 。
(4)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为_________________________ 。
实验二.性质探究
(5)常温下,用pH试纸测定0.1mol·L-1 Na2S2O3溶液pH值约为8,测定时的具体操作是_______________________________________________________ 。
(6)向新制氯水中滴加少量Na2S2O3溶液,氯水颜色变浅,有硫酸根离子生成,写出该反应的离子化学方程式________________________________________ 。
实验三.Na2S2O3的应用
(7)用Na2S2O3溶液测定废水中Ba2+浓度,步骤如下:取废水25.00mL,控制适当的酸度加入足量K2Cr2O7溶液,得BaCrO4沉淀;过滤、洗涤后,用适量稀盐酸溶解。此时CrO42-全部转化为Cr2O72-;再加过量KI溶液,充分反应后,加入淀粉溶液作指示剂,用0.0100mol·L-1的Na2S2O3标准溶液进行滴定,反应完全时,相关数据记录如下表所示:
部分反应的离子方程式为:
① Cr2O72-+6I-+14H+=3I2+2Cr3++7H2O
② I2+2S2O32-=S4O62-+2I-
滴定时Na2S2O3标准溶液应该用_____________________ (填仪器名称) 盛装,该废水中Ba2+的物质的量浓度为_______________________ 。

实验一.制备Na2S2O3·5H2O
通过查阅资料,该化学兴趣小组设计了如下的装置(略去部分夹持仪器)来制取Na2S2O3·5H2O晶体。
已知烧瓶C中发生如下三个反应:
Na2S(aq)+H2O(l)+SO2(g) = Na2SO3(aq)+H2S(aq)
2H2S(aq)+SO2(g) =3S(s)+2H2O(l);S(s)+Na2SO3(aq)
 Na2S2O3(aq)
Na2S2O3(aq)(1)写出A中的化学反应方程式
(2)装置B的作用之一是观察SO2的生成速率。控制SO2生成速率可以采取的措施有
(3)装置E的作用是
(4)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为
实验二.性质探究
(5)常温下,用pH试纸测定0.1mol·L-1 Na2S2O3溶液pH值约为8,测定时的具体操作是
(6)向新制氯水中滴加少量Na2S2O3溶液,氯水颜色变浅,有硫酸根离子生成,写出该反应的离子化学方程式
实验三.Na2S2O3的应用
(7)用Na2S2O3溶液测定废水中Ba2+浓度,步骤如下:取废水25.00mL,控制适当的酸度加入足量K2Cr2O7溶液,得BaCrO4沉淀;过滤、洗涤后,用适量稀盐酸溶解。此时CrO42-全部转化为Cr2O72-;再加过量KI溶液,充分反应后,加入淀粉溶液作指示剂,用0.0100mol·L-1的Na2S2O3标准溶液进行滴定,反应完全时,相关数据记录如下表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
| 消耗Na2S2O3标准溶液的体积/mL | 18.02 | 20.03 | 17.98 | 18.00 |
① Cr2O72-+6I-+14H+=3I2+2Cr3++7H2O
② I2+2S2O32-=S4O62-+2I-
滴定时Na2S2O3标准溶液应该用
您最近一年使用:0次
2018-05-13更新
|
842次组卷
|
3卷引用:西藏自治区拉萨市拉萨中学2021届高三第一次月考理综化学试题
3 . 某化学实验小组为了验证SO2和C12的漂白性,设计了如图所示的实验装置:
(1)已知制备SO2的原理为Na2SO3+H2SO4=Na2SO4+H2O+SO2↑,使用A装置;制备Cl2采用实验室制法,反应方程式为_______________ 。
(2)E装置中盛放浓盐酸的仪器为_________ ,作用为_________ ;
(3)反应开始后,发现B、D试管中的品红溶液都褪色,停止通气后,给B、D两个试管中的溶液加热,B、D试管中的现象是_________ 。
(4) 装置C的作用是_________ 。
(5)该小组同学将两种气体混合后通入品红溶液,一段时间后,品红溶液几乎不褪色查阅资料得知:两种气体按体积比1:1混合,再与水反应可生成两种常见酸,因而失去漂白作用。该反应的化学方程式为_________ 。

(1)已知制备SO2的原理为Na2SO3+H2SO4=Na2SO4+H2O+SO2↑,使用A装置;制备Cl2采用实验室制法,反应方程式为
(2)E装置中盛放浓盐酸的仪器为
(3)反应开始后,发现B、D试管中的品红溶液都褪色,停止通气后,给B、D两个试管中的溶液加热,B、D试管中的现象是
(4) 装置C的作用是
(5)该小组同学将两种气体混合后通入品红溶液,一段时间后,品红溶液几乎不褪色查阅资料得知:两种气体按体积比1:1混合,再与水反应可生成两种常见酸,因而失去漂白作用。该反应的化学方程式为
您最近一年使用:0次
名校
解题方法
4 . 实验题。查阅资料知:Br2的沸点为58.8℃,密度为3.119g·cm-3微溶于水,有毒。
Ⅰ.(1)常温下,单质溴通常呈________ 态,保存时通常在盛溴的试剂瓶中加入少量__________ 。
Ⅱ.工业生产中,海水提取溴常用空气吹出法。其生产流程可用下图表示:
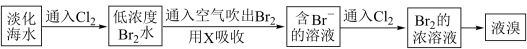
某化学实验小组模拟该法设计了如下实验装置(夹持装置略去)从浓缩的海水中提取液溴
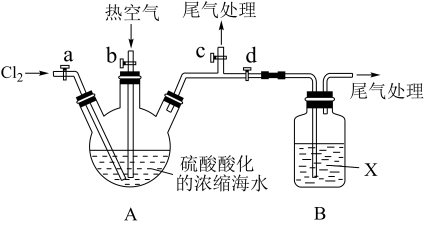
实验步骤如下:
① 关闭活塞b、d,打开活塞a、c,向A中缓慢通入Cl2至反应结束;
② 关闭a、c,打开b、d,向A中鼓入足量热空气;
③ 关闭b,打开a,再通过A向B中通入足量的Cl2;
④ 将B中所得液体进行蒸馏,收集液溴。
(2)当观察到A中液面上方出现_________ (实验现象)即可判断步骤①中反应已经结束。
(3)X试剂可以是_________ (填序号),尾气处理选用_________ (填序号)。
a.H2O b.饱和食盐水 c.氢氧化钠溶液 D.饱和Na2SO3溶液
B中X试剂发生反应的离子方程式为________________________ 。
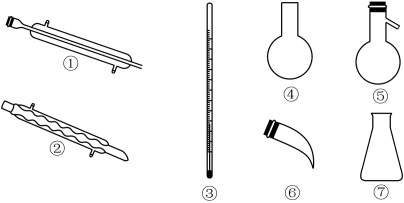
(4)蒸馏时应该选择_________ ,操作中应控制的关键实验条件为__________________ 。
Ⅰ.(1)常温下,单质溴通常呈
Ⅱ.工业生产中,海水提取溴常用空气吹出法。其生产流程可用下图表示:
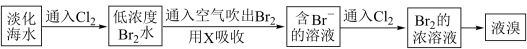
某化学实验小组模拟该法设计了如下实验装置(夹持装置略去)从浓缩的海水中提取液溴

实验步骤如下:
① 关闭活塞b、d,打开活塞a、c,向A中缓慢通入Cl2至反应结束;
② 关闭a、c,打开b、d,向A中鼓入足量热空气;
③ 关闭b,打开a,再通过A向B中通入足量的Cl2;
④ 将B中所得液体进行蒸馏,收集液溴。
(2)当观察到A中液面上方出现
(3)X试剂可以是
a.H2O b.饱和食盐水 c.氢氧化钠溶液 D.饱和Na2SO3溶液
B中X试剂发生反应的离子方程式为
(4)蒸馏时应该选择

您最近一年使用:0次
2017-02-17更新
|
275次组卷
|
3卷引用:2017届西藏林芝一中高三上月考四化学试卷
名校
5 . W、X、Y、Z均为短周期元素,W的最外层电子数与核外电子总数之比为3:8;X与W同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反应为黄色。下列判断正确的是( )
| A.原子半径:Y>Z |
| B.简单氢化物的沸点:X>W |
| C.离子的还原性:X>W |
| D.Y、Z的最高价氧化物对应的水化物的碱性:Y>Z |
您最近一年使用:0次
2020-11-25更新
|
293次组卷
|
4卷引用:西藏林芝市第二高级中学2021届高三上学期第四次月考理综化学试题
6 . 某实验小组设计如下实验探究二价铁的还原性。
(1)实验所用的FeSO4溶液由Fe2(SO4)3溶液和足量铁粉反应制得,发生反应的离子方程式为______ 。
(2)实验Ⅰ中白色沉淀变为红褐色,发生反应的化学方程式为_____________ 。
(3)探究实验Ⅱ中白色沉淀的组成。
①预测沉淀的组成。已知Fe(HCO3)2在水中不存在。
假设a:依据NaHCO3溶液显___ 性,推测白色沉淀可能为Fe(OH)2
假设b:白色沉淀还可能为______ (填化学式)。
②实验探究沉淀的组成。
i.取少量白色沉淀,充分洗涤,向其中加入稀硫酸,沉淀完全溶解,产生无色气泡。
ii向i所得溶液中滴入KSCN溶液,溶液几乎不变红。
iii向ⅱ溶液中再滴入少量H2O2,溶液立即变为红色。
由此可知,白色沉淀中一定含有的离子为________________ (填离子符号)。
③探究过程中发现白色沉淀在空气中久置,最终变为红褐色。则该沉淀比实验Ⅰ中所得的Fe(OH)2_________ (填“难”或“易”)于被空气氧化。
| 序号 | 实验方案 | 现象 |
| Ⅰ |  | 现象a:生成白色沉淀,3min后沉淀基本变为红色 |
| Ⅱ | 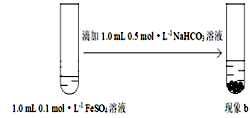 | 现象b:生成白色沉淀,3min后沉淀颜色几乎不变 |
(2)实验Ⅰ中白色沉淀变为红褐色,发生反应的化学方程式为
(3)探究实验Ⅱ中白色沉淀的组成。
①预测沉淀的组成。已知Fe(HCO3)2在水中不存在。
假设a:依据NaHCO3溶液显
假设b:白色沉淀还可能为
②实验探究沉淀的组成。
i.取少量白色沉淀,充分洗涤,向其中加入稀硫酸,沉淀完全溶解,产生无色气泡。
ii向i所得溶液中滴入KSCN溶液,溶液几乎不变红。
iii向ⅱ溶液中再滴入少量H2O2,溶液立即变为红色。
由此可知,白色沉淀中一定含有的离子为
③探究过程中发现白色沉淀在空气中久置,最终变为红褐色。则该沉淀比实验Ⅰ中所得的Fe(OH)2
您最近一年使用:0次
2020-05-15更新
|
1472次组卷
|
5卷引用:西藏自治区林芝市第二高级中学2021届高三上学期第二次月考理综化学试题
名校
解题方法
7 . 葡萄酒中的酒精是葡萄果实中的糖发酵后的产物(C6H12O6 2CH3CH2OH+2CO2↑)。
2CH3CH2OH+2CO2↑)。
Ⅰ.已知:实验室制乙烯原理为CH3CH2OH CH2=CH2↑+H2O,产生的气体能使Br2的四氯化碳溶液褪色,甲、乙同学用下列实验验证。(气密性已检验,部分夹持装置略)。实验操作和现象:
CH2=CH2↑+H2O,产生的气体能使Br2的四氯化碳溶液褪色,甲、乙同学用下列实验验证。(气密性已检验,部分夹持装置略)。实验操作和现象:
(1)溶液“渐渐变黑”,说明浓硫酸具有___ 性。
(2)对产生的气体进行分析,甲认为是C2H4,乙认为不能排除SO2的作用。
①写出实验室制取SO2的化学反应方程式是___ ;
②乙根据现象认为实验中产生的SO2和___ ,使B中有色物质反应褪色。
③为证实各自观点,甲、乙重新实验,设计与现象如下:
甲:在A、B间增加一个装有某种试剂的洗气瓶;现象:Br2的CCl4溶液褪色。
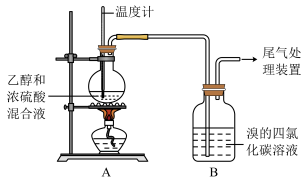
乙:用下列装置按一定顺序与A连接:(尾气处理装置略)

现象:C中溶液由红棕色变为浅红棕色时,E中溶液褪色。
请回答下列问题:
a.甲设计实验中A、B间洗气瓶中盛放的试剂是___ ;乙设计的实验D中盛放的试剂是___ ,装置连接顺序为___ (用仪器接口字母编号)。
b.能说明确实是SO2使E中溶液褪色的实验是___ 。
c.乙为进一步验证其观点,取少量C中溶液,加入几滴BaCl2溶液,振荡,产生大量白色沉淀,浅红棕色消失,发生反应的离子方程式是___ 。由此可得出的干燥的SO2不能使Br2的四氯化碳溶液褪色。
Ⅱ.葡萄酒中常用Na2S2O5做抗氧化剂。
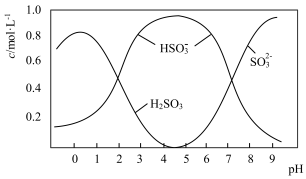
(3)0.5molNa2S2O5溶于水配成1L溶液,该溶液的pH=4.5。溶液中部分微粒浓度随溶液酸碱性变化如图所示。写出Na2S2O5溶于水时溶液中离子浓度由大到小的排列顺序___ 。
(4)已知:Ksp[BaSO4]=1×10-10,Ksp[BaSO3]=5×10-7。把部分被空气氧化的该溶液的pH调为10,向溶液中滴加BaCl2溶液使SO42-沉淀完全[c(SO42-)≤1×10-5mol·L-1],此时溶液中c(SO32-)≤___ mol·L-1。
 2CH3CH2OH+2CO2↑)。
2CH3CH2OH+2CO2↑)。Ⅰ.已知:实验室制乙烯原理为CH3CH2OH
 CH2=CH2↑+H2O,产生的气体能使Br2的四氯化碳溶液褪色,甲、乙同学用下列实验验证。(气密性已检验,部分夹持装置略)。实验操作和现象:
CH2=CH2↑+H2O,产生的气体能使Br2的四氯化碳溶液褪色,甲、乙同学用下列实验验证。(气密性已检验,部分夹持装置略)。实验操作和现象:
| 操作 | 现象 |
| 点燃酒精灯,加热至170℃ | Ⅰ:A中烧瓶内液体渐渐变黑 Ⅱ:B内气泡连续冒出,溶液逐渐褪色 |
| …… | |
| 实验完毕,清洗烧瓶 | Ⅲ:A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |
(2)对产生的气体进行分析,甲认为是C2H4,乙认为不能排除SO2的作用。
①写出实验室制取SO2的化学反应方程式是
②乙根据现象认为实验中产生的SO2和
③为证实各自观点,甲、乙重新实验,设计与现象如下:
甲:在A、B间增加一个装有某种试剂的洗气瓶;现象:Br2的CCl4溶液褪色。
乙:用下列装置按一定顺序与A连接:(尾气处理装置略)

现象:C中溶液由红棕色变为浅红棕色时,E中溶液褪色。
请回答下列问题:
a.甲设计实验中A、B间洗气瓶中盛放的试剂是
b.能说明确实是SO2使E中溶液褪色的实验是
c.乙为进一步验证其观点,取少量C中溶液,加入几滴BaCl2溶液,振荡,产生大量白色沉淀,浅红棕色消失,发生反应的离子方程式是
Ⅱ.葡萄酒中常用Na2S2O5做抗氧化剂。
(3)0.5molNa2S2O5溶于水配成1L溶液,该溶液的pH=4.5。溶液中部分微粒浓度随溶液酸碱性变化如图所示。写出Na2S2O5溶于水时溶液中离子浓度由大到小的排列顺序

(4)已知:Ksp[BaSO4]=1×10-10,Ksp[BaSO3]=5×10-7。把部分被空气氧化的该溶液的pH调为10,向溶液中滴加BaCl2溶液使SO42-沉淀完全[c(SO42-)≤1×10-5mol·L-1],此时溶液中c(SO32-)≤
您最近一年使用:0次
2020-04-13更新
|
181次组卷
|
2卷引用:西藏自治区拉萨市那曲第二高级中学2020届高三全真模拟联考理综化学试题
8 . 下列说法正确的是
A.HF、 、 、 、 、 的熔沸点、还原性都依次升高(增强) 的熔沸点、还原性都依次升高(增强) |
B. 、 、 分子构型均为正四面体,键角也相同 分子构型均为正四面体,键角也相同 |
| C.通常测定氟化氢的相对分子质量大于理论值,因分子间存在氢键 |
D.氯的各种含氧酸的酸性由强到弱排列为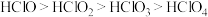 |
您最近一年使用:0次
名校
9 . 实验室进行二氧化硫制备与性质实验的组合装置如图所示,部分夹持装置未画出。
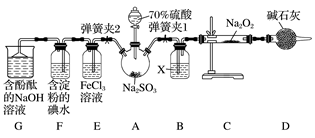
请回答下列问题:
(1)在组装好装置后,首先要进行的实验操作为_______________ 。
(2)为检验SO2与Na2O2的反应是否有氧气生成,装置B中盛放的试剂X应为________ ,装置D中碱石灰的作用是_______________________________________________ 。
(3)关闭弹簧夹2,打开弹簧夹1,注入70%的硫酸至浸没三颈烧瓶中的固体,检验SO2与Na2O2反应是否有氧气生成的操作及现象是_____________________________________ 。
(4)关闭弹簧夹1,打开弹簧夹2,残余气体进入装置E、F、G中,能说明I-的还原性弱于SO2的现象为_________________ 。发生反应的离子方程式是_______________ 。
(5)为了验证装置E中SO2与FeCl3发生了氧化还原反应,某学生设计了如下实验:取少量装置E中的溶液于试管中,向其中加入稀硝酸酸化的BaCl2溶液,产生白色沉淀,并由此判断SO2与FeCl3发生了氧化还原反应。上述方案是否合理?________ (填“合理”或“不合理”),原因是________ 。

请回答下列问题:
(1)在组装好装置后,首先要进行的实验操作为
(2)为检验SO2与Na2O2的反应是否有氧气生成,装置B中盛放的试剂X应为
(3)关闭弹簧夹2,打开弹簧夹1,注入70%的硫酸至浸没三颈烧瓶中的固体,检验SO2与Na2O2反应是否有氧气生成的操作及现象是
(4)关闭弹簧夹1,打开弹簧夹2,残余气体进入装置E、F、G中,能说明I-的还原性弱于SO2的现象为
(5)为了验证装置E中SO2与FeCl3发生了氧化还原反应,某学生设计了如下实验:取少量装置E中的溶液于试管中,向其中加入稀硝酸酸化的BaCl2溶液,产生白色沉淀,并由此判断SO2与FeCl3发生了氧化还原反应。上述方案是否合理?
您最近一年使用:0次
2017-06-03更新
|
607次组卷
|
5卷引用:西藏山南地区第二高级中学2017届高三第三次模拟考试理综化学试题
西藏山南地区第二高级中学2017届高三第三次模拟考试理综化学试题【全国百强校】陕西省西安中学2019届高三上学期期中考试化学试题陕西省咸阳百灵中学2020届高三上学期期中考试化学试题浙江省杭州地区(含周边)重点中学2020-2021学年高一下学期期中考试化学试题(已下线)【2023】【高一下】【其他】【杭高-期中复习卷】【高中化学】【刘尼尼收集】



