名校
1 . 氮的化合物种类繁多,性质也各不相同。请回答下列问题:
(1)已知:
①SO3(g)+NO(g)=NO2(g)+SO2(g) ∆H1=+41.8kJ·mol-1
②2SO2(g)+O2(g)=2SO3(g) ∆H2=-196.6kJ·mol-1
则2NO2(g)=2NO(g)+O2(g)的∆H=_______ 。
(2)NO作为主要空气污染物,其主要来源是汽车尾气,研究人员用活性炭对汽车尾气中的NO进行吸附,并发生反应:C(s)+2NO(g)⇌N2(g)+CO2(g) ∆H<0.在恒压密闭容器中加入足量活性炭和一定量NO气体,反应相同时间时,测得NO的转化率α(NO)随温度的变化如图所示:
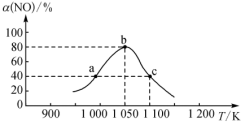
图中a、b、c三点中,达到平衡的点是_______ ;温度为1100K时,N2的平衡体积分数为_______ 。
(3)现代技术用氨气将汽车尾气中的NOx还原为N2和H2O,反应原理是NO(g)+NO2(g)+2NH3(g) 3H2O(g)+2N2(g) ∆H<0。
3H2O(g)+2N2(g) ∆H<0。
①实际生产中NO(g)+NO2(g)+2NH3(g) 3H2O(g)+2N2(g)的反应温度不宜过高的原因是
3H2O(g)+2N2(g)的反应温度不宜过高的原因是_______ 。
②500℃时,在2L恒容密闭容器中充入1molNO、1molNO2和2molNH3,8min时反应达到平衡,此时NH3的转化率为40%,体系压强为p0MPa,则0~8min内用N2表示的平均反应速率v(N2)=_______ mol·L-1·min-1,500℃时该反应的平衡常数Kp=_______ MPa(用含p0的代数式表示,Kp为以分压表示的平衡常数,分压=总压×物质的量分数)。
(1)已知:
①SO3(g)+NO(g)=NO2(g)+SO2(g) ∆H1=+41.8kJ·mol-1
②2SO2(g)+O2(g)=2SO3(g) ∆H2=-196.6kJ·mol-1
则2NO2(g)=2NO(g)+O2(g)的∆H=
(2)NO作为主要空气污染物,其主要来源是汽车尾气,研究人员用活性炭对汽车尾气中的NO进行吸附,并发生反应:C(s)+2NO(g)⇌N2(g)+CO2(g) ∆H<0.在恒压密闭容器中加入足量活性炭和一定量NO气体,反应相同时间时,测得NO的转化率α(NO)随温度的变化如图所示:

图中a、b、c三点中,达到平衡的点是
(3)现代技术用氨气将汽车尾气中的NOx还原为N2和H2O,反应原理是NO(g)+NO2(g)+2NH3(g)
 3H2O(g)+2N2(g) ∆H<0。
3H2O(g)+2N2(g) ∆H<0。①实际生产中NO(g)+NO2(g)+2NH3(g)
 3H2O(g)+2N2(g)的反应温度不宜过高的原因是
3H2O(g)+2N2(g)的反应温度不宜过高的原因是②500℃时,在2L恒容密闭容器中充入1molNO、1molNO2和2molNH3,8min时反应达到平衡,此时NH3的转化率为40%,体系压强为p0MPa,则0~8min内用N2表示的平均反应速率v(N2)=
您最近一年使用:0次
2021-07-13更新
|
3547次组卷
|
8卷引用:青海省西宁市大通回族土族自治县2021届高三下学期高考二模化学试题
名校
解题方法
2 . 以下是氮循环的一部分:
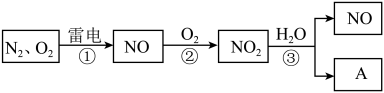
(1)反应②的化学方程式是___________ 。
(2)NO2易溶于水并和水发生化学反应,该反应中氧化剂和还原剂物质的量之比为________ 。
(3)实验室收集NO的方法为___________ 。
(4)化合物A的化学式是___________ 。
(5)治理汽车尾气的一种方法是用催化剂使NO与CO发生反应:2NO+2CO=2CO2+N2,当生成1molN2时,被还原的NO为___________ mol。

(1)反应②的化学方程式是
(2)NO2易溶于水并和水发生化学反应,该反应中氧化剂和还原剂物质的量之比为
(3)实验室收集NO的方法为
(4)化合物A的化学式是
(5)治理汽车尾气的一种方法是用催化剂使NO与CO发生反应:2NO+2CO=2CO2+N2,当生成1molN2时,被还原的NO为
您最近一年使用:0次
2022-03-29更新
|
1949次组卷
|
5卷引用:青海省西宁市湟中区多巴高级中学2021-2022学年高一下学期第一次月考化学试题
解题方法
3 . (1)已知实验室制备氧气可以用加热高锰酸钾的方法实现,其发生的反应为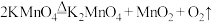 ,其中被氧化的元素是
,其中被氧化的元素是___ (填元素符号),还原产物是____ (填化学式)
(2)查阅资料可知,铜和浓 共热,发生反应
共热,发生反应 ,该反应中氧化剂与还原剂的个数之比为
,该反应中氧化剂与还原剂的个数之比为____ ,其中 在反应中表现
在反应中表现____ 。
(3)请配平下列反应方程式:___ 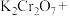
___ 
___ 
___ 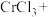
___ 
___  ,若反应中发生氧化反应的
,若反应中发生氧化反应的 个数为12,则反应中转移的电子数为
个数为12,则反应中转移的电子数为______ 。
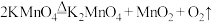 ,其中被氧化的元素是
,其中被氧化的元素是(2)查阅资料可知,铜和浓
 共热,发生反应
共热,发生反应 ,该反应中氧化剂与还原剂的个数之比为
,该反应中氧化剂与还原剂的个数之比为 在反应中表现
在反应中表现(3)请配平下列反应方程式:
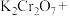


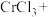

 ,若反应中发生氧化反应的
,若反应中发生氧化反应的 个数为12,则反应中转移的电子数为
个数为12,则反应中转移的电子数为
您最近一年使用:0次
2020-10-01更新
|
2881次组卷
|
5卷引用:青海省西宁市海湖中学2021届高三上学期第一阶段测试化学试题
青海省西宁市海湖中学2021届高三上学期第一阶段测试化学试题青海省西宁市海湖中学2021-2022学年高三上学期第一次月考化学试题人教版(2019)高一必修第一册 第一章 物质及其变化 章末综合检测卷(已下线)1.3.2 氧化剂和还原剂-2021-2022学年高一化学课后培优练(人教版2019必修第一册)(已下线)必考点05 氧化还原反应的规律及综合判断-【对点变式题】2021-2022学年高一化学上学期期中期末必考题精准练(人教版2019)
4 . I.某化学兴趣小组欲在实验室制备二氧化硫,并探究相关物质的一些性质。根据要求完成下列各小题。_______ 。
(2)如何验证生成二氧化硫_______ 。
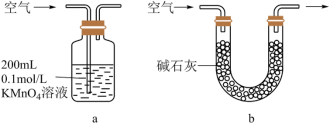
(3)某同学拟用如图装置测定空气中SO2的含量(假设空气中无其他还原性气体)。_____ (填“a”或“b”),理由是_______ 。
II.某中学化学研究性学习小组利用消石灰和氯化铵制取氨气,装置如图制取并探究氨气的性质。
(4)写出A中反应的化学方程式________ 。
(5)实验室收集氨气的方法是_______ 。
(6)C、D装置中颜色会发生变化的是________ (填“C”或“D”)。
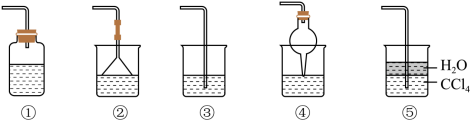
(7)为防止环境污染,以下装置(除⑤标明外,其余盛放的液体均为水)可用于吸收多余氨气的是_______ (填序号)。
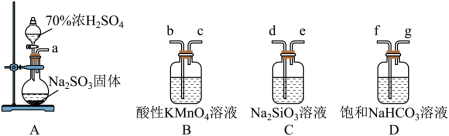
(2)如何验证生成二氧化硫
(3)某同学拟用如图装置测定空气中SO2的含量(假设空气中无其他还原性气体)。
II.某中学化学研究性学习小组利用消石灰和氯化铵制取氨气,装置如图制取并探究氨气的性质。
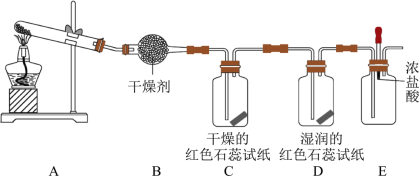
(4)写出A中反应的化学方程式
(5)实验室收集氨气的方法是
(6)C、D装置中颜色会发生变化的是
(7)为防止环境污染,以下装置(除⑤标明外,其余盛放的液体均为水)可用于吸收多余氨气的是
您最近一年使用:0次
2024-03-17更新
|
717次组卷
|
2卷引用:青海省西宁市第十四中学2023-2024学年高一下学期4月月考化学试卷
名校
解题方法
5 . 在一密闭容器中充入1 mol H2和1 mol I2,压强为p(Pa),并在一定温度下使其发生反应:H2(g)+I2(g)=2HI(g)
(1)保持容器容积不变,向其中充入1 mol H2,反应速率_________ 。
(2)升高温度,反应速率________ 。
(3)扩大容器体积,反应速率______ 。
(4)保持容器内气体压强不变,向其中充入1 mol H2(g)和1 mol I2(g),反应速率________ 。
(5)保持容器体积不变,向其中充入1 mol N2,反应速率________ 。
(6)保持容器内气体压强不变,向其中充入1 mol N2,反应速率________ 。
(1)保持容器容积不变,向其中充入1 mol H2,反应速率
(2)升高温度,反应速率
(3)扩大容器体积,反应速率
(4)保持容器内气体压强不变,向其中充入1 mol H2(g)和1 mol I2(g),反应速率
(5)保持容器体积不变,向其中充入1 mol N2,反应速率
(6)保持容器内气体压强不变,向其中充入1 mol N2,反应速率
您最近一年使用:0次
2021-05-25更新
|
2523次组卷
|
9卷引用:青海省海东市第二中学2020-2021学年高二4月月考化学试题
青海省海东市第二中学2020-2021学年高二4月月考化学试题(已下线)第二章 第二节 影响化学反应速率的因素(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)(已下线)2.2 影响化学反应速率的因素-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)2.1.2 影响化学反应速率的因素-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)第2章 化学反应速率与化学平衡(基础过关卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)(已下线)2.1.2 影响化学反应速率的因素(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)第06讲 影响化学反应速率的因素(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)(已下线)第二章 化学反应速率与化学平衡(A卷·知识通关练)【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)湖南省长长沙市德成学校2023-2024学年高二上学期11月期中考试化学试题
解题方法
6 . 填空。
(1)现有下列6种物质:①稀豆浆②K2CO3溶液③Cl2④SO2⑤稀盐酸⑥氢氧化钠。
其中属于胶体的是_______ (填序号、下同),属于非电解质的是_______ ,属于单质的是_______ ,属于电解质的是_______ 。K2CO3的电离方程式是_______ 。
(2)在下列物质中,请选择正确的序号填空:①熔融的氢氧化钠②蔗糖③盐酸④金属钠⑤硫酸⑥二氧化硫气体⑦硫粉⑧石膏(CaSO4·2H2O)⑨酒精溶液
a.属于电解质的有_______ 。
b.属于非电解质的有_______ 。
c.上述状态下能导电的有_______ 。
d.上述状态下的电解质不能导电的有_______ 。
(1)现有下列6种物质:①稀豆浆②K2CO3溶液③Cl2④SO2⑤稀盐酸⑥氢氧化钠。
其中属于胶体的是
(2)在下列物质中,请选择正确的序号填空:①熔融的氢氧化钠②蔗糖③盐酸④金属钠⑤硫酸⑥二氧化硫气体⑦硫粉⑧石膏(CaSO4·2H2O)⑨酒精溶液
a.属于电解质的有
b.属于非电解质的有
c.上述状态下能导电的有
d.上述状态下的电解质不能导电的有
您最近一年使用:0次
名校
解题方法
7 . 有机物的表示方法多种多样,下面是常用的有机物的表示方法:
①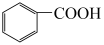 ②
② ③
③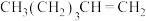 ④
④ ⑤
⑤ ⑥
⑥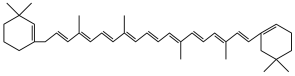 ⑦
⑦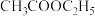 ⑧
⑧ ⑨
⑨ ⑩
⑩ ⑪
⑪
(1)写出⑧的分子式___________ ;
(2)用系统命名法给⑨命名,其名称为___________ 。
(3)属于酯的是___________ (填序号,下同),与②互为同分异构体的是___________ 。
(4)上述表示方法中属于结构式的为___________ ;属于键线式的为___________ ;
①
 ②
② ③
③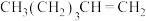 ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦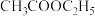 ⑧
⑧ ⑨
⑨ ⑩
⑩ ⑪
⑪
(1)写出⑧的分子式
(2)用系统命名法给⑨命名,其名称为
(3)属于酯的是
(4)上述表示方法中属于结构式的为
您最近一年使用:0次
2022-05-10更新
|
779次组卷
|
5卷引用:青海省西宁市青海湟川中学2022-2023学年高二上学期12月月考化学试题
青海省西宁市青海湟川中学2022-2023学年高二上学期12月月考化学试题吉林省前郭尔罗斯蒙古族自治县蒙古族中学2020-2021学年高二下学期第二次月考化学试题(已下线)1.1.2 有机化合物中的共价键 同分异构现象(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修3)湖南省长沙市明德中学2021-2022学年高二下学期期中考试化学试题(已下线)【知识图鉴】单元讲练测必修第二册第七单元03巩固练
名校
8 . 用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH=+64.39 kJ·mol-1
2H2O2(l)=2H2O(l)+O2(g) ΔH=-196.46 kJ·mol-1
H2(g)+ O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1
(1)H2的燃烧热ΔH=_________ 。
(2)一定量的H2完全燃烧生成H2O(l)放出热量Q=1 143.36 kJ,则H2的质量为_________ g。
(3)在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为__________ 。
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH=+64.39 kJ·mol-1
2H2O2(l)=2H2O(l)+O2(g) ΔH=-196.46 kJ·mol-1
H2(g)+
 O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1(1)H2的燃烧热ΔH=
(2)一定量的H2完全燃烧生成H2O(l)放出热量Q=1 143.36 kJ,则H2的质量为
(3)在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为
您最近一年使用:0次
名校
解题方法
9 . 分类法在化学中起着非常重要的作用,现有下列物质:①Cl2、②NaOH溶液、③Cu、④冰水混合物、⑤Na2CO3•10H2O、⑥稀硫酸、⑦CO2、⑧镁铝合金。请回答下列问题:
(1)属于纯净物的有____ ,属于氧化物的有___ 。
(2)能导电的物质有____ ,属于电解质的有___ 。
(3)实验室中制取少量Fe(OH)3胶体的化学方程式为____ 。
(4)已知Cl2与NaOH反应的化学方程式是Cl2+2NaOH=NaCl+NaClO+H2O,该反应中氧化剂与还原剂的物质的量之比为____ ,标准状况下,11.2L的Cl2含有的原子数为____ 。
(1)属于纯净物的有
(2)能导电的物质有
(3)实验室中制取少量Fe(OH)3胶体的化学方程式为
(4)已知Cl2与NaOH反应的化学方程式是Cl2+2NaOH=NaCl+NaClO+H2O,该反应中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
解题方法
10 . 有以下几种物质:
A.硝酸钾固体 B.稀盐酸 C.胆矾(CuSO4∙5H2O)晶体 D.熔融的BaCl2 E.乙醇 F.氯气G.干冰 H.铝 I.碳酸氢钠固体 J.硫酸钾溶液
按要求回答下列问题:
(1)①以上物质中能导电的是___________ (填字母,下同)。
②以上物质中属于电解质的是___________ 。
③以上物质中属于氧化物的是___________ 。
④以上物质中属于混合物的是___________ 。
⑤以上物质中属于有机化合物的是___________ 。
⑥以上物质中属于单质且在氧化还原反应中只作还原剂的是___________ 。
(2)I溶于水的电离方程式为___________ ;D的水溶液与J反应的离子方程式为___________ 。
A.硝酸钾固体 B.稀盐酸 C.胆矾(CuSO4∙5H2O)晶体 D.熔融的BaCl2 E.乙醇 F.氯气G.干冰 H.铝 I.碳酸氢钠固体 J.硫酸钾溶液
按要求回答下列问题:
(1)①以上物质中能导电的是
②以上物质中属于电解质的是
③以上物质中属于氧化物的是
④以上物质中属于混合物的是
⑤以上物质中属于有机化合物的是
⑥以上物质中属于单质且在氧化还原反应中只作还原剂的是
(2)I溶于水的电离方程式为
您最近一年使用:0次
2022-06-22更新
|
550次组卷
|
2卷引用:青海玉树州三校2021-2022学年高一上学期期末考试化学试题



