名校
1 . 准确掌握化学基本概念和研究方法是学好化学的重要手段。按要求回答下列问题:
(1)有以下物质:
①熔融氯化钠 ②铝 ③乙醇 ④氨水 ⑤氯化氢气体 ⑥NaHSO4固体
ⅰ.其中能导电的是___________ (填序号,下同);属于非电解质的是___________ ;属于电解质的是___________ ;属于混合物的是___________ 。
ⅱ.写出物质⑥溶于水时的电离方程式:___________ 。
(2)关于酸、碱、盐的下列各种说法中,正确的是___________(填字母)。
(1)有以下物质:
①熔融氯化钠 ②铝 ③乙醇 ④氨水 ⑤氯化氢气体 ⑥NaHSO4固体
ⅰ.其中能导电的是
ⅱ.写出物质⑥溶于水时的电离方程式:
(2)关于酸、碱、盐的下列各种说法中,正确的是___________(填字母)。
| A.化合物电离时,生成的阳离子有氢离子的是酸 |
| B.化合物电离时,生成的阴离子有氢氧根离子的是碱 |
| C.化合物电离时,生成金属阳离子(或铵根离子)和酸根离子的是盐 |
| D.酸溶液一定显酸性,碱溶液一定显碱性,盐溶液一定显中性 |
您最近一年使用:0次
2023-08-17更新
|
1300次组卷
|
2卷引用:安徽省淮南第三中学2023-2024学年高一上学期10月月考化学试题
名校
解题方法
2 . 实验室中常用二氧化锰与浓盐酸共热制取氯气。某化学兴趣小组为制取较为纯净、干燥的氯气,设计了如图实验装置。
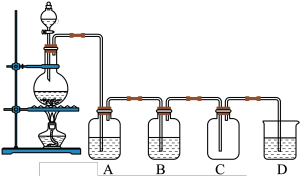
请回答下列问题:
(1)实验室制取Cl2的化学方程式为___________
(2)向烧瓶里加入少量___________ 粉末,分液漏斗中注入___________ 。
(3)A中盛放的是___________ ,其作用为___________ 。
(4)B中盛放的是___________ ,其作用为___________ 。
(5)D中盛放的是___________ ,其作用为___________ 。

请回答下列问题:
(1)实验室制取Cl2的化学方程式为
(2)向烧瓶里加入少量
(3)A中盛放的是
(4)B中盛放的是
(5)D中盛放的是
您最近一年使用:0次
2023-08-11更新
|
1069次组卷
|
4卷引用:安徽省舒城晓天中学2023-2024学年高一上学期第三次月考化学试卷
3 . 按要求回答下列问题:
(1)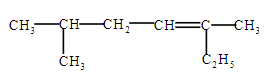 系统命名的名称为:
系统命名的名称为:___________ 。
(2)写出 2-丁烯在一定条件下加聚产物的结构简式_____
(3)某烃 A 0.2mol 在氧气中完全燃烧后,生成化合物 B、C 各 1.2mol,试回答:
①烃A的分子式为_______________
②若烃 A 不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯代物只有一种,则此烃A的结构简式为___________ 。
③若烃 A 能使溴水褪色,在催化剂作用下与 H2加成,其加成产物分子中含有 4 个甲基,烃 A 可能的结构简式为___________ ,___________ ,___________ 。
(1)
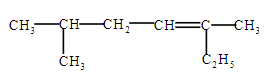 系统命名的名称为:
系统命名的名称为:(2)写出 2-丁烯在一定条件下加聚产物的结构简式
(3)某烃 A 0.2mol 在氧气中完全燃烧后,生成化合物 B、C 各 1.2mol,试回答:
①烃A的分子式为
②若烃 A 不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯代物只有一种,则此烃A的结构简式为
③若烃 A 能使溴水褪色,在催化剂作用下与 H2加成,其加成产物分子中含有 4 个甲基,烃 A 可能的结构简式为
您最近一年使用:0次
2021-03-22更新
|
2755次组卷
|
6卷引用:安徽省滁州市定远县育才学校2020-2021学年高二下学期期中考试化学试题
安徽省滁州市定远县育才学校2020-2021学年高二下学期期中考试化学试题江西省上饶市横峰中学2020-2021学年高二下学期入学考试(统招班)化学试题(已下线)2.1 脂肪烃(B级能力练)-2020-2021学年高二化学章节分层检测ABC(人教版选修5)(已下线)2.2 烯烃 炔烃(B级能力练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修3)(已下线)第2章 烃和卤代烃(基础过关卷)-2020-2021学年高二化学选修5章末集训必刷卷(人教版)陕西省延安市富县高级中学2021-2022学年高二上学期期末考试化学试题
4 . 回答下列问题:
(1)实验室制备氧气可以用加热高锰酸钾的方法实现,其发生的反应为2KMnO4 K2MnO4+MnO2+O2↑,其中被氧化的元素是
K2MnO4+MnO2+O2↑,其中被氧化的元素是___________ (填元素符号),还原产物是___________ (填化学式)。
(2)反应方程式:K2Cr2O7+14HCl 2KCl+2CrCl3+3Cl2↑+7H2O中还原剂是
2KCl+2CrCl3+3Cl2↑+7H2O中还原剂是___________ ,氧化产物是___________ 。
(3)下面三个方法都可以用来制氯气:
①4HCl(浓)+MnO2 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
②KClO3+6HCl(浓)=3Cl2↑+KCl+3H2O
③KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O(未配平)
根据以上三个反应,回答下列有关问题:
1、反应②的离子方程式为___________ 。
II、反应①中,氧化产物与还原产物的质量比为___________ 。
III、已知反应④:4HCl+O2 2Cl2+2H2O(g),该反应也能制得氯气。提示:反应条件越简单反应越容易发生,说明性质越强烈。则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为
2Cl2+2H2O(g),该反应也能制得氯气。提示:反应条件越简单反应越容易发生,说明性质越强烈。则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为___________ 。
IV、配平③______KMnO4+_____HCl(浓)=_____KCl+____MnCl2+_____Cl2↑+____H2O,___________
(1)实验室制备氧气可以用加热高锰酸钾的方法实现,其发生的反应为2KMnO4
 K2MnO4+MnO2+O2↑,其中被氧化的元素是
K2MnO4+MnO2+O2↑,其中被氧化的元素是(2)反应方程式:K2Cr2O7+14HCl
 2KCl+2CrCl3+3Cl2↑+7H2O中还原剂是
2KCl+2CrCl3+3Cl2↑+7H2O中还原剂是(3)下面三个方法都可以用来制氯气:
①4HCl(浓)+MnO2
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O②KClO3+6HCl(浓)=3Cl2↑+KCl+3H2O
③KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O(未配平)
根据以上三个反应,回答下列有关问题:
1、反应②的离子方程式为
II、反应①中,氧化产物与还原产物的质量比为
III、已知反应④:4HCl+O2
 2Cl2+2H2O(g),该反应也能制得氯气。提示:反应条件越简单反应越容易发生,说明性质越强烈。则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为
2Cl2+2H2O(g),该反应也能制得氯气。提示:反应条件越简单反应越容易发生,说明性质越强烈。则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为IV、配平③______KMnO4+_____HCl(浓)=_____KCl+____MnCl2+_____Cl2↑+____H2O,
您最近一年使用:0次
2022-04-05更新
|
2256次组卷
|
4卷引用: 安徽省定远中学2023-2024学年高一上学期第一次月考化学试题
安徽省定远中学2023-2024学年高一上学期第一次月考化学试题重庆市杨家坪中学2021-2022学年高一上学期第一次月考化学试题(已下线)第一章《物质及其变化》基础过关单元检测-【帮课堂】2022-2023学年高一化学必修第一册精品讲义(人教版2019)河北省石家庄市第二十四中学2023-2024学年高一上学期期中考试化学试题
解题方法
5 . 回答下面各题。
I.近年我国大力加强温室气体CO2催化氢化合成甲醇技术的工业化研究,实现可持续发展。
(1)已知:CO2(g)+H2(g)=H2O(g)+CO(g) ∆H1=+41.1kJ/mol
CO(g)+2H2(g)=CH3OH(g) ∆H2=-90.0kJ/mol
则CO2催化氢化合成甲醇的热化学方程式:___________ 。
II.工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
(2)判断反应达到平衡状态的依据是(填字母序号)___________。
(3)如表所列数据是反应在不同温度下的化学平衡常数(K)。
①由表中数据判断该反应的∆H___________ 0(填“>”、“=”或“<”);
②在250℃,将2mol CO和6mol H2充入2L的密闭容器中,充分反应后,某时刻测得c(CO)=0.3mol/L,则此时化学反应向___________ 方向移动 (填“正向”,“逆向”或“平衡”)。
(4)要提高CO的转化率,可以采取的措施是(填字母序号)___________ 。
a.增加CO的浓度 b.加入H2 c.分离出甲醇d. 加入催化剂 e.加入惰性气体 f.升温
III.在一定条件下, A(g)+3B(g) C(g)+D(g) ∆H=-49.0kJ/mol,体系中A的平衡转化率(α)与L和X的关系如图所示,L和X分别表示温度或压强。
C(g)+D(g) ∆H=-49.0kJ/mol,体系中A的平衡转化率(α)与L和X的关系如图所示,L和X分别表示温度或压强。

(5)X表示的物理量是___________ 。
(6)判断L1与L2的大小关系:L1___________ L2 (填“<”,“=”或“>”)。
I.近年我国大力加强温室气体CO2催化氢化合成甲醇技术的工业化研究,实现可持续发展。
(1)已知:CO2(g)+H2(g)=H2O(g)+CO(g) ∆H1=+41.1kJ/mol
CO(g)+2H2(g)=CH3OH(g) ∆H2=-90.0kJ/mol
则CO2催化氢化合成甲醇的热化学方程式:
II.工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:CO(g)+2H2(g)
 CH3OH(g)
CH3OH(g)(2)判断反应达到平衡状态的依据是(填字母序号)___________。
| A.生成CH3OH的速率与消耗CO的速率相等 |
| B.CH3OH、CO、H2的浓度都不再发生变化 |
| C.混合气体的相对平均分子质量不变 |
| D.混合气体的密度不变 |
| 温度℃ | 250 | 300 | 350 |
| K | 2.041 | 0.270 | 0.012 |
②在250℃,将2mol CO和6mol H2充入2L的密闭容器中,充分反应后,某时刻测得c(CO)=0.3mol/L,则此时化学反应向
(4)要提高CO的转化率,可以采取的措施是(填字母序号)
a.增加CO的浓度 b.加入H2 c.分离出甲醇d. 加入催化剂 e.加入惰性气体 f.升温
III.在一定条件下, A(g)+3B(g)
 C(g)+D(g) ∆H=-49.0kJ/mol,体系中A的平衡转化率(α)与L和X的关系如图所示,L和X分别表示温度或压强。
C(g)+D(g) ∆H=-49.0kJ/mol,体系中A的平衡转化率(α)与L和X的关系如图所示,L和X分别表示温度或压强。
(5)X表示的物理量是
(6)判断L1与L2的大小关系:L1
您最近一年使用:0次
名校
解题方法
6 . 党的二十大报告中强调“实现碳达峰碳中和是一场广泛而深刻的经济社会系统性变革”。 的转化和利用是实现碳中和的有效途径。回答下列问题。
的转化和利用是实现碳中和的有效途径。回答下列问题。
I.利用 合成淀粉的研究成果已经被我国科学家发表在Nature杂志上。其涉及的关键反应如下:
合成淀粉的研究成果已经被我国科学家发表在Nature杂志上。其涉及的关键反应如下:
①
②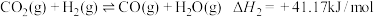
③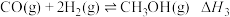
(1)反应③中
_______ ,该反应的自发条件是_______ (填“高温自发”“低温自发”或“任何温度下都自发”),该反应中活化能 (正)
(正)_______ (填“>”或“<”) (逆)。
(逆)。
(2)在催化剂作用下,按 的比例向某密闭容器中通入一定量的原料气只发生①②两个反应。维持压强为
的比例向某密闭容器中通入一定量的原料气只发生①②两个反应。维持压强为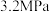 ,测得不同温度下,反应经过相同时间时
,测得不同温度下,反应经过相同时间时 的转化率、甲醇的选择性如图所示:
的转化率、甲醇的选择性如图所示:

已知:甲醇的选择性 。
。
①从图中曲线的变化趋势也可以判断出反应①是放热的,判断的依据是_______ ,在实际工业生产中压强不能过高也不能过低的原因是_______ 。
② 时,若反应从开始到达到a点所用时间为
时,若反应从开始到达到a点所用时间为 ,则
,则 的分压=
的分压=_______  ,
,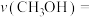
_______  ,反应②的
,反应②的
_______ ( 指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压=A的物质的量分数
指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压=A的物质的量分数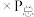 ,最终结果用分数表示)。
,最终结果用分数表示)。
II.近年来,有研究人员用 通过电催化生成多种燃料,实现
通过电催化生成多种燃料,实现 的回收利用,其工作原理如图所示。
的回收利用,其工作原理如图所示。

(3)请写出 电极上产生
电极上产生 的电极反应式:
的电极反应式:_______ 。
 的转化和利用是实现碳中和的有效途径。回答下列问题。
的转化和利用是实现碳中和的有效途径。回答下列问题。I.利用
 合成淀粉的研究成果已经被我国科学家发表在Nature杂志上。其涉及的关键反应如下:
合成淀粉的研究成果已经被我国科学家发表在Nature杂志上。其涉及的关键反应如下:①

②
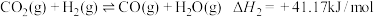
③
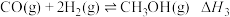
(1)反应③中

 (正)
(正) (逆)。
(逆)。(2)在催化剂作用下,按
 的比例向某密闭容器中通入一定量的原料气只发生①②两个反应。维持压强为
的比例向某密闭容器中通入一定量的原料气只发生①②两个反应。维持压强为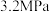 ,测得不同温度下,反应经过相同时间时
,测得不同温度下,反应经过相同时间时 的转化率、甲醇的选择性如图所示:
的转化率、甲醇的选择性如图所示:
已知:甲醇的选择性
 。
。①从图中曲线的变化趋势也可以判断出反应①是放热的,判断的依据是
②
 时,若反应从开始到达到a点所用时间为
时,若反应从开始到达到a点所用时间为 ,则
,则 的分压=
的分压= ,
,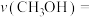
 ,反应②的
,反应②的
 指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压=A的物质的量分数
指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压=A的物质的量分数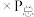 ,最终结果用分数表示)。
,最终结果用分数表示)。II.近年来,有研究人员用
 通过电催化生成多种燃料,实现
通过电催化生成多种燃料,实现 的回收利用,其工作原理如图所示。
的回收利用,其工作原理如图所示。
(3)请写出
 电极上产生
电极上产生 的电极反应式:
的电极反应式:
您最近一年使用:0次
2023-01-08更新
|
1608次组卷
|
3卷引用:安徽省皖北县中2022-2023学年高三上学期第一次五校联考化学试题
名校
解题方法
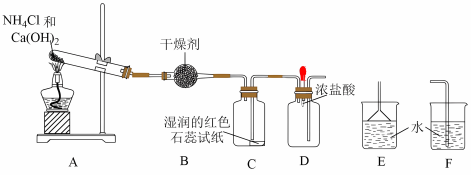
7 . 某实验小组利用以下装置制取氨气并探究氨气的性质:_____ 。
(2)装置B中的干燥剂是_____ (填名称)。
(3)装置C中的现象是_____ 。
(4)实验进行一段时间后,挤压装置D中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是_____ ,发生反应的化学方程式为_____ 。
(5)为防止过量氨气外逸,需在上述装置末端增加尾气吸收装置,应选用的装置是_____ (填“E”或“F”)。
(2)装置B中的干燥剂是
(3)装置C中的现象是
(4)实验进行一段时间后,挤压装置D中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
(5)为防止过量氨气外逸,需在上述装置末端增加尾气吸收装置,应选用的装置是
您最近一年使用:0次
2024-02-03更新
|
940次组卷
|
5卷引用:安徽省蚌埠市2023-2024学年高一上学期期末考试化学试题
解题方法
8 . (1)键线式 表示的物质的分子式为
表示的物质的分子式为___________ 。
(2) 中含有的官能团的名称为
中含有的官能团的名称为___________ 。
(3)戊烷的某种同分异构体只有一种一氯代物,试书写它的结构简式:___________ 。
(4)某芳香烃的结构为 ,它的分子式为
,它的分子式为___________ ,一氯代物有种___________ 。
(5)分子式为 的某烃的所有碳原子都在同一平面上,则该烃的结构简式为
的某烃的所有碳原子都在同一平面上,则该烃的结构简式为___________ ,若分子式为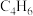 的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为
的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为___________ 。
 表示的物质的分子式为
表示的物质的分子式为(2)
 中含有的官能团的名称为
中含有的官能团的名称为(3)戊烷的某种同分异构体只有一种一氯代物,试书写它的结构简式:
(4)某芳香烃的结构为
 ,它的分子式为
,它的分子式为(5)分子式为
 的某烃的所有碳原子都在同一平面上,则该烃的结构简式为
的某烃的所有碳原子都在同一平面上,则该烃的结构简式为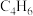 的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为
的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为
您最近一年使用:0次
2021-02-07更新
|
2407次组卷
|
4卷引用:安徽省合肥市庐巢七校联考2022-2023学年高二下学期期中考试化学试题
安徽省合肥市庐巢七校联考2022-2023学年高二下学期期中考试化学试题高二选择性必修3(人教版2019)第一章 有机化合物的结构特点与研究方法 第一节 有机化合物的结构特点 课时3 有机化合物的同分异构现象(已下线)第1章 认识有机化合物(基础过关卷)-2020-2021学年高二化学选修5章末集训必刷卷(人教版)(已下线)第02讲 同分异构(word讲义)-【帮课堂】2021-2022学年高二化学同步精品讲义(人教2019选择性必修3)
名校
解题方法
9 . CO2是一种廉价的碳资源,其综合利用具有重要意义。在容积为1L的恒容密闭容器中,充入1.00molCO2(g)和3.00molH2(g),一定条件下发生反应得到CH3OH(g)和H2O(g),测得反应物X和CH3OH(g)的浓度随时间的变化如图所示。
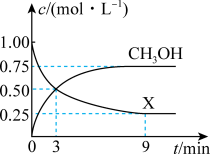
(1)0~3min内,v(CH3OH)=_______ (保留三位有效数字)mol·L-1·min-1。
(2)该反应的化学方程式为_______ 。
(3)X代表的物质为_______ (填化学式),理由是_______ 。
(4)9min后,保持其他条件不变,向容器中再通入1.00molCO2(g)和3.00molH2(g),则该反应的速率将_______ (填“增大”、“减小”或“不变”)。
(5)下列可以作为该反应已达到平衡的判据的是_______ (填标号)。
A.气体的压强不变 B.v正(CO2)=v逆(H2O)
C.CH3OH(g)与H2O(g)的浓度相同 D.容器内气体的密度不变

(1)0~3min内,v(CH3OH)=
(2)该反应的化学方程式为
(3)X代表的物质为
(4)9min后,保持其他条件不变,向容器中再通入1.00molCO2(g)和3.00molH2(g),则该反应的速率将
(5)下列可以作为该反应已达到平衡的判据的是
A.气体的压强不变 B.v正(CO2)=v逆(H2O)
C.CH3OH(g)与H2O(g)的浓度相同 D.容器内气体的密度不变
您最近一年使用:0次
2021-06-04更新
|
2235次组卷
|
7卷引用:安徽省皖八联盟2020-2021学年高一下学期统测化学试题
安徽省皖八联盟2020-2021学年高一下学期统测化学试题(已下线)第二章 第三节 化学平衡(第1课时 化学平衡状态)(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)(已下线)第2章 化学反应速率与化学平衡(基础过关卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)辽宁省庄河市高级中学2021-2022学年高二上学期10月月考化学试题(已下线)2.2.1 化学平衡状态(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)广东省佛山市第一中学2021-2022学年高一下学期期中考试化学试题山西省大同市第一中学校2023-2024学年高二上学期10月月考化学试题
名校
解题方法
10 . 某科学小组为研究不同价态含硫物质的转化设计了如图实验,请回答有关问题。

(1)装置A中发生反应的化学方程式为________ 。该反应体现了浓硫酸的_________ 性。
(2)B处实验现象是___________ ,由此推测硫元素从+4价变为+6价。
(3)检验B处有 生成的方法是
生成的方法是___________ 。
(4)C处观察到蘸有 溶液的棉花上出现黄色固体,可推测此反应过程中硫元素的价态变化分别是
溶液的棉花上出现黄色固体,可推测此反应过程中硫元素的价态变化分别是___________ 。
(5)D装置的作用是___________ ,发生反应的化学方程式为___________ 。
(6)工业上煅烧硫铁矿制取硫酸,煅烧 含
含 的硫铁矿石(杂质不参加反应),假设还有质量分数为4%的硫留在炉渣里,计算理论上可制备
的硫铁矿石(杂质不参加反应),假设还有质量分数为4%的硫留在炉渣里,计算理论上可制备 浓硫酸的质量为
浓硫酸的质量为___________  (提示:化合物中某元素的损失率=该化合物损失率)。
(提示:化合物中某元素的损失率=该化合物损失率)。

(1)装置A中发生反应的化学方程式为
(2)B处实验现象是
(3)检验B处有
 生成的方法是
生成的方法是(4)C处观察到蘸有
 溶液的棉花上出现黄色固体,可推测此反应过程中硫元素的价态变化分别是
溶液的棉花上出现黄色固体,可推测此反应过程中硫元素的价态变化分别是(5)D装置的作用是
(6)工业上煅烧硫铁矿制取硫酸,煅烧
 含
含 的硫铁矿石(杂质不参加反应),假设还有质量分数为4%的硫留在炉渣里,计算理论上可制备
的硫铁矿石(杂质不参加反应),假设还有质量分数为4%的硫留在炉渣里,计算理论上可制备 浓硫酸的质量为
浓硫酸的质量为 (提示:化合物中某元素的损失率=该化合物损失率)。
(提示:化合物中某元素的损失率=该化合物损失率)。
您最近一年使用:0次
2024-02-21更新
|
869次组卷
|
2卷引用:安徽省亳州市第二完全中学2023-2024学年高一下学期3月第一次月考化学试题



