2024高三·全国·专题练习
1 . 除去废水中Cr( )的方法有多种。请按要求回答下列问题。
)的方法有多种。请按要求回答下列问题。
(1)NaHSO3与熟石灰除Cr( )法:向酸性废水中加入NaHSO3,再加入熟石灰,使Cr3+沉淀。
)法:向酸性废水中加入NaHSO3,再加入熟石灰,使Cr3+沉淀。
①实验中NaHSO3的作用是___________ 。
②Cr( )在水溶液中的存在形态分布如图1所示。当pH>12时,Cr(
)在水溶液中的存在形态分布如图1所示。当pH>12时,Cr( )去除率下降的原因可用离子方程式表示为
)去除率下降的原因可用离子方程式表示为___________ 。
用硫酸盐还原菌(SRB)处理含Cr( )的废水时,Cr(
)的废水时,Cr( )去除率随温度的变化如图2所示。55 ℃时,Cr(Ⅵ)去除率很低的原因是
)去除率随温度的变化如图2所示。55 ℃时,Cr(Ⅵ)去除率很低的原因是___________ 。
①“酸浸、还原”时,反应的化学方程式为___________ 。
该步骤若pH过低,则消耗Na2S2O5的量比理论值高出许多,其原因是___________ (文字叙述)。
②“沉铬”时所发生反应的离子方程式为___________ 。能不能将纯碱改为足量NaOH溶液?___________ 。(给出结论,并结合离子方程式给出理由)
 )的方法有多种。请按要求回答下列问题。
)的方法有多种。请按要求回答下列问题。(1)NaHSO3与熟石灰除Cr(
 )法:向酸性废水中加入NaHSO3,再加入熟石灰,使Cr3+沉淀。
)法:向酸性废水中加入NaHSO3,再加入熟石灰,使Cr3+沉淀。①实验中NaHSO3的作用是
②Cr(
 )在水溶液中的存在形态分布如图1所示。当pH>12时,Cr(
)在水溶液中的存在形态分布如图1所示。当pH>12时,Cr( )去除率下降的原因可用离子方程式表示为
)去除率下降的原因可用离子方程式表示为
用硫酸盐还原菌(SRB)处理含Cr(
 )的废水时,Cr(
)的废水时,Cr( )去除率随温度的变化如图2所示。55 ℃时,Cr(Ⅵ)去除率很低的原因是
)去除率随温度的变化如图2所示。55 ℃时,Cr(Ⅵ)去除率很低的原因是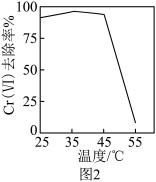

①“酸浸、还原”时,反应的化学方程式为
该步骤若pH过低,则消耗Na2S2O5的量比理论值高出许多,其原因是
②“沉铬”时所发生反应的离子方程式为
您最近半年使用:0次
2 . 下列玻璃仪器在相应实验中选用不合理的是
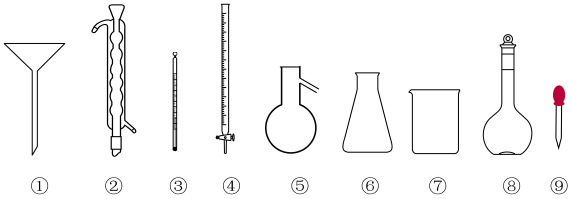
| A.蒸馏法分离乙醇和乙醚:③⑤⑥ |
B.重结晶法提纯 (含少量 (含少量 ):①②③ ):①②③ |
C.可用 硫酸溶液配制 硫酸溶液配制 硫酸溶液:④⑦⑧⑨ 硫酸溶液:④⑦⑧⑨ |
D.用 溶液滴定水中游离氯:④⑥ 溶液滴定水中游离氯:④⑥ |
您最近半年使用:0次
3 . 研究从含锌资源中获取Zn的途径具有重要意义。
Ⅰ.工业上酸浸提锌
氧化锌矿中含有ZnO、 、FeO、PbO、
、FeO、PbO、 、CaO、
、CaO、 等。
等。
ⅰ.几种难溶电解质的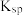
ⅱ.浸出液中主要金属阳离子浓度
(1)浸出渣的主要成分有 、
、 和
和 。PbO和
。PbO和 反应的离子方程式是
反应的离子方程式是___________ 。
(2)加入试剂a的目的是___________ 。
(3)电解前,含 溶液中铁和铝的离子浓度均需小于
溶液中铁和铝的离子浓度均需小于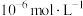 ,应调节pH的范围是(忽略①和②导致的体积变化)
,应调节pH的范围是(忽略①和②导致的体积变化)___________ 。
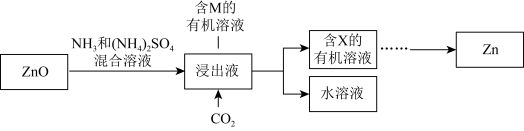
Ⅱ.实验室中氨浸提锌
ⅲ.

ⅳ.M的结构简式如图所示,R为 ,两个羟基中、酚羟基酸性较强。
,两个羟基中、酚羟基酸性较强。 浸取ZnO发生反应的离子方程式是
浸取ZnO发生反应的离子方程式是___________ 。
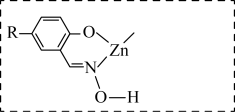
(5)M能与 形成稳定的配合物X,相关反应为
形成稳定的配合物X,相关反应为 。
。
①补全图中X的结构并用“…”标出氢键_______ 。 的萃取,原因可能是
的萃取,原因可能是___________ 。
(6)从平衡移动的角度解释 能提高有机溶液中X含量的原因:
能提高有机溶液中X含量的原因:___________ 。
Ⅰ.工业上酸浸提锌
氧化锌矿中含有ZnO、
 、FeO、PbO、
、FeO、PbO、 、CaO、
、CaO、 等。
等。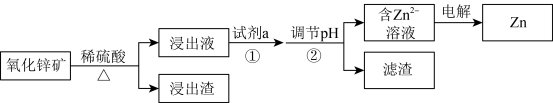
ⅰ.几种难溶电解质的
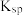
| 难溶电解质 |  |  |  |  |
 |  |  | 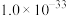 |  |
| 粒子 |  |  和Fe 和Fe | Al |
| 浓度(mol/L) | 0.3 | 0.1 | 0.1 |
(1)浸出渣的主要成分有
 、
、 和
和 。PbO和
。PbO和 反应的离子方程式是
反应的离子方程式是(2)加入试剂a的目的是
(3)电解前,含
 溶液中铁和铝的离子浓度均需小于
溶液中铁和铝的离子浓度均需小于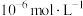 ,应调节pH的范围是(忽略①和②导致的体积变化)
,应调节pH的范围是(忽略①和②导致的体积变化)Ⅱ.实验室中氨浸提锌
ⅲ.


ⅳ.M的结构简式如图所示,R为
 ,两个羟基中、酚羟基酸性较强。
,两个羟基中、酚羟基酸性较强。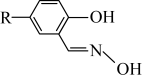
 浸取ZnO发生反应的离子方程式是
浸取ZnO发生反应的离子方程式是(5)M能与
 形成稳定的配合物X,相关反应为
形成稳定的配合物X,相关反应为 。
。①补全图中X的结构并用“…”标出氢键
 的萃取,原因可能是
的萃取,原因可能是(6)从平衡移动的角度解释
 能提高有机溶液中X含量的原因:
能提高有机溶液中X含量的原因:
您最近半年使用:0次
解题方法
4 . 科技强国,我国科学家在诸多领域取得新突破。
(1)芯片制造会经过六个最为关键的步骤:沉积、光刻胶涂覆、光刻、刻蚀、离子注入和封装。
其中“刻蚀”过程可能用到刻蚀剂 、
、 及清洗剂
及清洗剂 。
。
①基态F原子核外电子有_____ 种空间运动状态,下列为氟原子激发态的电子排布式的是_____ (填标号)。
A. B.
B. C.
C. D.
D.
②C、N、O、F四种元素的第一电离能由大到小的顺序为__________ 。
③氟硼酸铵( )中B的杂化方式为
)中B的杂化方式为__________ , 的空间构型为
的空间构型为__________ 。
(2)复兴号高铁车体材质用到了Mn、Co等元素。Mn的一种配合物的化学式为[Mn(CO)5(CH3CN)],CH3CN与Mn原子配位时,提供孤电子对的是__________ (填元素符号),Mn原子的配位数为__________ ,CH3CN中 键与
键与 键数目之比为
键数目之比为__________ 。
(3)超导材料 具有
具有 型结构(如图),晶胞参数(晶胞边长)为a pm,该氮化钛晶体的密度为
型结构(如图),晶胞参数(晶胞边长)为a pm,该氮化钛晶体的密度为__________ (列出计算式即可) 。
。
(1)芯片制造会经过六个最为关键的步骤:沉积、光刻胶涂覆、光刻、刻蚀、离子注入和封装。
其中“刻蚀”过程可能用到刻蚀剂
 、
、 及清洗剂
及清洗剂 。
。①基态F原子核外电子有
A.
 B.
B. C.
C. D.
D.
②C、N、O、F四种元素的第一电离能由大到小的顺序为
③氟硼酸铵(
 )中B的杂化方式为
)中B的杂化方式为 的空间构型为
的空间构型为(2)复兴号高铁车体材质用到了Mn、Co等元素。Mn的一种配合物的化学式为[Mn(CO)5(CH3CN)],CH3CN与Mn原子配位时,提供孤电子对的是
 键与
键与 键数目之比为
键数目之比为(3)超导材料
 具有
具有 型结构(如图),晶胞参数(晶胞边长)为a pm,该氮化钛晶体的密度为
型结构(如图),晶胞参数(晶胞边长)为a pm,该氮化钛晶体的密度为 。
。
您最近半年使用:0次
5 . 化学在“国之重器”的打造中发挥着重要作用。下列说法不正确的是
| A.“库车绿氢”用光伏发电电解水制氢,能有效减少碳排放 |
B.国产大飞机“ ”使用的芳纶蜂窝材料属于有机高分子材料 ”使用的芳纶蜂窝材料属于有机高分子材料 |
C.国产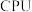 “龙芯 “龙芯 ”的主要材料与光导纤维的材料相同 ”的主要材料与光导纤维的材料相同 |
| D.“鲲龙”水陆两栖飞机所用的航空煤油是石油分馏产品 |
您最近半年使用:0次
名校
6 . 钇是稀土元素之一。我国蕴藏着丰富的钇矿石(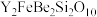 ),用NaOH初步处理钇矿石可以得到
),用NaOH初步处理钇矿石可以得到 、
、 、
、 和
和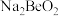 的共熔物。工业上利用该共熔物制取
的共熔物。工业上利用该共熔物制取 ,并获得副产物BeO,流程如图:
,并获得副产物BeO,流程如图:
ⅱ.在室温的条件下, ;
;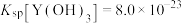 ;水的离子积
;水的离子积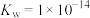 。
。
(1)基态铍原子的核外电子排布式为___________ 。
(2)滤渣1的主要成分是___________ 。沉铍时,过量的试剂最好选用___________ (填序号)。
A.NaOH溶液 B.氨水 C. D.CaO
D.CaO
(3)制取 时,第一次加氨水调pH的目的是
时,第一次加氨水调pH的目的是___________ 。
(4)计算常温下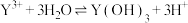 的平衡常数
的平衡常数
___________ 。
(5)过滤2所得的滤液经过一系列处理可得到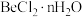 ,将
,将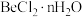 与足量的
与足量的 共热可以制备无水
共热可以制备无水 ,写出该过程的化学反应方程式:
,写出该过程的化学反应方程式:___________ 。
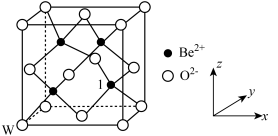
(6)BeO的立方晶胞如图所示:___________ 。
②若BeO晶体的密度为 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则晶胞中
,则晶胞中 与最近
与最近 之间的距离为
之间的距离为___________ nm。
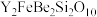 ),用NaOH初步处理钇矿石可以得到
),用NaOH初步处理钇矿石可以得到 、
、 、
、 和
和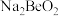 的共熔物。工业上利用该共熔物制取
的共熔物。工业上利用该共熔物制取 ,并获得副产物BeO,流程如图:
,并获得副产物BeO,流程如图: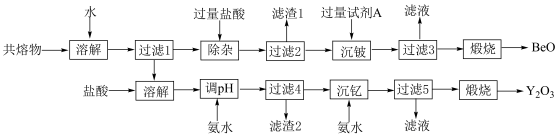
ⅱ.在室温的条件下,
 ;
;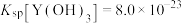 ;水的离子积
;水的离子积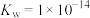 。
。(1)基态铍原子的核外电子排布式为
(2)滤渣1的主要成分是
A.NaOH溶液 B.氨水 C.
 D.CaO
D.CaO(3)制取
 时,第一次加氨水调pH的目的是
时,第一次加氨水调pH的目的是(4)计算常温下
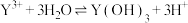 的平衡常数
的平衡常数
(5)过滤2所得的滤液经过一系列处理可得到
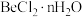 ,将
,将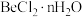 与足量的
与足量的 共热可以制备无水
共热可以制备无水 ,写出该过程的化学反应方程式:
,写出该过程的化学反应方程式:(6)BeO的立方晶胞如图所示:
②若BeO晶体的密度为
 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则晶胞中
,则晶胞中 与最近
与最近 之间的距离为
之间的距离为
您最近半年使用:0次
名校
7 . 氨合成已经塑造了我们的现代文明。如图是以苯酚(图中的BH)作为质子穿梭剂和缓冲液,用氮气( )和
)和 作为原料,利用电解原理在非水电解质中实现氨气的合成。
作为原料,利用电解原理在非水电解质中实现氨气的合成。
 )和
)和 作为原料,利用电解原理在非水电解质中实现氨气的合成。
作为原料,利用电解原理在非水电解质中实现氨气的合成。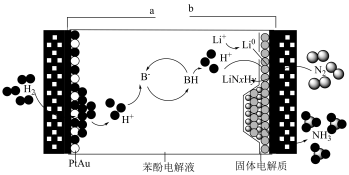
| A.a接电源的正极 |
B.将苯酚电解液换成纯水,消耗相同电量时, 的产量会降低 的产量会降低 |
C.生成氨气的电极反应式为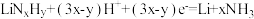 |
D.若消耗标准状况下22.4L的 ,则b极上质量增加14g ,则b极上质量增加14g |
您最近半年使用:0次
名校
8 . 如图所示,Ti和Au可以形成 和
和 两种不同类型的合金。在
两种不同类型的合金。在 类型晶胞(
类型晶胞( ,
,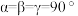 )中,Au原子位于顶点,Ti原子位于面心。在
)中,Au原子位于顶点,Ti原子位于面心。在 型晶胞(
型晶胞(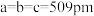 ,
, )中,Au原子位于顶点和体心,每个晶胞面上有两个Ti原子,它们之间的连线平行于晶胞的棱且连线中点为面心,它们之间的距离恰好是晶胞棱长的一半。
)中,Au原子位于顶点和体心,每个晶胞面上有两个Ti原子,它们之间的连线平行于晶胞的棱且连线中点为面心,它们之间的距离恰好是晶胞棱长的一半。
 和
和 两种不同类型的合金。在
两种不同类型的合金。在 类型晶胞(
类型晶胞( ,
,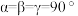 )中,Au原子位于顶点,Ti原子位于面心。在
)中,Au原子位于顶点,Ti原子位于面心。在 型晶胞(
型晶胞(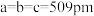 ,
, )中,Au原子位于顶点和体心,每个晶胞面上有两个Ti原子,它们之间的连线平行于晶胞的棱且连线中点为面心,它们之间的距离恰好是晶胞棱长的一半。
)中,Au原子位于顶点和体心,每个晶胞面上有两个Ti原子,它们之间的连线平行于晶胞的棱且连线中点为面心,它们之间的距离恰好是晶胞棱长的一半。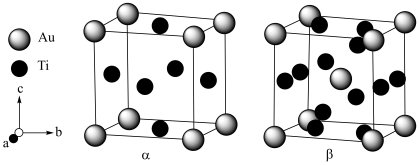
A. 和 和 两种合金的化学式都是 两种合金的化学式都是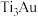 |
B. 和 和 两种晶胞中Ti的配位数均为6 两种晶胞中Ti的配位数均为6 |
C. 晶体的密度为 晶体的密度为 |
D. 型的合金硬度更高 型的合金硬度更高 |
您最近半年使用:0次
名校
9 . 一种直接以水作为氢源,低成本CO作为氧受体的无 乙炔加氢制乙烯过程如图所示。Au和
乙炔加氢制乙烯过程如图所示。Au和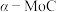 两种催化剂边界生成羟基作为温和还原剂,使乙炔选择性氢化,再以CO去除残留O。这一过程避免了经典路线中对
两种催化剂边界生成羟基作为温和还原剂,使乙炔选择性氢化,再以CO去除残留O。这一过程避免了经典路线中对 的需求,为低温下的乙炔水氢化开辟了途径。
的需求,为低温下的乙炔水氢化开辟了途径。
 乙炔加氢制乙烯过程如图所示。Au和
乙炔加氢制乙烯过程如图所示。Au和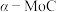 两种催化剂边界生成羟基作为温和还原剂,使乙炔选择性氢化,再以CO去除残留O。这一过程避免了经典路线中对
两种催化剂边界生成羟基作为温和还原剂,使乙炔选择性氢化,再以CO去除残留O。这一过程避免了经典路线中对 的需求,为低温下的乙炔水氢化开辟了途径。
的需求,为低温下的乙炔水氢化开辟了途径。
| A.步骤1→2,会放出能量 |
B.反应过程中Au和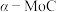 的作用都是改变反应的焓变 的作用都是改变反应的焓变 |
C.生成 的总反应为 的总反应为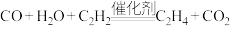 |
| D.步骤3→4,有极性键和非极性键的断裂 |
您最近半年使用:0次
名校
解题方法
10 . W、X、Y、Z、T五种元素原子序数依次增大,W的核外电子数等于其周期数,X、Y、Z为同周期且相邻的主族元素,Y的基态原子核外有3个单电子,T的价电子排布式为 ,5种元素可形成配位化合物
,5种元素可形成配位化合物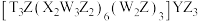 。下列说法不正确的是
。下列说法不正确的是
 ,5种元素可形成配位化合物
,5种元素可形成配位化合物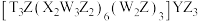 。下列说法不正确的是
。下列说法不正确的是| A.T位于元素周期表的第Ⅷ族 |
| B.配合物中T的化合价为+3 |
| C.X、Y、Z三种元素中,第一电离能最大的是Z |
| D.该配合物中存在的化学键类型有离子键、极性键、非极性键 |
您最近半年使用:0次



