解题方法
1 . 学校研究性学习小组欲用下图所示的装置证明H2SO3和HClO的酸性强弱(已知:H2SO3的酸性强于H2CO3)。下列有关说法错误的是
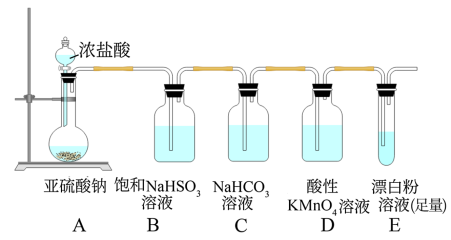

| A.装置C的作用是制备CO2气体 |
| B.通过本实验可以得出Cl元素的非金属性比S元素强 |
| C.直接将SO2气体通入Ca(ClO)2溶液中无法证明H2SO3和HClO的酸性强弱 |
| D.装置D颜色变浅但不褪色,且E中产生白色沉淀即可证明H2SO3酸性强于HClO |
您最近一年使用:0次
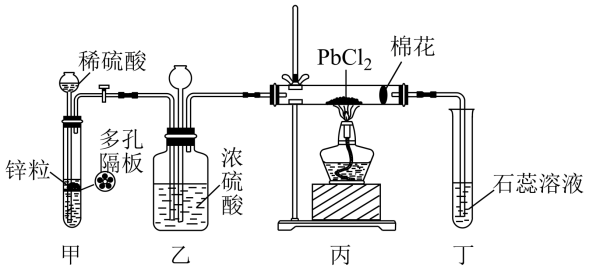
2 . 二氯化铅常温下为白色固体,沸点为 ,工业上常用作助焊剂。某小组同学欲证明氢气能否在加热的条件下还原二氯化铅,设计如下实验。下列说法错误的是
,工业上常用作助焊剂。某小组同学欲证明氢气能否在加热的条件下还原二氯化铅,设计如下实验。下列说法错误的是
 ,工业上常用作助焊剂。某小组同学欲证明氢气能否在加热的条件下还原二氯化铅,设计如下实验。下列说法错误的是
,工业上常用作助焊剂。某小组同学欲证明氢气能否在加热的条件下还原二氯化铅,设计如下实验。下列说法错误的是
| A.乙中长颈漏斗的作用是平衡压强 |
| B.点燃丙中酒精灯后,应先对直形玻璃管进行预热,然后再集中加热 |
| C.若丁中溶液变红,则可证明氢气能在加热的条件下还原二氯化铅 |
| D.甲中试剂可用浓盐酸代替,丁中试剂可用硝酸银溶液代替 |
您最近一年使用:0次
名校
解题方法
3 . 如图是实验室进行二氧化硫制备与性质探究实验的组合装置,部分固定装置未画出。下列有关说法正确的是


| A.关闭K1,打开K2,试剂X是酸性KMnO4或H2O2溶液,均可证明SO2有还原性 |
| B.关闭K2,打开K1,滴加H2SO4溶液,则装置B中每消耗1.5mol Na2O2,转移电子数为2NA |
| C.为防止环境污染,装置C和E中的试剂均取用氢氧化钠溶液 |
| D.实验过程中体现了H2SO4的酸性、难挥发性、强氧化性 |
您最近一年使用:0次
名校
4 . 某学生利用如图装置对电解质溶液导电性进行实验探究。下列说法中正确的是
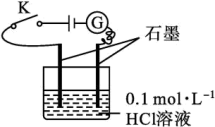

A.闭合开关 ,检流计指针发生偏转,证明 ,检流计指针发生偏转,证明 是电解质 是电解质 |
B.闭合开关 ,向烧杯中加入 ,向烧杯中加入 固体,由于 固体,由于 与 与 不反应,故检流计指针不发生变化 不反应,故检流计指针不发生变化 |
C.闭合开关 ,向溶液中加入少量 ,向溶液中加入少量 固体,检流计示数基本不变 固体,检流计示数基本不变 |
D.选取相同浓度的硫酸替换 的 的 溶液,检流计的示数相同 溶液,检流计的示数相同 |
您最近一年使用:0次
2021-11-18更新
|
145次组卷
|
2卷引用:山东省泰安市第一中学2021-2022学年高一上学期期中考试化学试题
名校
5 . 室温下,通过下列实验探究NaHS溶液的性质。
下列有关说法正确的是
| 实验 | 实验操作和现象 |
| 1 | 向0.1mol•L-1NaHS溶液中滴加几滴酚酞试剂,溶液变红 |
| 2 | 向0.1mol•L-1NaHS溶液中加入等体积0.1mol•L-1NaOH溶液充分混合 |
| 3 | 向0.1mol•L-1NaHS溶液中通入过氯气,无淡黄色沉淀产生 |
| 4 | 向0.1mol•L-1NaHS溶液中滴加过CuCl2溶液,产生黑色沉淀 |
| A.0.1mol/LNaHS溶液中:c(HS-)>c(S2-)>c(H2S) |
| B.实验2所得溶液中:c(Na+)-c(S2-)-c(HS-)-c(H2S)=0.05mol•L-1 |
| C.实验3证明HS-不能被氧化 |
| D.实验4反应静置后的上层清液中有c(Cu2+)•c(S2-)<Ksp(CuS) |
您最近一年使用:0次
2021-12-22更新
|
656次组卷
|
9卷引用:江苏省前黄高级中学、如东中学、姜堰中学2021-2022学年高三上学期12月份阶段性测试化学试题
江苏省前黄高级中学、如东中学、姜堰中学2021-2022学年高三上学期12月份阶段性测试化学试题江苏省姜堰中学、如东中学、前黄中学三校2021- 2022学年高三联考化学试题(已下线)解密10 水溶液中的离子平衡(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)江苏省徐州市第七中学2021-2022学年高三下学期2月检测化学试题(已下线)回归教材重难点04 水溶液中的离子平衡-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)回归教材重难点04 水溶液中的离子平衡-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)江苏省盐城市东台创新高级中学2021-2022学年高二4月份月检测化学试题江苏省盐城市东台创新高级中学2021-2022学年高二下学期5月份月检测化学试题江苏省泰州市靖江高级中学2023-2024学年高二下学期4月期中考试化学试题
名校
解题方法
6 . 氯气的水溶液称“氯水”,氯水中含有多种分子和离子,因此氯水有多重性质,下列有关新制氯水的说法中不正确的是
| A.新制氯水呈浅黄绿色,且有刺激性气味,说明氯水中含有Cl2 |
| B.新制氯水滴在蓝色石蕊试纸上,试纸先变红色后褪色,可说明氯水中含有 Cl2 |
| C.向淀粉碘化钾溶液中加入氯水,溶液变为蓝色,可证明Cl2的氧化性强于I2 |
| D.新制氯水滴到NaHCO3 溶液中,有气体产生,说明氯水中含有H+ |
您最近一年使用:0次
名校
7 . 如图是实验室进行二氧化硫制备与性质探究实验的组合装置,部分固定装置未画出。下列有关说法正确的是
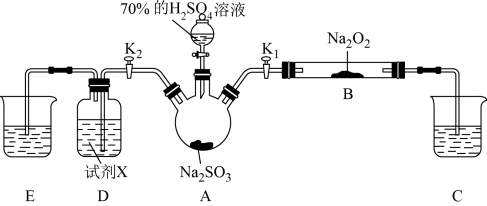

| A.关闭K1,打开K2,试剂X是酸性KMnO4或H2O2溶液,均可证明SO2有还原性 |
| B.关闭K2,打开K1,滴加H2SO4溶液,则装置B中每消耗1.5molNa2O2,转移电子数为3NA |
| C.为防止环境污染,装置C和E中的试剂均取用氢氧化钠溶液 |
| D.实验过程中体现了H2SO4的酸性、难挥发性、强氧化性 |
您最近一年使用:0次
2021-11-03更新
|
325次组卷
|
5卷引用:山东省潍坊市昌乐二中2021-2022学年高三10月月考化学试题
名校
8 . 某实验小组为探究草酸亚铁受热分解的气体产物的成分,设计了如图装置。已知:PdCl2溶液可用于检验CO,反应的化学方程式为CO+PdCl2+H2O=CO2+2HCl+Pd↓(产生黑色金属钯粉末,使溶液变浑浊)。下列说法错误的是
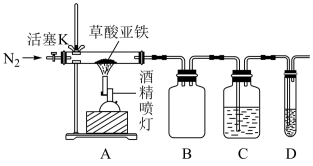

| A.B装置做安全瓶,有防倒吸的作用 |
| B.D装置中盛的是澄清石灰水 |
| C.PdCl2溶液中未观察到黑色浑浊证明分解产物中没有CO |
| D.加热前通入氮气目的是排净装置内的空气 |
您最近一年使用:0次
2021-11-07更新
|
75次组卷
|
2卷引用:河南省六市重点高中2021-2022学年高三上学期11月联合考试化学试题
名校
9 . 在人类社会的发展进程中,金属起着重要的作用。请回答下列问题:
(1)金属元素的原子结构决定了金属元素的性质、在自然界中的存在形式及冶炼方法。金属的冶炼一般有下列方法:
a.焦炭法 b.水煤气(氢气和一氧化碳)法 c.活泼金属置换法 d.电解法
请从上述四种方法中选择相应的字母填入表中空格:
(2)人类最早使用的金属材料的主要成分是铜。下列有关铜元素的说法中,不正确的是___________(填字母)
(3)铁及其化合物在生产生活中具有广泛应用。一定条件下,铁及其化合物之间发生相互的转化。
①在给定条件下,下列选项所示的物质间转化均能实现的是___________ 。
A.Fe2O3(s)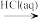 FeCl3(aq)
FeCl3(aq) Fe(s)
Fe(s)
B.FeS2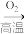 SO2
SO2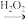 H2SO3
H2SO3
C.Fe2O3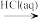 FeCl3(aq)
FeCl3(aq) 无水FeCl3
无水FeCl3
D.Fe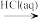 FeCl2(aq)
FeCl2(aq)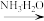 Fe(OH)2
Fe(OH)2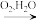 Fe(OH)3
Fe(OH)3
②NaFeO2可完全水解成Fe(OH)3,水解反应的离子方程式:___________ 。
(4)某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”;“纸漏斗的下部被烧穿,有熔融物落入沙中”。由化学手册查阅得有关物质的熔、沸点数据如表。
①该同学推测,铝热反应所得到的熔融物应是铁铝合金。理由是该反应放出的热量使铁熔化,而铝的熔点比铁的低,此时液态的铁和铝熔合成铁铝合金,你认为他的解释是否合理___________ (填“合理”或“不合理”)。
②设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是___________ ,反应的离子方程式为___________ 。
③另一同学推测铝热反应得到的熔融物中还含有Fe2O3,他设计了如下方案来验证:
取一块该熔融物冷却后投入到少量稀硫酸中,向反应后的混合液中滴加物质甲的溶液,观察到溶液颜色未变红,证明该熔融物中不含有Fe2O3.则物质甲是___________ (填化学式)。该同学的实验方案是否合理?___________ (填“合理”或“不合理”)。理由:___________ 。
(1)金属元素的原子结构决定了金属元素的性质、在自然界中的存在形式及冶炼方法。金属的冶炼一般有下列方法:
a.焦炭法 b.水煤气(氢气和一氧化碳)法 c.活泼金属置换法 d.电解法
请从上述四种方法中选择相应的字母填入表中空格:
| 高炉炼铁 | 湿法炼铜 | 铝热法炼铁 |
(2)人类最早使用的金属材料的主要成分是铜。下列有关铜元素的说法中,不正确的是___________(填字母)
| A.青铜、不锈钢、硬铝都是合金 |
| B.铜表面易形成致密的氧化膜 |
| C.铜与O2反应生成黑色的CuO |
| D.CuSO4·5H2O是一种混合物,加热后变为白色固体 |
①在给定条件下,下列选项所示的物质间转化均能实现的是
A.Fe2O3(s)
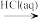 FeCl3(aq)
FeCl3(aq) Fe(s)
Fe(s)B.FeS2
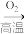 SO2
SO2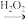 H2SO3
H2SO3C.Fe2O3
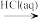 FeCl3(aq)
FeCl3(aq) 无水FeCl3
无水FeCl3D.Fe
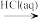 FeCl2(aq)
FeCl2(aq)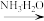 Fe(OH)2
Fe(OH)2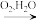 Fe(OH)3
Fe(OH)3②NaFeO2可完全水解成Fe(OH)3,水解反应的离子方程式:
(4)某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”;“纸漏斗的下部被烧穿,有熔融物落入沙中”。由化学手册查阅得有关物质的熔、沸点数据如表。
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1460 |
| 沸点/℃ | 2467 | 2980 | 2750 |
①该同学推测,铝热反应所得到的熔融物应是铁铝合金。理由是该反应放出的热量使铁熔化,而铝的熔点比铁的低,此时液态的铁和铝熔合成铁铝合金,你认为他的解释是否合理
②设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是
③另一同学推测铝热反应得到的熔融物中还含有Fe2O3,他设计了如下方案来验证:
取一块该熔融物冷却后投入到少量稀硫酸中,向反应后的混合液中滴加物质甲的溶液,观察到溶液颜色未变红,证明该熔融物中不含有Fe2O3.则物质甲是
您最近一年使用:0次
名校
10 . 下列说法不正确的是
| A.容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶无“0”刻度,滴定管有“0”刻度;使用时滴定管水洗后还需润洗,容量瓶水洗后不用润洗 |
| B.因为盐的水解是吸热过程,所以加热可提高盐的水解速率 |
C.为了证明氯化铵溶液可促进 固体的溶解,可向两份等量 固体的溶解,可向两份等量 固体中分别加入等体积蒸馏水和 固体中分别加入等体积蒸馏水和 溶液 溶液 |
D.在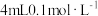 的 的 溶液中滴加数滴1mol/L的NaOH溶液,溶液颜色从橙色变成黄色 溶液中滴加数滴1mol/L的NaOH溶液,溶液颜色从橙色变成黄色 |
您最近一年使用:0次



