名校
1 . 将 和
和 两种引发温室效应气体转化为合成气(
两种引发温室效应气体转化为合成气( 和
和 ),可以实现能量综合利用,对环境保护具有十分重要的意义。
),可以实现能量综合利用,对环境保护具有十分重要的意义。
(1)甲烷二氧化碳干式重整涉及以下反应
a.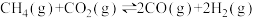
 平衡常数为
平衡常数为
b.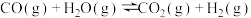
 平衡常数为
平衡常数为
c.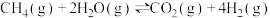
 平衡常数为
平衡常数为
① 为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1mol该物质的焓变。对于稳定相态单质,其
为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1mol该物质的焓变。对于稳定相态单质,其 为零。根据下表所示数据,计算反应a的反应热
为零。根据下表所示数据,计算反应a的反应热
_______ ,该反应在_______ (填“高温”或“低温”)下能自发进行。
②以上三个反应的平衡常数K与温度T存在函数关系: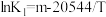 ,
,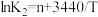 ,
,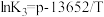 ,其中m、n、p为常数,则
,其中m、n、p为常数,则 的数值范围是
的数值范围是_______ (填序号)。
A. B.
B.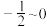 C.
C.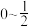 D.
D.
(2)甲烷的水蒸气重整涉及以下反应
Ⅰ.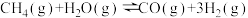
Ⅱ.
在一密闭容器中,通入1mol 和3mol
和3mol 发生甲烷的水蒸气重整反应。
发生甲烷的水蒸气重整反应。
①压强为 kPa时,分别在加
kPa时,分别在加 和不加
和不加 时,平衡体系中
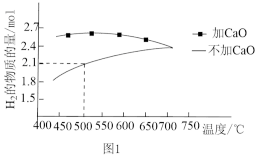
时,平衡体系中 的物质的量随温度变化如图1所示。温度低于700℃时,加入
的物质的量随温度变化如图1所示。温度低于700℃时,加入 可明显提高混合气中
可明显提高混合气中 的量,原因是
的量,原因是_______ 。
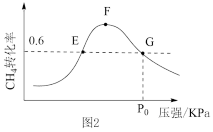
②500℃时,反应相同时间后测得 的转化率(α)随压强的变化如图2所示。则图2中E点和G点
的转化率(α)随压强的变化如图2所示。则图2中E点和G点 的浓度大小关系为
的浓度大小关系为
_______  (填“>”“<”或“=”),此温度下反应Ⅱ的分压平衡常数
(填“>”“<”或“=”),此温度下反应Ⅱ的分压平衡常数 (用分压代替浓度,分压等于总压×物质的量分数)为
(用分压代替浓度,分压等于总压×物质的量分数)为_______ 。
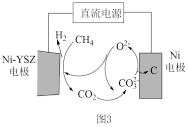
③甲烷蒸汽重整工业制氢面临着大量的“碳排放”,我国科技工作者发明了一种电化学分解甲烷的方法,其电化学反应原理如图3所示。请写出Ni-YSZ电极上发生的电极反应方程式:_______ 。
 和
和 两种引发温室效应气体转化为合成气(
两种引发温室效应气体转化为合成气( 和
和 ),可以实现能量综合利用,对环境保护具有十分重要的意义。
),可以实现能量综合利用,对环境保护具有十分重要的意义。(1)甲烷二氧化碳干式重整涉及以下反应
a.
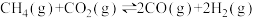
 平衡常数为
平衡常数为
b.
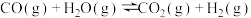
 平衡常数为
平衡常数为
c.
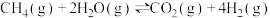
 平衡常数为
平衡常数为
①
 为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1mol该物质的焓变。对于稳定相态单质,其
为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1mol该物质的焓变。对于稳定相态单质,其 为零。根据下表所示数据,计算反应a的反应热
为零。根据下表所示数据,计算反应a的反应热
| 物质 |  |  |  |
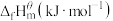 | -74.8 | -393.5 | -110.5 |
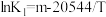 ,
,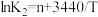 ,
,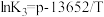 ,其中m、n、p为常数,则
,其中m、n、p为常数,则 的数值范围是
的数值范围是A.
 B.
B.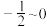 C.
C.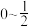 D.
D.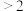
(2)甲烷的水蒸气重整涉及以下反应
Ⅰ.
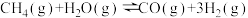
Ⅱ.

在一密闭容器中,通入1mol
 和3mol
和3mol 发生甲烷的水蒸气重整反应。
发生甲烷的水蒸气重整反应。①压强为
 kPa时,分别在加
kPa时,分别在加 和不加
和不加 时,平衡体系中
时,平衡体系中 的物质的量随温度变化如图1所示。温度低于700℃时,加入
的物质的量随温度变化如图1所示。温度低于700℃时,加入 可明显提高混合气中
可明显提高混合气中 的量,原因是
的量,原因是
②500℃时,反应相同时间后测得
 的转化率(α)随压强的变化如图2所示。则图2中E点和G点
的转化率(α)随压强的变化如图2所示。则图2中E点和G点 的浓度大小关系为
的浓度大小关系为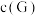
 (填“>”“<”或“=”),此温度下反应Ⅱ的分压平衡常数
(填“>”“<”或“=”),此温度下反应Ⅱ的分压平衡常数 (用分压代替浓度,分压等于总压×物质的量分数)为
(用分压代替浓度,分压等于总压×物质的量分数)为
③甲烷蒸汽重整工业制氢面临着大量的“碳排放”,我国科技工作者发明了一种电化学分解甲烷的方法,其电化学反应原理如图3所示。请写出Ni-YSZ电极上发生的电极反应方程式:

您最近一年使用:0次
2022-01-11更新
|
535次组卷
|
2卷引用:八省八校(T8联考湖北版)2021-2022学年高三上学期第一次联考化学试题
解题方法
2 . Pd/Al2O3是常见的汽车尾气催化剂。一种废Pd/Al2O3纳米催化剂主要成分及含量:Pd 0.3%,Al2O3 92.8%,SiO2 5.0%,Co、Pt和炭共约1.0%。采用如下工艺从中提取金属Co和Pd。
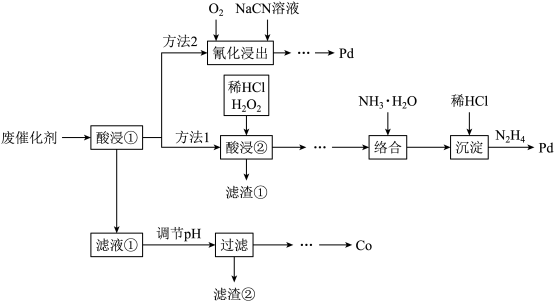
请回答下列问题:
(1)方法2比方法1后续回收流程相对简单,但工业上不常用方法2,从绿色化学角度分析原因是_______ 。
(2)“酸浸②”时,Pt和Pd分别转化为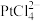 和
和 ,请写出Pd转化为
,请写出Pd转化为 的离子方程式为
的离子方程式为_______ 。
(3)“酸浸②”时,可用NaClO替代H2O2,两者相比,_______ (填化学式)的氧化效率更高(氧化效率以单位质量得到的电子数表示)。
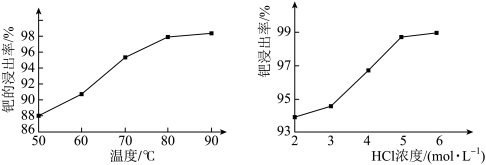
(4)酸浸②在一定温度下充分浸取钯,得到氯亚钯酸(H2PdCl4)溶液,钯的浸出率与反应的温度、HCl浓度的关系如图所示。最佳的浸取温度和HCl浓度分别为_______ 。
(5)“络合”过程后得到 和
和 ,“沉淀”时,搅拌滴加盐酸调节pH将
,“沉淀”时,搅拌滴加盐酸调节pH将 转化为
转化为 沉淀,结合平衡移动原理解释实现该转化的原因
沉淀,结合平衡移动原理解释实现该转化的原因_______ 。
(6)已知:常温下,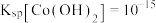 ,
, 。若滤液①中
。若滤液①中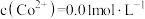 ,则分离出Al(OH)3沉淀需调节pH的范围是
,则分离出Al(OH)3沉淀需调节pH的范围是_______ 。(当离子浓度小于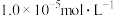 时认为已沉淀完全),调节pH可以选择的最佳物质是
时认为已沉淀完全),调节pH可以选择的最佳物质是_______ (填序号)。
A. B.
B. C.
C. D.
D.

请回答下列问题:
(1)方法2比方法1后续回收流程相对简单,但工业上不常用方法2,从绿色化学角度分析原因是
(2)“酸浸②”时,Pt和Pd分别转化为
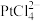 和
和 ,请写出Pd转化为
,请写出Pd转化为 的离子方程式为
的离子方程式为(3)“酸浸②”时,可用NaClO替代H2O2,两者相比,
(4)酸浸②在一定温度下充分浸取钯,得到氯亚钯酸(H2PdCl4)溶液,钯的浸出率与反应的温度、HCl浓度的关系如图所示。最佳的浸取温度和HCl浓度分别为

(5)“络合”过程后得到
 和
和 ,“沉淀”时,搅拌滴加盐酸调节pH将
,“沉淀”时,搅拌滴加盐酸调节pH将 转化为
转化为 沉淀,结合平衡移动原理解释实现该转化的原因
沉淀,结合平衡移动原理解释实现该转化的原因(6)已知:常温下,
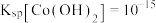 ,
, 。若滤液①中
。若滤液①中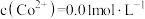 ,则分离出Al(OH)3沉淀需调节pH的范围是
,则分离出Al(OH)3沉淀需调节pH的范围是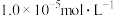 时认为已沉淀完全),调节pH可以选择的最佳物质是
时认为已沉淀完全),调节pH可以选择的最佳物质是A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次
3 . 奥希替尼(osimertinib)是一种重要而昂贵的肺癌靶向药,纳入我国医保后,大大减轻了患者的经济负担。其合成路线如下图所示:
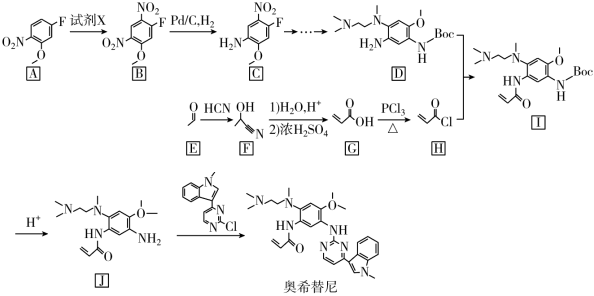
已知信息:①R’-C≡N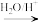 R’-COOH (其中R’为烃基)。
R’-COOH (其中R’为烃基)。
②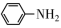 难以直接与羧基反应。
难以直接与羧基反应。
(1)A→B反应的试剂和条件:_______ ;B中含氧官能团的名称:_______ 。
(2)B→C,E→F反应类型分别为_______ ,_______ 。
(3)请写出G与苯甲醇(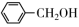 )发生酯化反应的化学方程式:
)发生酯化反应的化学方程式:_______ 。
(4)G与苯甲醇发生酯化反应生成的酯有多种同分异构体,其中同时满足下列条件的有_______ 种。
(ⅰ)官能团种类和数目均不变;(ⅱ)不能发生银镜反应;(ⅲ)苯环上有两个取代基
(5)参照上述合成路线,以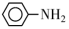 和丙酮(
和丙酮( )为原料,设计合成
)为原料,设计合成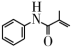 的路线(其他无机试剂任选):
的路线(其他无机试剂任选):_______ 。

已知信息:①R’-C≡N
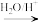 R’-COOH (其中R’为烃基)。
R’-COOH (其中R’为烃基)。②
 难以直接与羧基反应。
难以直接与羧基反应。(1)A→B反应的试剂和条件:
(2)B→C,E→F反应类型分别为
(3)请写出G与苯甲醇(
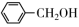 )发生酯化反应的化学方程式:
)发生酯化反应的化学方程式:(4)G与苯甲醇发生酯化反应生成的酯有多种同分异构体,其中同时满足下列条件的有
(ⅰ)官能团种类和数目均不变;(ⅱ)不能发生银镜反应;(ⅲ)苯环上有两个取代基
(5)参照上述合成路线,以
 和丙酮(
和丙酮( )为原料,设计合成
)为原料,设计合成 的路线(其他无机试剂任选):
的路线(其他无机试剂任选):
您最近一年使用:0次
名校
解题方法
4 . 煤的间接液化可先转化为一氧化碳和氢气,后在催化剂作用下合成甲醇,其中一氧化碳与氢气的反应历程如图,吸附在催化剂表面上的物种用*标注。
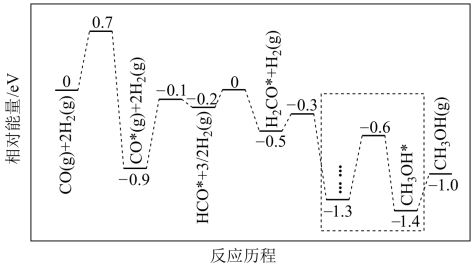
下列说法正确的是

下列说法正确的是
| A.煤中含有苯和甲苯,可以通过分馏的方式将它们分离出来 |
| B.该反应历程中决速步骤的活化能为1.6eV |
| C.石油裂解和煤的干馏都是化学变化,而石油的分馏和煤的气化都是物理变化 |
D.虚线框内发生的化学反应方程式可能为 |
您最近一年使用:0次
2022-01-11更新
|
319次组卷
|
3卷引用:八省八校(T8联考湖北版)2021-2022学年高三上学期第一次联考化学试题
八省八校(T8联考湖北版)2021-2022学年高三上学期第一次联考化学试题(已下线)专题03 化学反应速率及影响因素、活化能【考题猜想】(9大题型)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)广东省普宁二中实验学校2023-2024学年高二上学期第三次月考化学试题
名校
解题方法
5 . 下列“类比”结果说法正确的是
| A.油脂在碱性条件下能发生水解反应,则石蜡油在碱性条件下也能发生水解反应 |
B.分子式为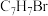 的芳香族化合物的同分异构体有4种,则分子式为 的芳香族化合物的同分异构体有4种,则分子式为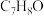 的芳香族化合物的同分异构体也是4种 的芳香族化合物的同分异构体也是4种 |
C.由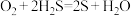 ,说明非金属性 ,说明非金属性 ,则高温下 ,则高温下 ,说明非金属性 ,说明非金属性 |
D. 溶液中滴加 溶液中滴加 溶液能产生沉淀,则 溶液能产生沉淀,则 溶液中加入 溶液中加入 溶液也能产生沉淀 溶液也能产生沉淀 |
您最近一年使用:0次
2022-01-11更新
|
381次组卷
|
2卷引用:八省八校(T8联考湖北版)2021-2022学年高三上学期第一次联考化学试题
名校
解题方法
6 . 氮化钼作为锂离子电池负极材料具有很好的发展前景。它属于填隙式氮化物,N原子部分填充在Mo原子立方晶格的八面体空隙中,晶胞结构如图所示,其中氮化钼晶胞参数为a nm,下列说法正确的是
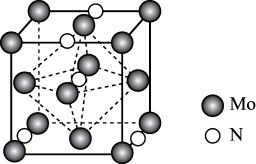

A.相邻两个最近的N原子的距离为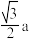 nm nm |
B.氮化钼的化学式为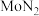 |
| C.每个钼原子周围与其距离最近的钼原子有12个 |
D.晶体的密度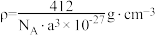 |
您最近一年使用:0次
2022-01-11更新
|
424次组卷
|
3卷引用:八省八校(T8联考湖北版)2021-2022学年高三上学期第一次联考化学试题
名校
解题方法
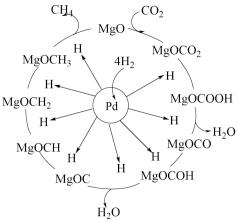
7 .  甲烷化也是实现“碳达峰”的重要途径,反应机理如下图。下列说法错误的是
甲烷化也是实现“碳达峰”的重要途径,反应机理如下图。下列说法错误的是
 甲烷化也是实现“碳达峰”的重要途径,反应机理如下图。下列说法错误的是
甲烷化也是实现“碳达峰”的重要途径,反应机理如下图。下列说法错误的是
A.该反应使用的催化剂既加快了甲烷化速率,又提高 的平衡转化率 的平衡转化率 |
B. 吸附在催化剂Pd表面而发生反应 吸附在催化剂Pd表面而发生反应 |
C.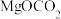 和 和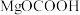 均为该反应过程的中间产物 均为该反应过程的中间产物 |
D.上述甲烷化过程总反应可表示为 |
您最近一年使用:0次
2022-01-11更新
|
724次组卷
|
7卷引用:八省八校(T8联考湖北版)2021-2022学年高三上学期第一次联考化学试题
八省八校(T8联考湖北版)2021-2022学年高三上学期第一次联考化学试题(已下线)专题09 反应机理—2022年高考化学二轮复习讲练测(全国版)-练习福建省厦门市湖滨中学2022-2023学年高二上学期期中考试化学试题(已下线)化学(湖南A卷)-学易金卷:2023年高考化学第一次模拟考试卷(已下线)化学(山东A卷)-学易金卷:2023年高考第一次模拟考试卷湖南省株洲市第一中学2022-2023学年高二上学期期中考试化学试题山东省实验中学2022-2023学年高三下学期开学考试化学试题
8 . 下列有关说法正确的是
A.咪唑为平面结构,结构为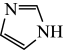 ,形成的大π键可表示为 ,形成的大π键可表示为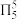 |
B. 、 、 、 、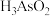 三种酸中酸性最强的是 三种酸中酸性最强的是 |
C.某含钛配合物,化学式为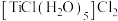 ,1 mol该配合物中 ,1 mol该配合物中 键的数目为 键的数目为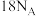 |
D. 和 和 受热均可分解,且分解温度: 受热均可分解,且分解温度: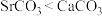 |
您最近一年使用:0次
解题方法
9 . 纳米级Cu2O可以作为太阳光分解水的催化剂,有这重要的应用前景。在加热的条件下用液态肼(N2H4)还原新制Cu(OH)2可制备纳米级Cu2O,同时生成N2,写出该反应的化学方程式_______ 。当收集的N2体积为3.36L(标准状况),计算制得纳米Cu2O的质量_______ 和转移电子数_______ 。
您最近一年使用:0次
10 . 测定溶液中的钙离子浓度的基本操作为:向溶液中加入(NH4)2C2O4将钙离子转化为CaC2O4沉淀,滤出沉淀,将沉淀溶于硫酸中,生成H2C2O4和CaSO4稀溶液。然后加入KMnO4标准溶液,将H2C2O4完全氧化。再用 (NH4)2Fe(SO4)2 溶液滴定过量的KMnO4,现取20.00mL某溶液进行上述处理。加入0.1000mol/LKMnO4标准溶液12.00mL,消耗0.2000mol/L的(NH4)2Fe(SO4)2溶液20.00mL。
(1)写出KMnO4与H2C2O4反应的离子方程式___________ 。
(2)求溶液中钙离子的浓度___________ 。
(1)写出KMnO4与H2C2O4反应的离子方程式
(2)求溶液中钙离子的浓度
您最近一年使用:0次



