解题方法
1 . 元素周期表揭示了元素间的内在联系,是学习化学的重要工具,我们可以通过元素所在的位置预测和解释元素的性质。

(1)b元素的名称是_____ ,写出b的单质与水反应的化学方程式:_____ 。
(2)d的最高价氧化物与g的最高价氧化物对应水化物的溶液反应的离子方程式为_____ 。
(3)元素c、d、f的简单离子半径由大到小的顺序为_____ (用离子符号表示)。
(4)下面关于h元素及单质性质推断错误的是_____ (填标号)。
A.常温常压下,h单质为气态
B.h元素的最高正化合价为
C.h单质的水溶液滴加到淀粉 溶液中,溶液变为蓝色
溶液中,溶液变为蓝色
(5)写出氢氧燃料(碱式)电池负极、正极电极反应式:负极_____ ;正极_____

(1)b元素的名称是
(2)d的最高价氧化物与g的最高价氧化物对应水化物的溶液反应的离子方程式为
(3)元素c、d、f的简单离子半径由大到小的顺序为
(4)下面关于h元素及单质性质推断错误的是
A.常温常压下,h单质为气态
B.h元素的最高正化合价为

C.h单质的水溶液滴加到淀粉
 溶液中,溶液变为蓝色
溶液中,溶液变为蓝色(5)写出氢氧燃料(碱式)电池负极、正极电极反应式:负极
您最近一年使用:0次
2 . 用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.1molN2所含有的原子数为NA |
| B.标准状况下,16gNH3中含有的分子数为NA |
| C.标准状况下,22.4L氯化氢所含的原子数为NA |
| D.500mL1.0mol•L﹣1硫酸钠溶液中所含的钠离子数为NA |
您最近一年使用:0次
解题方法
3 . 下列烷烃进行一氯取代反应后,生成的取代产物的数目最多的是
A.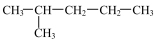 | B.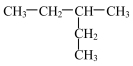 |
C.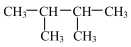 | D. |
您最近一年使用:0次
解题方法
4 . 以黄铁矿(主要成分FeS2)为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如图所示。
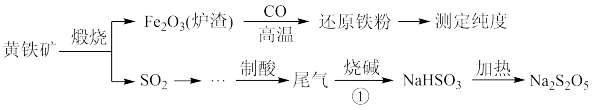
Na2S2O5:焦亚硫酸钠,白色粉末,水溶液显酸性,受潮易分解,遇强酸则放出一种刺激性气味的气体,是一种化工原料,常用作抗氧化剂。
(1)煅烧前,黄铁矿需要研磨,目的是_________________________________ 。
(2)煅烧黄铁矿的化学方程式是_________________________________ 。
(3)因为Na2S2O5具有_________ 性,导致商品Na2S2O5中不可避免地存在Na2SO4。检验其中含有SO 的方法是
的方法是_______________________________________ 。
(4)Na2S2O5可用于葡萄酒的抗氧化剂。用碘标准液可测定葡萄酒中Na2S2O5的残留量,请配平该反应的离子方程式:________ 。
____ S2O + _____I2 + _______ = _______ + _______ + _______
+ _____I2 + _______ = _______ + _______ + _______
(5)查阅资料知:“尾气”可用双碱脱硫法处理,其过程如图所示。
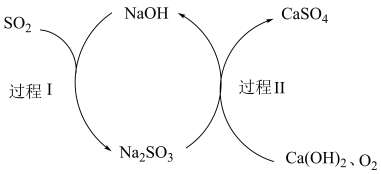
①写出过程I的离子反应方程式__________________________ 。

Na2S2O5:焦亚硫酸钠,白色粉末,水溶液显酸性,受潮易分解,遇强酸则放出一种刺激性气味的气体,是一种化工原料,常用作抗氧化剂。
(1)煅烧前,黄铁矿需要研磨,目的是
(2)煅烧黄铁矿的化学方程式是
(3)因为Na2S2O5具有
 的方法是
的方法是(4)Na2S2O5可用于葡萄酒的抗氧化剂。用碘标准液可测定葡萄酒中Na2S2O5的残留量,请配平该反应的离子方程式:
____ S2O
 + _____I2 + _______ = _______ + _______ + _______
+ _____I2 + _______ = _______ + _______ + _______(5)查阅资料知:“尾气”可用双碱脱硫法处理,其过程如图所示。

①写出过程I的离子反应方程式
②过程II反应中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
解题方法
5 . 按要求回答下列问题:
(1)某物质结构如图所示,分子式为
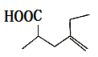
(2)现有A、B、C、D四种烃,其结构模型如图:

①等质量的以上物质完全燃烧时耗去O2的量最多的是
②将1molA和适量的Cl2混合后光照,充分反应后生成的CH3Cl、CH2Cl2、CHCl3、CCl4四种有机产物的物质的量依次增大0.1mol,则参加反应的Cl2的物质的量为
(3)某烷烃相对分子质量为86,若该分子中含有4个甲基(—CH3),则其该烷烃的结构简式为
您最近一年使用:0次
解题方法
6 . 为提纯下列物质(括号内为杂质),所用的除杂试剂和分离方法都正确的是
| 选项 | 不纯物 | 除杂试剂 | 分离方法 |
| A | CH4(C2H4) | 酸性KMnO4溶液 | 洗气 |
| B | C2H5OH(H2O) | 新制生石灰 | 蒸馏 |
| C | 乙酸乙酯(乙酸) | NaOH溶液 | 分液 |
| D | 苯(Br2) | NaOH溶液 | 过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
7 . 一定条件下,反应C(s)+H2O(g) CO(g)+H2(g)在一容积可变的密闭容器中进行。下列条件的改变能明显加快化学反应速率的是
CO(g)+H2(g)在一容积可变的密闭容器中进行。下列条件的改变能明显加快化学反应速率的是
 CO(g)+H2(g)在一容积可变的密闭容器中进行。下列条件的改变能明显加快化学反应速率的是
CO(g)+H2(g)在一容积可变的密闭容器中进行。下列条件的改变能明显加快化学反应速率的是| A.增加碳的量 | B.保持容积不变,充入氩气使容器内的压强增大 |
| C.升高温度 | D.保持压强不变,充入氦气使容器的容积变大 |
您最近一年使用:0次
8 . 某有机物的结构如图所示,则下列说法正确的是
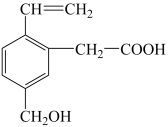

| A.该有机物中有4种官能团 |
| B.1mol该有机物能与2molNa、1molNaHCO3反应,且产生的气体体积之比为2:1 |
| C.该有机物中能使酸性高锰酸钾溶液褪色的官能团有2种 |
| D.该有机物能使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且反应原理相同 |
您最近一年使用:0次
9 . 高铁酸钾(K2FeO4)是一种既能杀菌、消毒、又能絮凝净水的水处理剂。工业制备高铁酸钾的反应离子方程式为:2Fe(OH)3 + 3ClO- + 4OH- = 2 + 3Cl- + 2H2O。下列有关说法不正确的是
+ 3Cl- + 2H2O。下列有关说法不正确的是
A.由上述反应可知,C1O- 的氧化性强于FeO |
| B.高铁酸钾中铁显+6价 |
| C.上述反应中氧化剂和还原剂的物质的量之比为2:3 |
| D.K2FeO4处理水时,不仅能消毒杀菌,而且生成的Fe3+水解形成Fe(OH)3胶体能吸附水中的悬浮杂质 |
您最近一年使用:0次
解题方法
10 . 下列离子方程式正确的是
| A.FeBr2溶液中通入过量氯气:2Fe2++Cl2=2Fe3++2Cl- |
| B.石灰石溶于醋酸:CaCO3+2CH3COOH=2CH3COO-+Ca2++CO2↑+H2O |
C.铜与浓硝酸反应:3Cu+8H++2NO =3Cu2++2NO↑+4H2O =3Cu2++2NO↑+4H2O |
D.碳酸氢铵与足量的NaOH溶液反应:HCO +OH-=CO2↑+H2O +OH-=CO2↑+H2O |
您最近一年使用:0次



