名校
解题方法
1 . Ⅰ.现代工业常以氯化钠为原料制备纯碱,部分工艺流程如图:
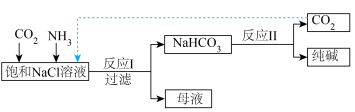
已知 在低温下溶解度较小。
在低温下溶解度较小。
(1)母液中主要含有NaCl、 和
和______ 。
(2)设计 循环的目的是
循环的目的是______ .
(3)可以利用加热的方法来鉴别碳酸钠和碳酸氢钠,反应的化学方程式为______ 。
Ⅱ.是一种重要的供氧剂。
(4)取一定量 ,加入足量的水,反应的化学方程式为
,加入足量的水,反应的化学方程式为______ .
(5)收集并测量生成 的体积,发现体积小于理论计算值。
的体积,发现体积小于理论计算值。
某小组研究产生这一差异的原因,进行如下探究。
查阅资料:
a.过氧化钠与水反应的过程中还可能存在以下两个复分解反应:
ⅰ.
ⅱ.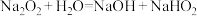
b.与 类似,
类似,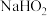 也能在
也能在 催化的条件下分解生成
催化的条件下分解生成 。
。
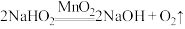
依据资料设计如下实验:取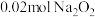 与足量水反应,140s时不再产生气泡,180s时向所得溶液中加入少量
与足量水反应,140s时不再产生气泡,180s时向所得溶液中加入少量 ,立即产生无色气体。过程中溶液的体积始终约为40mL。反应过程中pH变化如图所示。已知:溶液中
,立即产生无色气体。过程中溶液的体积始终约为40mL。反应过程中pH变化如图所示。已知:溶液中 越大,溶液pH越大。
越大,溶液pH越大。

数据分析:
①小组同学根据pH的变化判断反应过程中一定发生反应______ (填“ⅰ”或“ⅱ”),理由是______ 。
②根据140s~180s的pH计算出溶液的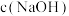 为
为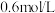 ,则此时段内溶液中
,则此时段内溶液中 为
为______ mol。

已知
 在低温下溶解度较小。
在低温下溶解度较小。(1)母液中主要含有NaCl、
 和
和(2)设计
 循环的目的是
循环的目的是(3)可以利用加热的方法来鉴别碳酸钠和碳酸氢钠,反应的化学方程式为
Ⅱ.是一种重要的供氧剂。
(4)取一定量
 ,加入足量的水,反应的化学方程式为
,加入足量的水,反应的化学方程式为(5)收集并测量生成
 的体积,发现体积小于理论计算值。
的体积,发现体积小于理论计算值。某小组研究产生这一差异的原因,进行如下探究。
查阅资料:
a.过氧化钠与水反应的过程中还可能存在以下两个复分解反应:
ⅰ.

ⅱ.
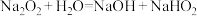
b.与
 类似,
类似,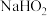 也能在
也能在 催化的条件下分解生成
催化的条件下分解生成 。
。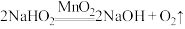
依据资料设计如下实验:取
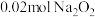 与足量水反应,140s时不再产生气泡,180s时向所得溶液中加入少量
与足量水反应,140s时不再产生气泡,180s时向所得溶液中加入少量 ,立即产生无色气体。过程中溶液的体积始终约为40mL。反应过程中pH变化如图所示。已知:溶液中
,立即产生无色气体。过程中溶液的体积始终约为40mL。反应过程中pH变化如图所示。已知:溶液中 越大,溶液pH越大。
越大,溶液pH越大。
数据分析:
①小组同学根据pH的变化判断反应过程中一定发生反应
②根据140s~180s的pH计算出溶液的
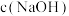 为
为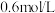 ,则此时段内溶液中
,则此时段内溶液中 为
为
您最近一年使用:0次
名校
解题方法
2 . 下图为一些常见物质的转化关系(部分物质已略去)。其中A是一种重要的化工原料,室温下C为黄绿色气体,D为淡黄色固体粉末。
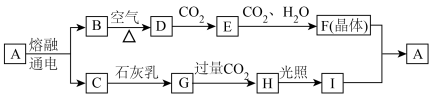
请回答:
(1)其中物质B对应元素的原子结构示意图为______ ,G的化学式为______ .
(2)物质D与 反应除生成E,还生成另一种物质
反应除生成E,还生成另一种物质______ (填名称)。
(3)写出F的溶液与I反应的离子方程式______ 。
(4)写出G→H的离子方程式( 过量)
过量)______ 。
(5)写出H→I的化学方程式______ 。
(6)检验A的溶液中阴离子的方法是______ 。

请回答:
(1)其中物质B对应元素的原子结构示意图为
(2)物质D与
 反应除生成E,还生成另一种物质
反应除生成E,还生成另一种物质(3)写出F的溶液与I反应的离子方程式
(4)写出G→H的离子方程式(
 过量)
过量)(5)写出H→I的化学方程式
(6)检验A的溶液中阴离子的方法是
您最近一年使用:0次
名校
解题方法
3 . 下列叙述或表述正确的是
| A.在化学反应中,得电子越多的氧化剂,其氧化性就越强 |
| B.元素的单质一定由氧化或还原该元素的化合物制得 |
| C.阳离子只能得到电子被还原,阴离子只能失去电子被氧化 |
D.双线桥: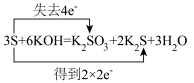 |
您最近一年使用:0次
名校
解题方法
4 . 高铁酸钾( )作净水剂,既能消毒杀菌,也能吸附水中悬浮物。
)作净水剂,既能消毒杀菌,也能吸附水中悬浮物。 制备方法为:
制备方法为: ,下列说法正确的是
,下列说法正确的是
 )作净水剂,既能消毒杀菌,也能吸附水中悬浮物。
)作净水剂,既能消毒杀菌,也能吸附水中悬浮物。 制备方法为:
制备方法为: ,下列说法正确的是
,下列说法正确的是| A.该反应为复分解反应 | B. 是还原剂 是还原剂 |
C. 是氧化剂 是氧化剂 | D.KCIO发生氧化反应 |
您最近一年使用:0次
2023-12-02更新
|
84次组卷
|
3卷引用:云南省昆明市第一中学2023-2024学年高一上学期期中考试化学试题
名校
解题方法
5 . 下列操作不符合安全要求的是
| A.在通风橱内制备有毒气体 |
| B.当火灾现场存放有大量活泼金属时,需要用干燥的沙土来灭火 |
| C.眼睛溅进酸液,先用大量水冲洗,再用饱和碳酸钠溶液冲洗 |
| D.电器起火,先切断电源,再用二氧化碳灭火器灭火 |
您最近一年使用:0次
2023-12-02更新
|
128次组卷
|
2卷引用:云南省昆明市第一中学2023-2024学年高一上学期期中考试化学试题
名校
解题方法
6 . 目前市场上有一种专门为婴幼儿设计的电解质饮料,适合在婴幼儿感冒、发烧时快速补充体内流失的电解质成分。下列物质可用作该饮料中的电解质的是
| A.Fe | B.葡萄糖 | C.KCl | D. |
您最近一年使用:0次
名校
7 . CO2的减排策略主要有三种:减少排放、捕集封存、转化利用。其中CO2转化利用生产高能燃料和高附加值化学品,有利于实现碳资源的有效循环。回答下列问题:
(1)以CO2与NH3为原料可合成尿素。已知:
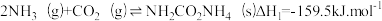
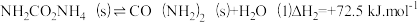
反应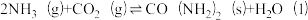 的△H=
的△H=______________ kJ.mol-1;欲提高氨气的平衡转化率,可采取的一种措施是_______________ 。
(2)二氧化碳加氢制乙烯的反应为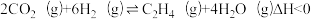 。在恒压密闭容器中,起始时
。在恒压密闭容器中,起始时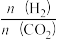 =3,在不同温度下,平衡时各组分的体积分数随温度的变化如图所示。
=3,在不同温度下,平衡时各组分的体积分数随温度的变化如图所示。

表示CO2、C2H4的体积分数随温度变化的曲线分别是______________ 、______________ (填序号)。
②A、B、C三点对应的化学平衡常数KA、KB、KC的大小关系为______________ ,其判断理由是______________ 。
③357℃时,CO2的平衡转化率a=_____________ ;若总压为pMPa,该温度下的平衡常数Kp=______________ (列出计算式,用平衡分压代替平衡浓度,分压=物质的量分数×总压)。
(1)以CO2与NH3为原料可合成尿素。已知:
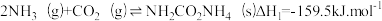
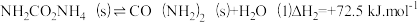
反应
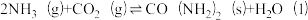 的△H=
的△H=(2)二氧化碳加氢制乙烯的反应为
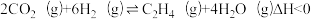 。在恒压密闭容器中,起始时
。在恒压密闭容器中,起始时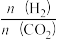 =3,在不同温度下,平衡时各组分的体积分数随温度的变化如图所示。
=3,在不同温度下,平衡时各组分的体积分数随温度的变化如图所示。
表示CO2、C2H4的体积分数随温度变化的曲线分别是
②A、B、C三点对应的化学平衡常数KA、KB、KC的大小关系为
③357℃时,CO2的平衡转化率a=
您最近一年使用:0次
名校
8 . 已知25℃时,电离平衡常数:
回答下列问题:
(1)①CH3COOH;②H2CO3;③HCO3-;④HClO四种粒子电离出质子的能力由大到小的顺序是_______________ (用标号表示);碳酸氢钠在水中的电离方程式为_______________ 。
(2)下列反应的离子方程式错误的是_______________(填标号)。
(3)用蒸馏水稀释0.10mol.L-1的醋酸,下列各式表示的数值随水量的增加而增大的是_____________(填标号)。
(4)已知 ,lg1.32=0.12。近似计算0.10mol.L-1醋酸溶液中CH3COOH的电离度≈
,lg1.32=0.12。近似计算0.10mol.L-1醋酸溶液中CH3COOH的电离度≈_______________ ;溶液的pH为_______________ 。
(5)向2mL0.02 mol.L-1HClO溶液中滴加2mL稀硫酸,测得溶液的pH为1,则溶液中c(ClO-)=_______________ ;加入稀硫酸对HClO电离度的影响是_______________ (填“增大”“减小”或“无影响”)。
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 |  | 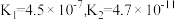 |  |
(1)①CH3COOH;②H2CO3;③HCO3-;④HClO四种粒子电离出质子的能力由大到小的顺序是
(2)下列反应的离子方程式错误的是_______________(填标号)。
A.足量醋酸滴加到碳酸钠溶液中: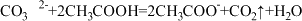 |
B.次氯酸钠溶液中滴加醋酸: |
C.次氯酸钠溶液中通入少量二氧化碳: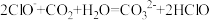 |
D.次氯酸钙溶液中通入少量二氧化疏: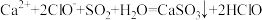 |
(3)用蒸馏水稀释0.10mol.L-1的醋酸,下列各式表示的数值随水量的增加而增大的是_____________(填标号)。
A. | B. |
C. | D. |
(4)已知
 ,lg1.32=0.12。近似计算0.10mol.L-1醋酸溶液中CH3COOH的电离度≈
,lg1.32=0.12。近似计算0.10mol.L-1醋酸溶液中CH3COOH的电离度≈(5)向2mL0.02 mol.L-1HClO溶液中滴加2mL稀硫酸,测得溶液的pH为1,则溶液中c(ClO-)=
您最近一年使用:0次
名校
解题方法
9 . 铂铼双金属催化剂是石油化工行业的高活性催化剂,使用时,催化剂表面的积炭和铂晶粒的烧结使催化剂逐渐失效。从失效催化剂(主要成分为Al2O3,含少量SiO2、Fe2O3、Pt、Re和积炭)中回收金属铼(Re)、铂(Pt)的工艺流程如下:

回答下列问题:
(1)铂铼双金属催化剂中A12O3的作用是__________________ 。
(2)利用空气“氧化焙烧”时,生成气体的分子式为______________ ,同时铼被氧化为酸性氧化物Re2O7。
(3)“碱焙烧”时,多种成分都能与NaOH反应,其中生成NaReO4的化学方程式为_______________ 。
(4)“滤渣1”回收铂时,先用王水溶解铂生成H2PtC16,再用氯化铵生成(NH4)2PtCl6沉淀,最后煅烧(NH4)2PtC16使其分解生成单质Pt和氮气等产物,该分解反应的化学方程式为_______________ 。
(5)“滤渣2”主要成分的化学式是_______________ 。
(6)“冷冻结晶”时析出含杂质的高铼酸钾(KReO4)晶体,可用_______________ (填方法的名称)提纯。
(7)用氢气高温还原KReO4的化学方程式为_______________ 。

回答下列问题:
(1)铂铼双金属催化剂中A12O3的作用是
(2)利用空气“氧化焙烧”时,生成气体的分子式为
(3)“碱焙烧”时,多种成分都能与NaOH反应,其中生成NaReO4的化学方程式为
(4)“滤渣1”回收铂时,先用王水溶解铂生成H2PtC16,再用氯化铵生成(NH4)2PtCl6沉淀,最后煅烧(NH4)2PtC16使其分解生成单质Pt和氮气等产物,该分解反应的化学方程式为
(5)“滤渣2”主要成分的化学式是
(6)“冷冻结晶”时析出含杂质的高铼酸钾(KReO4)晶体,可用
(7)用氢气高温还原KReO4的化学方程式为
您最近一年使用:0次
10-11高二上·江西新余·期中
名校
解题方法
10 . 常温下,pH=13的强碱溶液与pH=2的强酸溶液混合,所得混合液的pH=11,则强碱与强酸的体积比是
| A.1:9 | B.9:1 | C.1:11 | D.11:1 |
您最近一年使用:0次
2023-12-02更新
|
235次组卷
|
90卷引用:云南省昆明市第一中学2023-2024学年高二上学期期中化学试题
云南省昆明市第一中学2023-2024学年高二上学期期中化学试题(已下线)2010-2011学年云南省昆明一中高二下学期期中考试化学试卷(已下线)2012-2013学年云南省昆明三中、滇池中学高二下学期期末考试化学卷重庆市为明学校2022-2023学年高二上学期期末检测化学试题北京首都师范大学附属中学2023-2024学年高二上学期10月月考化学试题陕西省/渭南市蒲城县尧山中学2023-2024学年高二上学期第三次月考化学试题安徽省马鞍山市第二中学2023-2024学年高二上学期期末检测化学试题(已下线)2010年江西省新余一中高二上学期期中考试化学卷(已下线)2010年河南省周口市高二上学期期中考试化学卷(已下线)2011年河南省卫辉市第一中学高二1月月考化学试卷(已下线)2010—2011学年浙江省杭州学军中学高二下学期期中考试化学试卷(已下线)2011-2012年山西省太原五中高二上学期期中考试化学(理)试卷(已下线)2011-2012学年内蒙古巴彦淖尔市中学高二期中考试化学试卷(已下线)2011-2012学年黑龙江龙东地区高二第一学期高中教学联合体期末考试化学试卷(已下线)2011-2012学年陕西省宝鸡中学高二下学期期中考试化学试题(已下线)2011-2012学年天津市蓟县一中高二第三次月考化学试卷(已下线)2012-2013学年黑龙江省哈三中高二上学期期中考试化学试卷(已下线)2012年鲁科版高中化学选修4 3.1水溶液卷练习卷(已下线)2012年苏教版高中化学选修4 3.2溶液的酸碱性练习卷(已下线)2013-2014学年福建省福州市八县高二上学期期末考试化学试卷(已下线)2013-2014学年安徽省宿州市高二上学期期末考试化学试卷2014-2015学年湖北省长阳县第一高级中学高二上学期期中化学试卷2014-2015学年重庆复旦中学高二上学期期中化学试卷2014-2015甘肃省兰州一中高二上学期期末化学试卷2014-2015四川省重点中学高二下学期期中考试化学试卷2014-2015学年北京市房山区周口店中学高二下期中考试化学试卷2015-2016学年河北省冀州中学高二上第二次月考化学试卷2015-2016学年广东省揭阳一中高二上第二次段考化学试卷2015-2016学年福建晨曦、冷曦、正曦、岐滨四校高二上联考化学卷2015-2016学年内蒙古巴彦淖尔一中高二上期中化学试卷2015-2016学年西藏日喀则高级中学高二上期末化学试卷2015-2016学年四川省彭州中学高二下2月月考化学试卷2015-2016学年吉林省延边二中高二上期末化学试卷2015-2016学年内蒙古巴彦淖尔一中高二普通班上期中化学试卷2015-2016学年青海省平安一中高二下期末化学试卷2016-2017学年辽宁省沈阳铁路中学高二上第一次月考化学试卷2016-2017学年河北省秦皇岛北戴河中学高二上月考化学试卷2016-2017学年河北省涿鹿县涿鹿中学高二上调研三化学卷黑龙江省牡丹江市第一高级中学2017-2018学年高二10月月考(理)化学试题黑龙江省大庆实验中学2017-2018学年高二10月月考化学试题河南省商丘市九校2017-2018学年高二上学期期中联考化学试题山西省吕梁市临县第一中学2017-2018学年高二上学期期中考试化学试题湖北省武汉2017-2018学年高二化学上学期期末考试题吉林省辽源市田家炳高级中学等五校2017-2018学年高二上学期期末联考化学试题黑龙江省哈尔滨市第六中学2017-2018学年高二3月月考化学试题山东省济南市历城第二中学2017-2018学年高二下学期开学考试化学试题四川省棠湖中学2017-2018学年高二下学期第一次月考理综化学试题辽宁省实验中学2017-2018学年高二上学期期中考试化学试题河南省鹤壁市淇县第一中学2018-2019学年高二上学期第一次月考化学试题【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高二上学期10月月考化学试题安徽省阜阳三中2018-2019学年高二第一学期第一次调研考试化学试题湖南省邵东县第十中学2018-2019学年高二上学期期中考试理科班化学试题高二人教版选修4 第三章 第二节 水的电离和溶液的酸碱性吉林省汪清县第六中学2019-2020学年高二上学期期中考试化学试题陕西省咸阳百灵中学2019-2020学年高二上学期第二次月考化学(理)试题甘肃省张掖市山丹县第一中学2017—2018学年高二上学期期末质量检测化学试题辽宁省实验中学东戴河分校2019-2020学年高二12月月考化学试题甘肃省古浪县第二中学2019-2020学年高二12月基础知识竞赛化学试题河北省沧州市沧县风化店中学2019-2020学年高二上学期期末考试化学试题新疆博尔塔拉蒙古自治州第五师高级中学2019-2020学年高二上学期第二次月考化学试题重庆市凤鸣山中学2018-2019学年高二上学期期中考试化学试题河北省沧州市河间市第四中学2019-2020学年高二下学期期末模拟考试化学试卷宁夏银川市宁夏大学附属中学2019-2020学年高二下期第二次月考化学试题重庆市万州第二高级中学2020-2021学年高二上学期10月月考化学试题江苏省南通市2020-2021学年高二上学期期中考试化学试题鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 第1节 水与水溶液 课时2 溶液的酸碱性与pH湖南省临澧县第一中学2020-2021学年高二上学期期中考试化学试题(选考)山西省长治市第二中学校2020-2021学年高二上学期期中考试化学试题重庆市万州第三中学2020-2021学年高二上学期期中考试化学试题安徽省六安市裕安区新安中学2020-2021学年高二上学期期中考试化学试题吉林省白山市抚松县第五中学2020-2021学年高二上学期期中考试化学试题四川省广安市北京师范大学广安实验学校2020-2021学年高二上学期12月考试化学试题新疆新源县第二中学2019-2020学年高二上学期期末考试化学试题北京东城区2019-2020学年高二下学期期中考试化学试题北京市首都师范大学附属中学2021-2022学年高二上学期期中考试化学试题(已下线)第2讲 水的电离及溶液PH-【微专题·大素养】备战2022年高考化学核心突破(水溶液中的离子反应与平衡)吉林省汪清县第六中学2021-2022学年高二上学期期中考试化学试题天津市外国语大学附属外国语学校2021-2022学年高二上学期期中阶段性检测化学试题宁夏青铜峡市高级中学2021-2022学年高二上学期期中考试化学试题黑龙江省哈尔滨市第九中学校2021-2022学年高二上学期期中学业阶段性评价考试化学(理)试题湖南省长沙市南雅中学2018-2019学年高二上学期期中考试化学试题宁夏青铜峡市高级中学2021-2022学年高二上学期11月测试化学试题黑龙江省哈尔滨市宾县第二中学2021-2022学年高二上学期期末考试化学试题黑龙江省哈尔滨市阿城区第一中学2022-2023学年高二上学期第一次月考化学试题辽宁省重点高中沈阳市郊联体2022-2023学年高二上学期期中考试化学试题辽宁省沈阳市辽中区第二高级中学2022-2023学年高二上学期期中考试化学试题山西省晋中市平遥县第二中学校2021-2022学年高二上学期期中考试化学试题广东省连平县忠信中学2020-2021学年高二下学期第二次段考化学试题宁夏贺兰县景博中学2022-2023学年高二上学期第二次月考化学试题上海市进才中学2023-2024学年高一下学期期中考试化学试卷(等级)



