1 . 铁器时代是人类发展史中一个极为重要的时代,铁及其化合物在人类的生产、生活中都起了巨大的作用。
(1)长期放置的FeSO4溶液易被氧化而变质,实验室用绿矾FeSO4·xH2O配制FeSO4溶液时为了防止FeSO4溶液变质,经常向其中加入铁粉,其原因是_______ (用离子方程式表示)。
(2)利用部分变质的FeSO4溶液制备Fe2O3:
部分变质的FeSO4溶液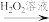 溶液I
溶液I  沉淀II
沉淀II 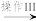 Fe2O3
Fe2O3
①H2O2溶液的作用是_______ 。
②“溶液I”的溶质为_______ (填化学式),写 出由“溶液I”到“沉淀II”反应的离子方程式:_______ 。
③“操作III”的名称为_______ 。
(3)为测定某绿矾FeSO4·xH2O中结晶水的含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将该绿矾FeSO4·xH2O样品装入石英玻璃管中,再次将装置A称重,记为m2g。按图示连接好装置进行实验。

①将下列实验操作步骤正确排序:_______ (填标号);重复上述操作步骤,直至装置A恒重,记为m3 g。
a.点燃酒精灯,加热
b.熄灭酒精灯
c.关闭K1和K2
d.打开K1和K2,缓缓通入N2
e.称量装置A
f.冷却至室温
②根据实验记录,计算绿矾FeSO4·xH2O化学式中结晶水的数目x=_______ (列出计算式即可)。
(1)长期放置的FeSO4溶液易被氧化而变质,实验室用绿矾FeSO4·xH2O配制FeSO4溶液时为了防止FeSO4溶液变质,经常向其中加入铁粉,其原因是
(2)利用部分变质的FeSO4溶液制备Fe2O3:
部分变质的FeSO4溶液
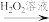 溶液I
溶液I  沉淀II
沉淀II 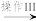 Fe2O3
Fe2O3①H2O2溶液的作用是
②“溶液I”的溶质为
③“操作III”的名称为
(3)为测定某绿矾FeSO4·xH2O中结晶水的含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将该绿矾FeSO4·xH2O样品装入石英玻璃管中,再次将装置A称重,记为m2g。按图示连接好装置进行实验。

①将下列实验操作步骤正确排序:
a.点燃酒精灯,加热
b.熄灭酒精灯
c.关闭K1和K2
d.打开K1和K2,缓缓通入N2
e.称量装置A
f.冷却至室温
②根据实验记录,计算绿矾FeSO4·xH2O化学式中结晶水的数目x=
您最近一年使用:0次
名校
解题方法
2 . 下列实验方案中,可以达到实验目的的是( )
| 选项 | 实验操作与现象 | 目的或结论 |
| A | 向装有溴水的分液漏斗中加入裂化汽油,充分振荡、静置后分层 | 裂化汽油可萃取溴 |
| B | 用pH试纸分别测定相同温度和相同浓度的CH3COONa溶液和NaClO溶液的pH | 验证酸性: CH3COOH>HClO |
| C | 将Fe(NO3)2样品溶于稀硫酸后,滴加KSCN溶液,溶液变红 | Fe(NO3)2晶体已氧化变质 |
| D | 取少量某无色弱酸性溶液,加入过量NaOH溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝 | 溶液中一定含有NH4+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 从古至今,铁及其化合物在人类的生产生活中都起了巨大的作用。
(1)古代中国四大发明之一的指南针是由天然磁石制成的,其主要成分是_________________ 。
A.Fe B.FeO C.Fe3O4 D.Fe2O3
(2)在现代化工生产中,常利用FeCl3腐蚀铜的原理制作印刷线路板,写出该原理的化学方程式_________________________________ 。
(3)实验室用绿矾FeSO4·xH2O配制FeSO4溶液时为了防止FeSO4溶液变质,经常向其中加入铁粉,其原因是_____________________ (用离子方程式表示)。
(4)某同学甲取2 mL FeSO4溶液,加入1滴KSCN溶液,再加入几滴氯水,溶液变红,说明Cl2可将Fe2+氧化。绿矾溶液与氯水反应的离子方程式为_______ 。
(5)同学乙认为甲同学的实验不够严谨,该同学在2 mL FeSO4溶液中先加入0.5 mL煤油,再于液面下依次加入1滴KSCN溶液和几滴氯水,溶液变红,煤油的作用是_____________ 。
(6)为测定某绿矾FeSO4·xH2O中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1 g;将样品装入石英玻璃管中,再次将装置A称重,记为 m2 g;按下图连接好装置进行实验:
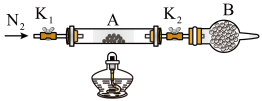
①仪器B的名称是____________ 。
②将下列实验操作步骤正确排序__________ (填标号);重复上述操作步骤,直至A恒重,记为m3 g。
a.点燃酒精灯,加热
b.熄灭酒精灯
c.关闭K1和K2
d.打开K1和K2,缓缓通入N2
e.称量A
f.冷却至室温
③根据实验记录,计算绿矾FeSO4·xH2O化学式中结晶水数目x=_______________________ (列式表示)。
(1)古代中国四大发明之一的指南针是由天然磁石制成的,其主要成分是
A.Fe B.FeO C.Fe3O4 D.Fe2O3
(2)在现代化工生产中,常利用FeCl3腐蚀铜的原理制作印刷线路板,写出该原理的化学方程式
(3)实验室用绿矾FeSO4·xH2O配制FeSO4溶液时为了防止FeSO4溶液变质,经常向其中加入铁粉,其原因是
(4)某同学甲取2 mL FeSO4溶液,加入1滴KSCN溶液,再加入几滴氯水,溶液变红,说明Cl2可将Fe2+氧化。绿矾溶液与氯水反应的离子方程式为
(5)同学乙认为甲同学的实验不够严谨,该同学在2 mL FeSO4溶液中先加入0.5 mL煤油,再于液面下依次加入1滴KSCN溶液和几滴氯水,溶液变红,煤油的作用是
(6)为测定某绿矾FeSO4·xH2O中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1 g;将样品装入石英玻璃管中,再次将装置A称重,记为 m2 g;按下图连接好装置进行实验:

①仪器B的名称是
②将下列实验操作步骤正确排序
a.点燃酒精灯,加热
b.熄灭酒精灯
c.关闭K1和K2
d.打开K1和K2,缓缓通入N2
e.称量A
f.冷却至室温
③根据实验记录,计算绿矾FeSO4·xH2O化学式中结晶水数目x=
您最近一年使用:0次
名校
解题方法
4 . “五⋅一”节后,小丽带着快乐的心情返回学校。当她来到实验室时,意外地发现实验桌上有瓶敞口放置已久的NaOH溶液,由此,激发了她的探究欲望。
[提出问题]这瓶NaOH溶液一定变质了,其变质程度如何呢?
[提出猜想]小丽的猜想:NaOH溶液部分变质。你的新猜想:_____________ 。
[实验探究]小丽设计如下实验来验证自己的猜想,请根据表中的内容填写空格:
假设你的猜想正确,并按小丽的实验方案进行实验,则你观察到的实验现象是:_______________________
[实验反思]
(1)下列物质①BaCl2溶液、②Ca(NO3)2溶液、③Ca(OH)2溶液、④Ba(OH)2溶液,不能替代小丽实验中CaCl2溶液的是___ (填序号)。
(2)小丽第二次滴加的试剂除用指示剂外,还可以用___________ 替代。
[拓展应用]保存NaOH溶液的方法是______________ 。
[提出问题]这瓶NaOH溶液一定变质了,其变质程度如何呢?
[提出猜想]小丽的猜想:NaOH溶液部分变质。你的新猜想:
[实验探究]小丽设计如下实验来验证自己的猜想,请根据表中的内容填写空格:
| 实验步骤 | 现象 | 结论 |
| 取少量NaOH溶液样品于试管中,先滴加足量的CaCl2溶液,然后再滴加酚酞试液。 | NaOH溶液部分变质。 |
假设你的猜想正确,并按小丽的实验方案进行实验,则你观察到的实验现象是:
[实验反思]
(1)下列物质①BaCl2溶液、②Ca(NO3)2溶液、③Ca(OH)2溶液、④Ba(OH)2溶液,不能替代小丽实验中CaCl2溶液的是
(2)小丽第二次滴加的试剂除用指示剂外,还可以用
[拓展应用]保存NaOH溶液的方法是
您最近一年使用:0次
2019-11-26更新
|
38次组卷
|
2卷引用:陕西省渭南市杜桥中学2019-2020学年高一上学期期中考试化学试题
名校
解题方法
5 . 下列操作能达到相应实验目的的是
| 选项 | 试验目的 | 操作 |
| A | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀盐酸后,滴加KSCN溶液,观察溶液是否变红 |
| B | 测定“84”消毒液的pH | 用洁净的玻璃棒蘸取少量“84”消毒液滴在pH试纸上 |
| C | 验证铁的吸氧腐蚀 | 将未生锈的铁钉放入试管中,用稀硫酸浸没 |
| D | 比较H2C2O4与H2CO3的酸性强弱 | 在H2C2O4溶液中滴加Na2CO3溶液,观察现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-05-04更新
|
477次组卷
|
4卷引用:陕西省宝鸡市、汉中市部分校联考2022-2023学年高三上学期11月月考化学试题
名校
解题方法
6 . 氨基甲酸铵( )是一种易分解、易水解的白色固体,可用于化肥、灭火剂、洗涤剂等。某化学兴趣小组模拟工业原理制备氨基甲酸铵。反应式:
)是一种易分解、易水解的白色固体,可用于化肥、灭火剂、洗涤剂等。某化学兴趣小组模拟工业原理制备氨基甲酸铵。反应式: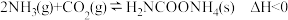 。
。
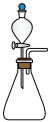
(1)如果使用如图所示的装置制取 ,你所选择的试剂是
,你所选择的试剂是__________________ 。
(2)制备氨基甲酸铵的装置如图,把氨和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中,当悬浮物较多时,停止制备。(注:四氯化碳与液体石蜡均为惰性介质。)
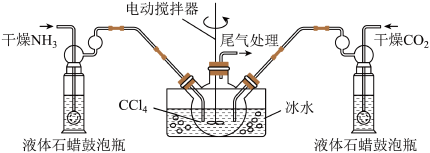
①发生器用冰水冷却的原因是________________________________________________ ;液体石蜡鼓泡瓶的作用是__________________________ ;发生反应的仪器名称是_______________ 。
②从反应后的混合物中过滤分离出产品。为了得到干燥产品,应采取的方法是_______________ (选填序号)
a.常压加热烘干 b.高压加热烘干 c.真空40℃以下烘干
(3)尾气有污染,吸收处理所用试剂为浓硫酸,它的作用是_________________________ 。
(4)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品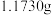 ,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为
,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为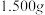 。样品中氨基甲酸铵的质量分数为
。样品中氨基甲酸铵的质量分数为_______________ 。[已知 ]
]
 )是一种易分解、易水解的白色固体,可用于化肥、灭火剂、洗涤剂等。某化学兴趣小组模拟工业原理制备氨基甲酸铵。反应式:
)是一种易分解、易水解的白色固体,可用于化肥、灭火剂、洗涤剂等。某化学兴趣小组模拟工业原理制备氨基甲酸铵。反应式: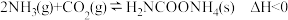 。
。
(1)如果使用如图所示的装置制取
 ,你所选择的试剂是
,你所选择的试剂是(2)制备氨基甲酸铵的装置如图,把氨和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中,当悬浮物较多时,停止制备。(注:四氯化碳与液体石蜡均为惰性介质。)

①发生器用冰水冷却的原因是
②从反应后的混合物中过滤分离出产品。为了得到干燥产品,应采取的方法是
a.常压加热烘干 b.高压加热烘干 c.真空40℃以下烘干
(3)尾气有污染,吸收处理所用试剂为浓硫酸,它的作用是
(4)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品
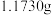 ,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为
,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为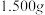 。样品中氨基甲酸铵的质量分数为
。样品中氨基甲酸铵的质量分数为 ]
]
您最近一年使用:0次
2018·陕西·高考模拟
名校
7 . 下列根据实验操作和实验现象所得出的结论不正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将FeCl2样品溶于盐酸后,滴加KSCN溶液 | 溶液变成红色 | 原FeCl2样品已变质 |
| B | 将Na2SO3样品溶于水,滴加入稀盐酸酸化的Ba(NO3)2溶液 | 产生白色沉淀 | 原Na2SO3样品已变质 |
| C | 向淀粉KI溶液中滴入3滴稀盐酸,再加入10%的H2O2溶液 | 滴入稀硫酸未见溶液变蓝;加入H2O2溶液后,溶液立即变蓝 | 酸性条件下,H2O2氧化性强于I2 |
| D | 向5mL 0.5mol/NaHCO3溶液中滴入2 mL 1mol/L BaCl2溶液 | 产生白色沉淀,且有无色气体生成 | 反应的化学方程式为2 NaHCO3+BaCl2=BaCO3↓+2NaCl+CO2↑+H2O |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 过氧化钠常作漂白剂、杀菌剂、消毒剂。过氧化钠保存不当容易吸收空气中CO2而变质。
(1)某课外活动小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,加入___ 溶液,充分振荡后有白色沉淀,证明Na2O2已经变质。
(2)该课外活动小组为了粗略测定过氧化钠的纯度,他们称取ag样品,并设计用如图装置来测定过氧化钠的质量分数。
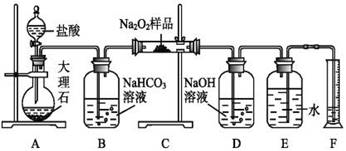
①A中发生反应离子方程式为____________________________________ 。
②将仪器连接好以后,必须进行的第一步操作是___________________________ 。
③B装置出来的气体是否需要干燥____ (填“是”或“否”)。
④D中NaOH溶液的作用_______________________
⑤读出量筒内水的体积后,折算成标准状况下氧气的体积为VmL,则样品中过氧化钠的质量分数为_______________
⑥实验完成后E到F之间导管内残留水的体积会使测量结果________ (填“偏大”“偏小”或“不影响”)。
(1)某课外活动小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,加入
(2)该课外活动小组为了粗略测定过氧化钠的纯度,他们称取ag样品,并设计用如图装置来测定过氧化钠的质量分数。

①A中发生反应离子方程式为
②将仪器连接好以后,必须进行的第一步操作是
③B装置出来的气体是否需要干燥
④D中NaOH溶液的作用
⑤读出量筒内水的体积后,折算成标准状况下氧气的体积为VmL,则样品中过氧化钠的质量分数为
⑥实验完成后E到F之间导管内残留水的体积会使测量结果
您最近一年使用:0次
名校
9 . 下列实验操作所得的现象及结论均正确 的是
| 实验操作 | 现象及结论 | |
| A | 将AlC13溶液加热蒸干 | 得到白色固体,成分为纯净的AlC13 |
| B | 将少量Na2SO3样品溶于水,滴加足量盐酸酸化的Ba(NO3)2溶液 | 有白色沉淀产生,则Na2SO3已变质 |
| C | 向Na2SiO3溶液中通入CO2 | 有白色沉淀产生,则碳酸的酸性比硅酸强 |
| D | 向FeI2溶液中通入少量C12 | 溶液变黄,则C12的氧化性强于Fe3+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-12-14更新
|
910次组卷
|
5卷引用:陕西省渭南中学2019届高三上学期第五次质量检测化学试题
10 . 下列根据实验操作和现象所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 蘸有浓氨水的玻璃棒靠近溶液X | 有白烟产生 | 溶液X是浓盐酸 |
| B | 用玻璃棒蘸取溶液Y进行焰色反应实验 | 火焰呈黄色 | 溶液Y中含Na+ |
| C | 用煮沸过的蒸馏水将Na2SO3固体样品溶解,加稀盐酸酸化,再加入氯化钡溶液 | 有白色沉淀产生 | Na2SO3样品已变质 |
| D | 向Fe(NO3)2溶液中滴加硫酸酸化的H2O2溶液 | 溶液变黄 | 氧化性:H2O2:>Fe3+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2017-10-11更新
|
171次组卷
|
2卷引用:陕西省渭南市2018届高三第一次联考(3)化学试题



