名校
1 . 某无色溶液中可能含有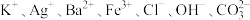 中的几种,对其进行如下实验操作:
中的几种,对其进行如下实验操作:
(1)取少量溶液,用 计测得
计测得 ;
;
(2)另取少量溶液,加入足量 溶液,产生白色沉淀;
溶液,产生白色沉淀;
(3)将(2)所得混合物过滤,向滤液中加入 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。
(1)此溶液中一定大量存在的离子为______ 。
(2)向原溶液中滴加少量盐酸,反应的离子方程式为______ 。
(3)若溶液中仅含有三种离子,向原溶液中加入 溶液,过滤,向沉淀中加入过量蒸馏水进行洗涤,可通过
溶液,过滤,向沉淀中加入过量蒸馏水进行洗涤,可通过 试纸检测来判断沉淀表面的阳离子是否洗净,其理由是
试纸检测来判断沉淀表面的阳离子是否洗净,其理由是______ 。
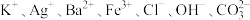 中的几种,对其进行如下实验操作:
中的几种,对其进行如下实验操作:(1)取少量溶液,用
 计测得
计测得 ;
;(2)另取少量溶液,加入足量
 溶液,产生白色沉淀;
溶液,产生白色沉淀;(3)将(2)所得混合物过滤,向滤液中加入
 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。(1)此溶液中一定大量存在的离子为
(2)向原溶液中滴加少量盐酸,反应的离子方程式为
(3)若溶液中仅含有三种离子,向原溶液中加入
 溶液,过滤,向沉淀中加入过量蒸馏水进行洗涤,可通过
溶液,过滤,向沉淀中加入过量蒸馏水进行洗涤,可通过 试纸检测来判断沉淀表面的阳离子是否洗净,其理由是
试纸检测来判断沉淀表面的阳离子是否洗净,其理由是
您最近一年使用:0次
名校
2 . Ⅰ:某学校化学兴趣小组对附近工厂排出的污水进行了监测,发现污水中含有的某些金属离子对水质和环境造成了严重污染,于是便对该厂排出的污水进行取样、过滤,对滤液进行了多次检测,其中三次的检测结果如下:
回答下列问题:
(1)通过分析发现在上述三次水样检测的结果中第______ 组水样检测的结果不正确。
(2)根据检测结果(有错误的一组不考虑)以及学过的化学知识,同学们提出建议:用一种含钠离子的化合物来处理污水,既可以除去检测出的金属离子又可以调节水体的酸碱性。
①这种化合物是______ (填化学式)。
②若将这种钠的化合物只加入第二组水样中,发生反应的离子方程式分别为______ 、______ 、______ 。
Ⅱ:某学校化学兴趣小组为证实 溶液和
溶液和 溶液的反应是离子反应,设计了如下实验。请把该实验报告补充完整。
溶液的反应是离子反应,设计了如下实验。请把该实验报告补充完整。
【实验装置】如图1所示。
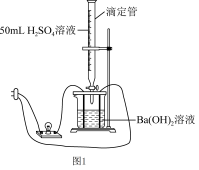
(3)【实验原理】溶液的导电性由溶液中离子的浓度及离子电荷数决定。观察______ ,据此判断溶液中自由移动的离子浓度的变化,从而证明反应是离子反应。
【实验过程与记录】
(4)实验现象是____________ 。
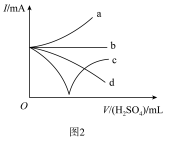
(5)整个过程中混合溶液的导电能力(用电流强度Ⅰ表示)可近似用图2中的曲线______ (填字母)表示。
水样 | 检测结果 |
第一组 |
|
第二组 |
|
第三组 |
|
(1)通过分析发现在上述三次水样检测的结果中第
(2)根据检测结果(有错误的一组不考虑)以及学过的化学知识,同学们提出建议:用一种含钠离子的化合物来处理污水,既可以除去检测出的金属离子又可以调节水体的酸碱性。
①这种化合物是
②若将这种钠的化合物只加入第二组水样中,发生反应的离子方程式分别为
Ⅱ:某学校化学兴趣小组为证实
 溶液和
溶液和 溶液的反应是离子反应,设计了如下实验。请把该实验报告补充完整。
溶液的反应是离子反应,设计了如下实验。请把该实验报告补充完整。【实验装置】如图1所示。

(3)【实验原理】溶液的导电性由溶液中离子的浓度及离子电荷数决定。观察
【实验过程与记录】
实验步骤 | 实验现象 | 实验结论 |
连接好装置,向烧杯中加入25mL一定浓度的 溶液和2滴酚酞溶液,逐滴滴加一定浓度的 溶液和2滴酚酞溶液,逐滴滴加一定浓度的 溶液直至过量,边滴边振荡 溶液直至过量,边滴边振荡 | ____________(填写支持实验结论的证据) |  溶液和 溶液和 溶液的反应是离子反应 溶液的反应是离子反应 |
(4)实验现象是
(5)整个过程中混合溶液的导电能力(用电流强度Ⅰ表示)可近似用图2中的曲线

您最近一年使用:0次
名校
解题方法
3 . 某溶液由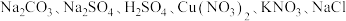 六种中的两种组成。
六种中的两种组成。
对该溶液进行如下实验,所观察到的现象记录在下表中。试根据各步实验及现象先进行分步推断,再综合推断该溶液的可能组成。
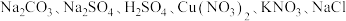 六种中的两种组成。
六种中的两种组成。对该溶液进行如下实验,所观察到的现象记录在下表中。试根据各步实验及现象先进行分步推断,再综合推断该溶液的可能组成。
| 实验操作步骤 | 实验现象 | 对溶液组成分步推断的结论 | 离子反应 |
| 1.取溶液少许,观察 | 溶液无色、澄清 | —— | |
2.用 试纸测定溶液的 试纸测定溶液的 |  | —— | |
3.向溶液中滴加过量的 溶液 溶液 | 有白色沉淀 | ||
4.过滤,向滤液中滴加 溶液 溶液 | 无明显现象 | —— | |
| 溶液的可能组成(写出溶质的化学式,有几组要写几组) | |||
您最近一年使用:0次
名校
解题方法
4 . 某无色透明酸性溶液中可能大量存在Ba2+、Mg2+、Cu2+、K+、 、
、 中的几种。请填写下列空白:
中的几种。请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是_________________ 。
(2)取少量原溶液,加入过量BaCl2溶液,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中 肯定不存在的离子是________________ 。
(3)取(2)中的滤液,加入过量的氢氧化钠溶液,出现白色沉淀,说明原溶液中肯定有_________ ,有关的离子方程式为_____________________________________ 。
(4)原溶液可能大量共存的阴离子是______(填序号)。
 、
、 中的几种。请填写下列空白:
中的几种。请填写下列空白:(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,加入过量BaCl2溶液,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中 肯定不存在的离子是
(3)取(2)中的滤液,加入过量的氢氧化钠溶液,出现白色沉淀,说明原溶液中肯定有
(4)原溶液可能大量共存的阴离子是______(填序号)。
| A.Cl- | B. | C. | D.OH- |
您最近一年使用:0次
名校
解题方法
5 . 化学是一门以实验为基础的学科.
i.现有甲、乙、丙三名同学进行氢氧化铁胶体的制备实验,三位同学的操作如下:
a.甲同学:取一小烧杯,加入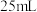 蒸馏水加热至沸腾,向沸水中逐滴加入
蒸馏水加热至沸腾,向沸水中逐滴加入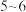 滴氯化铁饱和溶液,继续煮沸至混合液呈红褐色,停止加热;
滴氯化铁饱和溶液,继续煮沸至混合液呈红褐色,停止加热;
b.乙同学:直接加热饱和氯化铁溶液;
c.丙同学:向沸水中滴加饱和氯化铁溶液,为了使反应进行充分,煮沸10分钟;
(1)三位同学中能制得氢氧化铁胶体的是____________(填序号).
(2)证明有氢氧化铁胶体生成,可利用的胶体性质是____________ .
(3)制备氢氧化铁胶体的化学方程式为__________________________________ .
(4) 胶体区别于
胶体区别于 溶液最本质的特征是____________(填序号).
溶液最本质的特征是____________(填序号).
(5)分离蛋白质溶液和氯化钠溶液可以通过下列装置中的____________ (填序号).

ⅱ.现有一种固体混合物,可能含有硫酸钠、硫酸铜、碳酸钠、氯化钙、硝酸钾几种物质,为了检验这一固体混合物的成分,某兴趣小组进行了如下实验:
a.将适量固体混合物溶于水中.得到无色透明溶液
b.向a所得溶液中滴加硝酸钡溶液产生白色沉淀
c.向b所得悬浊液中滴加过量稀硝酸.白色沉淀全部消失.
(6)根据上述实验.原混合固体中一定含有的物质是____________ (填化学式),一定不含的物质是____________ (填化学式),可能含有的物质是____________ (填化学式).
i.现有甲、乙、丙三名同学进行氢氧化铁胶体的制备实验,三位同学的操作如下:
a.甲同学:取一小烧杯,加入
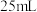 蒸馏水加热至沸腾,向沸水中逐滴加入
蒸馏水加热至沸腾,向沸水中逐滴加入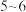 滴氯化铁饱和溶液,继续煮沸至混合液呈红褐色,停止加热;
滴氯化铁饱和溶液,继续煮沸至混合液呈红褐色,停止加热;b.乙同学:直接加热饱和氯化铁溶液;
c.丙同学:向沸水中滴加饱和氯化铁溶液,为了使反应进行充分,煮沸10分钟;
(1)三位同学中能制得氢氧化铁胶体的是____________(填序号).
| A.甲 | B.乙 | C.丙 |
(2)证明有氢氧化铁胶体生成,可利用的胶体性质是
(3)制备氢氧化铁胶体的化学方程式为
(4)
 胶体区别于
胶体区别于 溶液最本质的特征是____________(填序号).
溶液最本质的特征是____________(填序号).A. 胶体具有丁达尔效应 胶体具有丁达尔效应 | B. 胶体粒子的大小在 胶体粒子的大小在 之间 之间 |
C. 胶体是均一的分散系 胶体是均一的分散系 | D. 胶体的分散质能通过滤纸 胶体的分散质能通过滤纸 |
(5)分离蛋白质溶液和氯化钠溶液可以通过下列装置中的

ⅱ.现有一种固体混合物,可能含有硫酸钠、硫酸铜、碳酸钠、氯化钙、硝酸钾几种物质,为了检验这一固体混合物的成分,某兴趣小组进行了如下实验:
a.将适量固体混合物溶于水中.得到无色透明溶液
b.向a所得溶液中滴加硝酸钡溶液产生白色沉淀
c.向b所得悬浊液中滴加过量稀硝酸.白色沉淀全部消失.
(6)根据上述实验.原混合固体中一定含有的物质是
您最近一年使用:0次
名校
6 . Ⅰ.某溶液中只可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 。当加入一种淡黄色固体并加热时,有刺激性气体放出和白色沉淀产生,加入淡黄色固体的物质的量(横坐标)与析出的沉淀和产生气体的物质的量(纵坐标)的关系如下图所示。
。当加入一种淡黄色固体并加热时,有刺激性气体放出和白色沉淀产生,加入淡黄色固体的物质的量(横坐标)与析出的沉淀和产生气体的物质的量(纵坐标)的关系如下图所示。
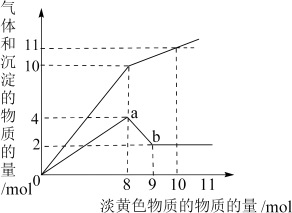
(1)该淡黄色物质做焰色反应实验显黄色。可知溶液中含有的离子是_______ ;所含离子的物质的量浓度之比为_______ ;所加的淡黄色固体是_______ 。
Ⅱ.湿法制备高铁酸钾 的反应体系中有六种粒子:
的反应体系中有六种粒子: 、
、 、
、 、
、 、
、 、
、 。
。
(2)写出并配平湿法制高铁酸钾反应的离子方程式:_______ 。
(3)每生成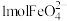 转移
转移_______  电子,若反应过程中转移了0.3mol电子,则还原产物的物质的量为
电子,若反应过程中转移了0.3mol电子,则还原产物的物质的量为_______  。
。
Ⅲ.已知在稀硫酸中, 和
和 能发生以下反应(均未配平):
能发生以下反应(均未配平):


(4)试比较在酸性条件下 、
、 、
、 、
、 氧化性的强弱:
氧化性的强弱:_______ 。
(5)以下离子方程式错误的是_______ (选填答案编号)。
a.
b.
c.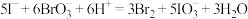
d.
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 。当加入一种淡黄色固体并加热时,有刺激性气体放出和白色沉淀产生,加入淡黄色固体的物质的量(横坐标)与析出的沉淀和产生气体的物质的量(纵坐标)的关系如下图所示。
。当加入一种淡黄色固体并加热时,有刺激性气体放出和白色沉淀产生,加入淡黄色固体的物质的量(横坐标)与析出的沉淀和产生气体的物质的量(纵坐标)的关系如下图所示。
(1)该淡黄色物质做焰色反应实验显黄色。可知溶液中含有的离子是
Ⅱ.湿法制备高铁酸钾
 的反应体系中有六种粒子:
的反应体系中有六种粒子: 、
、 、
、 、
、 、
、 、
、 。
。(2)写出并配平湿法制高铁酸钾反应的离子方程式:
(3)每生成
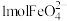 转移
转移 电子,若反应过程中转移了0.3mol电子,则还原产物的物质的量为
电子,若反应过程中转移了0.3mol电子,则还原产物的物质的量为 。
。Ⅲ.已知在稀硫酸中,
 和
和 能发生以下反应(均未配平):
能发生以下反应(均未配平):

(4)试比较在酸性条件下
 、
、 、
、 、
、 氧化性的强弱:
氧化性的强弱:(5)以下离子方程式错误的是
a.

b.

c.
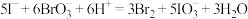
d.

您最近一年使用:0次
名校
7 . 某无色透明溶液中可能大量存在Ag+、Ca2+、Cu2+、Fe3+、Na+中的几种。回答下列问题:
(1)不做任何实验就可以肯定原溶液中不存在的离子是___________ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是___________ 。
(3)取(2)中的滤液,加入过量的碳酸钠溶液,出现白色沉淀,说明原溶液中肯定有___________ ,有关的离子方程式为___________ 。
(4)原溶液可能大量共存的阴离子是___________(填字母)。
(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是
(3)取(2)中的滤液,加入过量的碳酸钠溶液,出现白色沉淀,说明原溶液中肯定有
(4)原溶液可能大量共存的阴离子是___________(填字母)。
| A.OH- | B.SO | C.NO | D.Cl- |
您最近一年使用:0次
2023-10-20更新
|
104次组卷
|
3卷引用:河北省石家庄市第二十五中学2023-2024学年高一上学期第一次月考化学试题
名校
解题方法
8 . 碱式氯化铜有多种组成,可表示为Cua(OH)bClc•xH2O。
(1)碱式氯化铜制法之一;先制备CuCl2,再与石灰乳反应生成碱式氯化铜Cua(OH)bClc•xH2O。已知Cu与稀盐酸在持续通入空气和Fe3+催化下反应生成CuCl2,试写出此反应化学方程式________ ,反应类型为________ 。
(2)为测定某碱式氯化铜[Cua(OH)bClc•xH2O]的组成,进行下列实验:
称取样品1.1160g,用少量稀HNO3溶解后配成100.00mL溶液A;取25.00mL溶液A,加入足量AgNO3溶液,得AgCl(Mr为143.5)0.1722g;另取25.00mL溶液A,调节pH至4~5,用浓度为0.08000mol•L-1的EDTA(Na2H2Y•2H2O)标准溶液与Cu2+反应(离子方程式为Cu2++H2Y2-=CuY2-+2H+),消耗标准溶液30.00mL时恰好完全反应。
①溶液A中加入AgNO3溶液的目的是为了获得AgCl沉淀而测定Cl-的含量,简述实验中确认AgNO3溶液已加至足量的实验方法:__________ 。
②通过计算确定该样品的化学式(写出必要计算过程)_________ 。
(1)碱式氯化铜制法之一;先制备CuCl2,再与石灰乳反应生成碱式氯化铜Cua(OH)bClc•xH2O。已知Cu与稀盐酸在持续通入空气和Fe3+催化下反应生成CuCl2,试写出此反应化学方程式
(2)为测定某碱式氯化铜[Cua(OH)bClc•xH2O]的组成,进行下列实验:
称取样品1.1160g,用少量稀HNO3溶解后配成100.00mL溶液A;取25.00mL溶液A,加入足量AgNO3溶液,得AgCl(Mr为143.5)0.1722g;另取25.00mL溶液A,调节pH至4~5,用浓度为0.08000mol•L-1的EDTA(Na2H2Y•2H2O)标准溶液与Cu2+反应(离子方程式为Cu2++H2Y2-=CuY2-+2H+),消耗标准溶液30.00mL时恰好完全反应。
①溶液A中加入AgNO3溶液的目的是为了获得AgCl沉淀而测定Cl-的含量,简述实验中确认AgNO3溶液已加至足量的实验方法:
②通过计算确定该样品的化学式(写出必要计算过程)
您最近一年使用:0次
名校
9 . 某溶液中可能含有以下离子中的若干种: 、
、 、
、 、
、 、
、 、
、 、
、 。分别取三份该溶液各100mL进行如下实验:
。分别取三份该溶液各100mL进行如下实验:
①向第一份溶液中加入 溶液,有白色沉淀产生。
溶液,有白色沉淀产生。
②向第二份溶液中加入足量NaOH溶液并加热,有气体产生。
③向第三份溶液中加入足量 溶液,得到沉淀6.27g,经足量稀盐酸洗涤、干燥后,沉淀质量变为2.33g。
溶液,得到沉淀6.27g,经足量稀盐酸洗涤、干燥后,沉淀质量变为2.33g。
回答下列问题:
(1)根据实验结果判断该溶液中一定存在的离子是_______ (填离子符号,下同),一定不存在的离子是_______ 。
(2)②中反应的离子方程式为_______ ;②中产生的气体_______ (填“能”或“不能”)使湿润的红色石蕊试纸变成蓝色。
(3)2.33g沉淀的成分是_______ (填化学式),该物质_______ (填“是”或“不是”)电解质。
(4)用离子方程式表示③中沉淀质量减少的原因:_______ 。
 、
、 、
、 、
、 、
、 、
、 、
、 。分别取三份该溶液各100mL进行如下实验:
。分别取三份该溶液各100mL进行如下实验:①向第一份溶液中加入
 溶液,有白色沉淀产生。
溶液,有白色沉淀产生。②向第二份溶液中加入足量NaOH溶液并加热,有气体产生。
③向第三份溶液中加入足量
 溶液,得到沉淀6.27g,经足量稀盐酸洗涤、干燥后,沉淀质量变为2.33g。
溶液,得到沉淀6.27g,经足量稀盐酸洗涤、干燥后,沉淀质量变为2.33g。回答下列问题:
(1)根据实验结果判断该溶液中一定存在的离子是
(2)②中反应的离子方程式为
(3)2.33g沉淀的成分是
(4)用离子方程式表示③中沉淀质量减少的原因:
您最近一年使用:0次
名校
解题方法
10 . 现有下列10种物质:①钠 ②纯醋酸 ③氨气 ④浓盐酸 ⑤ 溶液 ⑥
溶液 ⑥ 固体 ⑦熔融的
固体 ⑦熔融的 ⑧
⑧ 固体 ⑨高锰酸钾粉末 ⑩氢氧化铁胶体。回答下列问题:
固体 ⑨高锰酸钾粉末 ⑩氢氧化铁胶体。回答下列问题:
(1)上述物质中能导电的有_______ (填序号,下同);属于电解质的有_______ 。
(2)⑧属于_______ (填“酸”、“碱”或“盐”),⑧与⑤在溶液中反应的离子方程式为_______ 。
(3)写出实验室制备⑩的化学方程式_______ 。
(4)书写电离方程式 (水溶液中):
①硫酸氢钠:_______ 。
② :
:_______ 。
(5)书写离子方程式 :
①稀硫酸除铁锈:_______ 。
②实验室检验 气体:
气体:_______ 。
(6)某有色电解质溶液中,可能大量存在 、
、 、
、 、
、 、
、 、
、 ,你认为:
,你认为:
①一定含有的离子是_______ ,(用离子符号表示,下同)
②一定没有的离子是_______ ,
③还需进一步确认的离子是_______ 。
 溶液 ⑥
溶液 ⑥ 固体 ⑦熔融的
固体 ⑦熔融的 ⑧
⑧ 固体 ⑨高锰酸钾粉末 ⑩氢氧化铁胶体。回答下列问题:
固体 ⑨高锰酸钾粉末 ⑩氢氧化铁胶体。回答下列问题:(1)上述物质中能导电的有
(2)⑧属于
(3)写出实验室制备⑩的化学方程式
(4)书写
①硫酸氢钠:
②
 :
:(5)书写
①稀硫酸除铁锈:
②实验室检验
 气体:
气体:(6)某有色电解质溶液中,可能大量存在
 、
、 、
、 、
、 、
、 、
、 ,你认为:
,你认为:①一定含有的离子是
②一定没有的离子是
③还需进一步确认的离子是
您最近一年使用:0次

 、
、

