1 . 人类社会的发展离不开“求知求真”.某化学兴趣小组以 溶液与
溶液与 溶液的反应为素材,探究盐溶液之间的反应情况,体悟反应的复杂性。
溶液的反应为素材,探究盐溶液之间的反应情况,体悟反应的复杂性。
(1)实验预测
(2)实验探究
实验一:探究 与
与 能否发生反应①,设计装置如下图,能证明反应已经发生的现象有
能否发生反应①,设计装置如下图,能证明反应已经发生的现象有_______ [已知: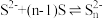 ]。
]。

实验二:探究 与
与 能否发生反应②和③,设计如下实验:
能否发生反应②和③,设计如下实验:
实验结论
 与
与 在溶液中相遇,会因为二者的浓度、用量等不同而反应不同,但都会先发生复分解反应。
在溶液中相遇,会因为二者的浓度、用量等不同而反应不同,但都会先发生复分解反应。
 溶液与
溶液与 溶液的反应为素材,探究盐溶液之间的反应情况,体悟反应的复杂性。
溶液的反应为素材,探究盐溶液之间的反应情况,体悟反应的复杂性。(1)实验预测
| 推测可能发生的反应 | 推测依据 | 预期的实验现象 |
| ①氧化还原反应 |  具有一定的氧化性, 具有一定的氧化性, 具有较强的还原性 具有较强的还原性 | 若 过量,则有淡黄色沉淀(S)生成若 过量,则有淡黄色沉淀(S)生成若 过量,则有黑色沉淀 过量,则有黑色沉淀 |
| ②复分解反应 |  为黑色难溶物, 为黑色难溶物,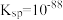 | 有黑色固体生成 |
| ③彻底双水解反应 |  、 、 水解能力均较强 水解能力均较强 | 有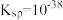 )产生,同时有臭鸡蛋气味的气体(H2S)生成 )产生,同时有臭鸡蛋气味的气体(H2S)生成 |
实验一:探究
 与
与 能否发生反应①,设计装置如下图,能证明反应已经发生的现象有
能否发生反应①,设计装置如下图,能证明反应已经发生的现象有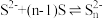 ]。
]。
实验二:探究
 与
与 能否发生反应②和③,设计如下实验:
能否发生反应②和③,设计如下实验:| 实验步骤 | 实验现象 | 实验解释或结论 |
ⅰ.向 饱和 饱和 溶液中,滴加2滴饱和 溶液中,滴加2滴饱和 溶液 溶液 | 有黑色沉淀生成,而后黑色沉淀消失,出现淡黄色沉淀 | 用离子方程式解释黑色沉淀消失的原因: |
ⅱ.将 饱和 饱和 溶液与 溶液与 饱和 饱和 溶液直接混合 溶液直接混合 | 先有黑色和另一种颜色的沉淀生成,而后都变为黑色;同时有臭鸡蛋气味的气体生成 | 试解释:沉淀最终都变为黑色的原因是 |
ⅲ.取ⅱ中最终生成的黑色沉淀样品,用无水乙醇多次洗涤后,干燥称量得 黑色固体,然后在空气中灼烧至恒重 黑色固体,然后在空气中灼烧至恒重 | 灼烧后,所得红棕色固体质量为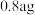 | 经计算判断,黑色固体样品的成份为 |
 与
与 在溶液中相遇,会因为二者的浓度、用量等不同而反应不同,但都会先发生复分解反应。
在溶液中相遇,会因为二者的浓度、用量等不同而反应不同,但都会先发生复分解反应。
您最近一年使用:0次
解题方法
2 . 碲(Te)广泛应用于冶金、航空航天、电子等领域。从精炼钢的阳极泥中(主要成分为Cu2Te,还含有金、银、铂等)回收碲的工艺流程如下:
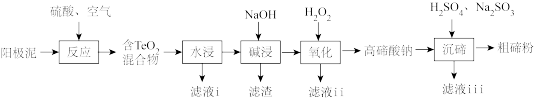
已知:TeO2有强还原性,且TeO2、Cu2TeO4难溶于水;高碲酸钠的化学式:Na2TeO4
回答下列问题:
(1)为提高“反应”效率,可采取的措施为_______ (任答一条)。
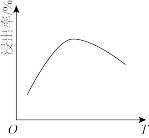
(2)滤液i的主要成分是_______ (写化学式)。滤液i中溶质的浸出率与温度关系如图所示,解释铜的浸出率随温度变化的可能原因_______ 。
(3)“氧化”过程中发生反应的离子方程式为_______ 。滤液ii可循环使用,应将其导入到_______ (写操作单元名称)操作中。
(4)“沉碲”过程中发生反应的离子方程式为_______ 。
(5)粗碲粉中碲质量分数的测定步骤如下:取mg粗碲粉,加入酸使其转化为亚碲酸(H2TeO3),配制成100mL溶液,取25.00mL于锥形瓶中。向锥形瓶中加入V1mLc1mol·L-1酸性K2Cr2O7溶液,充分反应使亚碲酸转化为碲酸(H6TeO6)。用c2mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]标准溶液滴定剩余的酸性K2Cr2O7溶液,消耗V2mL硫酸亚铁铵标准溶液。该粗碲粉中碲的质量分数为_______ 。

已知:TeO2有强还原性,且TeO2、Cu2TeO4难溶于水;高碲酸钠的化学式:Na2TeO4
回答下列问题:
(1)为提高“反应”效率,可采取的措施为
(2)滤液i的主要成分是

(3)“氧化”过程中发生反应的离子方程式为
(4)“沉碲”过程中发生反应的离子方程式为
(5)粗碲粉中碲质量分数的测定步骤如下:取mg粗碲粉,加入酸使其转化为亚碲酸(H2TeO3),配制成100mL溶液,取25.00mL于锥形瓶中。向锥形瓶中加入V1mLc1mol·L-1酸性K2Cr2O7溶液,充分反应使亚碲酸转化为碲酸(H6TeO6)。用c2mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]标准溶液滴定剩余的酸性K2Cr2O7溶液,消耗V2mL硫酸亚铁铵标准溶液。该粗碲粉中碲的质量分数为
您最近一年使用:0次
3 . 绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了一种熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产生废弃物,实现了Cr—Fe—Al—Mg的深度利用和 内循环。工艺流程如图:
内循环。工艺流程如图:
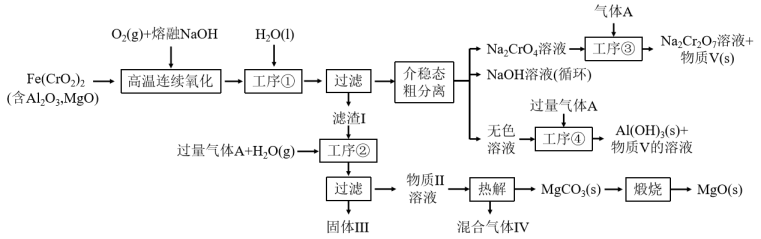
回答下列问题:
(1) 中Cr元素的化合价为+3价,写出高温连续氧化工序中该物质发生反应的化学方程式为
中Cr元素的化合价为+3价,写出高温连续氧化工序中该物质发生反应的化学方程式为_______ 。
(2)工序③操作名称为_______ 。
(3)滤渣I的主要成分是_______ (填化学式)。气体A的化学式为_______ 。
(4)工序④中发生反应的离子方程式为_______ 。
(5)热解工序产生的混合气体最适宜返回工序_______ (填“①”或“②”或“③”或“④”)参与内循环。
(6)工序④溶液中的铝元素恰好完全转化为沉淀的pH为_______ 。(通常认为溶液中离子浓度小于 为沉淀完全;
为沉淀完全;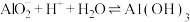 :
: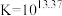 )
)
 内循环。工艺流程如图:
内循环。工艺流程如图:
回答下列问题:
(1)
 中Cr元素的化合价为+3价,写出高温连续氧化工序中该物质发生反应的化学方程式为
中Cr元素的化合价为+3价,写出高温连续氧化工序中该物质发生反应的化学方程式为(2)工序③操作名称为
(3)滤渣I的主要成分是
(4)工序④中发生反应的离子方程式为
(5)热解工序产生的混合气体最适宜返回工序
(6)工序④溶液中的铝元素恰好完全转化为沉淀的pH为
 为沉淀完全;
为沉淀完全;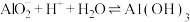 :
: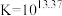 )
)
您最近一年使用:0次
21-22高三上·广东广州·期末
4 . 铼(Re)是熔点和沸点较高的金属单质之一,用于制造高效能喷射引擎和火箭引擎。钼酸锂(Li2MoO4)的外观为白色结晶粉末,用于电极材料、金属陶瓷的制作。从辉钼矿氧化焙烧后的烟道灰(主要成分有SiO2、Re2O7、MoO3、CuO、Fe3O4)中提取铼粉和制钼酸锂的流程如下图所示。
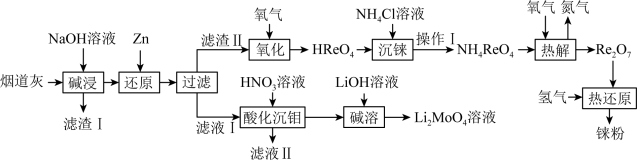
已知:
I.Re2O7是酸性氧化物,过铼酸(HReO4)是易溶于水的一元强酸,但不具有强氧化性。
Ⅱ.过铼酸铵(NH4ReO4)是白色片状晶体,微溶于冷水,溶于热水。
回答下列问题:
(1)“碱浸”时,Re2O7和MoO3分别与NaOH发生以下反应_______ (填写化学方程式)、MoO3+2NaOH=NaMoO4+H2O,则“滤渣I”的主要成分为_______ (填化学式)。
(2)“还原”时,Zn被氧化成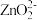 ,铼的化合物被还原生成难溶的2ReO2·2H2O,该反应的离子方程式为
,铼的化合物被还原生成难溶的2ReO2·2H2O,该反应的离子方程式为___________ 。
(3)“沉铼”时,加入热NH4C1溶液至产生白色沉淀,为使沉淀充分析出并分离得到纯净NH4ReO4晶体,“操作I”包括___________ 、___________ 、洗涤、干燥。
(4)“热解”时,发生反应的化学方程式为___________ 。
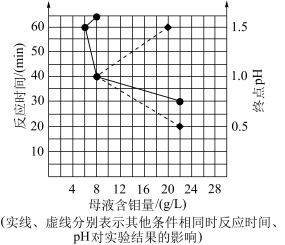
(5)“酸化沉钼”过程溶液pH和反应时间对钼酸的析出有很大影响,根据下图中数据判断最佳的“酸化沉钼”条件:反应时间为___________ min、pH为___________ 。
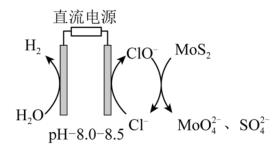
(6)电氧化法是一种极具发展前景的钼精矿冶金工艺,其工作原理如图所示。电解时,若维持电流强度为0.5A(相当于每秒通过5×10-6mol电子),电解90min,理论上消耗MoS2的质量为______ g。

已知:
I.Re2O7是酸性氧化物,过铼酸(HReO4)是易溶于水的一元强酸,但不具有强氧化性。
Ⅱ.过铼酸铵(NH4ReO4)是白色片状晶体,微溶于冷水,溶于热水。
回答下列问题:
(1)“碱浸”时,Re2O7和MoO3分别与NaOH发生以下反应
(2)“还原”时,Zn被氧化成
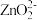 ,铼的化合物被还原生成难溶的2ReO2·2H2O,该反应的离子方程式为
,铼的化合物被还原生成难溶的2ReO2·2H2O,该反应的离子方程式为(3)“沉铼”时,加入热NH4C1溶液至产生白色沉淀,为使沉淀充分析出并分离得到纯净NH4ReO4晶体,“操作I”包括
(4)“热解”时,发生反应的化学方程式为
(5)“酸化沉钼”过程溶液pH和反应时间对钼酸的析出有很大影响,根据下图中数据判断最佳的“酸化沉钼”条件:反应时间为

(6)电氧化法是一种极具发展前景的钼精矿冶金工艺,其工作原理如图所示。电解时,若维持电流强度为0.5A(相当于每秒通过5×10-6mol电子),电解90min,理论上消耗MoS2的质量为

您最近一年使用:0次
2022-03-08更新
|
862次组卷
|
6卷引用:广东省华师附中、实验中学、深圳中学、广雅中学四校2021-2022学年高三上学期期末联考化学试题
(已下线)广东省华师附中、实验中学、深圳中学、广雅中学四校2021-2022学年高三上学期期末联考化学试题湖南省衡阳市第八中学2021-2022学年高三下学期开学考试(第六次月考)化学试题广东名校2021-2022学年高三下学期开学测试化学试题湖南省永州市第四中学2022届高三下学期期中考试化学试题湖南省株洲市第四中学2022-2023学年高三上学期第四次月考化学试题湖南省株洲市九方中学2022-2023学年高三上学期第二次月考化学试题
21-22高三上·江苏南通·期末
名校
解题方法
5 . 用化学方法降解水中有机物已成为污水处理领域的重要研究方向。
(1)酸性条件下,铁炭混合物处理污水中硝基苯时的物质转化示意图如图1所示。
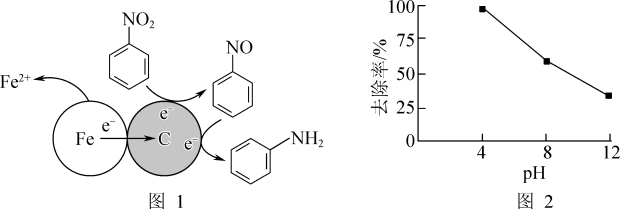
①该物质转化示意图可以描述为_______ 。
②其他条件一定,反应相同时间,硝基苯的去除率与pH的关系如图2所示。pH越大,硝基苯的去除率越低的原因是_______ 。
(2)向含Fe2+和苯胺(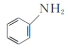 )的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H2O2=Fe3++HO·+H2O
)的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H2O2=Fe3++HO·+H2O
①HO·(羟基自由基)具有强氧化性,能将溶液中的苯胺氧化成CO2和N2。写出该反应的离子方程式:_______ 。
②H2O2也具有氧化性,设计验证苯胺是被HO·氧化而不是被H2O2氧化的实验方案:_______ 。
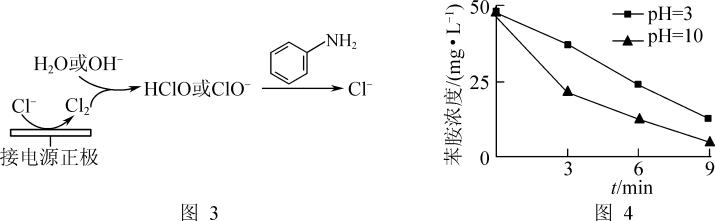
(3)利用电化学装置通过间接氧化法能氧化含苯胺的污水,其原理如图3所示。其他条件一定,测得不同初始pH条件下,溶液中苯胺的浓度与时间的关系如图4所示。反应相同时间,初始溶液pH=3时苯胺浓度大于pH=10时的原因是_______ 。[已知氧化性:HClO(H+)>ClO-(OH-)]
(1)酸性条件下,铁炭混合物处理污水中硝基苯时的物质转化示意图如图1所示。

①该物质转化示意图可以描述为
②其他条件一定,反应相同时间,硝基苯的去除率与pH的关系如图2所示。pH越大,硝基苯的去除率越低的原因是
(2)向含Fe2+和苯胺(
 )的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H2O2=Fe3++HO·+H2O
)的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H2O2=Fe3++HO·+H2O①HO·(羟基自由基)具有强氧化性,能将溶液中的苯胺氧化成CO2和N2。写出该反应的离子方程式:
②H2O2也具有氧化性,设计验证苯胺是被HO·氧化而不是被H2O2氧化的实验方案:
(3)利用电化学装置通过间接氧化法能氧化含苯胺的污水,其原理如图3所示。其他条件一定,测得不同初始pH条件下,溶液中苯胺的浓度与时间的关系如图4所示。反应相同时间,初始溶液pH=3时苯胺浓度大于pH=10时的原因是

您最近一年使用:0次
6 . 锡酸钠晶体(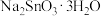 )在电镀、媒染等工业应用广泛,碲(
)在电镀、媒染等工业应用广泛,碲( )被誉为“国防与尖端技术的维生素”。以锡碲渣废料(主要成分为
)被誉为“国防与尖端技术的维生素”。以锡碲渣废料(主要成分为 、
、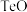 ,还含有少量铁、砷、铅等元素的氧化物)为原料,制备锡酸钠晶体和碲的工艺流程如下:
,还含有少量铁、砷、铅等元素的氧化物)为原料,制备锡酸钠晶体和碲的工艺流程如下:
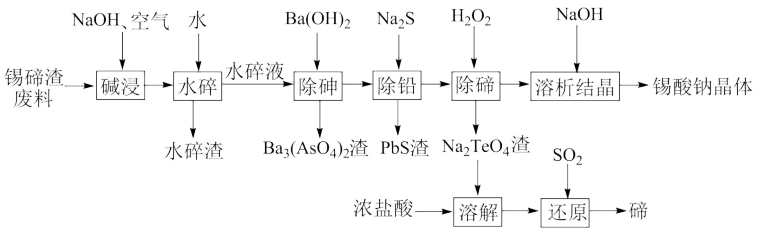
已知:①水碎液中溶质主要成分为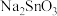 、
、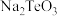 、
、 和
和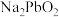 ;
;
②碱性条件下,锡酸钠在水中的溶解度随温度的升高而减小。
回答下列问题:
(1)“碱浸”时, 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(2)“除砷”时,若要使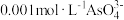 沉淀完全(离子浓度不大于
沉淀完全(离子浓度不大于 ),则需要加入等体积的
),则需要加入等体积的 溶液的物质的量浓度至少为
溶液的物质的量浓度至少为___________ (已知常温下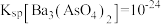 )。
)。
(3)“除铅”时,加入 所发生反应的化学方程式为
所发生反应的化学方程式为___________ 。
(4)“溶析结晶”的操作是___________ ,洗涤,干燥,得到锡酸钠晶体。
(5)“还原”反应中氧化剂与还原剂的物质的量之比为___________ ;
所得碲产品中碲的纯度测定步骤如下:
①取 碲产品,加入酸使其转化为亚碲酸
碲产品,加入酸使其转化为亚碲酸 ,将其配制成
,将其配制成 溶液,取
溶液,取 于锥形瓶中。
于锥形瓶中。
②往锥形瓶中加入 酸性
酸性 溶液,充分反应使亚碲酸转化为碲酸
溶液,充分反应使亚碲酸转化为碲酸 。
。
③用 硫酸亚铁铵
硫酸亚铁铵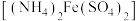 标准溶液滴定剩余的酸性
标准溶液滴定剩余的酸性 溶液,滴入几滴试亚铁灵指示剂至终点显红色,进行三次平行实验,平均消耗
溶液,滴入几滴试亚铁灵指示剂至终点显红色,进行三次平行实验,平均消耗 硫酸亚铁铵标准溶液。
硫酸亚铁铵标准溶液。
计算所得碲产品中碲的纯度为___________ 。
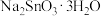 )在电镀、媒染等工业应用广泛,碲(
)在电镀、媒染等工业应用广泛,碲( )被誉为“国防与尖端技术的维生素”。以锡碲渣废料(主要成分为
)被誉为“国防与尖端技术的维生素”。以锡碲渣废料(主要成分为 、
、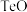 ,还含有少量铁、砷、铅等元素的氧化物)为原料,制备锡酸钠晶体和碲的工艺流程如下:
,还含有少量铁、砷、铅等元素的氧化物)为原料,制备锡酸钠晶体和碲的工艺流程如下:
已知:①水碎液中溶质主要成分为
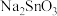 、
、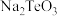 、
、 和
和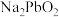 ;
;②碱性条件下,锡酸钠在水中的溶解度随温度的升高而减小。
回答下列问题:
(1)“碱浸”时,
 发生反应的离子方程式为
发生反应的离子方程式为(2)“除砷”时,若要使
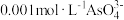 沉淀完全(离子浓度不大于
沉淀完全(离子浓度不大于 ),则需要加入等体积的
),则需要加入等体积的 溶液的物质的量浓度至少为
溶液的物质的量浓度至少为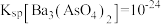 )。
)。(3)“除铅”时,加入
 所发生反应的化学方程式为
所发生反应的化学方程式为(4)“溶析结晶”的操作是
(5)“还原”反应中氧化剂与还原剂的物质的量之比为
所得碲产品中碲的纯度测定步骤如下:
①取
 碲产品,加入酸使其转化为亚碲酸
碲产品,加入酸使其转化为亚碲酸 ,将其配制成
,将其配制成 溶液,取
溶液,取 于锥形瓶中。
于锥形瓶中。②往锥形瓶中加入
 酸性
酸性 溶液,充分反应使亚碲酸转化为碲酸
溶液,充分反应使亚碲酸转化为碲酸 。
。③用
 硫酸亚铁铵
硫酸亚铁铵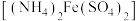 标准溶液滴定剩余的酸性
标准溶液滴定剩余的酸性 溶液,滴入几滴试亚铁灵指示剂至终点显红色,进行三次平行实验,平均消耗
溶液,滴入几滴试亚铁灵指示剂至终点显红色,进行三次平行实验,平均消耗 硫酸亚铁铵标准溶液。
硫酸亚铁铵标准溶液。计算所得碲产品中碲的纯度为
您最近一年使用:0次
名校
解题方法
7 . X、Y、Z、M为短周期元素,原子序数依次增大。A~J均由该四种元素构成的单质或化合物,其转化关系如图所示,部分生成物省略。
已知:①A、B、C、G都是由两种元素构成的化合物,其中A、G分子所含的电子数为10e-,B、C分子所含的电子数为18e-;D为空气的主要成分之一、
②另取16.8gJ在真空条件下,控制温度350~400oC加热至完全分解,得到F和8.96L(已折算成标准状况)A两种物质。

请回答下列问题:
(1)写出C的化学式是___________ ;D的电子式是___________ 。
(2)请写出金属单质E在生产生活中的一种作用___________ 。
(3)写出次氯酸钠与过量气体A反应生成B的化学方程式是___________ ;B在制备过程中,气体A需要过量的理由是___________ 。
(4)写出F和G反应生成H和A的化学方程式是___________ 。
(5)B在加热条件下与CuO反应可生成气体D和金属单质,请设计实验方案,验证B与CuO反应后固体的成分(不考虑其他反应)___________ 。
(6)写出J在已知②条件下受热分解的化学方程式是___________ 。
已知:①A、B、C、G都是由两种元素构成的化合物,其中A、G分子所含的电子数为10e-,B、C分子所含的电子数为18e-;D为空气的主要成分之一、
②另取16.8gJ在真空条件下,控制温度350~400oC加热至完全分解,得到F和8.96L(已折算成标准状况)A两种物质。

请回答下列问题:
(1)写出C的化学式是
(2)请写出金属单质E在生产生活中的一种作用
(3)写出次氯酸钠与过量气体A反应生成B的化学方程式是
(4)写出F和G反应生成H和A的化学方程式是
(5)B在加热条件下与CuO反应可生成气体D和金属单质,请设计实验方案,验证B与CuO反应后固体的成分(不考虑其他反应)
(6)写出J在已知②条件下受热分解的化学方程式是
您最近一年使用:0次
2021-11-05更新
|
1092次组卷
|
2卷引用:浙江省诸暨市2018-2019学年高二下学期期末考试化学试题
解题方法
8 . 化学正在走向精准。当代化学的三大支柱是:理论、实验和计算。
Ⅰ.某溶液为硫酸和硝酸混合后的稀溶液,取200.00mL,该溶液加入过量锌粉充分反应。反应后溶液中只含有一种溶质,其浓度为 (溶液体积不变),收集到无色气体6.72L(标准状况),请列式计算溶液中硫酸和硝酸的浓度比,及产生的氢气的体积(标准状况)。
(溶液体积不变),收集到无色气体6.72L(标准状况),请列式计算溶液中硫酸和硝酸的浓度比,及产生的氢气的体积(标准状况)。______
Ⅱ.某硫铜矿的主要成分为 ,可用于冶炼金属铜,为测定矿石中
,可用于冶炼金属铜,为测定矿石中 的质量分数,进行如下实验(杂质不参加反应):
的质量分数,进行如下实验(杂质不参加反应):
步骤1:在1.00g试样中加入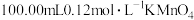 的酸性溶液,加热,硫元素全部转化为
的酸性溶液,加热,硫元素全部转化为 ,铜元素全部转化为
,铜元素全部转化为 ,滤去不溶性杂质。
,滤去不溶性杂质。
步骤2:收集步骤1所得滤液至250mL容量瓶中,定容。取25.00mL溶液,用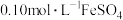 溶液与剩余
溶液与剩余 恰好反应,消耗10.00mL。列式计算
恰好反应,消耗10.00mL。列式计算 的质量分数
的质量分数______ 。
Ⅰ.某溶液为硫酸和硝酸混合后的稀溶液,取200.00mL,该溶液加入过量锌粉充分反应。反应后溶液中只含有一种溶质,其浓度为
 (溶液体积不变),收集到无色气体6.72L(标准状况),请列式计算溶液中硫酸和硝酸的浓度比,及产生的氢气的体积(标准状况)。
(溶液体积不变),收集到无色气体6.72L(标准状况),请列式计算溶液中硫酸和硝酸的浓度比,及产生的氢气的体积(标准状况)。Ⅱ.某硫铜矿的主要成分为
 ,可用于冶炼金属铜,为测定矿石中
,可用于冶炼金属铜,为测定矿石中 的质量分数,进行如下实验(杂质不参加反应):
的质量分数,进行如下实验(杂质不参加反应):步骤1:在1.00g试样中加入
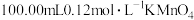 的酸性溶液,加热,硫元素全部转化为
的酸性溶液,加热,硫元素全部转化为 ,铜元素全部转化为
,铜元素全部转化为 ,滤去不溶性杂质。
,滤去不溶性杂质。步骤2:收集步骤1所得滤液至250mL容量瓶中,定容。取25.00mL溶液,用
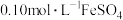 溶液与剩余
溶液与剩余 恰好反应,消耗10.00mL。列式计算
恰好反应,消耗10.00mL。列式计算 的质量分数
的质量分数
您最近一年使用:0次
名校
9 . 酸性废水中的砷元素主要以亚砷酸(H3AsO3)形式存在。已知As2S3难溶于水,也不溶于稀硫酸、稀盐酸等无机酸。
(1)工业上采用硫化法(通常用Na2S)去除废水中的砷。
①向酸性废水中加入Na2S,产生的H2S与H3ASO3反应生成As2S3的化学方程式为_______ 。
②沉淀后,若废水中c(S2-)=1.0×10-4mol·L-1,则c(As3+)=_______ 。[Ksp(As2S3)=4.0×10-38]。
③为了防止As2S3与过量的S2-形成络合离子而溶解,通常需添加适量的FeSO4溶液,形成FeS,与As2S3共沉淀。验证沉淀中含有FeS的实验方法是_______ 。
(2)用硫代硫酸钠(Na2S2O3)替代Na2S处理含砷酸性废水可避免H2S污染。
①Na2S2O3去除酸性废水中H3AsO3的反应机理如图1所示,S2O 经过“途径I”的除砷过程可描述为
经过“途径I”的除砷过程可描述为________ (图中“HS·”为自由基,“·”表示孤单电子)。
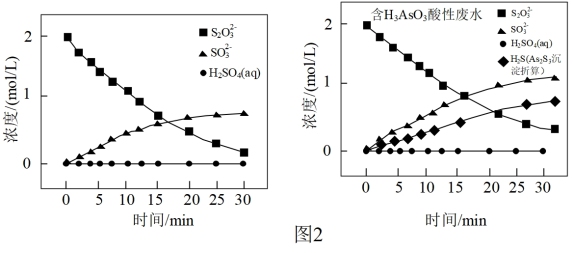
②其他条件相同时,在紫外线照射下,将Na2S2O3分别加入到不含H3AsO3的酸性废水和含H3AsO3的酸性废水中,监测到反应过程中部分物质的浓度变化如图2所示,发现均不释放H2S,其原因是_______ 。
(1)工业上采用硫化法(通常用Na2S)去除废水中的砷。
①向酸性废水中加入Na2S,产生的H2S与H3ASO3反应生成As2S3的化学方程式为
②沉淀后,若废水中c(S2-)=1.0×10-4mol·L-1,则c(As3+)=
③为了防止As2S3与过量的S2-形成络合离子而溶解,通常需添加适量的FeSO4溶液,形成FeS,与As2S3共沉淀。验证沉淀中含有FeS的实验方法是
(2)用硫代硫酸钠(Na2S2O3)替代Na2S处理含砷酸性废水可避免H2S污染。
①Na2S2O3去除酸性废水中H3AsO3的反应机理如图1所示,S2O
 经过“途径I”的除砷过程可描述为
经过“途径I”的除砷过程可描述为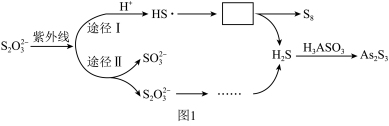
②其他条件相同时,在紫外线照射下,将Na2S2O3分别加入到不含H3AsO3的酸性废水和含H3AsO3的酸性废水中,监测到反应过程中部分物质的浓度变化如图2所示,发现均不释放H2S,其原因是

您最近一年使用:0次
2021-03-27更新
|
1495次组卷
|
2卷引用:江苏省南京市盐城市2021届高三第二次模拟考试化学试题
解题方法
10 . 金属元素A的单质为面心立方结构,晶胞参数a=383.9pm,密度为22.50g/cm3。A与氟气反应得到一种八面体型的氟化物分子B。B与氢气按2:1计量关系反应,得到分子C,C为四聚体,其理想模型有四次旋转轴。A在空气中加热得氧化物D,D属四方晶系,晶胞如下图所示。B与水反应亦可得到D。C与A的单质按1:1计量关系在400℃下反应得化合物E。近期在质谱中捕捉到A的一种四面体型氧合正离子F。(阿伏加德罗常数6.022×1023mol-1)
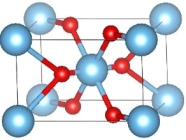
(1)通过计算,确定A是哪种元素______ 。
(2)写出B~F的分子式(或化学式):B______ ,C______ ,D______ ,E______ ,F______ 。
(3)画出C分子的结构示意图______ 。
(4)写出如下反应方程式(要求系数为最简整数比)。
①B与水反应______ ;
②C和A反应生成E______ 。

(1)通过计算,确定A是哪种元素
(2)写出B~F的分子式(或化学式):B
(3)画出C分子的结构示意图
(4)写出如下反应方程式(要求系数为最简整数比)。
①B与水反应
②C和A反应生成E
您最近一年使用:0次



