1 . 2022年6月5日10时44分,神舟十四号载人飞船在酒泉卫星发射中心点火发射。飞船返回地球时,为了减弱返回舱着陆的速度,反推发动机的燃料是高氯酸铵 和铝粉混合物。请回答与高氮酸铵和铝粉相关元素的问题:
和铝粉混合物。请回答与高氮酸铵和铝粉相关元素的问题:
(1)二氧化氯 和过氧化氢均能有效灭杀新冠病毒。
和过氧化氢均能有效灭杀新冠病毒。
① 中氯元素的化合价是
中氯元素的化合价是_______ , 的结构式是
的结构式是_______ 。
②在酸性条件下,由 和双氧水反应制备
和双氧水反应制备 ,其反应的离子方程式为
,其反应的离子方程式为_______ ;该反应中还原剂与氧化剂的物质的量之比为_______ 。
(2)高氯酸铵中铵根离子的电子式为_______ ;高氯酸铵和铝粉中的元素所形成的简单离子中,核外电子数相同、半径由小到大的顺序是_______ (用离子符号表示)。
(3)氮元素的非金属性较强,可 分子的性质比较稳定,其原因是
分子的性质比较稳定,其原因是_______ 。
(4)高氯酸铵和铝粉反应除了生成 和
和 外,还有另外两种不含氮元素的物质生成,请写出其化学方程式
外,还有另外两种不含氮元素的物质生成,请写出其化学方程式_______ 。
 和铝粉混合物。请回答与高氮酸铵和铝粉相关元素的问题:
和铝粉混合物。请回答与高氮酸铵和铝粉相关元素的问题:(1)二氧化氯
 和过氧化氢均能有效灭杀新冠病毒。
和过氧化氢均能有效灭杀新冠病毒。①
 中氯元素的化合价是
中氯元素的化合价是 的结构式是
的结构式是②在酸性条件下,由
 和双氧水反应制备
和双氧水反应制备 ,其反应的离子方程式为
,其反应的离子方程式为(2)高氯酸铵中铵根离子的电子式为
(3)氮元素的非金属性较强,可
 分子的性质比较稳定,其原因是
分子的性质比较稳定,其原因是(4)高氯酸铵和铝粉反应除了生成
 和
和 外,还有另外两种不含氮元素的物质生成,请写出其化学方程式
外,还有另外两种不含氮元素的物质生成,请写出其化学方程式
您最近一年使用:0次
2 . 实验室常用 溶于KI溶液配制高浓度碘水,发生反应:
溶于KI溶液配制高浓度碘水,发生反应: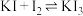 ,低温条件下可制得
,低温条件下可制得 。下列说法不正确的是
。下列说法不正确的是
 溶于KI溶液配制高浓度碘水,发生反应:
溶于KI溶液配制高浓度碘水,发生反应: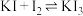 ,低温条件下可制得
,低温条件下可制得 。下列说法不正确的是
。下列说法不正确的是A.向 溶液中加入淀粉溶液,溶液变蓝色 溶液中加入淀粉溶液,溶液变蓝色 |
B.向碘水中滴加 溶液,溶液酸性增强 溶液,溶液酸性增强 |
C. 代替KIO3作食盐加碘剂,高温下可减少碘损失 代替KIO3作食盐加碘剂,高温下可减少碘损失 |
| D.利用上述原理可以除去硫粉中少量的碘单质 |
您最近一年使用:0次
2023-07-16更新
|
412次组卷
|
2卷引用:浙江省杭州市2023届高三上学期11月份教学质量检测化学试题
解题方法
3 . 实验室从含碘废液(含有KI、 等)中回收碘,其实验流程如下:
等)中回收碘,其实验流程如下:

(1)第①步发生的反应______ (填“是”或者“否”)氧化还原反应;
(2)第②步实验操作的名称为______ 。为使 尽可能多地从水相转移至有机相,采取的操作:向装有含
尽可能多地从水相转移至有机相,采取的操作:向装有含 溶液的
溶液的______ (填实验仪器)中加入一定量的 ,
,______ 、静置、分液,并重复多次。
(3)第③步发生反应的化学方程式为______ 。
(4)检验第④步反应的产物碘单质存在的实验方案______ 。
 等)中回收碘,其实验流程如下:
等)中回收碘,其实验流程如下:
(1)第①步发生的反应
(2)第②步实验操作的名称为
 尽可能多地从水相转移至有机相,采取的操作:向装有含
尽可能多地从水相转移至有机相,采取的操作:向装有含 溶液的
溶液的 ,
,(3)第③步发生反应的化学方程式为
(4)检验第④步反应的产物碘单质存在的实验方案
您最近一年使用:0次
名校
解题方法
4 . ClO2是一种杀菌消毒效率高、二次污染小的水处理剂。下列反应可制得ClO2:NaClO3+ H2O2+ H2SO4→ClO2↑+Na2SO4+O2↑+H2O(未配平)
(1)反应中被氧化的元素是________ ,每生成2a个ClO2时有______ 个电子转移。
(2)写出配平后的方程式:___________ ,并用双线桥表示电子转移的方向和数目。
(3)高铁酸钠(Na2FeO4)是一种新型、高效、多功能水处理剂。其工业合成原理是下列物质间发生氧化还原反应:Fe(OH)3、NaCl、H2O 、NaOH 、NaClO、 Na2FeO4。写出并配平化学方程式:_____________________ 。
(4)SO2能使酸性酸性KMnO4溶液褪色,其反应原理是SO2在酸性条件下将 还原为Mn2+,自己转化为
还原为Mn2+,自己转化为 ,写出反应的离子方程式:
,写出反应的离子方程式:___________ 。
(1)反应中被氧化的元素是
(2)写出配平后的方程式:
(3)高铁酸钠(Na2FeO4)是一种新型、高效、多功能水处理剂。其工业合成原理是下列物质间发生氧化还原反应:Fe(OH)3、NaCl、H2O 、NaOH 、NaClO、 Na2FeO4。写出并配平化学方程式:
(4)SO2能使酸性酸性KMnO4溶液褪色,其反应原理是SO2在酸性条件下将
 还原为Mn2+,自己转化为
还原为Mn2+,自己转化为 ,写出反应的离子方程式:
,写出反应的离子方程式:
您最近一年使用:0次
名校
5 . 下列氧化还原反应常识说法正确的是
A.分别由 、 、 、 、 产生等质量的 产生等质量的 时,转移的电子数之比为1∶1∶1 时,转移的电子数之比为1∶1∶1 |
B. 可用作野外生氢剂,作生氢剂时发生氧化还原反应 可用作野外生氢剂,作生氢剂时发生氧化还原反应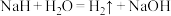 ,则该反应中 ,则该反应中 既是氧化产物又是还原产物,且之比为1∶1 既是氧化产物又是还原产物,且之比为1∶1 |
C. (高铁酸钾)是一种新型绿色消毒剂,常用 (高铁酸钾)是一种新型绿色消毒剂,常用 和 和 在 在 溶液中反应制得,同时生成 溶液中反应制得,同时生成 ,则该反应的氧化剂与还原剂之比为2∶3 ,则该反应的氧化剂与还原剂之比为2∶3 |
D.以二硫化亚铁铜为原料进行火法炼铜,发生反应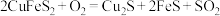 , , 仅作还原剂,硫元素被氧化 仅作还原剂,硫元素被氧化 |
您最近一年使用:0次
名校
解题方法
6 . 物质的性质决定用途,下列物质的应用与其性质没有对应关系的是
| A.铁粉用作食品的保鲜抗氧化剂 |
| B.呼吸面具中用过氧化钠作供氧剂 |
| C.金属元素发生化学反应用以制五彩缤纷的烟花 |
| D.面团中加入小苏打,蒸出的馒头疏松多孔 |
您最近一年使用:0次
2023-07-05更新
|
262次组卷
|
3卷引用:重庆市西南大学附属中学2022-2023学年高一上学期期中考试化学试题
7 . “价—类”二维图是认识和预测元素化合物及其转化关系的重要认知模型。下列有关说法不正确的是


| A.X的浓溶液需保存在棕色试剂瓶中 | B.NO既有氧化性又有还原性 |
| C.NH3能直接转化为NO | D.反应①属于氧化还原反应 |
您最近一年使用:0次
解题方法
8 .  与
与 重整可减少大气中
重整可减少大气中 的排放,重整反应主要分两个过程,其原理如图所示,下列说法错误的是
的排放,重整反应主要分两个过程,其原理如图所示,下列说法错误的是
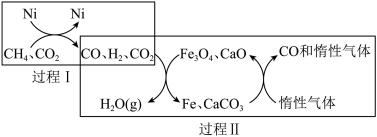
 与
与 重整可减少大气中
重整可减少大气中 的排放,重整反应主要分两个过程,其原理如图所示,下列说法错误的是
的排放,重整反应主要分两个过程,其原理如图所示,下列说法错误的是
A.若过程Ⅰ中有1mol 参与反应,转移电子数为 参与反应,转移电子数为 |
| B.CO是过程Ⅰ的产物,未参与过程Ⅱ的反应 |
C.Fe、 过程Ⅱ反应的中间产物 过程Ⅱ反应的中间产物 |
D.重整过程的总反应为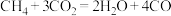 |
您最近一年使用:0次
名校
9 . 含氯物质在日常生活中具有许多重要用途,回答下列问题:
(1)亚氯酸钠(NaClO2)较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为___________(填标号)。
(2)我国从2000年起逐步用ClO2替代氯气进行消毒,工业上常利用反应 制备ClO2,
制备ClO2,___________ 是还原剂,___________ 是还原产物,用单线桥法表示反应中电子得失的方向和数目:___________ 。
(3)工业上可利用ClO2制备亚氯酸钠(NaClO2),反应体系中涉及下列物质:NaClO2、ClO2、H2O2、NaOH、H2O、O2写出反应的化学方程式:___________ 。
(4)某温度下将Cl2通入KOH溶液里,反应后得到KCl、KClO、KClO3的混合溶液,其中 与
与 的个数之比为11∶1,则Cl2与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为
的个数之比为11∶1,则Cl2与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为____ 。
(5)已知氧化性: ,写出少量氯气通入到碘化亚铁溶液中的离子方程式:
,写出少量氯气通入到碘化亚铁溶液中的离子方程式:_____ 。
(6)实验室用下列方法均可制取氯气
①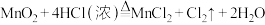
②
③
④
若各反应转移的电子数相同,①②③④生成的氯气质量比为___________ 。
(1)亚氯酸钠(NaClO2)较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为___________(填标号)。
| A.NaCl、Cl2 | B.NaCl、NaClO | C.NaClO3、NaClO4 | D.NaCl、NaClO3 |
 制备ClO2,
制备ClO2,(3)工业上可利用ClO2制备亚氯酸钠(NaClO2),反应体系中涉及下列物质:NaClO2、ClO2、H2O2、NaOH、H2O、O2写出反应的化学方程式:
(4)某温度下将Cl2通入KOH溶液里,反应后得到KCl、KClO、KClO3的混合溶液,其中
 与
与 的个数之比为11∶1,则Cl2与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为
的个数之比为11∶1,则Cl2与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为(5)已知氧化性:
 ,写出少量氯气通入到碘化亚铁溶液中的离子方程式:
,写出少量氯气通入到碘化亚铁溶液中的离子方程式:(6)实验室用下列方法均可制取氯气
①
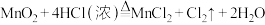
②

③

④

若各反应转移的电子数相同,①②③④生成的氯气质量比为
您最近一年使用:0次
10 . 钴元素是一种重要的战略资源,一种有机物净化钴渣梯级分离与富集钴新工艺如图。
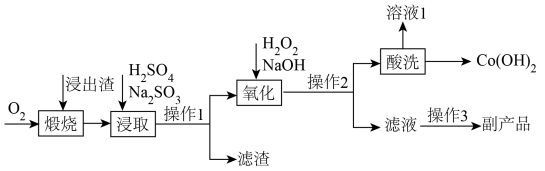
已知:用有机物净化钴渣后钴主要以有机整合物状态存在,在水溶液中难溶,可以水洗预处理得到浸出渣,进一步再继续处理富集钴,浸出渣中还含有Zn、Fe、Cd(与Zn同族)等元素。回答下列问题:
(1)“煅烧”的主要目的是________ 。
(2)“浸取”过程中发生氧化还原反应的离子方程式是________ 。操作2是________ ,得到的固体物质中含有________ (填化学式,下同);若副产品为含结晶水的固体,则其主要成分为_______ 。
(3)当溶液中可溶组分浓度c≤1.0×10-5mol•L-1时,可认为已除尽。
已知:①Ksp[Co(OH)3]=1×10-44
②金属离子开始沉淀和沉淀完全的pH数据如表所示:
则“酸洗”时溶液pH的理论范围为________ 。

已知:用有机物净化钴渣后钴主要以有机整合物状态存在,在水溶液中难溶,可以水洗预处理得到浸出渣,进一步再继续处理富集钴,浸出渣中还含有Zn、Fe、Cd(与Zn同族)等元素。回答下列问题:
(1)“煅烧”的主要目的是
(2)“浸取”过程中发生氧化还原反应的离子方程式是
(3)当溶液中可溶组分浓度c≤1.0×10-5mol•L-1时,可认为已除尽。
已知:①Ksp[Co(OH)3]=1×10-44
②金属离子开始沉淀和沉淀完全的pH数据如表所示:
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.5 | 3.3 |
| Cd2+ | 7.2 | 9.5 |
| Zn2+ | 6.2 | 8.0 |
您最近一年使用:0次



