1 . 在五千年的历史长河中,中华民族创造了辉煌灿烂的文化。下列说法正确的是
| A.“(火药)乃焰消(KNO3)、硫黄、杉木炭所合,以为烽燧铳机诸药者”,是利用了杉木炭的氧化性 |
| B.“凡造竹……用上好石灰化汁涂浆”,造纸利用了石灰的碱性 |
| C.“凡酸坏之酒,皆可蒸烧”,该过程主要发生的是化学变化 |
| D.“共煅五个时辰,其中砂末尽化成汞,布于满釜”,该金属的冶炼方法与银冶炼方法不同 |
您最近一年使用:0次
名校
解题方法
2 . 元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、 (橙红色)、
(橙红色)、 (黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,K2Cr2O7溶液中存在如下平衡:
(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,K2Cr2O7溶液中存在如下平衡: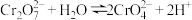
回答下列问题:
(1)探究外界因素对该平衡的影响。取三支相同(标号1,2,3)试管盛有相同体积 溶液进行实验,完成下列表格中的填空。
溶液进行实验,完成下列表格中的填空。
(2)利用(1)中所得溶液A、B探究pH对 溶液的氧化性强弱的影响。完成表格中的填空。
溶液的氧化性强弱的影响。完成表格中的填空。
(3)在化学分析中采用 为指示剂,以
为指示剂,以 标准溶液滴定溶液中的
标准溶液滴定溶液中的 ,利用
,利用 与
与 生成砖红色沉淀,指示到达滴定终点。滴定终点时,溶液中
生成砖红色沉淀,指示到达滴定终点。滴定终点时,溶液中 时,此时溶液中
时,此时溶液中 等于
等于_______  。[已知
。[已知 ]
]
 (橙红色)、
(橙红色)、 (黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,K2Cr2O7溶液中存在如下平衡:
(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,K2Cr2O7溶液中存在如下平衡: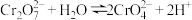
回答下列问题:
(1)探究外界因素对该平衡的影响。取三支相同(标号1,2,3)试管盛有相同体积
 溶液进行实验,完成下列表格中的填空。
溶液进行实验,完成下列表格中的填空。| 实验操作 | 实验现象 | 实验结论 |
| 向试管1中加入几滴浓NaOH溶液,得溶液A | 溶液变为① | 其他条件不变时,减小② |
| 向试管2中加入几滴较浓H2SO4溶液,得溶液B | 溶液变为④ | 其他条件不变时,增大生成物浓度,平衡向逆反应方向移动 |
| 向试管2中加入FeSO4,再加入适量NaOH溶液 | 先形成蓝紫色溶液,加入NaOH溶液后产生红褐色沉淀和⑤ | K2Cr2O7溶液具有氧化性,产物不溶于适量NaOH溶液 |
 溶液的氧化性强弱的影响。完成表格中的填空。
溶液的氧化性强弱的影响。完成表格中的填空。| 实验操作 | 实验现象 | 实验结论 |
| 相同量的溶液A、B中分别加入相同量甲醇溶液 | 向溶液A无明显现象,溶液B形成蓝紫色溶液 |
 为指示剂,以
为指示剂,以 标准溶液滴定溶液中的
标准溶液滴定溶液中的 ,利用
,利用 与
与 生成砖红色沉淀,指示到达滴定终点。滴定终点时,溶液中
生成砖红色沉淀,指示到达滴定终点。滴定终点时,溶液中 时,此时溶液中
时,此时溶液中 等于
等于 。[已知
。[已知 ]
]
您最近一年使用:0次
3 . 我省为沿海省份,海洋中有丰富的食品、矿产、能源、药物和水产等资源,海水资源的综合利用可以用下图表示。
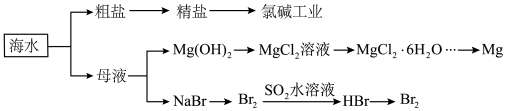
下列关于海水提取Br2的说法正确的是

下列关于海水提取Br2的说法正确的是
| A.将NaBr转化为Br2,可以选用Cl2、O2等还原剂 |
| B.将Br2转化为HBr,可利用溴单质易升华的特性用空气将溴吹出 |
C.将Br2转化为HBr的离子方程式为:SO2+2H2O+Br2=2H++SO +2HBr +2HBr |
| D.海水提取溴中出现了两次溴离子被氧化的过程 |
您最近一年使用:0次
名校
解题方法
4 . 氧化铬(Cr2O3)是重要的化工原料,以铬铁矿(主要成分为FeCr2O4)为原料制备Cr2O3的流 程如图所示:
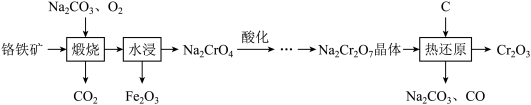
下列说法正确的是

下列说法正确的是
| A.“煅烧”,可以在氧化铝耐高温熔炉中进行 |
| B.“煅烧”,时Na2CrO4和 Fe2O3均为还原产物 |
| C.可以用盐酸也可以用硫酸"“酸化” |
| D.热还原,过程中氧化剂与还原剂的物质的量之比为 1 :2 |
您最近一年使用:0次
2023-04-24更新
|
128次组卷
|
2卷引用:河南省洛阳市新安县第一高级中学2022-2023学年高三上学期12月线上考试(实验班)化学试题
解题方法
5 . 如图是中学化学中常见物质的转化关系。E为红棕色气体,单质G可被磁铁吸引, 和
和 的浓溶液靠近会出现白烟。
的浓溶液靠近会出现白烟。
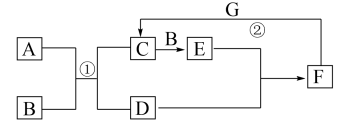
回答下列问题:
(1)D的电子式为_____ ,C的化学式是_____ 。
(2)实验室中常将F的浓溶液保存在_____ 色细口瓶中并置于阴凉处。用化学方程式解释原因______ 。
(3)过量G发生反应②后,向溶液中加入足量氢氧化钠溶液,现象为_____ 。
(4)为防止E污染环境,可用CH4与其反应生成无污染气体和水,写出该反应的化学方程式______ 。
 和
和 的浓溶液靠近会出现白烟。
的浓溶液靠近会出现白烟。
回答下列问题:
(1)D的电子式为
(2)实验室中常将F的浓溶液保存在
(3)过量G发生反应②后,向溶液中加入足量氢氧化钠溶液,现象为
(4)为防止E污染环境,可用CH4与其反应生成无污染气体和水,写出该反应的化学方程式
您最近一年使用:0次
名校
解题方法
6 . 氧化还原反应是中学阶段非常重要的知识,对它的认知和理解是分析问题的关键。
(1)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为: ,在此反应中,被还原的元素为
,在此反应中,被还原的元素为___________ (填元素符号),氧化产物是___________ (填化学式),6.4gS参加反应时,产生气体的体积为___________ L(标况下)。
(2)写出浓盐酸与二氧化锰反应产生氯气的化学方程式___________ ,该反应中体现了浓盐酸的___________ 性质,当生成1mol的氯气时,被氧化的HCl的物质的量___________ 。
(3)将等物质的量的Cl2和SO2通入BaCl2溶液中,能观察到白色沉淀,用离子方程式解释原因___________ 、___________ 。
(4)高锰酸钾和浓盐酸可以发生反应:2KMnO4+16HCl(浓)=5Cl2↑+2MnCl2+2KCl+8H2O
①用单线桥法表示此反应的电子转移的方向及数目___________ 。
②该反应的氧化剂与还原剂物质的量之比为___________ 。
(1)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为:
 ,在此反应中,被还原的元素为
,在此反应中,被还原的元素为(2)写出浓盐酸与二氧化锰反应产生氯气的化学方程式
(3)将等物质的量的Cl2和SO2通入BaCl2溶液中,能观察到白色沉淀,用离子方程式解释原因
(4)高锰酸钾和浓盐酸可以发生反应:2KMnO4+16HCl(浓)=5Cl2↑+2MnCl2+2KCl+8H2O
①用单线桥法表示此反应的电子转移的方向及数目
②该反应的氧化剂与还原剂物质的量之比为
您最近一年使用:0次
2023-04-20更新
|
267次组卷
|
4卷引用:山东省利津县高级中学2022-2023学年高一12月月考化学试题
7 . 空气吹出法工艺,是目前“海水(呈弱碱性)提溴”的最主要方法之一、其工艺流程如图所示。下列说法错误的是
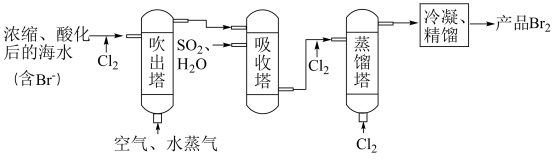

A.吸收塔内发生反应的离子方程式为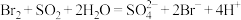 |
| B.每提取1mol溴,理论上消耗氯气22.4L(标准状况) |
C.工业溴中含少量 ,可用NaOH溶液除去 ,可用NaOH溶液除去 |
D.根据上述流程可判断氧化性强弱顺序: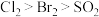 |
您最近一年使用:0次
8 . 尖晶石型锰酸锂(LiMn2O4)是一种环保绿色能源新型材料。实验室中可通过如下反应制备: ,下列关于该反应的说法错误的是
,下列关于该反应的说法错误的是
 ,下列关于该反应的说法错误的是
,下列关于该反应的说法错误的是| A.MnO2为氧化剂,O2为氧化产物 |
| B.反应中Mn元素被还原,O元素部分被氧化 |
C.每制备1molLiMn2O4,反应转移 |
| D.为节能减排,用NaOH溶液吸收CO2转化为正盐,理论上消耗的MnO2和NaOH的物质的量之比为4:1 |
您最近一年使用:0次
解题方法
9 . 汽车尾气及氮肥厂产生的氮氧化物等会造成光化学烟雾、雾霾及酸雨等,可危害环境。利用氮元素的价类二维图,寻找治理氮氧化物污染的途径。
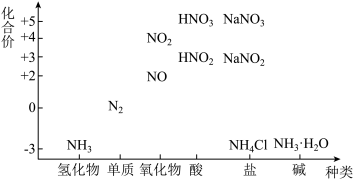
下列叙述错误的是

下列叙述错误的是
| A.从物质性质角度,需要将NO转变为无污染的氮气 |
| B.从化合价角度,将NO转变为无污染物需要寻找还原剂 |
| C.从氮元素角度,上述物质中既能作氧化剂又能作还原剂的物质有4种 |
| D.从反应类型角度,上述物质之间能发生的复分解反应有2个 |
您最近一年使用:0次
名校
10 . 海水化学资源开发利用中的提碘、提溴的部分过程如图所示。下列说法正确的是
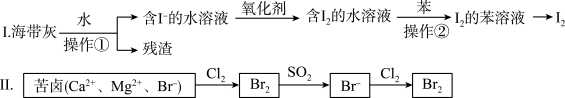
| A.I中操作①用到的玻璃仪器只有烧杯、玻璃棒、胶头滴管 |
| B.I中操作②的苯可用酒精代替 |
C.Ⅱ中SO2与Br2反应的化学方程式为: |
D.Ⅱ中还原性: |
您最近一年使用:0次
2023-04-08更新
|
631次组卷
|
3卷引用:山东省威海市2022-2023学年高一上学期期末考试化学试题



