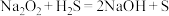1 . 研究表明,土壤中的 被土壤胶体吸附后,在硝化细菌的作用下转化为
被土壤胶体吸附后,在硝化细菌的作用下转化为 后,土壤中的
后,土壤中的 进一步将
进一步将 氧化为更易被植物吸收的
氧化为更易被植物吸收的 。在氧气较少的环境下,
。在氧气较少的环境下, 又可以在反硝化细菌的作用下与
又可以在反硝化细菌的作用下与 反应,使氮以
反应,使氮以 形式放出。下列说法不正确的是
形式放出。下列说法不正确的是
 被土壤胶体吸附后,在硝化细菌的作用下转化为
被土壤胶体吸附后,在硝化细菌的作用下转化为 后,土壤中的
后,土壤中的 进一步将
进一步将 氧化为更易被植物吸收的
氧化为更易被植物吸收的 。在氧气较少的环境下,
。在氧气较少的环境下, 又可以在反硝化细菌的作用下与
又可以在反硝化细菌的作用下与 反应,使氮以
反应,使氮以 形式放出。下列说法不正确的是
形式放出。下列说法不正确的是A. 被氧化为 被氧化为 的过程中, 的过程中, 与 与 的物质的量之比为2:1 的物质的量之比为2:1 |
| B.在反硝化过程中,土壤pH升高 |
C. 与 与 反应时,每生成 反应时,每生成 ,转移电子数为3.75mol ,转移电子数为3.75mol |
| D.适当疏松土壤,有利于提高铵态氮肥的肥效 |
您最近一年使用:0次
名校
解题方法
2 . 将17.9g由Cu、Al、Fe组成的合金溶于足量的NaOH溶液中,合金质量减少了2.7g。另取等质量的合金溶于过量稀 中,生成了6.72LNO(标准状况下),向反应后的溶液中加入过量的NaOH溶液,则沉淀的质量为
中,生成了6.72LNO(标准状况下),向反应后的溶液中加入过量的NaOH溶液,则沉淀的质量为
 中,生成了6.72LNO(标准状况下),向反应后的溶液中加入过量的NaOH溶液,则沉淀的质量为
中,生成了6.72LNO(标准状况下),向反应后的溶液中加入过量的NaOH溶液,则沉淀的质量为| A.22.1g | B.25.4g | C.33.2g | D.30.2g |
您最近一年使用:0次
3 . 高温结构陶瓷氮化硅是一种优异的无机非金属材料,可通过以下反应制备: (未配平),下列说法中错误的是
(未配平),下列说法中错误的是
 (未配平),下列说法中错误的是
(未配平),下列说法中错误的是A.氮化硅的化学式为 |
| B.该反应中氧化剂与还原剂的物质的量之比为3:1 |
C.反应生成22.4L一氧化碳(标准状况)时,消耗的 的质量为30g 的质量为30g |
| D.通入氮气的量不足时,产物中可能会混有硅单质 |
您最近一年使用:0次
名校
4 . 氧化还原反应在日常生活中有着广泛的应用,下列有关化学用语和相关说法均正确的是
选项 | 化学反应方程式 | 相关说法 |
A |
|  是氧化产物, 是氧化产物, 既是氧化剂又是还原剂 既是氧化剂又是还原剂 |
B |
| 均为单质被还原的置换反应 |
C |
| 每生成1mol |
D |
| 氧化性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 某处工厂排出的烟道气中含氮氧化物(主要为NO、 )、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图:
)、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图: 混合气体按一定比例被
混合气体按一定比例被 溶液完全吸收生成
溶液完全吸收生成 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式______________ ;若反应后尾气无残留,则参加反应的 、NO物质的量比值为
、NO物质的量比值为_____ (填字母)。
a.≥1 b.≤1 c.任意值
(2)可使用适量酸性 溶液,将溶液中的
溶液,将溶液中的 全部氧化为
全部氧化为 ,发生反应的离子方程式是
,发生反应的离子方程式是_______________ 。
(3)气囊用来储存处理后气体,其中可能含少量NO气体,可用酸性 溶液来处理。
溶液来处理。 氧化NO生成
氧化NO生成 和
和 ,发生反应的离子方程式是
,发生反应的离子方程式是_______________ 。
(4)有氧条件下,NO在催化剂作用下可被 还原为
还原为 。在钒基催化剂
。在钒基催化剂 作用下的脱硝反应机理如图所示:
作用下的脱硝反应机理如图所示: 在有氧条件下的总化学方程式是
在有氧条件下的总化学方程式是___________ 。
(5)羟基自由基( )也可以用于脱硫脱硝。如图表示光催化氧化技术可生成
)也可以用于脱硫脱硝。如图表示光催化氧化技术可生成 ﹔光照时,价带失去电子产生有强氧化性的空穴,价带上
﹔光照时,价带失去电子产生有强氧化性的空穴,价带上 直接转化为
直接转化为 ;描述产生
;描述产生 的另一种过程:
的另一种过程:______________ 。 等杂质,可以采用
等杂质,可以采用 测定含量。称取
测定含量。称取 该亚硝酸钠产品溶于水配制成
该亚硝酸钠产品溶于水配制成 的样品溶液。取
的样品溶液。取 该样品溶液于锥形瓶中,用稀
该样品溶液于锥形瓶中,用稀 酸化后,再向锥形瓶中滴加
酸化后,再向锥形瓶中滴加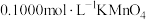 溶液,至恰好完全反应时,消耗
溶液,至恰好完全反应时,消耗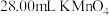 溶液。计算该产品中
溶液。计算该产品中 的质量分数
的质量分数__________ 。(写出计算过程)
 )、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图:
)、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图: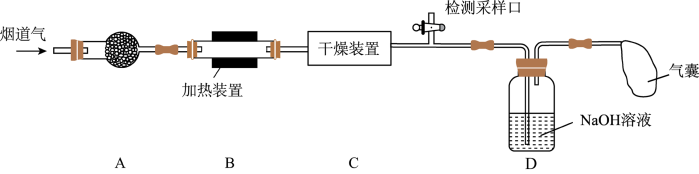
 混合气体按一定比例被
混合气体按一定比例被 溶液完全吸收生成
溶液完全吸收生成 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式 、NO物质的量比值为
、NO物质的量比值为a.≥1 b.≤1 c.任意值
(2)可使用适量酸性
 溶液,将溶液中的
溶液,将溶液中的 全部氧化为
全部氧化为 ,发生反应的离子方程式是
,发生反应的离子方程式是(3)气囊用来储存处理后气体,其中可能含少量NO气体,可用酸性
 溶液来处理。
溶液来处理。 氧化NO生成
氧化NO生成 和
和 ,发生反应的离子方程式是
,发生反应的离子方程式是(4)有氧条件下,NO在催化剂作用下可被
 还原为
还原为 。在钒基催化剂
。在钒基催化剂 作用下的脱硝反应机理如图所示:
作用下的脱硝反应机理如图所示: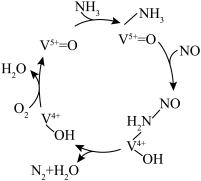
 在有氧条件下的总化学方程式是
在有氧条件下的总化学方程式是(5)羟基自由基(
 )也可以用于脱硫脱硝。如图表示光催化氧化技术可生成
)也可以用于脱硫脱硝。如图表示光催化氧化技术可生成 ﹔光照时,价带失去电子产生有强氧化性的空穴,价带上
﹔光照时,价带失去电子产生有强氧化性的空穴,价带上 直接转化为
直接转化为 ;描述产生
;描述产生 的另一种过程:
的另一种过程: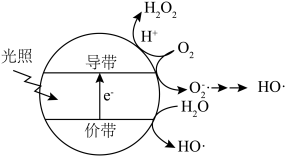
 等杂质,可以采用
等杂质,可以采用 测定含量。称取
测定含量。称取 该亚硝酸钠产品溶于水配制成
该亚硝酸钠产品溶于水配制成 的样品溶液。取
的样品溶液。取 该样品溶液于锥形瓶中,用稀
该样品溶液于锥形瓶中,用稀 酸化后,再向锥形瓶中滴加
酸化后,再向锥形瓶中滴加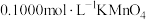 溶液,至恰好完全反应时,消耗
溶液,至恰好完全反应时,消耗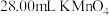 溶液。计算该产品中
溶液。计算该产品中 的质量分数
的质量分数
您最近一年使用:0次
2024-05-03更新
|
220次组卷
|
3卷引用:河南省焦作市博爱县第一中学2023-2024学年高一下学期4月期中考试化学试题
6 . 取2molFeS与2L一定浓度的硝酸反应,生成了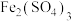 、
、 、NO、
、NO、 、
、 和
和 。反应后的溶液中
。反应后的溶液中 ,生成的NO、
,生成的NO、 和
和 的物质的量之比为1:1:1(溶液体积变化忽略不计),请回答:
的物质的量之比为1:1:1(溶液体积变化忽略不计),请回答:
(1)反应后溶液中 的浓度为
的浓度为______ 。
(2)参加反应的FeS与 的物质的量之比为
的物质的量之比为______ 。
(3)原硝酸的浓度为______ 。
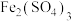 、
、 、NO、
、NO、 、
、 和
和 。反应后的溶液中
。反应后的溶液中 ,生成的NO、
,生成的NO、 和
和 的物质的量之比为1:1:1(溶液体积变化忽略不计),请回答:
的物质的量之比为1:1:1(溶液体积变化忽略不计),请回答:(1)反应后溶液中
 的浓度为
的浓度为(2)参加反应的FeS与
 的物质的量之比为
的物质的量之比为(3)原硝酸的浓度为
您最近一年使用:0次
7 . 铁及其化合物与生产、生活关系密切:
(1)下列铁化合物中,可以通过化合反应得到是_______(填字母序号)。
(2) 可作为铜电路板的腐蚀液,该反应的化学方程式
可作为铜电路板的腐蚀液,该反应的化学方程式_______ 。向反应后的溶液加入_______ (填名称),可回收Cu,并得到 溶液。
溶液。
(3)用废铁皮制取( )的部分流程示意图如下:
)的部分流程示意图如下:_______ 。
(4) 可制取新型、高效水处理剂高铁酸钾,反应原理为
可制取新型、高效水处理剂高铁酸钾,反应原理为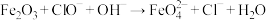 (未配平),该反应中氧化剂与还原剂的物质的量之比为
(未配平),该反应中氧化剂与还原剂的物质的量之比为_______ 。
(5) 可将氨氮废水中
可将氨氮废水中 的转化为
的转化为 除去。从价态角度分析,
除去。从价态角度分析, 能处理氨氮废水的原因是
能处理氨氮废水的原因是_______ 。当该反应转移1.2mol电子时,能产生_______ mol 。
。
(1)下列铁化合物中,可以通过化合反应得到是_______(填字母序号)。
A. | B. | C. | D. |
(2)
 可作为铜电路板的腐蚀液,该反应的化学方程式
可作为铜电路板的腐蚀液,该反应的化学方程式 溶液。
溶液。(3)用废铁皮制取(
 )的部分流程示意图如下:
)的部分流程示意图如下: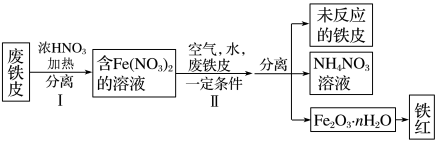
(4)
 可制取新型、高效水处理剂高铁酸钾,反应原理为
可制取新型、高效水处理剂高铁酸钾,反应原理为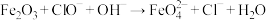 (未配平),该反应中氧化剂与还原剂的物质的量之比为
(未配平),该反应中氧化剂与还原剂的物质的量之比为(5)
 可将氨氮废水中
可将氨氮废水中 的转化为
的转化为 除去。从价态角度分析,
除去。从价态角度分析, 能处理氨氮废水的原因是
能处理氨氮废水的原因是 。
。
您最近一年使用:0次
2024-05-03更新
|
128次组卷
|
2卷引用:福建省莆田第二十五中学2023-2024学年高一下学期期中考试化学试题
8 . 向10.95g铜铝混合物(除铜、铝外无其他物质)中加入2 稀硝酸,充分反应后固体完全溶解,收集到V L(已换算成标准状况下的体积)NO气体(无其他气体生成),继续向反应后的混合溶液中滴加NaOH溶液至过量,经过滤﹑洗涤、干燥,得到14.7g固体。下列说法正确的是
稀硝酸,充分反应后固体完全溶解,收集到V L(已换算成标准状况下的体积)NO气体(无其他气体生成),继续向反应后的混合溶液中滴加NaOH溶液至过量,经过滤﹑洗涤、干燥,得到14.7g固体。下列说法正确的是
 稀硝酸,充分反应后固体完全溶解,收集到V L(已换算成标准状况下的体积)NO气体(无其他气体生成),继续向反应后的混合溶液中滴加NaOH溶液至过量,经过滤﹑洗涤、干燥,得到14.7g固体。下列说法正确的是
稀硝酸,充分反应后固体完全溶解,收集到V L(已换算成标准状况下的体积)NO气体(无其他气体生成),继续向反应后的混合溶液中滴加NaOH溶液至过量,经过滤﹑洗涤、干燥,得到14.7g固体。下列说法正确的是| A.V约为3.36 |
| B.混合物中铜与铝的物质的量之比为2∶1 |
| C.至少需要400mL稀硝酸 |
| D.滴加NaOH溶液的过程中,固体质量最大为18.2g |
您最近一年使用:0次
2024-05-03更新
|
110次组卷
|
2卷引用:湖北省部分学校2023-2024学年高一下学期4月期中考试化学试题
名校
9 . 过氧化钠( ,其中氧元素显
,其中氧元素显 价)和水的反应:
价)和水的反应: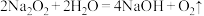 。用
。用 表示阿伏加德罗常数,下列说法正确的是
表示阿伏加德罗常数,下列说法正确的是
 ,其中氧元素显
,其中氧元素显 价)和水的反应:
价)和水的反应: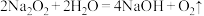 。用
。用 表示阿伏加德罗常数,下列说法正确的是
表示阿伏加德罗常数,下列说法正确的是A.每转移 个电子生成氧化产物1mol 个电子生成氧化产物1mol |
B.22.4L 含 含 个氧原子 个氧原子 |
C. 既是氧化产物又是还原产物 既是氧化产物又是还原产物 |
D.4gNaOH溶于100mL水中,所得溶液的物质的量浓度为 |
您最近一年使用:0次
10 . 硝酸是重要的化工原料。如图是以合成氨为基础的传统硝酸生产工艺流程(其中空气等基础原料已略去)。_____________ (填序号)。
 .合成氨是一种重要的人工固氮方法
.合成氨是一种重要的人工固氮方法
 .该反应过程中氮元素被氧化
.该反应过程中氮元素被氧化
 .合成的氨气还可以用于化肥工业
.合成的氨气还可以用于化肥工业
 .该反应采用高温、高压等苛刻条件,与
.该反应采用高温、高压等苛刻条件,与 化学性质很稳定有关
化学性质很稳定有关
(2)氨氧化装置中,产生的含氮物质主要为 ,反应的化学方程式为
,反应的化学方程式为_________ 。
(3)聚合、吸收装置中,含氮物质转化的主要反应包括① ;②
;②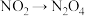 ;③
;③ ,其中属于氧化还原反应的是
,其中属于氧化还原反应的是_________ (填序号)。
(4)吸收装置中,发生的反应为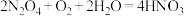 ,若用
,若用 稀硝酸作为吸收液,反应后得到
稀硝酸作为吸收液,反应后得到 的浓硝酸,则理论上吸收装置中需消耗的
的浓硝酸,则理论上吸收装置中需消耗的 的物质的量为
的物质的量为_________  (写出计算式)。
(写出计算式)。
(5)为实现制硝酸的绿色化改进,技术人员将①分离液态空气、②电解水等工艺整合在上述流程中。请在①、②中任选一种,说明该工艺的产物如何应用于硝酸生产流程:_____________ 。
(6) 催化还原氮氧化物
催化还原氮氧化物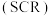 技术是目前应用最广泛的氮氧化物脱除技术,可用于上述硝酸生产工艺的废气处理,反应原理如图所示:
技术是目前应用最广泛的氮氧化物脱除技术,可用于上述硝酸生产工艺的废气处理,反应原理如图所示: 和
和 物质的量之比为
物质的量之比为 ,则总反应的化学方程式为
,则总反应的化学方程式为_________ 。
(7)据报道,意大利科学家获得了极具研究价值的 ,其分子结构如图所示。已知:Ⅰ.断裂
,其分子结构如图所示。已知:Ⅰ.断裂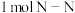 键吸收
键吸收 热量,形成
热量,形成 键放出
键放出 热量
热量
Ⅱ.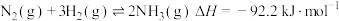
写出 和
和 反应合成
反应合成 的热化学方程式
的热化学方程式_____________________________ 。

 .合成氨是一种重要的人工固氮方法
.合成氨是一种重要的人工固氮方法 .该反应过程中氮元素被氧化
.该反应过程中氮元素被氧化 .合成的氨气还可以用于化肥工业
.合成的氨气还可以用于化肥工业 .该反应采用高温、高压等苛刻条件,与
.该反应采用高温、高压等苛刻条件,与 化学性质很稳定有关
化学性质很稳定有关(2)氨氧化装置中,产生的含氮物质主要为
 ,反应的化学方程式为
,反应的化学方程式为(3)聚合、吸收装置中,含氮物质转化的主要反应包括①
 ;②
;②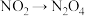 ;③
;③ ,其中属于氧化还原反应的是
,其中属于氧化还原反应的是(4)吸收装置中,发生的反应为
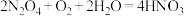 ,若用
,若用 稀硝酸作为吸收液,反应后得到
稀硝酸作为吸收液,反应后得到 的浓硝酸,则理论上吸收装置中需消耗的
的浓硝酸,则理论上吸收装置中需消耗的 的物质的量为
的物质的量为 (写出计算式)。
(写出计算式)。(5)为实现制硝酸的绿色化改进,技术人员将①分离液态空气、②电解水等工艺整合在上述流程中。请在①、②中任选一种,说明该工艺的产物如何应用于硝酸生产流程:
(6)
 催化还原氮氧化物
催化还原氮氧化物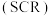 技术是目前应用最广泛的氮氧化物脱除技术,可用于上述硝酸生产工艺的废气处理,反应原理如图所示:
技术是目前应用最广泛的氮氧化物脱除技术,可用于上述硝酸生产工艺的废气处理,反应原理如图所示: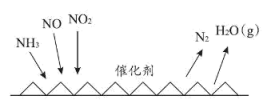
 和
和 物质的量之比为
物质的量之比为 ,则总反应的化学方程式为
,则总反应的化学方程式为(7)据报道,意大利科学家获得了极具研究价值的
 ,其分子结构如图所示。已知:Ⅰ.断裂
,其分子结构如图所示。已知:Ⅰ.断裂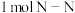 键吸收
键吸收 热量,形成
热量,形成 键放出
键放出 热量
热量Ⅱ.
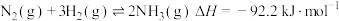
写出
 和
和 反应合成
反应合成 的热化学方程式
的热化学方程式
您最近一年使用:0次


 ,
,
 个电子
个电子