名校
解题方法
1 . 大力发展新能源汽车产业是我国兑现碳中和承诺的重要战略之一。随着这一产业的发展,如何处理废旧锂电池成为一个亟需解决的问题。某废弃的钴酸锂( )电池中含有少量氧化铝、氧化铁和碳单质,为回收利用有关元素,某小组设计如下实验流程:
)电池中含有少量氧化铝、氧化铁和碳单质,为回收利用有关元素,某小组设计如下实验流程:

已知: 与草酸根离子(
与草酸根离子( )结合生成较稳定的
)结合生成较稳定的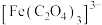 ,
,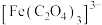 在强酸性条件下分解重新生成
在强酸性条件下分解重新生成 。
。
(1)操作①的名称为______ ;由此可推测,氧化铝______ (填“能”或“不能”)溶于氢氧化钠溶液。
(2)溶液②中所含主要溶质为LiCl、 ,请写出
,请写出 和盐酸反应的化学方程式中LiCoO2和HCl的最简系数比(提示:产物有氯气)
和盐酸反应的化学方程式中LiCoO2和HCl的最简系数比(提示:产物有氯气)______ 。
(3)将溶液中的 转化为
转化为 沉淀也是常用的沉钴方案。在此流程中选用草酸铵而不用碳酸盐的原因是
沉淀也是常用的沉钴方案。在此流程中选用草酸铵而不用碳酸盐的原因是__________________ 。
(4)为证明操作④获得的 沉淀表面的杂质已被洗涤干净,所需进行的实验操作为:取少量的最后一次洗涤液于试管中,加入
沉淀表面的杂质已被洗涤干净,所需进行的实验操作为:取少量的最后一次洗涤液于试管中,加入______ ,若无白色沉淀生成,则证明沉淀洗涤干净。
(5)取3.66 g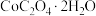 (相对分子质量183)隔绝空气加热,在205℃条件下反应完全后,剩余固体质量为2.94 g,此时分解产生的气体为
(相对分子质量183)隔绝空气加热,在205℃条件下反应完全后,剩余固体质量为2.94 g,此时分解产生的气体为______ (填化学式);在956℃条件下反应完全后,剩余固体相对最开始反应前失重59%,此时固体成分的化学式为 ,
,
______ 。
(6)某同学设计如图装置测定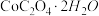 晶体中结晶水的含量以检验样品的纯度。下列有关说法不正确的是
晶体中结晶水的含量以检验样品的纯度。下列有关说法不正确的是______ (填选项)。

A. B中应装入浓硫酸,目的是除去水蒸气
B. 利用干燥管前后质量差可计算出结晶水的含量
C. 图中半透膜可让气体通过又可防止固体粉末进入导管
D. 反应结束后,应先停止加热,一段时间后再停止通空气
(7)溶液④中,铁元素主要以______ 离子形态存在,应加入______ 后再进行后续操作。
(8) 溶液在工业上常用于电路板的蚀刻,发生的反应为
溶液在工业上常用于电路板的蚀刻,发生的反应为 。某同学向含有
。某同学向含有 、
、 和
和 三种溶质的溶液中加入一定量的铁粉,若反应完成后有固体剩余,则固体的成分可能为
三种溶质的溶液中加入一定量的铁粉,若反应完成后有固体剩余,则固体的成分可能为______ (填选项)。
A. Fe B. Fe和Zn C. Fe和Cu D. Cu和Zn
(9)某a g混合粉末中含有铁、石墨、硫和碳酸氢铵,在空气中充分加热至完全反应后,重新称量剩余固体质量,仍为a g,则混合物中铁的质量分数为______ 。
 )电池中含有少量氧化铝、氧化铁和碳单质,为回收利用有关元素,某小组设计如下实验流程:
)电池中含有少量氧化铝、氧化铁和碳单质,为回收利用有关元素,某小组设计如下实验流程:
已知:
 与草酸根离子(
与草酸根离子( )结合生成较稳定的
)结合生成较稳定的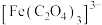 ,
,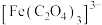 在强酸性条件下分解重新生成
在强酸性条件下分解重新生成 。
。(1)操作①的名称为
(2)溶液②中所含主要溶质为LiCl、
 ,请写出
,请写出 和盐酸反应的化学方程式中LiCoO2和HCl的最简系数比(提示:产物有氯气)
和盐酸反应的化学方程式中LiCoO2和HCl的最简系数比(提示:产物有氯气)(3)将溶液中的
 转化为
转化为 沉淀也是常用的沉钴方案。在此流程中选用草酸铵而不用碳酸盐的原因是
沉淀也是常用的沉钴方案。在此流程中选用草酸铵而不用碳酸盐的原因是(4)为证明操作④获得的
 沉淀表面的杂质已被洗涤干净,所需进行的实验操作为:取少量的最后一次洗涤液于试管中,加入
沉淀表面的杂质已被洗涤干净,所需进行的实验操作为:取少量的最后一次洗涤液于试管中,加入(5)取3.66 g
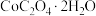 (相对分子质量183)隔绝空气加热,在205℃条件下反应完全后,剩余固体质量为2.94 g,此时分解产生的气体为
(相对分子质量183)隔绝空气加热,在205℃条件下反应完全后,剩余固体质量为2.94 g,此时分解产生的气体为 ,
,
(6)某同学设计如图装置测定
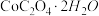 晶体中结晶水的含量以检验样品的纯度。下列有关说法不正确的是
晶体中结晶水的含量以检验样品的纯度。下列有关说法不正确的是
A. B中应装入浓硫酸,目的是除去水蒸气
B. 利用干燥管前后质量差可计算出结晶水的含量
C. 图中半透膜可让气体通过又可防止固体粉末进入导管
D. 反应结束后,应先停止加热,一段时间后再停止通空气
(7)溶液④中,铁元素主要以
(8)
 溶液在工业上常用于电路板的蚀刻,发生的反应为
溶液在工业上常用于电路板的蚀刻,发生的反应为 。某同学向含有
。某同学向含有 、
、 和
和 三种溶质的溶液中加入一定量的铁粉,若反应完成后有固体剩余,则固体的成分可能为
三种溶质的溶液中加入一定量的铁粉,若反应完成后有固体剩余,则固体的成分可能为A. Fe B. Fe和Zn C. Fe和Cu D. Cu和Zn
(9)某a g混合粉末中含有铁、石墨、硫和碳酸氢铵,在空气中充分加热至完全反应后,重新称量剩余固体质量,仍为a g,则混合物中铁的质量分数为
您最近一年使用:0次
解题方法
2 . 二氧化氯是高效、低毒的消毒剂。已知: 是极易溶于水的气体,实验室制备及性质探究装置如下图所示。回答下列问题:
是极易溶于水的气体,实验室制备及性质探究装置如下图所示。回答下列问题:
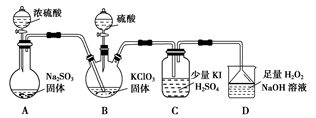
(1)装置 用于制备
用于制备 ,同时还生成一种酸式盐,该反应的化学方程式为
,同时还生成一种酸式盐,该反应的化学方程式为___________ 。装置 中滴有几滴淀粉溶液,反应时有蓝色出现,淀粉的作用是
中滴有几滴淀粉溶液,反应时有蓝色出现,淀粉的作用是___________ 。
(2) 静置的导管靠近而不接触液面,其目的是
静置的导管靠近而不接触液面,其目的是___________ 。
(3)装置 用于吸收尾气,若反应的氧化产物是一种单质,且氧化剂与氧化产物的物质的量之比是
用于吸收尾气,若反应的氧化产物是一种单质,且氧化剂与氧化产物的物质的量之比是 ,则还原产物的化学式是
,则还原产物的化学式是___________ 。
(4)若将 装置中的溶液改为
装置中的溶液改为 溶液,通入
溶液,通入 后溶液无明显现象。由此可以产生两种假设:
后溶液无明显现象。由此可以产生两种假设:
假设a: 与
与 不反应。假设b:
不反应。假设b: 与
与 反应。
反应。
①你认为哪种假设正确,阐述原因:___________ 。
②请设计实验证明你的假设(仅用离子方程式表示):___________ 。
 是极易溶于水的气体,实验室制备及性质探究装置如下图所示。回答下列问题:
是极易溶于水的气体,实验室制备及性质探究装置如下图所示。回答下列问题:
(1)装置
 用于制备
用于制备 ,同时还生成一种酸式盐,该反应的化学方程式为
,同时还生成一种酸式盐,该反应的化学方程式为 中滴有几滴淀粉溶液,反应时有蓝色出现,淀粉的作用是
中滴有几滴淀粉溶液,反应时有蓝色出现,淀粉的作用是(2)
 静置的导管靠近而不接触液面,其目的是
静置的导管靠近而不接触液面,其目的是(3)装置
 用于吸收尾气,若反应的氧化产物是一种单质,且氧化剂与氧化产物的物质的量之比是
用于吸收尾气,若反应的氧化产物是一种单质,且氧化剂与氧化产物的物质的量之比是 ,则还原产物的化学式是
,则还原产物的化学式是(4)若将
 装置中的溶液改为
装置中的溶液改为 溶液,通入
溶液,通入 后溶液无明显现象。由此可以产生两种假设:
后溶液无明显现象。由此可以产生两种假设:假设a:
 与
与 不反应。假设b:
不反应。假设b: 与
与 反应。
反应。①你认为哪种假设正确,阐述原因:
②请设计实验证明你的假设(仅用离子方程式表示):
您最近一年使用:0次
2021-09-08更新
|
120次组卷
|
3卷引用:山东省夏津第一中学2022届高三上学期9月入学考试化学试题
名校
解题方法
3 . 从干海带中提取碘的实验流程如下:
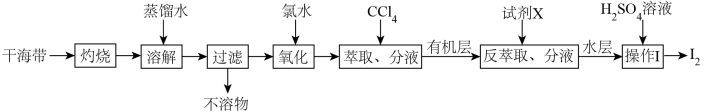
| A.氧化步骤中氯水可用过氧化氢代替 |
B.试剂X可以为 ,反萃取的离子方程式为: ,反萃取的离子方程式为: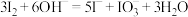 |
C. 可循环利用以有效提高干海带提碘的产率 可循环利用以有效提高干海带提碘的产率 |
| D.操作Ⅰ要用到普通漏斗、烧杯和玻璃棒 |
您最近一年使用:0次
2024-01-28更新
|
573次组卷
|
6卷引用:山东省烟台市莱州市第一中学2023-2024学年高一下学期开学化学试题
解题方法
4 . 在实验室中,由含硒废料(主要含S、Se、 、CuO、ZnO、
、CuO、ZnO、 等)制取硒的流程如图:
等)制取硒的流程如图:
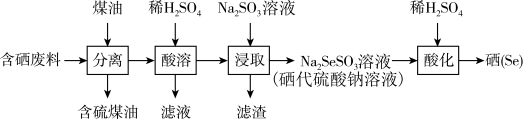
下列说法错误的是
 、CuO、ZnO、
、CuO、ZnO、 等)制取硒的流程如图:
等)制取硒的流程如图:
下列说法错误的是
| A.“分离”时得到含硫煤油的方法是分液 |
| B.“酸溶”操作的目的是除去废料中的金属氧化物 |
C.“浸取”后滤渣的主要成分是 |
D.“酸化”时发生反应的离子方程式: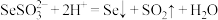 |
您最近一年使用:0次
名校
解题方法
5 . 查阅资料知:Bi位于周期表的第ⅤA族, 是难溶于水的盐,有强氧化性;溶液中
是难溶于水的盐,有强氧化性;溶液中 较稳定,无色;某实验小组探究含锰物质的化学性质,有关实验操作和现象如下:
较稳定,无色;某实验小组探究含锰物质的化学性质,有关实验操作和现象如下:
①向稀硫酸酸化的 溶液中加入适量
溶液中加入适量 ,溶液变为紫红色
,溶液变为紫红色
②继续滴加适量的 ,溶液紫红色恰好褪去,并有无色气泡产生
,溶液紫红色恰好褪去,并有无色气泡产生
③再向反应液中加入适量的 固体恰好反应完全,溶液又变为紫红色
固体恰好反应完全,溶液又变为紫红色
发生的反应为: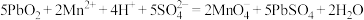
④继续向③的反应液中滴加浓盐酸,有黄绿色气体生成
下列有关说法正确的是
 是难溶于水的盐,有强氧化性;溶液中
是难溶于水的盐,有强氧化性;溶液中 较稳定,无色;某实验小组探究含锰物质的化学性质,有关实验操作和现象如下:
较稳定,无色;某实验小组探究含锰物质的化学性质,有关实验操作和现象如下:①向稀硫酸酸化的
 溶液中加入适量
溶液中加入适量 ,溶液变为紫红色
,溶液变为紫红色②继续滴加适量的
 ,溶液紫红色恰好褪去,并有无色气泡产生
,溶液紫红色恰好褪去,并有无色气泡产生③再向反应液中加入适量的
 固体恰好反应完全,溶液又变为紫红色
固体恰好反应完全,溶液又变为紫红色发生的反应为:
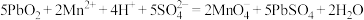
④继续向③的反应液中滴加浓盐酸,有黄绿色气体生成
下列有关说法正确的是
A. 可与浓盐酸发生反应生成相应的最高价含氧酸 可与浓盐酸发生反应生成相应的最高价含氧酸 |
B.根据上述现象可知氧化性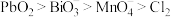 |
C.分别用 和 和 氧化 氧化 制取 制取 ,二者转移电子数不同 ,二者转移电子数不同 |
D.①中发生的反应方程式为: |
您最近一年使用:0次
2023-03-10更新
|
729次组卷
|
9卷引用:山东省济宁市2022-2023学年高一下学期开学考试(上学期期末)化学试题
山东省济宁市2022-2023学年高一下学期开学考试(上学期期末)化学试题山东省济宁市2022-2023学年高一上学期期末考试化学试题山东省济宁市2022-2023学年高一上学期2月期末化学试题山东省青岛市即墨区第一中学2023-2024学年高一上学期第二次阶段检测化学试题山西省晋城市第一中学校2022-2023学年高一下学期4月期中考试化学试题湖北省武昌实验中学2023-2024学年高一上学期10月月考化学试题(已下线)专项02 离子反应和氧化还原反应的应用-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)江西省三市八校联盟2023-2024学年高一上学期期中联考化学试卷广西柳州高级中学2023-2024学年高一上学期寒假月考化学试卷3
解题方法
6 . 回答下列问题:
(1)2022年3月13日,永恒的“微火”在万众瞩目中缓缓熄灭,为北京冬奥画上圆满的句号。北京作为双奥之城为世界奉献了一届简约、精彩、卓越的冬奥盛会。
①“微火”不微,照亮世界。奥运火炬“飞扬”的外壳是由聚硅氮烷树脂和碳纤维材料制成,能经受住1200℃的高温。“飞扬”火炬外壳属于____ (填“金属材料”“有机高分子材料”“复合材料”之一)。

②科技“战衣”,助力中国速度。短道速滑“战衣”所用面料能承受碰撞中冰刀的切割,它由聚乙烯(化学式为 )、聚氨基甲酸酯等化学纤维复合而成。在聚乙烯中,碳元素和氢元素的质量比为
)、聚氨基甲酸酯等化学纤维复合而成。在聚乙烯中,碳元素和氢元素的质量比为_____ (填最简整数比)。
③“氢”车上阵,助力绿色冬奥。氢氧燃料电池就像冬奥大巴车的“心脏”,在这种电池中,氢气和氧气通过化学反应生成水。下列有关说法中,不合理的是____ (填选项序号之一)。

A.H2和O2发生了氧化还原反应
B.该种电池的应用有利于环保
C.该电池的使用过程中,电能转化为化学能
(2)我国著名化学家侯德榜先生创立了侯氏制碱法,促进了世界制碱技术的发展。其生产过程中有下列反应:
NaCl+NH3+CO2+H2O=NaHCO3+NH4C1
2NaHCO3 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
Na2CO3和NaCl的溶解度曲线如图1所示,试回答下列问题:

①将t1℃时相同质量的Na2CO3饱和溶液和NaCl饱和溶液分别升温至t2℃,此时所得两溶液的溶质质量分数相比较是____ 。(选填“前者大”“后者大”“相等”之一)。
②t3℃时,将5 g Na2CO3放入试管中,加入10 g水,充分溶解,所得溶液的质量是____ g;然后将试管放入盛有水的烧杯中(如图2所示),再取适量硝酸铵固体放入烧杯内的水中,用玻璃棒搅拌溶解,此时可观察到试管底部固体____ (填“增加”“减少”“无变化”之一)。

③氨盐水比食盐水更容易吸收二氧化碳的原因是_____ 。
④生活在盐碱湖附近的人们有一句谚语“夏天晒盐,冬天捞碱”,请结合溶解度曲线,从化学角度说明这句谚语的原理:____ 。
(1)2022年3月13日,永恒的“微火”在万众瞩目中缓缓熄灭,为北京冬奥画上圆满的句号。北京作为双奥之城为世界奉献了一届简约、精彩、卓越的冬奥盛会。
①“微火”不微,照亮世界。奥运火炬“飞扬”的外壳是由聚硅氮烷树脂和碳纤维材料制成,能经受住1200℃的高温。“飞扬”火炬外壳属于

②科技“战衣”,助力中国速度。短道速滑“战衣”所用面料能承受碰撞中冰刀的切割,它由聚乙烯(化学式为
 )、聚氨基甲酸酯等化学纤维复合而成。在聚乙烯中,碳元素和氢元素的质量比为
)、聚氨基甲酸酯等化学纤维复合而成。在聚乙烯中,碳元素和氢元素的质量比为③“氢”车上阵,助力绿色冬奥。氢氧燃料电池就像冬奥大巴车的“心脏”,在这种电池中,氢气和氧气通过化学反应生成水。下列有关说法中,不合理的是

A.H2和O2发生了氧化还原反应
B.该种电池的应用有利于环保
C.该电池的使用过程中,电能转化为化学能
(2)我国著名化学家侯德榜先生创立了侯氏制碱法,促进了世界制碱技术的发展。其生产过程中有下列反应:
NaCl+NH3+CO2+H2O=NaHCO3+NH4C1
2NaHCO3
 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2ONa2CO3和NaCl的溶解度曲线如图1所示,试回答下列问题:

①将t1℃时相同质量的Na2CO3饱和溶液和NaCl饱和溶液分别升温至t2℃,此时所得两溶液的溶质质量分数相比较是
②t3℃时,将5 g Na2CO3放入试管中,加入10 g水,充分溶解,所得溶液的质量是

③氨盐水比食盐水更容易吸收二氧化碳的原因是
④生活在盐碱湖附近的人们有一句谚语“夏天晒盐,冬天捞碱”,请结合溶解度曲线,从化学角度说明这句谚语的原理:
您最近一年使用:0次
名校
7 . 一种利用有机胺(TBA)联合生产碳酸氢钠和二氯乙烷的工艺流程如图所示。
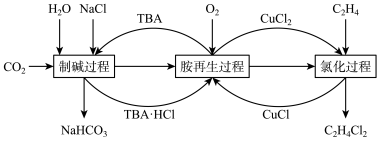
下列说法错误的是

下列说法错误的是
| A.“制碱过程”后通过加热蒸发结晶得到NaHCO3 |
| B.该工艺原子利用率100% |
| C.“氯化过程”每生成lmolC2H4Cl2,总反应中消耗0.5molO2 |
| D.“胺再生过程”反应为4CuCl+O2+4TBA·HCl=4CuCl2+4TBA+2H2O |
您最近一年使用:0次
2022-04-27更新
|
1439次组卷
|
7卷引用:山东省枣庄市第三中学2022-2023学年高三上学期开学考试化学试题
名校
8 . 某工厂废液中含有大量的 、
、 及少量的
及少量的 、
、 ,利用该废液制备
,利用该废液制备 的流程如下:
的流程如下:
称取m g产品溶解于大量较浓盐酸中,在 氛围下用适量还原剂恰好将
氛围下用适量还原剂恰好将 还原为
还原为 ,用
,用 的
的 标准液滴定,终点时消耗标准液V mL。
标准液滴定,终点时消耗标准液V mL。
已知:①氧化性 ;
;
②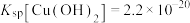 ,
, ;
;
③当溶液中离子浓度小于等于 时,可认为该离子沉淀完全。
时,可认为该离子沉淀完全。
根据上述产品含量测定的实验原理,下列说法错误的是
 、
、 及少量的
及少量的 、
、 ,利用该废液制备
,利用该废液制备 的流程如下:
的流程如下: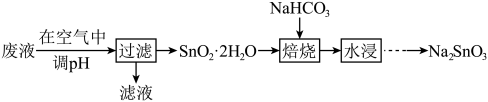
称取m g产品溶解于大量较浓盐酸中,在
 氛围下用适量还原剂恰好将
氛围下用适量还原剂恰好将 还原为
还原为 ,用
,用 的
的 标准液滴定,终点时消耗标准液V mL。
标准液滴定,终点时消耗标准液V mL。已知:①氧化性
 ;
;②
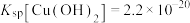 ,
, ;
;③当溶液中离子浓度小于等于
 时,可认为该离子沉淀完全。
时,可认为该离子沉淀完全。根据上述产品含量测定的实验原理,下列说法错误的是
A.实验室配制 溶液时需加入盐酸和锡粉 溶液时需加入盐酸和锡粉 |
| B.若加入的还原剂不足,则测定结果偏小 |
C.滴定时选用淀粉作指示剂,产生 的离子方程式: 的离子方程式: |
D.则产品中Sn的质量分数为 % % |
您最近一年使用:0次
名校
解题方法
9 .  (钴酸锂)常用作锂离子电池的正极材料。以某海水(含浓度较大的LiCl、少量
(钴酸锂)常用作锂离子电池的正极材料。以某海水(含浓度较大的LiCl、少量 、
、 、
、 等)为原料制备钴酸锂的一种流程如下:
等)为原料制备钴酸锂的一种流程如下:
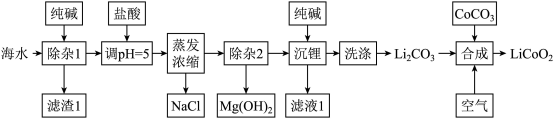
已知:① 的溶解度随温度升高而降低;
的溶解度随温度升高而降低;
②常温下,几种难溶物质的溶度积数据如下:
下列说法错误的是
 (钴酸锂)常用作锂离子电池的正极材料。以某海水(含浓度较大的LiCl、少量
(钴酸锂)常用作锂离子电池的正极材料。以某海水(含浓度较大的LiCl、少量 、
、 、
、 等)为原料制备钴酸锂的一种流程如下:
等)为原料制备钴酸锂的一种流程如下:
已知:①
 的溶解度随温度升高而降低;
的溶解度随温度升高而降低;②常温下,几种难溶物质的溶度积数据如下:
| 物质 |  |  |  |  |  |
 | 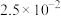 | 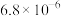 | 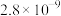 | 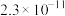 |  |
A.高温时“合成”反应的化学方程式为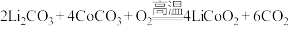 |
B.滤渣1主要成分有 、 、 |
C.“洗涤” 时最好选用冷水 时最好选用冷水 |
D.“除杂2”调pH=12时,溶液中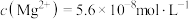 |
您最近一年使用:0次
2023-02-22更新
|
547次组卷
|
2卷引用:山东省菏泽市东明县第一中学2023-2024学年高二下学期开学化学试题
解题方法
10 . 用废铁屑(表面有油污)制备磁性胶体粒子,制取过程如下:
废铁屑 溶液A
溶液A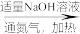 Fe3O4(胶体粒子)
Fe3O4(胶体粒子)
下列说法不正确的是
废铁屑
 溶液A
溶液A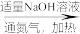 Fe3O4(胶体粒子)
Fe3O4(胶体粒子)下列说法不正确的是
| A.加入稀硫酸是为了使铁溶解生成硫酸铁 |
| B.通入N2是防止空气中的O2氧化Fe2+ |
| C.加适量的H2O2是为了将部分Fe2+氧化为Fe3+,涉及反应:H2O2+2Fe2++2H+ = 2Fe3++2H2O |
| D.溶液A中Fe2+和Fe3+的浓度比为2∶1 |
您最近一年使用:0次



