名校
解题方法
1 . 绿氢由于生产过程中100%绿色的特点备受青睐,发展前景最为广阔,光催化制氢机理研究取得新进展。如图是通过光催化循环在较低温度下由水分解制备氢气的反应原理。下列有关说法错误的是
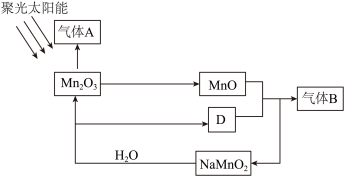
| A.该制氢过程中,消耗了水和太阳能,含锰化合物均为中间产物 |
| B.该制氢过程解决了气体A、B难分离的问题 |
| C.制氢过程中涉及Mn元素转化的反应不都是氧化还原反应 |
D.生成气体B的反应方程式为 |
您最近一年使用:0次
名校
解题方法
2 . 工业上采用酸性高浓度含砷废水主要以亚砷酸(H3AsO3)形式存在,提取As2O3的工艺流程如下:
Ⅰ.As2S3与过量的 存在以下反应:
存在以下反应: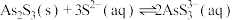 ;
;
Ⅱ.亚砷酸盐的溶解性大于相应砷酸盐。
回答下列问题:
(1)沉砷中FeSO4的作用是___________ :
(2)H2O2的作用是___________ ;滤渣I中含有FeAsO4、 、
、 和
和___________ (填化学式)。
(3)加生石灰和过氧化氢过程中,也可将砷元素转化为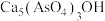 沉淀,发生的主要反应有:
沉淀,发生的主要反应有:
A.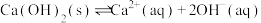

B.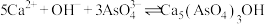

资料表明:“沉砷”的最佳温度是85℃,温度高于85℃,随温度升高沉淀率下降,从平衡移动角度分析其原因是___________ 。
(4)调节pH=0时,由Na3AsO4制备As2O3的离子方程式为___________ 。
(5)常温下,用NaOH溶液滴定H3AsO3时,各种微粒的物质的量分数随pH的变化曲线如图所示:___________ 。
(6)已知 的
的 ,含砷污染物允许排放标准为不大于0.5mg⋅L-1。若低浓度含砷废水(假设砷均以
,含砷污染物允许排放标准为不大于0.5mg⋅L-1。若低浓度含砷废水(假设砷均以 形式存在)中Fe3+的浓度为
形式存在)中Fe3+的浓度为 ,则低浓度含砷废水中
,则低浓度含砷废水中 的浓度为
的浓度为___________ mg⋅L-1,___________ (填“符合”或“不符合”)排放标准。

Ⅰ.As2S3与过量的
 存在以下反应:
存在以下反应: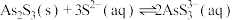 ;
;Ⅱ.亚砷酸盐的溶解性大于相应砷酸盐。
回答下列问题:
(1)沉砷中FeSO4的作用是
(2)H2O2的作用是
 、
、 和
和(3)加生石灰和过氧化氢过程中,也可将砷元素转化为
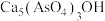 沉淀,发生的主要反应有:
沉淀,发生的主要反应有:A.
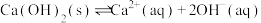

B.
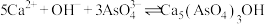

资料表明:“沉砷”的最佳温度是85℃,温度高于85℃,随温度升高沉淀率下降,从平衡移动角度分析其原因是
(4)调节pH=0时,由Na3AsO4制备As2O3的离子方程式为
(5)常温下,用NaOH溶液滴定H3AsO3时,各种微粒的物质的量分数随pH的变化曲线如图所示:

(6)已知
 的
的 ,含砷污染物允许排放标准为不大于0.5mg⋅L-1。若低浓度含砷废水(假设砷均以
,含砷污染物允许排放标准为不大于0.5mg⋅L-1。若低浓度含砷废水(假设砷均以 形式存在)中Fe3+的浓度为
形式存在)中Fe3+的浓度为 ,则低浓度含砷废水中
,则低浓度含砷废水中 的浓度为
的浓度为
您最近一年使用:0次
解题方法
3 . 金属钼在工业和国防建设中有重要的作用,其化合物钼酸钠晶体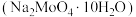 可制造金属缓释剂。由钼精矿(主要成分为
可制造金属缓释剂。由钼精矿(主要成分为 ,含有少量不反应的杂质)制备钼及钼酸钠晶体的工艺流程如图所示,回答下列问题:
,含有少量不反应的杂质)制备钼及钼酸钠晶体的工艺流程如图所示,回答下列问题:____________ 。
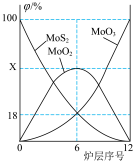
(2)焙烧过程中采用“多层逆流(空气从炉底进入,钼精矿经粉碎后从炉顶进入)焙烧”,下图为焙烧时各炉层固体物料的物质的量百分数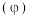 。
。____________ ;“多层逆流焙烧”的优点是_______________ ;
②某些生产工艺在焙烧时加入碳酸钙会更环保,其原因是________ (用化学方程式表示);
(3)碱浸时发生反应的离子方程式为_____________________ ;
(4)已知钼酸钠的溶解度曲线如图所示,要获得钼酸钠晶体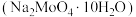 的操作2为
的操作2为________ 、_________ 、过滤、洗涤、干燥; 生成,用固体
生成,用固体 除去.在除
除去.在除 前测定碱浸液中
前测定碱浸液中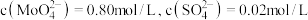 ,当
,当 开始沉淀时,
开始沉淀时, 的去除率为
的去除率为_____ %(保留整数)[已知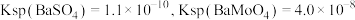 ,溶液体积变化忽略不计]。
,溶液体积变化忽略不计]。
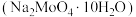 可制造金属缓释剂。由钼精矿(主要成分为
可制造金属缓释剂。由钼精矿(主要成分为 ,含有少量不反应的杂质)制备钼及钼酸钠晶体的工艺流程如图所示,回答下列问题:
,含有少量不反应的杂质)制备钼及钼酸钠晶体的工艺流程如图所示,回答下列问题: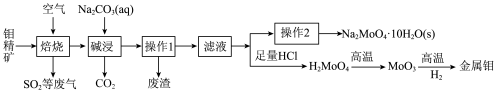
(2)焙烧过程中采用“多层逆流(空气从炉底进入,钼精矿经粉碎后从炉顶进入)焙烧”,下图为焙烧时各炉层固体物料的物质的量百分数
 。
。
②某些生产工艺在焙烧时加入碳酸钙会更环保,其原因是
(3)碱浸时发生反应的离子方程式为
(4)已知钼酸钠的溶解度曲线如图所示,要获得钼酸钠晶体
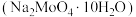 的操作2为
的操作2为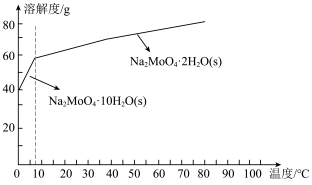
 生成,用固体
生成,用固体 除去.在除
除去.在除 前测定碱浸液中
前测定碱浸液中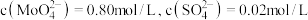 ,当
,当 开始沉淀时,
开始沉淀时, 的去除率为
的去除率为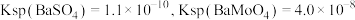 ,溶液体积变化忽略不计]。
,溶液体积变化忽略不计]。
您最近一年使用:0次
名校
解题方法
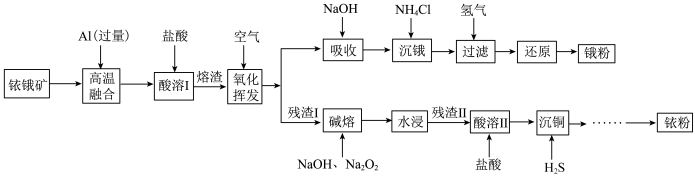
4 . 铱(77Ir)和锇(76Os)属于铂族金属,与金、银合称贵重金属,可以用于电气、精密仪表、催化剂等领域。铱锇矿的主要成分有Ir、Os、Ir2O3、OsO2,还含有CuO和SiO2等杂质,从铱锇矿中提取铱和锇的流程如下:
回答下列问题:
(1)“酸溶I”的目的是___________ ;酸溶I后溶渣的主要成分除Ir、Os外,还有___________ (填化学式)。
(2)“氧化挥发”是将溶渣置于300~800℃的管式炉内,通入空气氧化。再用NaOH溶液吸收OsO4生成Na2OsO4,该反应的离子方程式为___________ 。
(3)“沉锇”时,NH4Cl与Na2OsO4发生反应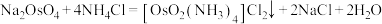 ,生成的锇盐要立即过滤,滤饼要经无水乙醇多次洗涤,用无水乙醇洗涤的优点是
,生成的锇盐要立即过滤,滤饼要经无水乙醇多次洗涤,用无水乙醇洗涤的优点是___________ 。
(4)“碱熔”时,“残渣I”中的Ir与Na2O2反应生成IrO2·nNa2O和O2,该反应的化学方程式为___________ 。
(5)“沉铜”过程中,当通入H2S达到饱和时测得溶液的pH=1,此时溶液中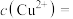
___________ mol/L。[已知:25℃,H2S溶于水形成饱和溶液时, ;H2S的电离常数
;H2S的电离常数 ,
, ;
;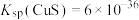 ]
]
(6)化合物 IrO2的四方晶格结构如图所示,其棱边夹角均为90°。已知IrO2晶体密度为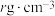 ,设NA为阿伏加德罗常数的值,则IrO2的摩尔质量为
,设NA为阿伏加德罗常数的值,则IrO2的摩尔质量为___________ (用代数式表示)g/mol。
回答下列问题:
(1)“酸溶I”的目的是
(2)“氧化挥发”是将溶渣置于300~800℃的管式炉内,通入空气氧化。再用NaOH溶液吸收OsO4生成Na2OsO4,该反应的离子方程式为
(3)“沉锇”时,NH4Cl与Na2OsO4发生反应
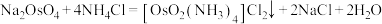 ,生成的锇盐要立即过滤,滤饼要经无水乙醇多次洗涤,用无水乙醇洗涤的优点是
,生成的锇盐要立即过滤,滤饼要经无水乙醇多次洗涤,用无水乙醇洗涤的优点是(4)“碱熔”时,“残渣I”中的Ir与Na2O2反应生成IrO2·nNa2O和O2,该反应的化学方程式为
(5)“沉铜”过程中,当通入H2S达到饱和时测得溶液的pH=1,此时溶液中
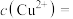
 ;H2S的电离常数
;H2S的电离常数 ,
, ;
;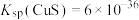 ]
](6)化合物 IrO2的四方晶格结构如图所示,其棱边夹角均为90°。已知IrO2晶体密度为
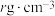 ,设NA为阿伏加德罗常数的值,则IrO2的摩尔质量为
,设NA为阿伏加德罗常数的值,则IrO2的摩尔质量为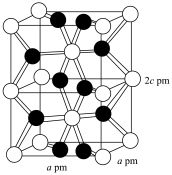
您最近一年使用:0次
2024-05-21更新
|
266次组卷
|
3卷引用:辽宁省协作校2023-2024学年高三下学期三模化学试题
名校
解题方法
5 . 宏观辨识与微观探析是化学学科核心素养之一、下列反应方程式书写正确的是
A.将少量 通入 通入 溶液中: 溶液中: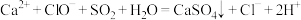 |
B.向甲醛溶液中加入足量的银氨溶液并加热: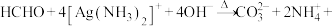  |
C.向摩尔盐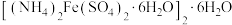 溶液中加入NaOH溶液至 溶液中加入NaOH溶液至 刚好反应完全: 刚好反应完全: |
D.往酸性 溶液中加入难溶于水的 溶液中加入难溶于水的 固体,溶液出现紫红色: 固体,溶液出现紫红色: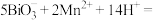 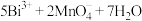 |
您最近一年使用:0次
2024-05-09更新
|
381次组卷
|
4卷引用:辽宁省凌源市2024届高三下学期第三次模拟考试化学试卷
辽宁省凌源市2024届高三下学期第三次模拟考试化学试卷湖北省十堰市2023-2024学年高三下学期4月调研考试化学试题2024届南昌市第十九中学高三下学期模拟预测化学试题(已下线)第02讲 离子反应、离子方程式(讲义)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
解题方法
6 . 铊(Tl)广泛应用于电子、军工、航天等领域。一种从铅精矿焙烧产生的富铊灰(主要成分为PbO、ZnO、FeO、Fe2O3、Tl2O)中回收铊的工艺流程如图所示:
①Tl+易被氧化为Tl3+
②在氯化物-硫酸水溶液中,Tl元素以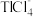 形式存在
形式存在
③萃取过程的反应原理为:H++CH3CONR2+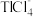
 [CH3CONR2H]TlCl4
[CH3CONR2H]TlCl4
④常温下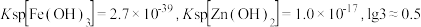
请回答下列问题:
(1)铊(81Tl)与铝同主族,基态 原子的价电子轨道表示式为
原子的价电子轨道表示式为________ 。
(2)“浸取Ⅰ”中Tl2O发生反应的化学方程式为________ 。
(3)滤渣的主要成分为________ 。
(4)常温下,向“萃取分液”后的水相中加入NaOH溶液,调pH回收铁。已知水相中c(Zn2+)=0.1mol/L,控制pH范围为_______ (已知当溶液中离子浓度小于10-5mol/L时,通常认为该离子沉淀完全,结果保留一位小数)。
(5)请从化学平衡的角度解释“反萃取”过程中加入CH3COONH4溶液的原因________ 。
(6)“还原氯化沉淀”中反应的离子方程式为_______ 。
(7)铊镉合金是原子能工业重要材料,其一种立方晶胞结构如图所示,已知该铊镉合金密度为 ,设
,设 为阿伏加德罗常数的值,则铊原子和镉原子之间的最短距离d=
为阿伏加德罗常数的值,则铊原子和镉原子之间的最短距离d=_____ nm(用含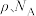 的代数式表示)。
的代数式表示)。
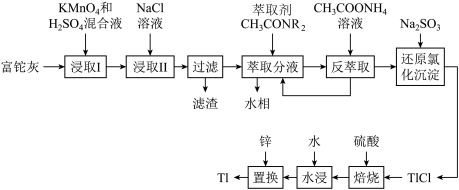
①Tl+易被氧化为Tl3+
②在氯化物-硫酸水溶液中,Tl元素以
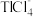 形式存在
形式存在③萃取过程的反应原理为:H++CH3CONR2+
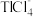
 [CH3CONR2H]TlCl4
[CH3CONR2H]TlCl4 ④常温下
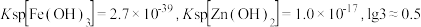
请回答下列问题:
(1)铊(81Tl)与铝同主族,基态
 原子的价电子轨道表示式为
原子的价电子轨道表示式为(2)“浸取Ⅰ”中Tl2O发生反应的化学方程式为
(3)滤渣的主要成分为
(4)常温下,向“萃取分液”后的水相中加入NaOH溶液,调pH回收铁。已知水相中c(Zn2+)=0.1mol/L,控制pH范围为
(5)请从化学平衡的角度解释“反萃取”过程中加入CH3COONH4溶液的原因
(6)“还原氯化沉淀”中反应的离子方程式为
(7)铊镉合金是原子能工业重要材料,其一种立方晶胞结构如图所示,已知该铊镉合金密度为
 ,设
,设 为阿伏加德罗常数的值,则铊原子和镉原子之间的最短距离d=
为阿伏加德罗常数的值,则铊原子和镉原子之间的最短距离d=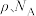 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
7 . 碲被誉为金属性最强的非金属,某科研小组从碲渣(主要含有Cu2Te )中提取粗碲的工艺流程如图所示。下列有关说法错误的是
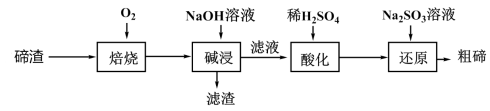
| A.“焙烧”后铜以Cu2O形式存在 |
| B.“碱浸”后过滤用到的主要仪器有:烧杯、漏斗、玻璃棒 |
| C.“酸化”后生成Te(SO4)2 |
| D.“还原”后,溶液的酸性减弱 |
您最近一年使用:0次
名校
解题方法
8 . 工业上一种利用废旧三元锂离子电池正极材料(主要成分为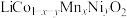 ,还含有铝箔、炭黑、有机粘合剂等)综合回收钴、锰、镍、锂的工艺流程如下图所示:
,还含有铝箔、炭黑、有机粘合剂等)综合回收钴、锰、镍、锂的工艺流程如下图所示: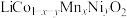 的基本结构单元如图所示,则据此计算
的基本结构单元如图所示,则据此计算
___________ ,
___________ 。___________ 。
(3)“碱浸”后滤液中大量存在的阴离子为___________ 和___________ 。
(4)已知: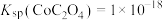 ,
,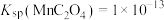 ,
,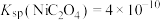 。若“酸浸”后溶液中
。若“酸浸”后溶液中 、
、 、
、 浓度均为0.1mol/L,理论计算欲使
浓度均为0.1mol/L,理论计算欲使 完全沉淀(离子浓度小于
完全沉淀(离子浓度小于 )而不沉淀
)而不沉淀 、
、 ,需调节
,需调节___________ mol/L<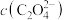 <
<___________ mol/L;实际“沉钴”时,在加入 之后
之后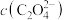 往往超出上述范围,因而须先加入一定量氨水,推测所加氨水的作用为
往往超出上述范围,因而须先加入一定量氨水,推测所加氨水的作用为___________ 。
(5)“沉锰”过程中加入 溶液后,溶液先变为紫红色,一段时间后紫红色又褪去,则溶液变为紫红色的原因为
溶液后,溶液先变为紫红色,一段时间后紫红色又褪去,则溶液变为紫红色的原因为___________ 。[用离子方程式表示,Mn(Ⅱ)写作 即可]。
即可]。
(6)“沉镍”过程中加入 溶液不能过量,原因为
溶液不能过量,原因为___________ 。
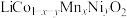 ,还含有铝箔、炭黑、有机粘合剂等)综合回收钴、锰、镍、锂的工艺流程如下图所示:
,还含有铝箔、炭黑、有机粘合剂等)综合回收钴、锰、镍、锂的工艺流程如下图所示: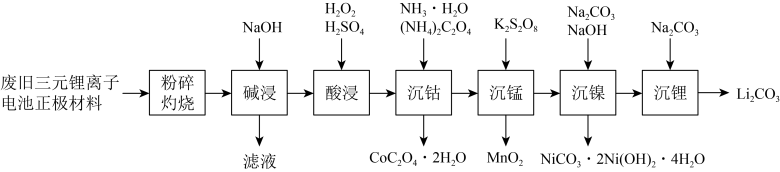
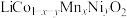 的基本结构单元如图所示,则据此计算
的基本结构单元如图所示,则据此计算

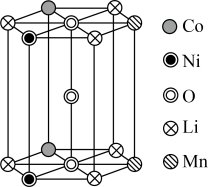
(3)“碱浸”后滤液中大量存在的阴离子为
(4)已知:
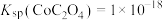 ,
,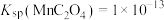 ,
,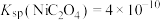 。若“酸浸”后溶液中
。若“酸浸”后溶液中 、
、 、
、 浓度均为0.1mol/L,理论计算欲使
浓度均为0.1mol/L,理论计算欲使 完全沉淀(离子浓度小于
完全沉淀(离子浓度小于 )而不沉淀
)而不沉淀 、
、 ,需调节
,需调节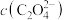 <
< 之后
之后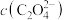 往往超出上述范围,因而须先加入一定量氨水,推测所加氨水的作用为
往往超出上述范围,因而须先加入一定量氨水,推测所加氨水的作用为(5)“沉锰”过程中加入
 溶液后,溶液先变为紫红色,一段时间后紫红色又褪去,则溶液变为紫红色的原因为
溶液后,溶液先变为紫红色,一段时间后紫红色又褪去,则溶液变为紫红色的原因为 即可]。
即可]。(6)“沉镍”过程中加入
 溶液不能过量,原因为
溶液不能过量,原因为
您最近一年使用:0次
名校
9 . 《开宝本草》记载“取钢煅作叶如笏或团,平面磨错令光净,以盐水洒之,于醋瓮中阴处埋之一百日,铁上衣生,铁华成矣”。铁华粉[主要成分为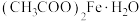 ]可用如下方法检测。下列相关说法不正确的是
]可用如下方法检测。下列相关说法不正确的是
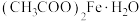 ]可用如下方法检测。下列相关说法不正确的是
]可用如下方法检测。下列相关说法不正确的是
A.制备铁华粉的主要反应为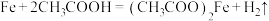 |
B.气体X为 |
| C.铁华粉中含铁单质 |
D.由上述实验可知, 结合 结合 的能力大于 的能力大于 |
您最近一年使用:0次
名校
10 . 能正确表示下列反应的离子方程式是
A.侯氏制碱法的反应原理: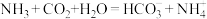 |
B.向酸性KMnO4溶液中滴入H2O2溶液: |
C.白色固体AgCl加入氨水中得到无色溶液: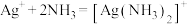 |
D.向NaHSO3溶液滴入酸性Ba(NO3)2溶液产生白色沉淀: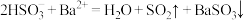 |
您最近一年使用:0次
2024-04-27更新
|
486次组卷
|
2卷引用:2024年辽宁省抚顺市普通高中高三下学期模拟考试化学试卷



