解题方法
1 . 下列过程对应的离子反应方程式书写正确的是
A. 溶液与过量澄清石灰水混合: 溶液与过量澄清石灰水混合: |
B.明矾溶液与过量氨水混合: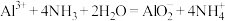 |
C.用 溶液吸收少量 溶液吸收少量 : : |
D.向水垢中滴加足量醋酸: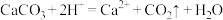 |
您最近一年使用:0次
2023-02-24更新
|
385次组卷
|
2卷引用:辽宁省葫芦岛市2023届高三下学期学业质量监测化学试题
名校
2 . 钪是一种稀土金属元素,在国防、航天、核能等领域具有重要应用。工业上利用固体废料“赤泥”(含FeO、Fe2O3、SiO2、Sc2O3、TiO2等)回收Sc2O3的工艺流程如图。

已知:TiO2难溶于盐酸;Ksp[Fe(OH)3]=1.0×10-38。
回答下列问题:
(1)为提高“酸浸”速率,对“赤泥”的处理方式为_____ ;滤渣I的主要成分是_____ (填化学式)。
(2)“氧化”时加入足量H2O2的目的是______ ;氧化后溶液中Fe3+浓度为0.001mol•L-1,常温下“调pH”时,若控制pH=3,则Fe3+的去除率为______ (忽略调pH前后溶液的体积变化)。
(3)已知25℃时,Kh1(C2O )=a,Kh2(C2O
)=a,Kh2(C2O )=b,Ksp[Sc2(C2O4)3]=c。“沉钪”时,发生反应:2Sc3++3H2C2O4
)=b,Ksp[Sc2(C2O4)3]=c。“沉钪”时,发生反应:2Sc3++3H2C2O4 Sc2(C2O4)3↓+6H+,该反应的平衡常数K=
Sc2(C2O4)3↓+6H+,该反应的平衡常数K=______ (用含a、b、c的代数式表示)。
(4)Sc2(C2O4)3·6H2O在空气中加热分解时, 随温度变化如图所示。已知:M[Sc2(C2O4)3·6H2O]=462g·mol-1。
随温度变化如图所示。已知:M[Sc2(C2O4)3·6H2O]=462g·mol-1。

250℃时固体的主要成分是_____ (填化学式);550~850℃时反应的化学方程式为______ 。

已知:TiO2难溶于盐酸;Ksp[Fe(OH)3]=1.0×10-38。
回答下列问题:
(1)为提高“酸浸”速率,对“赤泥”的处理方式为
(2)“氧化”时加入足量H2O2的目的是
(3)已知25℃时,Kh1(C2O
 )=a,Kh2(C2O
)=a,Kh2(C2O )=b,Ksp[Sc2(C2O4)3]=c。“沉钪”时,发生反应:2Sc3++3H2C2O4
)=b,Ksp[Sc2(C2O4)3]=c。“沉钪”时,发生反应:2Sc3++3H2C2O4 Sc2(C2O4)3↓+6H+,该反应的平衡常数K=
Sc2(C2O4)3↓+6H+,该反应的平衡常数K=(4)Sc2(C2O4)3·6H2O在空气中加热分解时,
 随温度变化如图所示。已知:M[Sc2(C2O4)3·6H2O]=462g·mol-1。
随温度变化如图所示。已知:M[Sc2(C2O4)3·6H2O]=462g·mol-1。
250℃时固体的主要成分是
您最近一年使用:0次
2023-02-22更新
|
1080次组卷
|
3卷引用:辽宁省大连市育明高级中学2023届高三下学期第1次模拟考试化学试题
名校
解题方法
3 . 工业烟气中含有较高浓度的氮氧化物,需进行脱除处理才能排放到大气中。下图是一种利用 在催化剂条件下脱除
在催化剂条件下脱除 的原理示意图:
的原理示意图:

下列说法错误的是
 在催化剂条件下脱除
在催化剂条件下脱除 的原理示意图:
的原理示意图:
下列说法错误的是
A.步骤①中 发生氧化反应 发生氧化反应 |
| B.步骤②中包含有σ键和π键的断裂 |
C.若参与反应的 和 和 的物质的量相等,则该过程的总反应化学方程式为 的物质的量相等,则该过程的总反应化学方程式为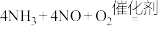  |
D.当消耗a  和b 和b  时,消耗 时,消耗 的物质的量为 的物质的量为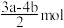 |
您最近一年使用:0次
2023-02-09更新
|
1194次组卷
|
4卷引用:辽宁省部分学校2022-2023学年高三下学期三模化学试题
名校
解题方法
4 . 以二氧化锰为原料制取高锰酸钾晶体的工艺流程如图所示。下列说法正确的是

| A.“灼烧”可在石英坩埚中进行 |
B.“母液”中的溶质仅有 、 、 |
| C.“结晶”过程宜采用蒸发结晶的方法 |
D.“转化”过程中的反应方程式为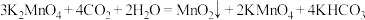 |
您最近一年使用:0次
2023-02-08更新
|
496次组卷
|
16卷引用:辽宁省东北育才学校高中部高三2021-2022下学期开学初第六次模拟考试化学试题
辽宁省东北育才学校高中部高三2021-2022下学期开学初第六次模拟考试化学试题辽宁省沈阳市法库县高级中学2022届高三下学期4月线上模拟考试化学试题(已下线)河北省普通高中学业水平选择性考试 化学预测卷(八)辽宁省沈阳市第五中学2021-2022学年高三下学期3月月考化学试题辽宁省沈阳市第二中学2022-2023学年高三上学期12月阶段测试化学试题湖北省部分重点中学2021-2022学年高三上学期期中第一次联考化学试题福建省福州第三中学2021-2022学年高三上学期第四次质量检测化学试题(已下线)学科特色7 工艺流程推断(已下线)易错点3不会前后上下结合推断工艺流程湖南省邵阳市第一中学2023届高三第五次月考化学试题湖南省娄底市双峰县第一中学2023届高三下学期第五次月考化学试题(已下线)湖北省七市(州)2023届高三3月联合统一调研测试化学试题变式题(选择题11-15)江西省南昌市三校(一中、十中、铁一中)2022-2023学年高三上学期11月期中联考化学试题吉林省白山市抚松县第一中学2022-2023学年高三上学期期末考试化学试题(已下线)选择题11-15湖南省衡阳市衡阳县第一中学2024届高三上学期11月月考化学试题
名校
解题方法
5 . 工业上利用石煤矿粉(主要含 及少量
及少量 、
、 )为原料生产
)为原料生产 ,工艺流程如下:
,工艺流程如下:

已知:①“水溶”、“转沉”、“转化”后,所得含钒物质依次为 、
、 、
、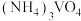 ;
;
②不同pH下,V(V)在溶液中的主要存在形式见下表:
③25℃时, 。
。
回答下列问题:
(1)“焙烧”时, 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
(2)滤液Ⅰ的成分为_______ (填化学式);先“转沉”后“转化”的目的是_______ 。
(3)“转化”时,滤渣Ⅱ经高温煅烧后水浸,所得物质可导入到_______ 操作单元中循环使用。
(4)“沉钒”中析出 晶体时,需要加入过量
晶体时,需要加入过量 ,其原因是①
,其原因是①_______ 。②_______ ;25℃时,测得“转化”后,滤液中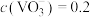 mol·L
mol·L ,为使“沉钒”时,钒元素的沉降率达到96%,应调节溶液中
,为使“沉钒”时,钒元素的沉降率达到96%,应调节溶液中 至少
至少_______ mol·L 。
。
(5)“煅烧”时, 制得产品
制得产品 。但反应体系中,若不及时分离气体Ⅱ,部分
。但反应体系中,若不及时分离气体Ⅱ,部分 会转化成
会转化成 ,反应中氧化剂与还原剂物质的量之比为3∶2,该反应的化学方程式为
,反应中氧化剂与还原剂物质的量之比为3∶2,该反应的化学方程式为_______ 。
 及少量
及少量 、
、 )为原料生产
)为原料生产 ,工艺流程如下:
,工艺流程如下:
已知:①“水溶”、“转沉”、“转化”后,所得含钒物质依次为
 、
、 、
、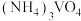 ;
;②不同pH下,V(V)在溶液中的主要存在形式见下表:
| pH | 4~6 | 6~8 | 8~10 | 10~12 |
| 主要离子 |  |  |  |  |
 。
。回答下列问题:
(1)“焙烧”时,
 发生反应的化学方程式为
发生反应的化学方程式为(2)滤液Ⅰ的成分为
(3)“转化”时,滤渣Ⅱ经高温煅烧后水浸,所得物质可导入到
(4)“沉钒”中析出
 晶体时,需要加入过量
晶体时,需要加入过量 ,其原因是①
,其原因是①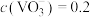 mol·L
mol·L ,为使“沉钒”时,钒元素的沉降率达到96%,应调节溶液中
,为使“沉钒”时,钒元素的沉降率达到96%,应调节溶液中 至少
至少 。
。(5)“煅烧”时,
 制得产品
制得产品 。但反应体系中,若不及时分离气体Ⅱ,部分
。但反应体系中,若不及时分离气体Ⅱ,部分 会转化成
会转化成 ,反应中氧化剂与还原剂物质的量之比为3∶2,该反应的化学方程式为
,反应中氧化剂与还原剂物质的量之比为3∶2,该反应的化学方程式为
您最近一年使用:0次
2023-02-08更新
|
2164次组卷
|
4卷引用:2024届辽宁省葫芦岛市高三下学期一模化学试题
名校
解题方法
6 . 硫化氢的转化是资源利用和环境保护的重要研究课题。将 和空气的混合气体通入
和空气的混合气体通入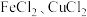 的混合溶液中反应回收S,其物质转化如图所示。下列说法错误的是
的混合溶液中反应回收S,其物质转化如图所示。下列说法错误的是

 和空气的混合气体通入
和空气的混合气体通入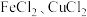 的混合溶液中反应回收S,其物质转化如图所示。下列说法错误的是
的混合溶液中反应回收S,其物质转化如图所示。下列说法错误的是
A.在图示的转化中, 和 和 是中间产物 是中间产物 |
| B.在图示的转化中,化合价不变的元素只有铜 |
C.图示转化的总反应是 |
D.当有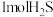 转化为硫单质时,需要消耗 转化为硫单质时,需要消耗 的物质的量为 的物质的量为 |
您最近一年使用:0次
2023-02-01更新
|
603次组卷
|
12卷引用:辽宁省丹东市2020届高三第一次模拟考试理科综合化学试题
辽宁省丹东市2020届高三第一次模拟考试理科综合化学试题河南省开封市2020届高三下学期3月模拟考试理综化学试题江苏省连云港市赣榆区2020届高三高考仿真训练化学试题辽宁省大连市金普新区省示范性高中2022届高三上学期第一次联合考试化学试题四川省宜宾市叙州区第二中学校2021届高三上学期阶段二考试理综化学试题人教版2019必修第二册 第五章 第一节综合拔高练四川省广安友谊中学2020-2021学年高一下学期3月月考化学试题重庆市南开中学校2021-2022学年高一下学期3月月考化学试题(已下线)第一部分 二轮专题突破 专题8 常见无机物性质的转化江苏省南京市燕子矶中学2022-2023 学年高一下学期期中考试化学试题广东省广州市第十六中学2022-2023学年高一下学期期中考试化学试题新疆生产建设兵团第一师高级中学2022-2023学年高一下学期3月月考化学试题
名校
7 . 叠氮化钠(NaN3)是一种防腐剂和分析试剂,在有机合成和汽车行业也有重要应用。学习小组对叠氮化钠的制备和产品纯度测定进行相关探究。制备NaN3的装置如图1所示。
查阅资料:①氨基钠(NaNH2)的熔点为208℃,易潮解和氧化;N2O有强氧化性,不与酸、碱反应;叠氮酸(HN3)不稳定,易分解爆炸。② ,
, 。
。
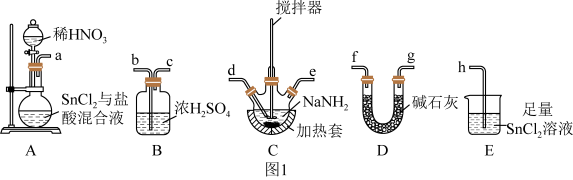
回答下列问题:
(1)①按气流方向,图1中装置的连接顺序为___________ (填仪器接口字母)。
②实验时装置E中生成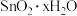 沉淀,反应的化学方程式为
沉淀,反应的化学方程式为______________________ 。
③装置C中物质充分反应后,停止加热,需继续进行的操作为__________________ ,其目的为_____________ 。
(2)用如图2所示装置测定(1)中所得产品的纯度。
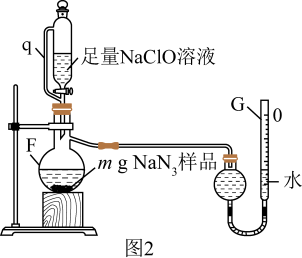
①装置F中发生反应的离子方程式为______________________ 。
②仪器q的作用为___________ 。
③若仪器G的初始读数为 ,实验结束时读数为
,实验结束时读数为 ,本实验条件下气体摩尔体积为
,本实验条件下气体摩尔体积为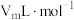 ,则产品中
,则产品中 的质量分数为
的质量分数为___________ (用含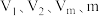 的式子表示)。
的式子表示)。
查阅资料:①氨基钠(NaNH2)的熔点为208℃,易潮解和氧化;N2O有强氧化性,不与酸、碱反应;叠氮酸(HN3)不稳定,易分解爆炸。②
 ,
, 。
。
回答下列问题:
(1)①按气流方向,图1中装置的连接顺序为
②实验时装置E中生成
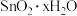 沉淀,反应的化学方程式为
沉淀,反应的化学方程式为③装置C中物质充分反应后,停止加热,需继续进行的操作为
(2)用如图2所示装置测定(1)中所得产品的纯度。

①装置F中发生反应的离子方程式为
②仪器q的作用为
③若仪器G的初始读数为
 ,实验结束时读数为
,实验结束时读数为 ,本实验条件下气体摩尔体积为
,本实验条件下气体摩尔体积为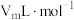 ,则产品中
,则产品中 的质量分数为
的质量分数为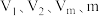 的式子表示)。
的式子表示)。
您最近一年使用:0次
2023-01-14更新
|
742次组卷
|
2卷引用:辽宁省大连市育明高级中学2023届高三下学期第1次模拟考试化学试题
解题方法
8 . 联氨(N2H4)可用于处理水中的溶解氧,其反应机理如下图所示:
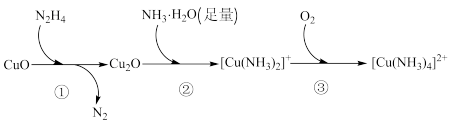
下列说法不正确 的是

下列说法
A. 分子的共价键只有 分子的共价键只有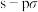 键 键 |
B. 具有还原性,在一定条件下可被 具有还原性,在一定条件下可被 氧化 氧化 |
C.②中反应产物是 而不是 而不是 ,说明 ,说明 相对较稳定 相对较稳定 |
D.③中发生反应: |
您最近一年使用:0次
2022-12-29更新
|
458次组卷
|
4卷引用:化学-2023年高考押题预测卷03(辽宁卷)(含考试版、全解全析、参考答案、答题卡)
(已下线)化学-2023年高考押题预测卷03(辽宁卷)(含考试版、全解全析、参考答案、答题卡)天津市南开区2022-2023学年高三下学期质量检测(一)化学试题北京市大兴区2022-2023学年高三上学期期末考试化学试题(已下线)专题12 化学反应机理(练)-2023年高考化学二轮复习讲练测(新高考专用)
名校
9 . 金属M与单质碘在无水醋酸中反应,得到化合物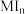 ,提纯干燥后测得其熔点为144.5℃。为确定
,提纯干燥后测得其熔点为144.5℃。为确定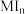 的组成,进行以下实验:称取0.6263g
的组成,进行以下实验:称取0.6263g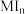 ,置于特制的梨形瓶中,加入50mL 6mol L-1的盐酸,同时加入适量
,置于特制的梨形瓶中,加入50mL 6mol L-1的盐酸,同时加入适量 ,用0.1000mol L-1的碘酸钾溶液进行滴定。随着碘酸钾溶液的加入,可观察到
,用0.1000mol L-1的碘酸钾溶液进行滴定。随着碘酸钾溶液的加入,可观察到 层呈紫色,后逐渐变浅,滴至紫色褪去为终点,此时
层呈紫色,后逐渐变浅,滴至紫色褪去为终点,此时 层呈淡黄色,滴定消耗碘酸钾溶液20.00mL。在
层呈淡黄色,滴定消耗碘酸钾溶液20.00mL。在 中显黄色的物质在历史上曾被误认为
中显黄色的物质在历史上曾被误认为 。下面有关实验细节的描述中,错误的是
。下面有关实验细节的描述中,错误的是
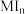 ,提纯干燥后测得其熔点为144.5℃。为确定
,提纯干燥后测得其熔点为144.5℃。为确定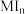 的组成,进行以下实验:称取0.6263g
的组成,进行以下实验:称取0.6263g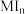 ,置于特制的梨形瓶中,加入50mL 6mol L-1的盐酸,同时加入适量
,置于特制的梨形瓶中,加入50mL 6mol L-1的盐酸,同时加入适量 ,用0.1000mol L-1的碘酸钾溶液进行滴定。随着碘酸钾溶液的加入,可观察到
,用0.1000mol L-1的碘酸钾溶液进行滴定。随着碘酸钾溶液的加入,可观察到 层呈紫色,后逐渐变浅,滴至紫色褪去为终点,此时
层呈紫色,后逐渐变浅,滴至紫色褪去为终点,此时 层呈淡黄色,滴定消耗碘酸钾溶液20.00mL。在
层呈淡黄色,滴定消耗碘酸钾溶液20.00mL。在 中显黄色的物质在历史上曾被误认为
中显黄色的物质在历史上曾被误认为 。下面有关实验细节的描述中,错误的是
。下面有关实验细节的描述中,错误的是| A.滴定终点时的操作:当滴入最后半滴标准液时,溶液恰好由紫色变为淡黄色,且半分钟不变色 |
B.滴定结束后 中主要的溶质为 中主要的溶质为 |
C.如果用过量的碘化钾溶液滴定碘酸钾溶液,则滴定过程中 层颜色逐渐加深,直至不变 层颜色逐渐加深,直至不变 |
D.紫色褪去反应的离子方程式为: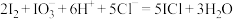 |
您最近一年使用:0次
2022-12-24更新
|
448次组卷
|
3卷引用:辽宁省部分学校2023年普通高等学校招生选择性考试模拟(一)化学试题
辽宁省部分学校2023年普通高等学校招生选择性考试模拟(一)化学试题(已下线)考点2 水的电离与溶液的pH (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)河南省周口恒大中学2023-2024学年高三下学期4月期中考试化学试题
解题方法
10 . 金属M与单质碘在无水醋酸中反应,得到化合物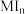 ,提纯干燥后测得其熔点为144.5℃。为确定
,提纯干燥后测得其熔点为144.5℃。为确定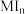 的组成,进行以下实验:称取0.6263g
的组成,进行以下实验:称取0.6263g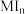 ,置于特制的梨形瓶中,加入50mL 6mol L-1的盐酸,同时加入适量
,置于特制的梨形瓶中,加入50mL 6mol L-1的盐酸,同时加入适量 ,用0.1000mol L-1的碘酸钾溶液进行滴定。随着碘酸钾溶液的加入,可观察到
,用0.1000mol L-1的碘酸钾溶液进行滴定。随着碘酸钾溶液的加入,可观察到 层呈紫色,后逐渐变浅,滴至紫色褪去为终点,此时
层呈紫色,后逐渐变浅,滴至紫色褪去为终点,此时 层呈淡黄色,滴定消耗碘酸钾溶液20.00mL。在
层呈淡黄色,滴定消耗碘酸钾溶液20.00mL。在 中显黄色的物质在历史上曾被误认为
中显黄色的物质在历史上曾被误认为 。
。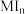 是
是
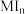 ,提纯干燥后测得其熔点为144.5℃。为确定
,提纯干燥后测得其熔点为144.5℃。为确定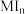 的组成,进行以下实验:称取0.6263g
的组成,进行以下实验:称取0.6263g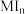 ,置于特制的梨形瓶中,加入50mL 6mol L-1的盐酸,同时加入适量
,置于特制的梨形瓶中,加入50mL 6mol L-1的盐酸,同时加入适量 ,用0.1000mol L-1的碘酸钾溶液进行滴定。随着碘酸钾溶液的加入,可观察到
,用0.1000mol L-1的碘酸钾溶液进行滴定。随着碘酸钾溶液的加入,可观察到 层呈紫色,后逐渐变浅,滴至紫色褪去为终点,此时
层呈紫色,后逐渐变浅,滴至紫色褪去为终点,此时 层呈淡黄色,滴定消耗碘酸钾溶液20.00mL。在
层呈淡黄色,滴定消耗碘酸钾溶液20.00mL。在 中显黄色的物质在历史上曾被误认为
中显黄色的物质在历史上曾被误认为 。
。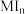 是
是A.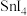 | B. | C.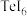 | D. |
您最近一年使用:0次



