名校
解题方法
1 . 综合题
 .铁在自然界中有多种存在形式,并且对环境也有重要影响,某化学兴趣小组对土壤中的铁的存在和含量进行了以下的研究:
.铁在自然界中有多种存在形式,并且对环境也有重要影响,某化学兴趣小组对土壤中的铁的存在和含量进行了以下的研究:
(1)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),酸性环境中Fe2+脱除水体中硝态氮(NO )且无污染,写出该反应的离子方程式:
)且无污染,写出该反应的离子方程式:___________ 。
(2)土壤中的铁元素含量的测定:
乙二胺四乙酸又叫 ,是化学中一种良好的配合剂,形成的配合物又叫螯合物。
,是化学中一种良好的配合剂,形成的配合物又叫螯合物。 在配位滴定中用到,一般是测定金属离子的含量。已知:
在配位滴定中用到,一般是测定金属离子的含量。已知: 配离子结构如图,M为Fe3+。
配离子结构如图,M为Fe3+。 中氮原子杂化方式
中氮原子杂化方式___________ ,该配合物中Fe3+配位数是___________ 。
②土壤中的铁元素含量测定步骤:
第一步:取ag土壤试样溶解,加入足量H2O2,将溶液充分加热。
第二步:将上述液体配成100mL溶液,取25.00mL,,滴入两滴二甲酚橙作指示剂,用bmol·L-1EDTA(简写成H2Y2-)标准溶液滴定,反应的离子方程式为Fe3++H2Y2-=FeY-+2H+。达到滴定终点时,消耗EDTA标准溶液的平均体积为12.50mL。该土壤中的铁元素质量分数为___________ (用含a、b的代数式表示)。
③第一步加入足量H2O2的目的是:___________ 。
④若在滴定操作中一些不当操作可能会引起误差,下列操作会使土壤中的铁元素质量分数测定结果偏高的是:___________ 。
A.滴定终点读数时,俯视滴定管的刻度
B.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.滴定到终点,读数时发现滴定管尖嘴处悬挂一滴溶液
D.盛放EDTA(简写成H2Y2-)标准溶液的滴定管用蒸馏水洗净后未用标准液润洗
 .铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。
.铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。___________ 。
(4)若该晶胞的边长为d nm,则该合金的密度为___________  。(列出计算式即可,设阿伏加德罗常数的值为NA)
。(列出计算式即可,设阿伏加德罗常数的值为NA)
(5)若该晶体储氢时,H2分子在晶胞的体心和棱心位置,则含镁 48g的该储氢合金可储存标准状况下H2的体积约为___________ L。
 .铁在自然界中有多种存在形式,并且对环境也有重要影响,某化学兴趣小组对土壤中的铁的存在和含量进行了以下的研究:
.铁在自然界中有多种存在形式,并且对环境也有重要影响,某化学兴趣小组对土壤中的铁的存在和含量进行了以下的研究:(1)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),酸性环境中Fe2+脱除水体中硝态氮(NO
 )且无污染,写出该反应的离子方程式:
)且无污染,写出该反应的离子方程式:(2)土壤中的铁元素含量的测定:
乙二胺四乙酸又叫
 ,是化学中一种良好的配合剂,形成的配合物又叫螯合物。
,是化学中一种良好的配合剂,形成的配合物又叫螯合物。 在配位滴定中用到,一般是测定金属离子的含量。已知:
在配位滴定中用到,一般是测定金属离子的含量。已知: 配离子结构如图,M为Fe3+。
配离子结构如图,M为Fe3+。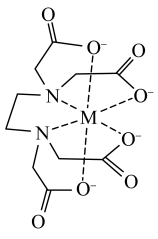
 中氮原子杂化方式
中氮原子杂化方式②土壤中的铁元素含量测定步骤:
第一步:取ag土壤试样溶解,加入足量H2O2,将溶液充分加热。
第二步:将上述液体配成100mL溶液,取25.00mL,,滴入两滴二甲酚橙作指示剂,用bmol·L-1EDTA(简写成H2Y2-)标准溶液滴定,反应的离子方程式为Fe3++H2Y2-=FeY-+2H+。达到滴定终点时,消耗EDTA标准溶液的平均体积为12.50mL。该土壤中的铁元素质量分数为
③第一步加入足量H2O2的目的是:
④若在滴定操作中一些不当操作可能会引起误差,下列操作会使土壤中的铁元素质量分数测定结果偏高的是:
A.滴定终点读数时,俯视滴定管的刻度
B.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.滴定到终点,读数时发现滴定管尖嘴处悬挂一滴溶液
D.盛放EDTA(简写成H2Y2-)标准溶液的滴定管用蒸馏水洗净后未用标准液润洗
 .铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。
.铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。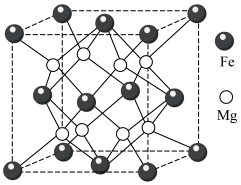
(4)若该晶胞的边长为d nm,则该合金的密度为
 。(列出计算式即可,设阿伏加德罗常数的值为NA)
。(列出计算式即可,设阿伏加德罗常数的值为NA)(5)若该晶体储氢时,H2分子在晶胞的体心和棱心位置,则含镁 48g的该储氢合金可储存标准状况下H2的体积约为
您最近一年使用:0次
2 . 钒的化合物能有效调节血糖,化合物丁有望成为抗糖尿病的新型药物,其制备流程如下:
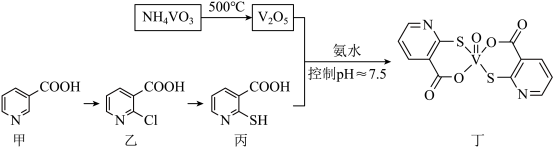
(1)钒在元素周期表中的位置为_______ ,基态V的原子结构示意图为_______ 。
(2) 转化为
转化为 的化学方程式是
的化学方程式是_______ 。
(3)下列说法正确的是_______(填字母)
(4)分析丙的分子结构与性质
①比较丙中 键角和
键角和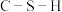 键角的大小并解释原因:
键角的大小并解释原因:_______
②丙为有机弱酸,请写出1mol丙与2mol一水合氨反应的离子方程式_______ 。
(5)多原子分子中各原子若在同一平面,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域 键”,下列物质中存在“离域
键”,下列物质中存在“离域 键”的是_______。
键”的是_______。
(6)丁是一种配合物含有化合物丁的样品中,含钒量的测定方法是:先把样品中的钒元素经处理转化为 溶液,再用硫酸酸化的
溶液,再用硫酸酸化的 标准溶液进行滴定,生成
标准溶液进行滴定,生成 。取样品10.2g,用上述方法测定其中钒的含量,消耗
。取样品10.2g,用上述方法测定其中钒的含量,消耗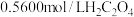 标准溶液25.00mL,则样品中钒元素的质量分数为
标准溶液25.00mL,则样品中钒元素的质量分数为_______ (写出计算结果)。

(1)钒在元素周期表中的位置为
(2)
 转化为
转化为 的化学方程式是
的化学方程式是(3)下列说法正确的是_______(填字母)
A.元素的第一电离能: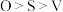 |
B.共价键的极性:丙中 乙中 乙中 |
| C.甲分子中所有原子可能在同一平面内 |
D.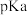 :乙>甲 :乙>甲 |
①比较丙中
 键角和
键角和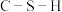 键角的大小并解释原因:
键角的大小并解释原因:②丙为有机弱酸,请写出1mol丙与2mol一水合氨反应的离子方程式
(5)多原子分子中各原子若在同一平面,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域
 键”,下列物质中存在“离域
键”,下列物质中存在“离域 键”的是_______。
键”的是_______。A. | B. | C. | D. |
 溶液,再用硫酸酸化的
溶液,再用硫酸酸化的 标准溶液进行滴定,生成
标准溶液进行滴定,生成 。取样品10.2g,用上述方法测定其中钒的含量,消耗
。取样品10.2g,用上述方法测定其中钒的含量,消耗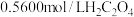 标准溶液25.00mL,则样品中钒元素的质量分数为
标准溶液25.00mL,则样品中钒元素的质量分数为
您最近一年使用:0次
解题方法
3 . 氮是动植物生长过程中不可缺少的元素,其单质及其化合物有着广泛的用途。回答下列问题:
(1)肼(N2H4)、偏二甲肼(C2H8N2)、四氧化二氮(N2O4)都可用作火箭的燃料。
①N2H4、C2H8N2、N2O4中氮元素的质量分数由小到大的顺序为__ 。
②液态肼与液态四氧化二氨发生反应生成空气中含量最多的气体和水蒸气,写出该反应的化学方程式:___ 。
(2)将28gFe完全溶于一定量的HNO3溶液中,若只产生N2O、NO两种气体,该混合气体体积为5.6L(标准状况下),并且检测到溶液中金属阳离子只有Fe2+。
①与N2O互为等电子体的一种分子为__ ,其空间构型为___ 。
②写出上述Fe与HNO3反应生成N2O的离子方程式:___ 。
③生成的N2O、NO的物质的量之比为___ 。
(1)肼(N2H4)、偏二甲肼(C2H8N2)、四氧化二氮(N2O4)都可用作火箭的燃料。
①N2H4、C2H8N2、N2O4中氮元素的质量分数由小到大的顺序为
②液态肼与液态四氧化二氨发生反应生成空气中含量最多的气体和水蒸气,写出该反应的化学方程式:
(2)将28gFe完全溶于一定量的HNO3溶液中,若只产生N2O、NO两种气体,该混合气体体积为5.6L(标准状况下),并且检测到溶液中金属阳离子只有Fe2+。
①与N2O互为等电子体的一种分子为
②写出上述Fe与HNO3反应生成N2O的离子方程式:
③生成的N2O、NO的物质的量之比为
您最近一年使用:0次
解题方法
4 . A、B、C、D、E、F为短周期元素, 原子序数依次增大。非金属元素A 最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。E+与D2-具有相同的电子层结构。A单质在F单质中燃烧,产物溶于水得到一种强酸M。回答下列问题:
(1)画出E的离子结构示意图___________ 。
(2)F在周期表中的位置是___________ 。
(3)B、D、E组成的一种常见盐,其中D的质量分数约为 45%,该盐与少量M溶液反应的离子方程式为___________ 。
(4)由这些元素组成的物质,相关信息如下:
①a的电子式为___________ 。 写出其与水反应的化学方程式:___________ 。
②b的一种常见用途为___________ 。
③已知c中所有原子均满足8 电子稳定结构,该化合物的结构式为___________ 。
(1)画出E的离子结构示意图
(2)F在周期表中的位置是
(3)B、D、E组成的一种常见盐,其中D的质量分数约为 45%,该盐与少量M溶液反应的离子方程式为
(4)由这些元素组成的物质,相关信息如下:
| 物质 | 组成和结构信息 |
| a | 由 A、E组成的离子化合物 |
| b | 由D、E组成的含非极性键的离子化合物,阴阳离子数之比为1:2 |
| c | 化学式为BDF2的共价化合物 |
②b的一种常见用途为
③已知c中所有原子均满足8 电子稳定结构,该化合物的结构式为
您最近一年使用:0次
名校
解题方法
5 . 钒具有广泛用途,利用含钒废催化剂(主要含有V2O5、VOSO4和不溶性硅酸盐)制备V2O5的新工艺流程如图:

已知:滤液1和滤液2中钒以VO2+的形式存在。回答下列问题:
(1)写出V基态原子核外电子排布式_______ 。
(2)在实验室中操作Ⅰ用到的玻璃仪器有_______ 。
(3)在滤渣1中加入Na2SO3和过量稀H2SO4溶液发生氧化还原反应,氧化剂和还原剂的物质的量之比为_______ 。
(4)混合溶液中加入KClO3,发生反应的离子方程式是_______ 。
(5)钒最后以NH4VO3的形式沉淀出来。沉钒率(NH4VO3沉淀中V的质量和废催化剂中V的质量之比)表示该工艺钒的回收率。图中是沉钒率随温度变化的关系曲线,“沉钒”时,温度超过80℃以后,沉钒率下降的可能原因是_______ (写一条即可)。

(6)称取w g所得产品,先用硫酸溶解,得到(VO2)2SO4溶液,再加入 的(NH4)2Fe(SO4)2溶液,最后用
的(NH4)2Fe(SO4)2溶液,最后用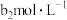 酸性KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗溶液KMnO4的体积为
酸性KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗溶液KMnO4的体积为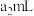 。假设杂质不参与反应,锰元素被还原为Mn2+。求产品中V2O5的质量分数为
。假设杂质不参与反应,锰元素被还原为Mn2+。求产品中V2O5的质量分数为_______ (写出计算过程)[已知(VO2)2SO4和(NH4)2Fe(SO4)2溶液反应的离子方程式为VO +2H++Fe2+=VO2++Fe3++H2O]
+2H++Fe2+=VO2++Fe3++H2O]

已知:滤液1和滤液2中钒以VO2+的形式存在。回答下列问题:
(1)写出V基态原子核外电子排布式
(2)在实验室中操作Ⅰ用到的玻璃仪器有
(3)在滤渣1中加入Na2SO3和过量稀H2SO4溶液发生氧化还原反应,氧化剂和还原剂的物质的量之比为
(4)混合溶液中加入KClO3,发生反应的离子方程式是
(5)钒最后以NH4VO3的形式沉淀出来。沉钒率(NH4VO3沉淀中V的质量和废催化剂中V的质量之比)表示该工艺钒的回收率。图中是沉钒率随温度变化的关系曲线,“沉钒”时,温度超过80℃以后,沉钒率下降的可能原因是

(6)称取w g所得产品,先用硫酸溶解,得到(VO2)2SO4溶液,再加入
 的(NH4)2Fe(SO4)2溶液,最后用
的(NH4)2Fe(SO4)2溶液,最后用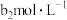 酸性KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗溶液KMnO4的体积为
酸性KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗溶液KMnO4的体积为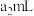 。假设杂质不参与反应,锰元素被还原为Mn2+。求产品中V2O5的质量分数为
。假设杂质不参与反应,锰元素被还原为Mn2+。求产品中V2O5的质量分数为 +2H++Fe2+=VO2++Fe3++H2O]
+2H++Fe2+=VO2++Fe3++H2O]
您最近一年使用:0次
2022-06-24更新
|
333次组卷
|
2卷引用:江苏省南京市六校联合体2021-2022学年高二下学期期末联考化学试题
6 . 用工业钒渣(含 、
、 、Fe)制备工业催化剂
、Fe)制备工业催化剂 的流程如图所示:
的流程如图所示:
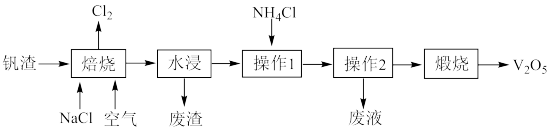
已知:
① 为白色或淡黄色晶体,易溶于水。
为白色或淡黄色晶体,易溶于水。
② 为白色的结晶性粉末,微溶于冷水,溶于热水。
为白色的结晶性粉末,微溶于冷水,溶于热水。
(1)硫酸工业中, 转化为
转化为 选用
选用 作催化剂,催化过程分两步完成,第二步方程式为
作催化剂,催化过程分两步完成,第二步方程式为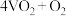
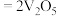 ,则第一步方程式为
,则第一步方程式为_______ 。
(2)“焙烧”过程的产物之一为 ,写出生成
,写出生成 的化学方程式:
的化学方程式:_______ 。废渣的主要成分为氧化铁和_______ 。
(3)“操作1”需要加入过量氯化铵,其目的是_______ ;实验室完成“操作2”时需要用到的玻璃仪器有_______ ;若操作后得到的目标产物纯度不够,则提纯目标产物的方法是_______ 。
(4)“煅烧”中,除生成 外,还生成
外,还生成_______ 。
(5)测定产品纯度的实验步骤如下:
①称取样品ag,加入硫酸,得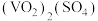 溶液;
溶液;
②加入b
 溶液V1mL(过量),发生如下反应:
溶液V1mL(过量),发生如下反应: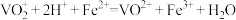
③过量的 用c
用c
 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液体积为
溶液体积为 mL。
mL。
当加入最后一滴 溶液时,溶液变为
溶液时,溶液变为_______ ,且半分钟内不恢复原色,说明达到滴定终点。假设杂质不参与反应,则产品中 的质量分数为
的质量分数为_______ %。
 、
、 、Fe)制备工业催化剂
、Fe)制备工业催化剂 的流程如图所示:
的流程如图所示:
已知:
①
 为白色或淡黄色晶体,易溶于水。
为白色或淡黄色晶体,易溶于水。②
 为白色的结晶性粉末,微溶于冷水,溶于热水。
为白色的结晶性粉末,微溶于冷水,溶于热水。(1)硫酸工业中,
 转化为
转化为 选用
选用 作催化剂,催化过程分两步完成,第二步方程式为
作催化剂,催化过程分两步完成,第二步方程式为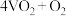
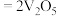 ,则第一步方程式为
,则第一步方程式为(2)“焙烧”过程的产物之一为
 ,写出生成
,写出生成 的化学方程式:
的化学方程式:(3)“操作1”需要加入过量氯化铵,其目的是
(4)“煅烧”中,除生成
 外,还生成
外,还生成(5)测定产品纯度的实验步骤如下:
①称取样品ag,加入硫酸,得
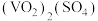 溶液;
溶液;②加入b

 溶液V1mL(过量),发生如下反应:
溶液V1mL(过量),发生如下反应: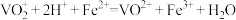
③过量的
 用c
用c
 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液体积为
溶液体积为 mL。
mL。当加入最后一滴
 溶液时,溶液变为
溶液时,溶液变为 的质量分数为
的质量分数为
您最近一年使用:0次
2022-05-22更新
|
178次组卷
|
2卷引用:重庆市第八中学校2022届高三高考适应性月考卷(七)化学试题
7 . Fe、Co、Ni是三种重要的金属元素。回答下列问题:
(1)Fe、Co、Ni在周期表中的位置为______ ,基态Co原子的价层电子排布式为______ ,与Ni同周期且与Ni具有相同未成对电子数的元素有_______ 种。
(2)Fe、Co、Ni能与Cl2反应,其中Co和Ni生成二氯化物。由此推断FeCl3、CoCl3和Cl2的氧化性由强到弱的顺序为____ 。Co(OH)3与盐酸反应有黄绿色气体生成,写出反应的离子方程式:_____ 。
(3)95℃时将Ni片浸在不同质量分数的硫酸中,经4小时腐蚀后的质量损失情况如图所示。
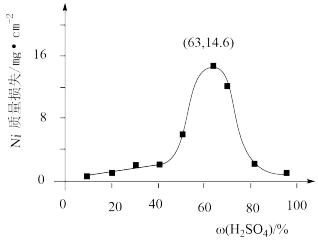
当w(H2SO4)大于63%时,Ni被腐蚀的速率逐渐降低的可能原因为_____ 。由于Ni与硫酸反应很慢,而与稀HNO3反应很快,工业上选用H2SO4和HNO3的混酸与Ni反应制备NiSO4,为了提高产物的纯度,在硫酸中添加HNO3的方式为_____ (填“一次过量”或“少量多次”),此法制备NiSO4的化学方程式为_____ 。
(1)Fe、Co、Ni在周期表中的位置为
(2)Fe、Co、Ni能与Cl2反应,其中Co和Ni生成二氯化物。由此推断FeCl3、CoCl3和Cl2的氧化性由强到弱的顺序为
(3)95℃时将Ni片浸在不同质量分数的硫酸中,经4小时腐蚀后的质量损失情况如图所示。

当w(H2SO4)大于63%时,Ni被腐蚀的速率逐渐降低的可能原因为
您最近一年使用:0次
解题方法
8 . A、B、C、D、E、F是元素周期表前四周期的六种常见元素,原子序数依次增大,它们有如下性质:
请完成以下问题:
(1)基态B原子的价层电子排布图为_______ 。
(2)A和B的简单氢化物中沸点更高的是_______ (填化学式),理由是_______ 。
(3)比较酸性强弱:
_______  (填“
(填“ ”或“
”或“ ”),依据是
”),依据是_______ 。
(4)B的一种氢化物 常用作火箭推进剂的燃料,
常用作火箭推进剂的燃料, 液态
液态 与
与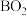 气体反应生成对环境友好的气态产物,放出
气体反应生成对环境友好的气态产物,放出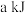 热量,写出该反应的热化学方程式
热量,写出该反应的热化学方程式_______ 。
(5)D元素的一种氧化物 常可作杀菌消毒剂和漂白剂,
常可作杀菌消毒剂和漂白剂, 的分子构型为
的分子构型为_______ ;工业上制取 的方法之一是:用D的单质与潮湿的碳酸钠反应,只生成
的方法之一是:用D的单质与潮湿的碳酸钠反应,只生成 和另外两种含钠的化合物,反应中无其他气体生成,写出该反应的化学方程式
和另外两种含钠的化合物,反应中无其他气体生成,写出该反应的化学方程式_______ 。
(6)用一个离子反应证明氧化性
_______ 。
| 元素 | 性质 |
| A | 自然界中有多种同素异形体,其中一种是自然界中最硬的单质 |
| C | 地壳中含量最多的元素 |
| D | 基态原子核外9个原子轨道上填充了电子且有1个未成对电子 |
| E | 常见的金属元素,可形成多种氧化物,其中一种氧化物常用作红色颜料 |
| F | 基态原子的M层全充满,N层没有成对电子,只有一个未成对电子 |
请完成以下问题:
(1)基态B原子的价层电子排布图为
(2)A和B的简单氢化物中沸点更高的是
(3)比较酸性强弱:

 (填“
(填“ ”或“
”或“ ”),依据是
”),依据是(4)B的一种氢化物
 常用作火箭推进剂的燃料,
常用作火箭推进剂的燃料, 液态
液态 与
与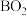 气体反应生成对环境友好的气态产物,放出
气体反应生成对环境友好的气态产物,放出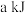 热量,写出该反应的热化学方程式
热量,写出该反应的热化学方程式(5)D元素的一种氧化物
 常可作杀菌消毒剂和漂白剂,
常可作杀菌消毒剂和漂白剂, 的分子构型为
的分子构型为 的方法之一是:用D的单质与潮湿的碳酸钠反应,只生成
的方法之一是:用D的单质与潮湿的碳酸钠反应,只生成 和另外两种含钠的化合物,反应中无其他气体生成,写出该反应的化学方程式
和另外两种含钠的化合物,反应中无其他气体生成,写出该反应的化学方程式(6)用一个离子反应证明氧化性

您最近一年使用:0次
2023-01-12更新
|
204次组卷
|
2卷引用:四川省内江市2022-2023学年高二上学期期末考试化学试题



