名校
解题方法
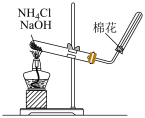
1 . 下列实验装置能用于相应实验的是
|
|
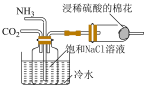
| A.制备氨气 | B.制备乙二酸 |
|
|
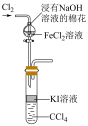
| C.证明碳酸酸性比硅酸强 | D.检验气体中含 和 和 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-06-02更新
|
206次组卷
|
2卷引用:2024届福建省厦门双十中学高三下学期模拟预测化学试题
2 . 某兴趣小组设计实验模拟探究氨气催化还原焦炉煤气中的 ,装置如图。
,装置如图。
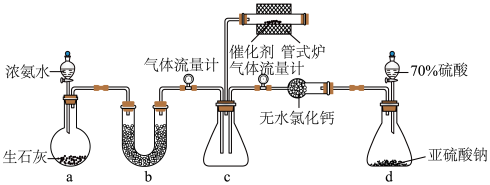
回答下列问题:
(1)装置a中盛装生石灰的仪器名称为________ 。
(2)装置d中发生反应的化学方程式为_________ 。
(3)装置b中应盛装的药品为_________(填标号)。
(4)管式炉中反应一段时间后,催化剂表面开始有淡黄色固体生成,反应为 。可以用一组化学方程式表示其反应进程,补充过程Ⅲ的化学方程式。
。可以用一组化学方程式表示其反应进程,补充过程Ⅲ的化学方程式。
过程Ⅰ:
过程Ⅱ: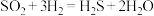
过程Ⅲ:___________ 。
(5)气体流量计可用于观察气体的流速。通过______ (填操作)调节气体流速,以控制装置c中 与
与 的比例。
的比例。
(6)该装置存在不足之处是_______ 。
 ,装置如图。
,装置如图。
回答下列问题:
(1)装置a中盛装生石灰的仪器名称为
(2)装置d中发生反应的化学方程式为
(3)装置b中应盛装的药品为_________(填标号)。
A.无水 | B.无水 | C.浓硫酸 | D.碱石灰 |
(4)管式炉中反应一段时间后,催化剂表面开始有淡黄色固体生成,反应为
 。可以用一组化学方程式表示其反应进程,补充过程Ⅲ的化学方程式。
。可以用一组化学方程式表示其反应进程,补充过程Ⅲ的化学方程式。过程Ⅰ:

过程Ⅱ:
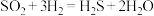
过程Ⅲ:
(5)气体流量计可用于观察气体的流速。通过
 与
与 的比例。
的比例。(6)该装置存在不足之处是
您最近一年使用:0次
名校
解题方法
3 . 下列装置正确并能达到实验目的的是
|
|
|
|
| 甲 | 乙 | 丙 | 丁 |
| A.图甲装置可用于实验室制取并收集NH3 |
| B.图乙装置可用于制备NaHCO3,其中CO2分子为直线形 |
| C.图丙装置可用于比较碳、硅元素非金属性大小 |
| D.图丁装置试管下层出现紫红色,可证明氧化性:Cl2>Fe3+>I2 |
您最近一年使用:0次
2023-10-05更新
|
69次组卷
|
2卷引用:福建省厦门第一中学2024届高三上学期10 月月考化学试题
解题方法
4 . 某研究性学习小组为了制取NH3,并探究NH3,铵盐相关的性质,进行了以下实验:

【制取氨气】
(1)A中发生反应的化学方程式为:_______________________ 。
(2)按图A装置制取NH3,生成的NH3,可用______ (填“浓H2SO4”或“碱石灰”)干燥,收集NH3应选择_______ (填“B”或“C”)装置。
(3)实验室制取O2、H2中,可选用A装置的气体是_________ 。
(4)若生成标准状况下22.4LNH3,至少需要NH4Cl的质量为___________ g(NH4Cl摩尔质量为53.5g·mol-1)。
【实验探究】
查阅资料可知:通常铵盐是白色晶体,易溶于水,受热易分,和碱反应能产生氨气。
(5)某同学用刚清洗过、含有较多水分的集气瓶收集氨气,__________ (填“能”或“不能”)收集到氨气。
(6)为确认某固体化肥样品中含有NH ,不必用到的试纸或试剂是
,不必用到的试纸或试剂是_____________ (只有一个正确选项)。
①NaOH溶液 ②红色石蕊试纸 ③稀H2SO4
(7)分别在两个集气瓶中滴入浓氨水和浓盐酸,盖上玻璃片,如图所示放置,然后抽去中间的玻璃片,观察到__________________ 现象。

【知识应用】
(8)为了防止碳酸氢铵肥效降低,你认为应该如何科学储存:_______________ (写出一种有效储存方法)。
(9)氨气的用途很广。如可利用氨气在催化剂存在的情况下与氧气反应来制取生产硝酸所需要的一氧化氮:4NH3+5O2 4NO+6H2O,在该反应中氨气体现
4NO+6H2O,在该反应中氨气体现 _________________ (选填“氧化性”或“还原性”)。请你列举氨气的另一种用途:______________ 。

【制取氨气】
(1)A中发生反应的化学方程式为:
(2)按图A装置制取NH3,生成的NH3,可用
(3)实验室制取O2、H2中,可选用A装置的气体是
(4)若生成标准状况下22.4LNH3,至少需要NH4Cl的质量为
【实验探究】
查阅资料可知:通常铵盐是白色晶体,易溶于水,受热易分,和碱反应能产生氨气。
(5)某同学用刚清洗过、含有较多水分的集气瓶收集氨气,
(6)为确认某固体化肥样品中含有NH
 ,不必用到的试纸或试剂是
,不必用到的试纸或试剂是①NaOH溶液 ②红色石蕊试纸 ③稀H2SO4
(7)分别在两个集气瓶中滴入浓氨水和浓盐酸,盖上玻璃片,如图所示放置,然后抽去中间的玻璃片,观察到

【知识应用】
(8)为了防止碳酸氢铵肥效降低,你认为应该如何科学储存:
(9)氨气的用途很广。如可利用氨气在催化剂存在的情况下与氧气反应来制取生产硝酸所需要的一氧化氮:4NH3+5O2
 4NO+6H2O,在该反应中氨气体现
4NO+6H2O,在该反应中氨气体现
您最近一年使用:0次
解题方法
5 . 微生物构成的氮的循环如图所示。
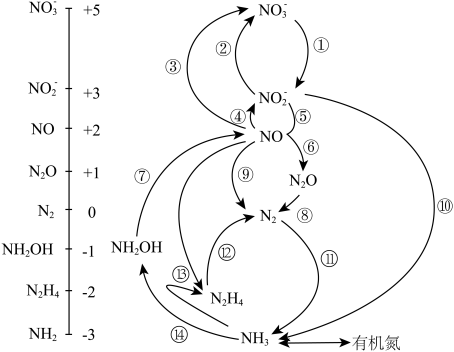
(1)NH3的电子式为___________ ,与N同周期的非金属元素的气态氢化物稳定性最强的为___________ 。
(2)实验室制备NH3的化学方程式为___________ 。检验NH3是否收集满的方法为___________ 。
(3)过程⑬的化学方程式为___________ 。反应中若将H替换成D(氘),当生成20gD2O时,产物中含有的N-D键的数目为___________ NA。
(4)羟胺(NH2OH)的结构式为___________ ,其与H2O2反应可实现⑦的转化,化学方程式为___________ ,为提高反应速率可适当升高温度,但温度过高该反应速率反而降低的原因是___________ 。

(1)NH3的电子式为
(2)实验室制备NH3的化学方程式为
(3)过程⑬的化学方程式为
(4)羟胺(NH2OH)的结构式为
您最近一年使用:0次
6 . 关于实验室制取氨气的说法正确的是


| A.虽然氨水受热分解可产生氨气,在实验室也不能用加热浓氨水的方法制取氨气 |
| B.用如图所示装置吸收NH3,是为了防止发生倒吸 |
| C.既可用向下排空气法收集NH3,又可用排水法收集NH3 |
| D.通常可选择浓硫酸为干燥剂,除去氨气中的水蒸气 |
您最近一年使用:0次
名校
解题方法
7 . 现用传感技术测定喷泉实验中的压强变化来认识喷泉实验的原理。下列说法正确的是

A.制取氨气时烧瓶中的固体常用 |
B.将湿润的蓝色石蕊试纸置于三颈烧瓶瓶口,试纸变红,说明 已经充满 已经充满 |
| C.关闭a,将单孔塞(插有吸入水的胶头滴管)塞紧颈口c,打开b,完成喷泉实验,电脑绘制三颈瓶内压强变化曲线如图2,则B点时喷泉最剧烈 |
D.若实验是在0℃、常压条件下完成,则在E点烧瓶中溶液溶质的物质的量浓度为 |
您最近一年使用:0次
2023-04-23更新
|
582次组卷
|
3卷引用:福建省厦门第一中学2023-2024学年高三暑期复习检测化学试题
名校
8 . 自然界中的氮循环部分过程如图所示,回答下列问题:

(1)①自然界中实现路径Ⅰ的固氮方式可能是___________ (任写一种)。
②在哈伯等科学家的努力下,路径Ⅱ已实现工业大规模合成氨,反应方程式为___________ 。
(2)①实验室制 的化学方程式为
的化学方程式为___________ ;
②干燥氨气不可以选用的试剂是___________ (填字母)。
a.浓硫酸 b.碱石灰 c.NaOH固体
(3)除反硝化作用外,铵态氮( )与亚硝态氮(
)与亚硝态氮( )也可以在细菌的作用下转化为氮气。请写出所涉及的离子反应方程式
)也可以在细菌的作用下转化为氮气。请写出所涉及的离子反应方程式___________ 。该反应中,当产生0.02mol氮气时,转移电子的物质的量为___________ 。
(4)工业制硝酸时尾气中含有NO、 ,可用以两种下方法吸收:
,可用以两种下方法吸收:
①水吸收法。请用化学方程式说明用水吸收 的缺陷
的缺陷___________ 。
②NaOH溶液吸收法。发生的反应有: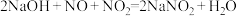 、
、 。用不同浓度NaOH溶液吸收
。用不同浓度NaOH溶液吸收 含量不同的尾气,氮氧化物吸收率与NaOH浓度间的关系如图所示(α表示尾气里
含量不同的尾气,氮氧化物吸收率与NaOH浓度间的关系如图所示(α表示尾气里 的含量):
的含量):

ⅰ.根据图中得知___________ (填字母)。
a.NaOH溶液浓度越大,氮氧化物的吸收率越大
b. 含量越大,氮氧化物的吸收率越大
含量越大,氮氧化物的吸收率越大
ⅱ.当α小于50%时,加入 能提升氮氧化物的吸收率,原因是
能提升氮氧化物的吸收率,原因是___________

(1)①自然界中实现路径Ⅰ的固氮方式可能是
②在哈伯等科学家的努力下,路径Ⅱ已实现工业大规模合成氨,反应方程式为
(2)①实验室制
 的化学方程式为
的化学方程式为②干燥氨气不可以选用的试剂是
a.浓硫酸 b.碱石灰 c.NaOH固体
(3)除反硝化作用外,铵态氮(
 )与亚硝态氮(
)与亚硝态氮( )也可以在细菌的作用下转化为氮气。请写出所涉及的离子反应方程式
)也可以在细菌的作用下转化为氮气。请写出所涉及的离子反应方程式(4)工业制硝酸时尾气中含有NO、
 ,可用以两种下方法吸收:
,可用以两种下方法吸收:①水吸收法。请用化学方程式说明用水吸收
 的缺陷
的缺陷②NaOH溶液吸收法。发生的反应有:
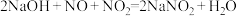 、
、 。用不同浓度NaOH溶液吸收
。用不同浓度NaOH溶液吸收 含量不同的尾气,氮氧化物吸收率与NaOH浓度间的关系如图所示(α表示尾气里
含量不同的尾气,氮氧化物吸收率与NaOH浓度间的关系如图所示(α表示尾气里 的含量):
的含量):
ⅰ.根据图中得知
a.NaOH溶液浓度越大,氮氧化物的吸收率越大
b.
 含量越大,氮氧化物的吸收率越大
含量越大,氮氧化物的吸收率越大ⅱ.当α小于50%时,加入
 能提升氮氧化物的吸收率,原因是
能提升氮氧化物的吸收率,原因是
您最近一年使用:0次
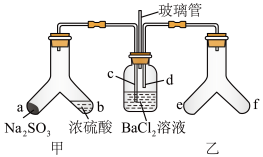
9 . Y形管是一种特殊的仪器,与其他仪器组合可以进行某些实验探究。利用如图装置可以探究 与
与 溶液反应生成沉淀的条件。下列判断错误的是
溶液反应生成沉淀的条件。下列判断错误的是
 与
与 溶液反应生成沉淀的条件。下列判断错误的是
溶液反应生成沉淀的条件。下列判断错误的是
A.e、f两管中的试剂可以分别是 固体和浓盐酸 固体和浓盐酸 |
| B.e、f两管中的试剂可以分别是NaOH固体和浓氨水 |
| C.为了使气体充分反应,c、d两导管均要插入液面下 |
| D.玻璃管的作用是连通大气,平衡压强,也可连接尾气处理装置 |
您最近一年使用:0次
2023-01-14更新
|
629次组卷
|
6卷引用:福建省厦门大学附属科技中学2023-2024学年高一上学期12月月考化学试卷
名校
解题方法
10 . 碳酸镧[La2(CO3)3]可用于治疗终末期肾病患者的高磷酸盐血症,制备反应原理为:2LaCl3+6NH4HCO3=La2(CO3)3↓+6NH4Cl+3CO2↑+3H2O,某化学兴趣小组利用下列实验装置模拟制备碳酸镧。下列说法不正确的是


| A.制备碳酸镧实验流程中导管从左向右的连接顺序为:F→A→B→D→E→C |
| B.X中盛放的试剂是浓硫酸,其作用为干燥 |
| C.Y中发生反应的化学方程式为NH3•H2O+CaO=Ca(OH)2+NH3↑ |
| D.Z中应先通入NH3,后通入过量的CO2 |
您最近一年使用:0次
2022-12-12更新
|
219次组卷
|
2卷引用:福建省厦门双十中学2022-2023学年高三上学期期中考试化学试题