名校
解题方法
1 . 室温下,下列各组离子在指定溶液中能大量共存的是( )
A.能使甲基橙变红的溶液:Na+、Ca2+、Br-、HCO |
B. =1×10-12的溶液:K+、Na+、CO =1×10-12的溶液:K+、Na+、CO 、AlO 、AlO |
C.0.1mol/LKFe(SO4)2溶液:Mg2+、Al3+、SCN-、NO |
D.0.1mol/LCa5NH4(NO3)11溶液:H+、Fe2+、Cl-、SO |
您最近一年使用:0次
2020-11-24更新
|
298次组卷
|
6卷引用:吉林白城市洮南市第一中学2020-2021学年高二下学期期末考试化学试题
解题方法
2 . 氯化铁是常见的水处理剂,利用废铁屑可制备无水氯化铁。实验室制备装置和工业制备流程图如图:
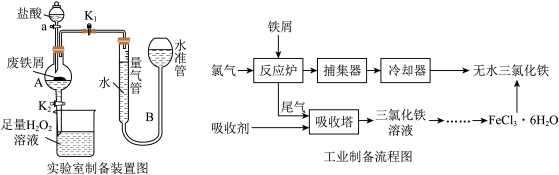
已知:(1)无水FeCl3的熔点为555K、沸点为588K。
(2)废铁屑中的杂质不与盐酸反应。
(3)不同温度下六水合氯化铁在水中的溶解度如下:
实验室制备操作步骤如下:
I.打开弹簧夹K1,关闭活塞K2,并打开活塞a,缓慢滴加盐酸;
II.当装置A中不产生气泡时,关闭弹簧夹K1,打开活塞K2,当A中溶液完全进入烧杯后关闭活塞a;
III.将烧杯中溶液经过一系列操作后得到FeCl3·6H2O晶体。
请回答:
(1)烧杯中足量的H2O2溶液的作用是__ 。
(2)从FeCl3溶液制得FeCl3·6H2O晶体的操作步骤是加入__ 后__ 、过滤、洗涤、干燥。
(3)试写出吸收塔中反应的离子方程式:___ 。
(4)捕集器温度超过673K时,存在相对分子质量为325的铁的氯化物,该物质的分子式(相对原子质量:Cl-35.5、Fe-56)为__ 。
(5)FeCl3的质量分数通常可用碘量法测定:称取mg无水氯化铁样品,溶于稀盐酸,配制成100mL溶液;取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入几滴淀粉溶液,并用cmol·L-1Na2S2O3溶液滴定,消耗VmL(已知:I2+2 =2I-+
=2I-+ )。
)。
①滴定终点的现象是__ ;
②样品中氯化铁的质量分数为__ 。

已知:(1)无水FeCl3的熔点为555K、沸点为588K。
(2)废铁屑中的杂质不与盐酸反应。
(3)不同温度下六水合氯化铁在水中的溶解度如下:
温度/℃ | 0 | 20 | 80 | 100 |
溶解度(g/100gH2O) | 74.4 | 91.8 | 525.8 | 535.7 |
I.打开弹簧夹K1,关闭活塞K2,并打开活塞a,缓慢滴加盐酸;
II.当装置A中不产生气泡时,关闭弹簧夹K1,打开活塞K2,当A中溶液完全进入烧杯后关闭活塞a;
III.将烧杯中溶液经过一系列操作后得到FeCl3·6H2O晶体。
请回答:
(1)烧杯中足量的H2O2溶液的作用是
(2)从FeCl3溶液制得FeCl3·6H2O晶体的操作步骤是加入
(3)试写出吸收塔中反应的离子方程式:
(4)捕集器温度超过673K时,存在相对分子质量为325的铁的氯化物,该物质的分子式(相对原子质量:Cl-35.5、Fe-56)为
(5)FeCl3的质量分数通常可用碘量法测定:称取mg无水氯化铁样品,溶于稀盐酸,配制成100mL溶液;取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入几滴淀粉溶液,并用cmol·L-1Na2S2O3溶液滴定,消耗VmL(已知:I2+2
 =2I-+
=2I-+ )。
)。①滴定终点的现象是
②样品中氯化铁的质量分数为
您最近一年使用:0次
名校
3 . 下列各项中操作或现象能达到预期实验目的的是
| 实验目的 | 操作或现象 | |
| A | 分离Fe2O3、Al2O3 | 将混合物置于足量NaOH溶液中,然后依次进行过滤、洗涤、蒸发、灼烧四项操作 |
| B | 验证FeCl3与KI的反应是可逆反应 | 向1ml 0.1mol/L FeCl3溶液中滴加5mL0.1 mol/L KI溶液,充分反应后,取少许混合液滴加KSCN溶液 |
| C | 确定FeCl2是否完全变质 | 取少量的FeCl2样品于试管中,逐滴加入酸性高锰酸钾溶液 |
| D | 除去Fe粉中的I2 | 加热使I2升华 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-11-02更新
|
560次组卷
|
4卷引用:吉林省白城市洮南一中2021届高三上学期第三次月考化学试题
吉林省白城市洮南一中2021届高三上学期第三次月考化学试题吉林省吉林市2021届高三上学期第一次调研考试化学试题(已下线)第15单元 实验设计与评价(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷吉林省长春外国语学校2021届高三上学期期末考试化学试题
名校
解题方法
4 . 硫酸亚铁的用途广泛,可以制备下图所示物质,下列说法错误的是
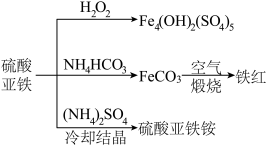

| A.Fe4(OH)2(SO4)5属于碱式盐,可用作净水剂 |
B.与足量NH4HCO3反应的离子方程式为:2 +Fe2+═FeCO3↓+CO2↑+H2O +Fe2+═FeCO3↓+CO2↑+H2O |
| C.可用稀硫酸和K3[Fe(CN)6]溶液检验铁红中是否含有FeCO3 |
| D.“冷却结晶”后的操作是过滤,“煅烧”操作的主要仪器有酒精灯、蒸发皿、玻璃棒 |
您最近一年使用:0次
2020-08-24更新
|
359次组卷
|
6卷引用:吉林省通榆县第一中学2021届高三上学期第二次月考化学试题
名校
解题方法
5 . 化学是以一门实验为基础的自然科学,许多实验有丰富的颜色变化,有关实验的颜色变化有错误的是
| A.向FeSO4和KSCN的混合溶液中滴加少量的新制氯水,溶液由浅绿色变为红色 |
| B.向FeSO4中滴加NaOH溶液,沉淀的颜色由白色迅速变为灰绿色,最后变为红褐色 |
| C.向Fe(NO3)2溶液中滴加稀硫酸,能使溶液由浅绿色变为棕黄色 |
| D.向FeSO4中滴加少量酸性高锰酸钾溶液,能使溶液由浅绿色变为浅紫红色 |
您最近一年使用:0次
2020-03-23更新
|
79次组卷
|
2卷引用:吉林省洮南市第一中学2020-2021学年高二上学期期中考试化学试题
名校
6 . 下列过程,观察不到颜色变化的是( )
| A.NO气体暴露在空气中 |
| B.往FeCl3溶液中滴入KSCN溶液 |
| C.Cl2通过湿润的有色布条 |
| D.往NaOH溶液中通入CO2 |
您最近一年使用:0次
2020-01-17更新
|
286次组卷
|
7卷引用:吉林省大安市第六中学校2021-2022学年高一下学期期中考试化学试题
解题方法
7 . 常温下,下列各组离子在指定溶液中能大量共存的是( )
A. 的溶液中: 的溶液中: 、 、 、 、 、 、 |
B.由水电离的c(H+)=1×10-14mol/L的溶液中: 、 、 、 、 、 、 |
C.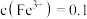  的溶液中: 的溶液中: 、 、 、 、 、 、 |
D. 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
名校
8 . 用过量的FeCl3溶液腐蚀铜制线路板,反应是Cu + 2FeCl3= 2FeCl2 + CuCl2 。取少量腐蚀反应完毕后的混合溶液,加入一定量的铁粉充分搅拌,发现仍有固体存在。则下列判断不正确 的是( )
| A.氧化性Fe3+ > Cu2+ | B.剩余固体中一定含Cu |
| C.有固体存在的溶液中一定无Cu2+ | D.有固体存在的溶液中一定含Fe2+ |
您最近一年使用:0次
2019-11-18更新
|
840次组卷
|
6卷引用:吉林省白城市洮南市第一中学2020-2021学年高一上学期第一次月考化学试题
名校
9 . 下列离子方程式正确的是
A.向明矾溶液中逐滴滴入Ba(OH)2溶液,至沉淀质量最大时反应为:2Al3++3 +3Ba2++6OH﹣=3BaSO4↓+2Al(OH)3↓ +3Ba2++6OH﹣=3BaSO4↓+2Al(OH)3↓ |
| B.氯化铁溶液腐蚀铜电路板:Cu+Fe3+=Fe2+ +Cu2+ |
| C.已知:2Br﹣+Cl2=2Cl﹣+Br2,Br2+2Fe2+=2Fe3++2Br﹣,向含0.2molFeBr2的溶液中通入标准状况下3.36LCl2时,发生的反应为:4Fe2++2Br﹣+3Cl2=4Fe3++Br2+6Cl﹣ |
D.向NaHSO4中滴入Ba(OH)2溶液至恰好显中性:H++ +Ba2++OH﹣=H2O+BaSO4↓ +Ba2++OH﹣=H2O+BaSO4↓ |
您最近一年使用:0次
2019-07-20更新
|
1539次组卷
|
6卷引用:吉林省白城市洮南市第一中学2021届高三上学期第一次月考化学试题
真题
名校
10 . 下列实验现象与实验操作不相匹配的是
| 实验操作 | 实验现象 | |
| A | 向盛有高锰酸钾酸性溶液的试管中通入足量的乙烯后静置 | 溶液的紫色逐渐褪去,静置后溶液分层 |
| B | 将镁条点燃后迅速伸入集满CO2的集气瓶 | 集气瓶中产生浓烟并有黑色颗粒产生 |
| C | 向盛有饱和硫代硫酸钠溶液的试管中滴加稀盐酸 | 有刺激性气味气体产生,溶液变浑浊 |
| D | 向盛有FeCl3溶液的试管中加过量铁粉,充分振荡后加1滴KSCN溶液 | 黄色逐渐消失,加KSCN后溶液颜色不变 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-06-09更新
|
16475次组卷
|
43卷引用:吉林省白城市通榆县第一中学2020届高三上学期第三次月考化学试题
吉林省白城市通榆县第一中学2020届高三上学期第三次月考化学试题吉林省白城市2020-2021学年高二下学期期末考试化学试题2019年全国统一考试化学试题(新课标Ⅱ)安徽省黄山市屯溪第一中学2019-2020学年高二上学期入学摸底考试化学试题安徽省阜阳市颍上二中等三校2020届高三上学期入学考试化学试题黑龙江省哈尔滨市呼兰区第一中学2020届高三上学期第一次(9月)月考化学试题(已下线)专题10.2 物质的分离、提纯、检验与鉴别(练)-《2020年高考一轮复习讲练测》(已下线)专题10.2 物质的分离、提纯、检验与鉴别(讲)-《2020年高考一轮复习讲练测》河南省南阳市2020届高三上学期期中质量评估化学试题四川省南充高级中学2019-2020学年高二12月月考化学试题天津市西青区2020届高三上学期期末考试化学试题浙江省温州市龙湾中学2019-2020学年高二下学期第1次居家月考化学试题西藏自治区林芝市第二高级中学2020届高三上学期第一次月考理科综合化学试题四川省成都实验中学2021届高三上学期入学考试化学试题(已下线)第02讲 物质的分离和提纯(精讲)——2021年高考化学一轮复习讲练测(已下线)小题必刷13 镁及其化合物——2021年高考化学一轮复习小题必刷(通用版)(已下线)小题必刷15 铁、铜及其化合物——2021年高考化学一轮复习小题必刷(通用版)(已下线)专题10 化学实验基础——备战2021年高考化学纠错笔记(已下线)解密11 化学实验(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密11 化学实验(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)小题05 表格型实验选择题(侧重实验原理、操作、现象结论) ——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)押全国卷理综第9题 化学实验基础-备战2021年高考化学临考题号押题(课标全国卷)河南省新乡县高级中学2020-2021学年高一下学期第二次月考化学试题(已下线)考点32 化学实验方案设计与评价-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点35 化学实验方案的设计与评价-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)课时53 简单实验方案的设计与评价-2022年高考化学一轮复习小题多维练(全国通用)广西罗城仫佬族自治县高级中学2021-2022学年高二上学期开学检测化学试题(已下线)第28讲 物质的分离、提纯、检验与鉴别(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)解密11 化学实验基础(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密11 化学实验(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题05 化学基础实验—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)卷13 化学基础实验(检验、鉴别、分离、提纯)-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)押全国卷理综第9题 化学实验基础-备战2022年高考化学临考题号押题(课标全国卷)(已下线)查补易混易错点08 化学实验基础-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题12化学实验方案的设计与评价-五年(2018~2022)高考真题汇编(全国卷)辽宁省凌源市实验中学2021-2022学年高一下学期6月月考化学试题(已下线)第26讲 物质的分离、提纯、检验与鉴别(讲)-2023年高考化学一轮复习讲练测(新教材新高考)宁夏银川市第六中学2022-2023学年高三上学期第二次月考化学试题黑龙江省牡丹江市第三高级中学2022-2023学年高三上学期第三次月考化学试题陕西省渭南中学2023届高三上学期第二次质量调研化学试题(已下线)第一部分 二轮专题突破 专题18 物质检验、鉴别简单实验方案的设计及评价(已下线)专题14 化学实验方案的设计与评价(已下线)T10-实验方案的设计与评价



