1 . FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小。常见水处理剂还有高铁酸盐及ClO2,请回答下列问题:
(1)FeCl3可以用来刻蚀铜箔制造电路板,写出对应离子方程式________________ ;高铁酸盐是一种绿色净水剂,其有效成分是高铁酸根FeO 。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:
。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:_______________
(2)ClO2是一种高效、低毒的消毒剂,工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为___________
(3)漂白粉在工业中常用氯气通入石灰乳来制备,写出对应化学方程式_________________
(4)描述实验室制备氢氧化铁胶体的方法______________ ;写出对应的化学方程式_______________
(5)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3,配平下列反应:_____ 。
___________ClO + _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
+ _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
(1)FeCl3可以用来刻蚀铜箔制造电路板,写出对应离子方程式
 。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:
。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:(2)ClO2是一种高效、低毒的消毒剂,工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为
(3)漂白粉在工业中常用氯气通入石灰乳来制备,写出对应化学方程式
(4)描述实验室制备氢氧化铁胶体的方法
(5)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3,配平下列反应:
___________ClO
 + _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
+ _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
您最近一年使用:0次
名校
解题方法
2 . 将Fe,Cu, ,
, 和
和 盛于同一容器中充分反应,如Fe有剩余,则容器中只能有
盛于同一容器中充分反应,如Fe有剩余,则容器中只能有
 ,
, 和
和 盛于同一容器中充分反应,如Fe有剩余,则容器中只能有
盛于同一容器中充分反应,如Fe有剩余,则容器中只能有A.Cu, | B. , , | C.Cu, ,Fe ,Fe | D.Cu, ,Fe ,Fe |
您最近一年使用:0次
2022-12-01更新
|
77次组卷
|
2卷引用:宁夏育才中学2022-2023学年高一下学期开学考试化学试题
名校
解题方法
3 . 铁是人类较早使用的金属之一,铁及其化合物之间的相互转化作用可用下式表示:
I.回答下列有关问题:
(1)若炽热的钢水不慎倒入有水的模具中,发生的反应为_______ 。
(2)电子工业需用30%的 溶液腐蚀敷在绝缘板上的铜,生成
溶液腐蚀敷在绝缘板上的铜,生成 和
和 ,制造印刷电路板。写出
,制造印刷电路板。写出 溶液腐蚀铜的离子反应方程式:
溶液腐蚀铜的离子反应方程式:_______ 。检验反应后溶液中还存在 的试剂是
的试剂是_______ 。
II.现有五种溶液,分别含下列离子:① ,②
,② ,③
,③ ,④
,④ ,⑤
,⑤ 。
。
(3)写出符合下列条件的离子符号:既能被氧化又能被还原的离子是_______ (填写离子符号),加铁粉后溶液增重的是_______ (填写离子符号)
(4)向 的溶液中滴加NaOH溶液,现象是
的溶液中滴加NaOH溶液,现象是_______ ,其中的反应为(用化学反应方程式表示):_______ ,_______ 。
I.回答下列有关问题:
(1)若炽热的钢水不慎倒入有水的模具中,发生的反应为
(2)电子工业需用30%的
 溶液腐蚀敷在绝缘板上的铜,生成
溶液腐蚀敷在绝缘板上的铜,生成 和
和 ,制造印刷电路板。写出
,制造印刷电路板。写出 溶液腐蚀铜的离子反应方程式:
溶液腐蚀铜的离子反应方程式: 的试剂是
的试剂是II.现有五种溶液,分别含下列离子:①
 ,②
,② ,③
,③ ,④
,④ ,⑤
,⑤ 。
。(3)写出符合下列条件的离子符号:既能被氧化又能被还原的离子是
(4)向
 的溶液中滴加NaOH溶液,现象是
的溶液中滴加NaOH溶液,现象是
您最近一年使用:0次
4 . 回答下列问题。
(1)实验室常用如图所示装置来制取和观察 在空气中被氧化时颜色的变化。
在空气中被氧化时颜色的变化。
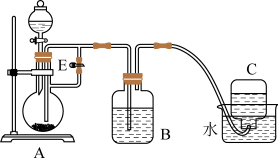
实验时在A中加入铁屑和稀硫酸,B中加入一定量的NaOH溶液,则A中发生的反应的离子方程式是:_________________ 。实验开始时先将活塞E___________ (填“打开”或“关闭”),C中收集到气体的主要成分是__________ 。实验结束后拔去装置B中的橡皮塞,使空气进入,装置B中发生的现象为_________________________ 。
(2)从制造印刷电路板的腐蚀废液(主要含 、
、 、
、 )中回收铜,并重新获得
)中回收铜,并重新获得 溶液,处理流程如图所示:
溶液,处理流程如图所示:
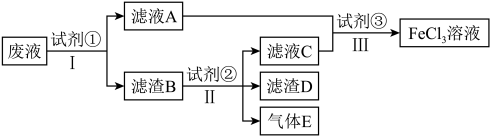
已知试剂①为铁,试剂②为稀盐酸,则滤渣B的成分为___________ ,若试剂③为氯水,则步骤Ⅱ的离子反应方程式为___________ ,检验废液中 存在的最佳试剂是
存在的最佳试剂是___________ (填标号),检验时实验现象为___________ 。
A.氢氧化钠溶液 B.酸性 溶液 C.氯水 D.KSCN溶液
溶液 C.氯水 D.KSCN溶液
(1)实验室常用如图所示装置来制取和观察
 在空气中被氧化时颜色的变化。
在空气中被氧化时颜色的变化。
实验时在A中加入铁屑和稀硫酸,B中加入一定量的NaOH溶液,则A中发生的反应的离子方程式是:
(2)从制造印刷电路板的腐蚀废液(主要含
 、
、 、
、 )中回收铜,并重新获得
)中回收铜,并重新获得 溶液,处理流程如图所示:
溶液,处理流程如图所示:
已知试剂①为铁,试剂②为稀盐酸,则滤渣B的成分为
 存在的最佳试剂是
存在的最佳试剂是A.氢氧化钠溶液 B.酸性
 溶液 C.氯水 D.KSCN溶液
溶液 C.氯水 D.KSCN溶液
您最近一年使用:0次
名校
解题方法
5 . 根据所学知识,完成下列问题。
(1)取少量 粉末于试管中加入适量盐酸,反应后得到的溶液呈
粉末于试管中加入适量盐酸,反应后得到的溶液呈______ 色。将该溶液中滴入NaOH溶液,可以观察到____________ 的现象,反应的离子反应方程式为________________ 。
(2)在小烧杯中加入25mL蒸馏水,加热至沸腾后,向沸水中加入2mL 溶液,继续煮沸至溶液呈红褐色,即可制得
溶液,继续煮沸至溶液呈红褐色,即可制得 胶体。该过程发生的化学反应方程式为:
胶体。该过程发生的化学反应方程式为:_______________________ ,用激光笔照射烧杯中的液体,可以看到________________ 。用制得的 胶体进行下列实验:
胶体进行下列实验:
①将其装入U形管中,用石墨电极接通直流电,通电一段时间后,发现阴极附近的颜色加深,这种现象称为___________________ 。
②向其中滴入过量稀硫酸,先产生红褐色沉淀,后沉淀全部溶解,其原因是_____________ 。
③提纯此分散系常用的方法是___________ 。
(1)取少量
 粉末于试管中加入适量盐酸,反应后得到的溶液呈
粉末于试管中加入适量盐酸,反应后得到的溶液呈(2)在小烧杯中加入25mL蒸馏水,加热至沸腾后,向沸水中加入2mL
 溶液,继续煮沸至溶液呈红褐色,即可制得
溶液,继续煮沸至溶液呈红褐色,即可制得 胶体。该过程发生的化学反应方程式为:
胶体。该过程发生的化学反应方程式为: 胶体进行下列实验:
胶体进行下列实验:①将其装入U形管中,用石墨电极接通直流电,通电一段时间后,发现阴极附近的颜色加深,这种现象称为
②向其中滴入过量稀硫酸,先产生红褐色沉淀,后沉淀全部溶解,其原因是
③提纯此分散系常用的方法是
您最近一年使用:0次
名校
解题方法
6 . 为除去下列物质中所含的杂质,选用的实验操作方法正确的是
A. 溶液( 溶液( ):加入稍过量的铁粉,过滤 ):加入稍过量的铁粉,过滤 |
B. (HCl气体):通过足量的NaOH溶液 (HCl气体):通过足量的NaOH溶液 |
C. (HCl):通过盛有饱和 (HCl):通过盛有饱和 溶液的洗气瓶 溶液的洗气瓶 |
D. 固体( 固体( ):加热至固体质量不再变化 ):加热至固体质量不再变化 |
您最近一年使用:0次
名校
解题方法
7 . 某矿石样品中可能含铁,为确定其成分,进行如下操作:
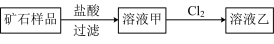
列有关说法正确的是

列有关说法正确的是
A.向溶液甲中滴加KSCN溶液,溶液颜色变红,则原矿石样品中存在 |
B.向溶液乙中滴加KSCN溶液,溶液颜色变红,则原矿石样品中存在 |
| C.向溶液乙中滴加少量氢氧化钠溶液,一定出现红褐色沉淀 |
| D.该矿石一定为赤铁矿 |
您最近一年使用:0次
2022-11-15更新
|
208次组卷
|
3卷引用:宁夏六盘山高级中学 2022-2023学年高一上学期期中联考化学试题
名校
解题方法
8 . 铁元素在地壳中的含量仅次于氧、硅和铝居第四位。铁及其化合物应用广泛。高铁酸钾( )是种新型、高效、多功能水处理剂,其制备原理如下:
)是种新型、高效、多功能水处理剂,其制备原理如下: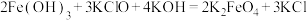
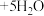 。下列铁及其化合物的性质与用途具有对应关系的是
。下列铁及其化合物的性质与用途具有对应关系的是
 )是种新型、高效、多功能水处理剂,其制备原理如下:
)是种新型、高效、多功能水处理剂,其制备原理如下: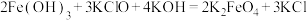
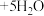 。下列铁及其化合物的性质与用途具有对应关系的是
。下列铁及其化合物的性质与用途具有对应关系的是A. 中铁的化合价为+6,有还原性,可用于净水 中铁的化合价为+6,有还原性,可用于净水 |
B. 受热易分解,可用于吸附杂质 受热易分解,可用于吸附杂质 |
C. 有氧化性,可用于制作印刷铜电路板 有氧化性,可用于制作印刷铜电路板 |
D. 能与盐酸反应,可用于制作油漆涂料 能与盐酸反应,可用于制作油漆涂料 |
您最近一年使用:0次
2022-11-15更新
|
245次组卷
|
2卷引用:宁夏六盘山高级中学 2022-2023学年高一上学期期中联考化学试题
9 . 铬及其化合物有许多独特的性质和用途。如炼钢时加入一定量的铬可得到不锈钢, 是实验中常用的强氧化剂之一,从含有铬、锌、钢、铁、镉(Cd)、钴(Co)等单质的工业废料回收铬的生产流程如图:
是实验中常用的强氧化剂之一,从含有铬、锌、钢、铁、镉(Cd)、钴(Co)等单质的工业废料回收铬的生产流程如图:

几种金属离子生成氢氧化物沉淀的 见表:
见表:
请回答下列问题:
(1)写出提高酸浸速率的措施_______ (写出两点)。
(2)酸浸时形成的金属离子的价态均相同,料渣中含有大量的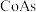 合金,写出除钴时反应的离子方程式
合金,写出除钴时反应的离子方程式_______ 。
(3)若仅从试剂的经济角度考虑,试剂X最好是_______ ,如果试剂X是 ,请写出其氧化
,请写出其氧化 的离子反应方程式
的离子反应方程式_______ 。
(4)已知氧化过程中铁、铬形成的离子均被完全氧化,则调 时应将
时应将 控制在
控制在_______ 范围内,单质铬与试剂Y反应时,反应中二者消耗量
_______ 。
(5)设计实验检验废液中是否含有 :
:_______ 。
 是实验中常用的强氧化剂之一,从含有铬、锌、钢、铁、镉(Cd)、钴(Co)等单质的工业废料回收铬的生产流程如图:
是实验中常用的强氧化剂之一,从含有铬、锌、钢、铁、镉(Cd)、钴(Co)等单质的工业废料回收铬的生产流程如图:
几种金属离子生成氢氧化物沉淀的
 见表:
见表:| 氢氧化物 |  |  | 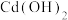 |  |
开始沉淀的 | 1.5 | 8 | 7.2 | 6 |
沉淀完全的 | 3.3 | 12 | 9.5 | 8 |
(1)写出提高酸浸速率的措施
(2)酸浸时形成的金属离子的价态均相同,料渣中含有大量的
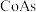 合金,写出除钴时反应的离子方程式
合金,写出除钴时反应的离子方程式(3)若仅从试剂的经济角度考虑,试剂X最好是
 ,请写出其氧化
,请写出其氧化 的离子反应方程式
的离子反应方程式(4)已知氧化过程中铁、铬形成的离子均被完全氧化,则调
 时应将
时应将 控制在
控制在
(5)设计实验检验废液中是否含有
 :
:
您最近一年使用:0次

 溶液保存时,通常在溶液中加少量的单质铁
溶液保存时,通常在溶液中加少量的单质铁

