名校
解题方法
1 . 以铁为阳极,铜为阴极,对足量的NaOH溶液进行电解。一段时间后得到4molFe(OH)3沉淀,此间共消耗的水的物质的量为
| A.8mol | B.10mol | C.11mol | D.12mol |
您最近一年使用:0次
2021-08-07更新
|
105次组卷
|
2卷引用:河北省顺平县中学2021-2022学年高二上学期第一次月考化学试题
解题方法
2 . 下列关于铁的叙述正确的是
①不能通过化合反应制得 和
和 ②铁在潮湿的空气中容易生锈 ③铁和水蒸气在高温作用下生成
②铁在潮湿的空气中容易生锈 ③铁和水蒸气在高温作用下生成 ④过量铁在氯气中燃烧生成
④过量铁在氯气中燃烧生成 ⑤铁能在氧气中剧烈燃烧生成
⑤铁能在氧气中剧烈燃烧生成
①不能通过化合反应制得
 和
和 ②铁在潮湿的空气中容易生锈 ③铁和水蒸气在高温作用下生成
②铁在潮湿的空气中容易生锈 ③铁和水蒸气在高温作用下生成 ④过量铁在氯气中燃烧生成
④过量铁在氯气中燃烧生成 ⑤铁能在氧气中剧烈燃烧生成
⑤铁能在氧气中剧烈燃烧生成
| A.②③⑤ | B.①②④ | C.②④⑤ | D.③④⑤ |
您最近一年使用:0次
3 . 已知:A为淡黄色固体,T、R为两种常见的前途很广金属单质,D是具有磁性的黑色晶体,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体。

(1)写出下列物质的化学式A___ ;H___ ;N___ 。
(2)按要求写下列反应方程式:
①检验W中阳离子的离子方程式___ 。
②H在潮湿空气中变成M的化学方程式___ 。
③B与R反应生成N的离子反应方程式___ 。

(1)写出下列物质的化学式A
(2)按要求写下列反应方程式:
①检验W中阳离子的离子方程式
②H在潮湿空气中变成M的化学方程式
③B与R反应生成N的离子反应方程式
您最近一年使用:0次
名校
4 . 下列物质能通过化合反应直接制得的是
①FeCl2 ②H2SO4 ③NH4Cl ④HCl ⑤Fe(OH)3 ⑥FeCl3
①FeCl2 ②H2SO4 ③NH4Cl ④HCl ⑤Fe(OH)3 ⑥FeCl3
| A.只有①②③⑥ | B.只有②③⑤⑥ |
| C.只有①③④ | D.全部 |
您最近一年使用:0次
名校
解题方法
5 . 现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。
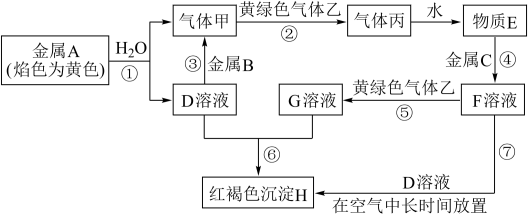
请根据以上信息完成下列各题:
(1)写出下列物质的化学式:C___ ,丙___ 。
(2)写出实验室制备黄绿色气体乙的化学方程式:___ ,过程⑦可能观察到的实验现象是:__ 。
(3)写出过程⑦涉及的化学方程式___ ,___ 。
(4)反应③中的离子方程式是___ 。

请根据以上信息完成下列各题:
(1)写出下列物质的化学式:C
(2)写出实验室制备黄绿色气体乙的化学方程式:
(3)写出过程⑦涉及的化学方程式
(4)反应③中的离子方程式是
您最近一年使用:0次
2021-04-29更新
|
245次组卷
|
3卷引用:河北省石家庄市新华中学2020-2021学年高三上学期10月月考化学试题
6 . 对下列事实的解释正确的是
| A.用NaOH和铝粉作家庭管道疏通剂,说明NaOH溶液和铝粉反应能产生大量气体 |
| B.葡萄酒中添加二氧化硫以起到杀菌、抗氧化作用说明二氧化硫是种无毒的气体 |
| C.氢氧化亚铁在空气中不稳定,会转化成氢氧化铁说明氢氧化亚铁具有强氧化性 |
| D.在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有吸水性 |
您最近一年使用:0次
2021-03-30更新
|
162次组卷
|
2卷引用:河北省衡水市第十四中学2020-2021学年高一下学期一调考试化学试题
名校
7 . 铁及其化合物在生产、生活中有着广泛的应用。
I.钢(一种铁碳合金)是用量最大、用途最广的合金。钢中碳的含量范围为_______ 。
a.4.3%~5% b.2%~4.3% c.0.03%~2%
II.FeSO4可作补血剂,用于治疗缺铁性贫血症。用 FeSO4溶液制备 Fe(OH)2的操作是用长滴管吸取不含 O2的 NaOH 溶液,插入 FeSO4溶液液面下,再挤出 NaOH 溶液。这样操作的原因是为了防止 Fe(OH)2被氧化,写出其被氧化的化学反应方程式_______ 。
III.高铁酸钾(K2FeO4)是一种新型、高效、无毒的多功能水处理剂。查阅资料已知:K2FeO4为紫色固体,微溶于KOH溶液,具有强氧化性,在酸性或中性溶液自身发生氧化还原生成Fe3+,并快速产生 O2,在碱性溶液中较稳定。
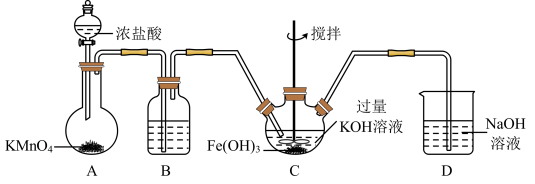
(1)制备K2FeO4
①在装置A中发生的化学反应中 HCl显示出来的性质为_______ 。
②C为制备K2FeO4装置,次氯酸钾与氢氧化铁在碱性环境中反应生成K2FeO4,该氧化还原反应中氧化剂与还原剂的物质的量之比为_______ 。
(2)探究K2FeO4的性质
取 C中浅紫红色溶液,加入稀硫酸,产生黄绿色气体,得溶液 a,经检验气体中含有 Cl2。为证明K2FeO4能否氧化 Cl-而产生 Cl2,设计如下方案:取少量溶液 a,滴加_______ 溶液至过量,溶液呈红色。由方案中溶液变红可知 a中含有 Fe3+,该离子的产生不能判断一定是由 K2FeO4被 Cl-还原而形成的,原因是_______ 。
(3)使用时经常通过测定高铁酸钾的纯度来判断其是否变质。K2FeO4在硫酸溶液中反应如下:
①完成并配平离子方程式:_______
_______FeO +_______H+=_______Fe3++_______O2↑+_______H2O
+_______H+=_______Fe3++_______O2↑+_______H2O
②现取C中洗涤并干燥后的样品10g,加入稀硫酸,收集到0.672L气体(标准状况)。则样品中高铁酸钾的质量分数为_______ 。(计算结果保留到 0.1%)
I.钢(一种铁碳合金)是用量最大、用途最广的合金。钢中碳的含量范围为
a.4.3%~5% b.2%~4.3% c.0.03%~2%
II.FeSO4可作补血剂,用于治疗缺铁性贫血症。用 FeSO4溶液制备 Fe(OH)2的操作是用长滴管吸取不含 O2的 NaOH 溶液,插入 FeSO4溶液液面下,再挤出 NaOH 溶液。这样操作的原因是为了防止 Fe(OH)2被氧化,写出其被氧化的化学反应方程式
III.高铁酸钾(K2FeO4)是一种新型、高效、无毒的多功能水处理剂。查阅资料已知:K2FeO4为紫色固体,微溶于KOH溶液,具有强氧化性,在酸性或中性溶液自身发生氧化还原生成Fe3+,并快速产生 O2,在碱性溶液中较稳定。

(1)制备K2FeO4
①在装置A中发生的化学反应中 HCl显示出来的性质为
②C为制备K2FeO4装置,次氯酸钾与氢氧化铁在碱性环境中反应生成K2FeO4,该氧化还原反应中氧化剂与还原剂的物质的量之比为
(2)探究K2FeO4的性质
取 C中浅紫红色溶液,加入稀硫酸,产生黄绿色气体,得溶液 a,经检验气体中含有 Cl2。为证明K2FeO4能否氧化 Cl-而产生 Cl2,设计如下方案:取少量溶液 a,滴加
(3)使用时经常通过测定高铁酸钾的纯度来判断其是否变质。K2FeO4在硫酸溶液中反应如下:
①完成并配平离子方程式:
_______FeO
 +_______H+=_______Fe3++_______O2↑+_______H2O
+_______H+=_______Fe3++_______O2↑+_______H2O②现取C中洗涤并干燥后的样品10g,加入稀硫酸,收集到0.672L气体(标准状况)。则样品中高铁酸钾的质量分数为
您最近一年使用:0次
8 . 下列有关实验的说法正确的是
| A.保存氢氟酸时,氢氟酸需贮存在带橡胶塞的细口玻璃瓶中 |
| B.用试管加热碳酸氢钠固体时,应使试管口向上倾斜 |
| C.用Na2O2或H2O2作反应物制氧气时,可选择相同的气体发生装置 |
| D.向NaOH溶液中滴入FeSO4溶液,出现颜色变化与氧化还原反应无关 |
您最近一年使用:0次
名校
解题方法
9 . 下面是制备Fe(OH)2白色沉淀的几种方案。请回答下列问题:
(1)用不含Fe3+的FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应制备Fe(OH)2。
①用硫酸亚铁晶体配制上述FeSO4溶液时还需要加入铁粉,其目的是_________________ (用离子方程式表示)。
②除去蒸馏水中溶解的O2常采用___________ 的方法。
③生成Fe(OH)2白色沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,发生反应的离子方程式___________ 。
(2)在如图所示的装置中,用NaOH溶液、铁粉、稀H2SO4等试剂制备。

①仪器a的名称是___________ 。
②关闭K3,打开K1和K2,向仪器c中加入适量稀硫酸,关闭K2,写出装置c中发生反应的离子方程式___________ 。同时c中有气体产生,该气体的作用是___________ 。
③当仪器b中产生均匀气泡后的操作是___________ 。写出仪器c、d中可能出现的实验现象___________ 。
(1)用不含Fe3+的FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应制备Fe(OH)2。
①用硫酸亚铁晶体配制上述FeSO4溶液时还需要加入铁粉,其目的是
②除去蒸馏水中溶解的O2常采用
③生成Fe(OH)2白色沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,发生反应的离子方程式
(2)在如图所示的装置中,用NaOH溶液、铁粉、稀H2SO4等试剂制备。

①仪器a的名称是
②关闭K3,打开K1和K2,向仪器c中加入适量稀硫酸,关闭K2,写出装置c中发生反应的离子方程式
③当仪器b中产生均匀气泡后的操作是
您最近一年使用:0次
2021-01-01更新
|
212次组卷
|
2卷引用:河北省邢台市巨鹿中学2020-2021学年高一上学期第三次月考化学试题
名校
解题方法
10 . 下列叙述不正确的是
| A.NaHCO3、Fe(OH)3、FeCl2 均可通过化合反应生成 |
| B.电解、电离、电镀均需要通电才可进行 |
| C.CO2、N2O5、SO2 均为酸性氧化物 |
| D.从铝土矿中获得氧化铝,电解熔融的氧化铝得到铝 |
您最近一年使用:0次



