名校
解题方法
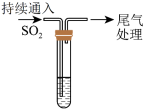
1 . 某校兴趣小组对SO2与新制Cu(OH)2悬浊液的反应进行探究,实验如下:
已知:CuCl为白色固体,难溶于水,能溶于浓盐酸。下列说法不正确的是
| 装置 |
| |
| 序号 | 试管中的药品 | 现象 |
| 实验Ⅰ | 1.5mL1mol·L-1CuSO4溶液和3.5mL1mol·L-1NaOH溶液混合 | 开始时有砖红色沉淀出现,一段时间后,砖红色沉淀消失,静置,试管底部有少量紫红色固体,溶液呈绿色 |
| 实验Ⅱ | 1.5mL1mol·L-1CuCl2溶液和3.5mL1mol·L-1NaOH溶液混合 | 开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈绿色 |
| A.取少量Cu2O固体于试管中,加入5mL0.1mol·L-1NaOH溶液,持续通入SO2,若试管底部有少量紫红色固体,溶液呈绿色,证明实验Ⅰ中砖红色沉淀为Cu2O |
| B.将实验Ⅱ中白色沉淀洗涤干净后,加入浓盐酸,沉淀溶解,然后加入蒸馏水,产生白色沉淀,证明白色沉淀为CuCl |
| C.实验Ⅱ与实验Ⅰ现象不同是因为阴离子不同造成的 |
D.实验Ⅰ、Ⅱ中不一定生成了SO |
您最近一年使用:0次
名校
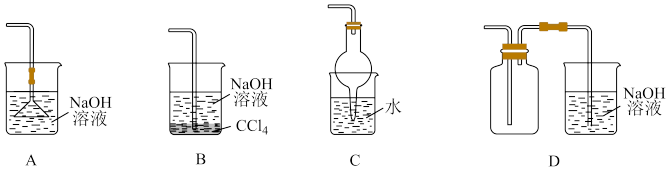
2 . 用如图装置(搅拌装置略)探究溶液离子浓度变化,灯光变化不可能 出现“亮→暗(或灭)→亮”现象的是
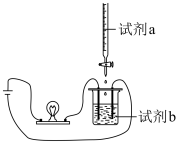

| 选项 | A | B | C | D |
| 试剂a |  |  |  |  |
| 试剂b |  |  |  |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 胆矾(CuSO4·5H2O)是一种重要化工原料。某研究小组以生锈的铜屑为原料(主要成分是Cu,含有少量的油污、CuO、CuCO3、Cu(OH)2)制备胆矾流程如图,下列说法不正确的是
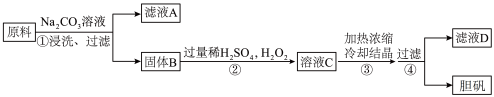

| A.步骤②中包含了氧化还原反应,氧化剂与还原剂的物质的量比为1∶1 |
| B.步骤③④得到的胆矾晶体,可以用水进行洗涤干燥 |
| C.往滤液D中加入淀粉-KI溶液,无明显现象 |
| D.将25g胆矾晶体与75g水混合,配制得到质量分数为16%的硫酸铜溶液 |
您最近一年使用:0次
解题方法
4 . SO2在生产生活中有重要作用。
(1)实验室用Na2SO3和浓硫酸制取SO2的化学方程式为_________ 。
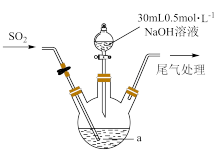
(2)下列装置适用于实验室对SO2进行尾气吸收的是_________ (填标号)。
(3)将SO2通入紫色石蕊溶液中,可观察到的现象是_________ 。
(4)某合作学习小组为探究SO2与新制Cu(OH)2悬浊液反应,设计并进行实验如下:
①经检测,实验Ⅰ、Ⅱ所得绿色溶液均能使品红溶液褪色,原因是_________ 。
②查阅资料可知,实验Ⅰ、Ⅱ所得黄色固体为Cu2O,则生成Cu2O的离子方程式为_________ ,(已知:Cu2O在酸性条件下不稳定, )
)
③为探究实验Ⅱ中白色沉淀的成分,该小组同学进行如下实验:
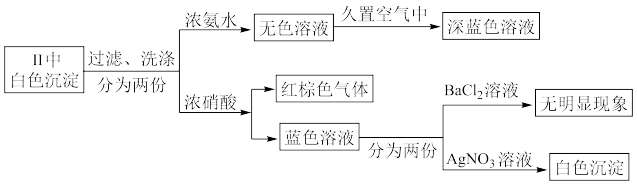
已知:[Cu(NH3)2]+无色,易被氧化为深蓝色[Cu(NH3)4]2+,由上可知,该白色沉淀为_________ (填化学式)。
④根据以上实验可知,SO2与新制Cu(OH)2悬浊液反应,与SO2的用量、_________ 等因素有关。
(1)实验室用Na2SO3和浓硫酸制取SO2的化学方程式为
(2)下列装置适用于实验室对SO2进行尾气吸收的是

(3)将SO2通入紫色石蕊溶液中,可观察到的现象是
(4)某合作学习小组为探究SO2与新制Cu(OH)2悬浊液反应,设计并进行实验如下:
| 装置 | 实验 | a中试剂 | 实验操作 | 通入SO2气体后a中现象 |
 | Ⅰ | 15mL CuSO4溶液 CuSO4溶液 | 先打开分液漏斗活塞,将NaOH溶液全部滴入a中,制得蓝色Cu(OH)2悬浊液;再关闭活塞,打开止水夹,持续通入SO2气体 | 开始可观察到局部有黄色固体生成,待Cu(OH)2全部溶解后,得到绿色溶液和少量紫红色固体。 |
| Ⅱ | 15mL CuCl2溶液 CuCl2溶液 | 开始可观察到局部有黄色固体生成,待Cu(OH)2全部溶解后,得到绿色溶液和大量白色固体, |
②查阅资料可知,实验Ⅰ、Ⅱ所得黄色固体为Cu2O,则生成Cu2O的离子方程式为
 )
)③为探究实验Ⅱ中白色沉淀的成分,该小组同学进行如下实验:

已知:[Cu(NH3)2]+无色,易被氧化为深蓝色[Cu(NH3)4]2+,由上可知,该白色沉淀为
④根据以上实验可知,SO2与新制Cu(OH)2悬浊液反应,与SO2的用量、
您最近一年使用:0次
名校
解题方法
5 . 某工厂的废金属屑中主要成分为Cu、Fe和Al,此外还含有少量 和
和 ,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体
,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体 和胆矾晶体。请回答下列问题:
和胆矾晶体。请回答下列问题:
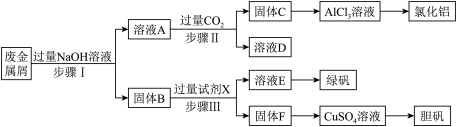
(1)写出步骤I反应的离子方程式__________________________________________________ ;
(2)步骤II中,溶液A中含铝化合物与过量 反应生成固体C的离⼦⽅程式为
反应生成固体C的离⼦⽅程式为____________ ;
(3)在步骤II时,⽤如图装置制取 并通入溶液A中。⼀段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可采取的改进措施是
并通入溶液A中。⼀段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可采取的改进措施是________ 。

(4)步骤III中试剂X是__________ 。
(5)取步骤III所得溶液E,滴加足量NaOH溶液,观察到的现象为__________ ,产生明显现象的化学方程式为__________ 。
 和
和 ,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体
,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体 和胆矾晶体。请回答下列问题:
和胆矾晶体。请回答下列问题:
(1)写出步骤I反应的离子方程式
(2)步骤II中,溶液A中含铝化合物与过量
 反应生成固体C的离⼦⽅程式为
反应生成固体C的离⼦⽅程式为(3)在步骤II时,⽤如图装置制取
 并通入溶液A中。⼀段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可采取的改进措施是
并通入溶液A中。⼀段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可采取的改进措施是
(4)步骤III中试剂X是
(5)取步骤III所得溶液E,滴加足量NaOH溶液,观察到的现象为
您最近一年使用:0次
2022-11-24更新
|
300次组卷
|
2卷引用:天津市第一中学2022-2023学年高一上学期第二次月考化学试题
名校
解题方法
6 . 某小组为了探究 溶液和
溶液和 溶液反应的情况,开展了如下活动。回答下列问题:
溶液反应的情况,开展了如下活动。回答下列问题:
【查阅资料】
①CuCl、CuI为难溶于水的白色固体;
② 在酸性环境中易歧化为Cu和
在酸性环境中易歧化为Cu和 ;
;
③ (无色溶液)
(无色溶液)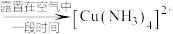 (深蓝色溶液)
(深蓝色溶液)
【理论预测】 溶液和
溶液和 溶液反应的主要含铜产物的可能情况:
溶液反应的主要含铜产物的可能情况:
(1)二者因发生复分解反应生成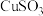 ;二者因发生双水解反应生成
;二者因发生双水解反应生成___________ ;二者因发生氧化还原反应生成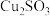 、CuCl;……
、CuCl;……
【实验探究一】 溶液和
溶液和 溶液反应
溶液反应
(2)取少量实验1中已洗净的白色沉淀于试管中,滴加足量浓氨水,先观察到___________ ,反应的离子方程式为___________ ;露置一段时间,又观察到___________ ,证明白色沉淀为CuCl。
【实验探究二】棕黄色沉淀的成分探究
(3)实验1中棕黄色沉淀存在时间较短,难以获得。实验小组将实验1中的 溶液替换为等体积等浓度的
溶液替换为等体积等浓度的___________ 溶液,成功制备了棕黄色沉淀,并进行了如下实验。
(4)实验2中可观察到现象:___________ ,证棕黄色沉淀中含有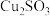 。
。
(5)实验3中因发生了反应___________ 、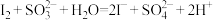 ,使得上层清液呈无色且不能使淀粉溶液变蓝;白色沉淀B是
,使得上层清液呈无色且不能使淀粉溶液变蓝;白色沉淀B是 ,试剂1是
,试剂1是___________ ;据此证明棕黄色沉淀中含有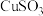 。
。
 溶液和
溶液和 溶液反应的情况,开展了如下活动。回答下列问题:
溶液反应的情况,开展了如下活动。回答下列问题:【查阅资料】
①CuCl、CuI为难溶于水的白色固体;
②
 在酸性环境中易歧化为Cu和
在酸性环境中易歧化为Cu和 ;
;③
 (无色溶液)
(无色溶液)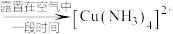 (深蓝色溶液)
(深蓝色溶液)【理论预测】
 溶液和
溶液和 溶液反应的主要含铜产物的可能情况:
溶液反应的主要含铜产物的可能情况:(1)二者因发生复分解反应生成
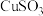 ;二者因发生双水解反应生成
;二者因发生双水解反应生成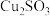 、CuCl;……
、CuCl;……【实验探究一】
 溶液和
溶液和 溶液反应
溶液反应| 编号 | 实验操作 | 实验现象 |
| 1 | 2mL0.2  溶液和1mL0.2 溶液和1mL0.2  溶液混合 溶液混合 | 立即有棕黄色沉淀生成,3min后沉淀颜色变浅并伴有少量白色沉淀产生,再振荡1min后沉淀全部变为白色 |
(2)取少量实验1中已洗净的白色沉淀于试管中,滴加足量浓氨水,先观察到
【实验探究二】棕黄色沉淀的成分探究
(3)实验1中棕黄色沉淀存在时间较短,难以获得。实验小组将实验1中的
 溶液替换为等体积等浓度的
溶液替换为等体积等浓度的| 编号 | 实验操作 |
| 2 | 取少量洗净的裟黄色沉淀于试管中,并加入一定量的稀硫酸 |
| 3 | 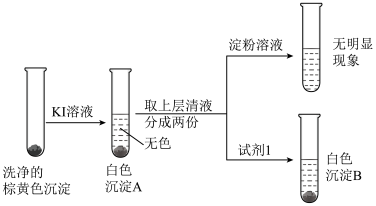 注:实验所用试剂均经过除氧处理 |
(4)实验2中可观察到现象:
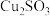 。
。(5)实验3中因发生了反应
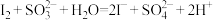 ,使得上层清液呈无色且不能使淀粉溶液变蓝;白色沉淀B是
,使得上层清液呈无色且不能使淀粉溶液变蓝;白色沉淀B是 ,试剂1是
,试剂1是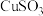 。
。
您最近一年使用:0次
7 . 硫酸亚铁铵是一种重要的化工原料,用途十分广泛。在无机化学工业中,它是制取其它铁化合物的原料,如用于制造氧化铁系颜料、磁性材料、黄血盐和其他铁盐等。
[查阅资料]隔绝空气加热至500℃时硫酸亚铁铵能完全分解,分解产物中含有铁氧化物、硫氧化物、氨气和水蒸气。某化学小组选用如图所示部分装置进行实验(夹持装置略),验证分解产物中含有氨气和水蒸气。
(1)加热之前应该先通氮气,防止空气中的_______ 干扰实验。
(2)所选用装置的正确连接顺序为_______ (填装置序号)。
(3)证明有水蒸气生成的实验现象为_______ 。
(4)证明有氨气生成的实验现象为_______ 。
(5)经检验C 中分解后只有红棕色粉末,用试管取少许与氢碘酸混合后,再加入少量的四氯化碳振荡,下层出现的现象为_______ ,该反应的离子方程式为_______ 。
(6)写出该实验中硫酸亚铁铵受热分解的化学方程式_______ 。
[查阅资料]隔绝空气加热至500℃时硫酸亚铁铵能完全分解,分解产物中含有铁氧化物、硫氧化物、氨气和水蒸气。某化学小组选用如图所示部分装置进行实验(夹持装置略),验证分解产物中含有氨气和水蒸气。

(1)加热之前应该先通氮气,防止空气中的
(2)所选用装置的正确连接顺序为
(3)证明有水蒸气生成的实验现象为
(4)证明有氨气生成的实验现象为
(5)经检验C 中分解后只有红棕色粉末,用试管取少许与氢碘酸混合后,再加入少量的四氯化碳振荡,下层出现的现象为
(6)写出该实验中硫酸亚铁铵受热分解的化学方程式
您最近一年使用:0次
8 . 某实验小组对 溶液分别与
溶液分别与 、
、 溶液的反应进行探究。
溶液的反应进行探究。
已知:Ⅰ.
Ⅱ.
回答下列问题:
(1)推测实验Ⅰ中的无色气体为 ,实验验证:用湿润的品红试纸接近试管口,视察到
,实验验证:用湿润的品红试纸接近试管口,视察到___________ ,将品红试纸在烘箱中低温烘干又观察到___________ 。
(2)推测实验Ⅰ中的白色沉淀为 ,实验验证步骤如下:
,实验验证步骤如下:
①实验Ⅰ完成后,立即过滤、洗涤。
②取少量已洗净的白色沉淀于试管中,滴加足量浓氨水,先观察到___________ ,反应的离子方程式为___________ ;露置一段时间,又观察到___________ 。
(3)对比实验Ⅰ、Ⅱ,提出假设, 增强了
增强了 的氧化性。
的氧化性。
①若假设合理,实物Ⅰ反应的离子方程式为___________ 和 。
。
②用以下实验来验证假设合理,装置如图所示。实验方案:闭合K,电压表的指针偏转至“Y”处;向U形管___________ (补全实验操作及现象)。
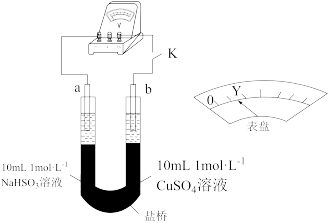
(4)将实验Ⅱ的溶液静置24h或加热后,得到红色沉淀。经检验,红色沉淀中含有 、
、 和
和 。甲、乙两位同学通过实验Ⅲ验证把红色沉淀中含有
。甲、乙两位同学通过实验Ⅲ验证把红色沉淀中含有 和
和 。
。
实验Ⅲ:
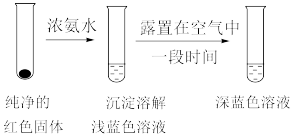
①甲同学认为红色沉淀中含有 ,他判断的理由是
,他判断的理由是___________ 。
②乙同学认为实验Ⅲ不足以证实红色沉淀中含有 ,理由是
,理由是___________ 。
 溶液分别与
溶液分别与 、
、 溶液的反应进行探究。
溶液的反应进行探究。| 实验 | 装置 | 试剂a | 操作及现象 |
| I |   溶液 溶液 |  溶液 溶液 | 加入 溶液,得到绿色溶液,30s时有无色气泡和白色沉淀产生,上层溶液颜色变浅。 溶液,得到绿色溶液,30s时有无色气泡和白色沉淀产生,上层溶液颜色变浅。 |
| Ⅱ |  溶液 溶液 | 加入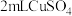 溶液,得到绿色溶液, 溶液,得到绿色溶液, 未见明显变化。 未见明显变化。 |
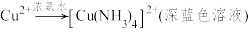
Ⅱ.

回答下列问题:
(1)推测实验Ⅰ中的无色气体为
 ,实验验证:用湿润的品红试纸接近试管口,视察到
,实验验证:用湿润的品红试纸接近试管口,视察到(2)推测实验Ⅰ中的白色沉淀为
 ,实验验证步骤如下:
,实验验证步骤如下:①实验Ⅰ完成后,立即过滤、洗涤。
②取少量已洗净的白色沉淀于试管中,滴加足量浓氨水,先观察到
(3)对比实验Ⅰ、Ⅱ,提出假设,
 增强了
增强了 的氧化性。
的氧化性。①若假设合理,实物Ⅰ反应的离子方程式为
 。
。②用以下实验来验证假设合理,装置如图所示。实验方案:闭合K,电压表的指针偏转至“Y”处;向U形管

(4)将实验Ⅱ的溶液静置24h或加热后,得到红色沉淀。经检验,红色沉淀中含有
 、
、 和
和 。甲、乙两位同学通过实验Ⅲ验证把红色沉淀中含有
。甲、乙两位同学通过实验Ⅲ验证把红色沉淀中含有 和
和 。
。实验Ⅲ:
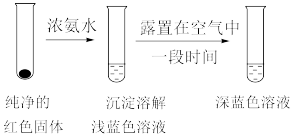
①甲同学认为红色沉淀中含有
 ,他判断的理由是
,他判断的理由是②乙同学认为实验Ⅲ不足以证实红色沉淀中含有
 ,理由是
,理由是
您最近一年使用:0次
9 . 胆矾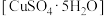 可做游泳池的消毒剂,其在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在
可做游泳池的消毒剂,其在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在 时隔绝空气加热A,至胆矾分解完全,确定分解产物的成分(试剂均足量)。
时隔绝空气加热A,至胆矾分解完全,确定分解产物的成分(试剂均足量)。
(1)B装置中 的作用是
的作用是___________ 。
(2)实验中,观察到B中有白色沉淀生成,C中无明显变化,可确定产物中一定有___________ 气体产生,写出B中发生反应的离子方程式___________ 。
(3)推测D中收集到的气体是___________ ,其检验方法为___________ 。
(4)A中固体完全分解后变为红色粉末,某同学设计实验验证固体残留物仅为 ,而不含
,而不含 ,请帮他完成表中内容。已知:
,请帮他完成表中内容。已知: (试剂,仪器和用品自选)。
(试剂,仪器和用品自选)。
(5)结合上述实验现象,写出胆矾在 时隔绝空气加热完全分解的化学方程式
时隔绝空气加热完全分解的化学方程式____ 。
 可做游泳池的消毒剂,其在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在
可做游泳池的消毒剂,其在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在 时隔绝空气加热A,至胆矾分解完全,确定分解产物的成分(试剂均足量)。
时隔绝空气加热A,至胆矾分解完全,确定分解产物的成分(试剂均足量)。
(1)B装置中
 的作用是
的作用是(2)实验中,观察到B中有白色沉淀生成,C中无明显变化,可确定产物中一定有
(3)推测D中收集到的气体是
(4)A中固体完全分解后变为红色粉末,某同学设计实验验证固体残留物仅为
 ,而不含
,而不含 ,请帮他完成表中内容。已知:
,请帮他完成表中内容。已知: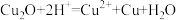 (试剂,仪器和用品自选)。
(试剂,仪器和用品自选)。| 实验步骤 | 实验预期 | 实验结论 |
准确称取 红色固体,加入足量 红色固体,加入足量 | 固体残留物仅为 |
 时隔绝空气加热完全分解的化学方程式
时隔绝空气加热完全分解的化学方程式
您最近一年使用:0次
名校
解题方法
10 . 在实验室制取乙烯时,其反应为CH3CH2OH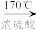 CH2=CH2↑+H2O。该实验常因温度控制不当而发生副反应生成SO2、CO2、水蒸气等。实验室设计如下实验装置以验证上述反应生成的混合气体中含乙烯、SO2和水蒸气。
CH2=CH2↑+H2O。该实验常因温度控制不当而发生副反应生成SO2、CO2、水蒸气等。实验室设计如下实验装置以验证上述反应生成的混合气体中含乙烯、SO2和水蒸气。
(1)仪器a的名称为___ 。
(2)请根据实验的要求完成下列填空:
①B中可观察到的现象为___ 。
②D中的试剂为___ 。
③E中的试剂为__ ,其作用为___ 。
④F中的试剂为___ ,可能的实验现象为___ 。
(3)简述装置B置于装置A、C之间的理由:___ 。
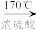 CH2=CH2↑+H2O。该实验常因温度控制不当而发生副反应生成SO2、CO2、水蒸气等。实验室设计如下实验装置以验证上述反应生成的混合气体中含乙烯、SO2和水蒸气。
CH2=CH2↑+H2O。该实验常因温度控制不当而发生副反应生成SO2、CO2、水蒸气等。实验室设计如下实验装置以验证上述反应生成的混合气体中含乙烯、SO2和水蒸气。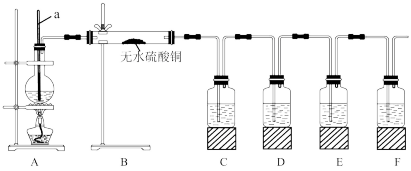
(1)仪器a的名称为
(2)请根据实验的要求完成下列填空:
①B中可观察到的现象为
②D中的试剂为
③E中的试剂为
④F中的试剂为
(3)简述装置B置于装置A、C之间的理由:
您最近一年使用:0次
2021-10-29更新
|
496次组卷
|
3卷引用:【石家庄新东方】河北省沧衡八校联盟2020-2021学年高一下学期期中考试化学试题