名校
1 . 近年来我国大力加强温室气体 催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。回答下列问题:
催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。回答下列问题:
(1)已知:


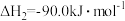
写出 催化氢化合成甲醇的热化学方程式
催化氢化合成甲醇的热化学方程式_____ 。
(2)为提高 的产率,理论上应采用的条件是
的产率,理论上应采用的条件是______ (填序号)。
a.高温高压 b.低温低压 c.高温低压 d.低温高压
(3)250℃时,在恒容密闭容器中由 催化氢化合成
催化氢化合成 ,如图为不同投料比
,如图为不同投料比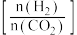 时某反应物X的平衡转化率的变化曲线。
时某反应物X的平衡转化率的变化曲线。
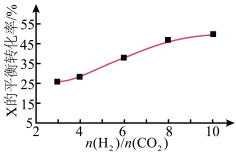
反应物X是___ (填“ ”或“
”或“ ”)。
”)。
(4)250℃时,在体积为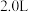 的恒容密闭容器中加入
的恒容密闭容器中加入 、
、 和催化剂,10min时反应达到平衡,测得
和催化剂,10min时反应达到平衡,测得 。
。
①前10min内 的平均反应速率
的平均反应速率
____  。
。
②化学平衡常数
________ 。
③催化剂和反应条件与反应物的转化率和产物的选择性高度相关。控制相同投料比和相同反应时间,得到如下四组实验数据:
根据上表所给数据,用 生产甲醇的最优条件为
生产甲醇的最优条件为___ (填实验编号)。
 催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。回答下列问题:
催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。回答下列问题:(1)已知:



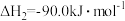
写出
 催化氢化合成甲醇的热化学方程式
催化氢化合成甲醇的热化学方程式(2)为提高
 的产率,理论上应采用的条件是
的产率,理论上应采用的条件是a.高温高压 b.低温低压 c.高温低压 d.低温高压
(3)250℃时,在恒容密闭容器中由
 催化氢化合成
催化氢化合成 ,如图为不同投料比
,如图为不同投料比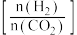 时某反应物X的平衡转化率的变化曲线。
时某反应物X的平衡转化率的变化曲线。
反应物X是
 ”或“
”或“ ”)。
”)。(4)250℃时,在体积为
 的恒容密闭容器中加入
的恒容密闭容器中加入 、
、 和催化剂,10min时反应达到平衡,测得
和催化剂,10min时反应达到平衡,测得 。
。①前10min内
 的平均反应速率
的平均反应速率
 。
。②化学平衡常数

③催化剂和反应条件与反应物的转化率和产物的选择性高度相关。控制相同投料比和相同反应时间,得到如下四组实验数据:
实验编号 | 温度/K | 催化剂 |
| 甲醇的选择性/% |
A | 543 |
|
|
|
B | 543 |
|
|
|
C | 553 |
|
|
|
D | 553 |
|
|
|
根据上表所给数据,用
 生产甲醇的最优条件为
生产甲醇的最优条件为
您最近一年使用:0次
2020-10-10更新
|
339次组卷
|
8卷引用:鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 第4节 化学反应条件的优化——工业合成氨 高效手册
鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 第4节 化学反应条件的优化——工业合成氨 高效手册人教版(2019)高二化学选择性必修1第二章 化学反应速率与化学平衡 第四节 化学反应的调控四川省成都新津为明学校2020-2021学年高二上学期期中测试化学试题甘肃省武威市民勤县第一中学2020-2021学年高二上学期12月月考化学试题(理科)湖北省沙市中学2022-2023学年高二上学期第二次月考化学试题广东省揭阳华侨高级中学2021-2022学年高二上学期期中考试化学试题广东省江门市新会区陈经纶中学2022-2023学年高二上学期第5段月考化学试题(已下线)化学反应速率与化学平衡——课时7化学反应的调控
名校
2 . 氮的氧化物是造成大气污染的主要物质。研究氮氧化物的反应机理对于消除环境污染有重要意义。
(1)已知:N2(g)+O2(g)=2NO(g);ΔH1=+180.5 kJ·mol-1
C(s)+O2(g)=CO2(g);ΔH2=-393.5 kJ·mol-1
2C(s)+O2(g)=2CO(g);ΔH3=-221 kJ·mol-1
反应2NO(g)+2CO(g)⇌N2(g)+2CO2(g)的ΔH=________ kJ·mol-1。
(2)催化氧化法去除NO是在一定条件下,用NH3消除NO污染,其反应原理为4NH3+6NO 5N2+6H2O。不同温度条件下,n(NH3)∶n(NO)的物质的量之比分别为4∶1、3∶1、1∶3时,得到NO脱除率曲线如图所示:
5N2+6H2O。不同温度条件下,n(NH3)∶n(NO)的物质的量之比分别为4∶1、3∶1、1∶3时,得到NO脱除率曲线如图所示:
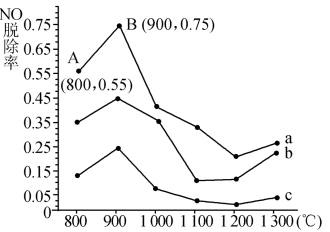
①n(NH3)∶n(NO)的物质的量之比为1∶3时,对应的是曲线________ (填“a”“b”或“c”)。
②由图可知,无论以何种比例反应,在温度超过900℃时NO脱除率都会骤然下降的原因可能是____________ 。
(3)NO氧化反应:2NO(g)+O2(g)⇌2NO2(g)分两步进行,其反应过程能量变化示意图如图:
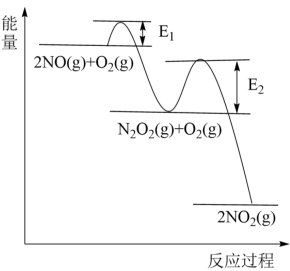
Ⅰ. 2NO(g)→N2O2(g);ΔH1
Ⅱ. N2O2(g)+O2(g)→2NO2(g);ΔH2
①化学反应速率有速率较慢的反应步骤决定。以上反应决定NO氧化反应速率的步骤是________ (填“Ⅰ”或“Ⅱ”)。
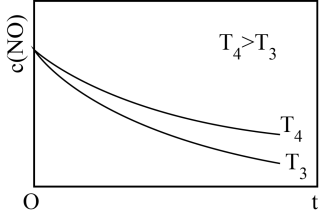
②在恒容的密闭容器中充入一定量的NO和O2气体,保持其他条件不变,控制反应温度分别为T3和T4(T4>T3),测得c(NO)随t(时间)的变化曲线如图。转化相同量的NO,在温度_____ (填“T3”或“T4”)下消耗的时间较长,试结合反应过程能量图分析其原因:______ 。
(4) NH3催化还原NO是重要的烟气脱硝技术,其反应过程与能量关系如图:
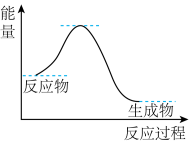
研究发现在以Fe2O3为主的催化剂上可能发生的反应过程如图,写出脱硝过程的总反应方程式:_______ 。

(1)已知:N2(g)+O2(g)=2NO(g);ΔH1=+180.5 kJ·mol-1
C(s)+O2(g)=CO2(g);ΔH2=-393.5 kJ·mol-1
2C(s)+O2(g)=2CO(g);ΔH3=-221 kJ·mol-1
反应2NO(g)+2CO(g)⇌N2(g)+2CO2(g)的ΔH=
(2)催化氧化法去除NO是在一定条件下,用NH3消除NO污染,其反应原理为4NH3+6NO
 5N2+6H2O。不同温度条件下,n(NH3)∶n(NO)的物质的量之比分别为4∶1、3∶1、1∶3时,得到NO脱除率曲线如图所示:
5N2+6H2O。不同温度条件下,n(NH3)∶n(NO)的物质的量之比分别为4∶1、3∶1、1∶3时,得到NO脱除率曲线如图所示:
①n(NH3)∶n(NO)的物质的量之比为1∶3时,对应的是曲线
②由图可知,无论以何种比例反应,在温度超过900℃时NO脱除率都会骤然下降的原因可能是
(3)NO氧化反应:2NO(g)+O2(g)⇌2NO2(g)分两步进行,其反应过程能量变化示意图如图:

Ⅰ. 2NO(g)→N2O2(g);ΔH1
Ⅱ. N2O2(g)+O2(g)→2NO2(g);ΔH2
①化学反应速率有速率较慢的反应步骤决定。以上反应决定NO氧化反应速率的步骤是
②在恒容的密闭容器中充入一定量的NO和O2气体,保持其他条件不变,控制反应温度分别为T3和T4(T4>T3),测得c(NO)随t(时间)的变化曲线如图。转化相同量的NO,在温度

(4) NH3催化还原NO是重要的烟气脱硝技术,其反应过程与能量关系如图:

研究发现在以Fe2O3为主的催化剂上可能发生的反应过程如图,写出脱硝过程的总反应方程式:

您最近一年使用:0次
2020-05-14更新
|
372次组卷
|
4卷引用:湖北省2020年荆、荆、襄、宜四地七校考试联盟高一联考化学模拟试题
3 . 氢气作为清洁能源有着广泛的应用前景,含硫天然气制备氢气的流程如下图所示。

请回答下列问题:
I.转化脱硫:将天然气压入吸收塔,30℃时,在T.F菌作用下,酸性环境中脱硫过程如图所示。
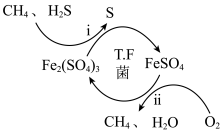
(1)过程i的氧化剂是_____________ 。
(2)过程ii的离子方程式是________________ 。
(3)已知:①Fe3+在pH=l.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T.F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如下表。
请结合以上信息,判断工业脱硫应选择的最合适的pH范围是____ <pH<____ 。
Ⅱ.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合下图回答问题。

(4)①该过程的热化学方程式是____________________ 。
②比较压强p1和p2的大小关系:p1____ p2(选填“>”、“<”或“=”)。
③在一定温度和一定压强下的体积可变的密闭容器中充入1mol CH4和1mol水蒸气充分反应达平衡后,测得起始时混合气体的密度是平衡时混合气体密度的1.4倍,则CH4的转化率为________ 。

请回答下列问题:
I.转化脱硫:将天然气压入吸收塔,30℃时,在T.F菌作用下,酸性环境中脱硫过程如图所示。

(1)过程i的氧化剂是
(2)过程ii的离子方程式是
(3)已知:①Fe3+在pH=l.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T.F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如下表。
| pH | 0.9 | 1.2 | 1.5 | 1.8 | 2.1 | 2.4 | 2.7 | 3.0 |
| Fe2+的氧化速率/g·L-1·h-1 | 4.5 | 5.3 | 6.2 | 6.8 | 7.0 | 6.6 | 6.2 | 5.6 |
Ⅱ.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合下图回答问题。

(4)①该过程的热化学方程式是
②比较压强p1和p2的大小关系:p1
③在一定温度和一定压强下的体积可变的密闭容器中充入1mol CH4和1mol水蒸气充分反应达平衡后,测得起始时混合气体的密度是平衡时混合气体密度的1.4倍,则CH4的转化率为
您最近一年使用:0次
2020-01-18更新
|
107次组卷
|
2卷引用:湖北省荆州中学、宜昌一中两校2019-2020学年高二上学期期末考试化学试题
名校
解题方法
4 . 甲醇既是基本有机化工原料,又可作为燃料用于替代矿物燃料。
(1)工业上合成甲醇的反应为:CO(g)+2H2(g) CH3OH(g) ΔH。下表所列数据是该反应在不同温度下的化学平衡常数(K)。
CH3OH(g) ΔH。下表所列数据是该反应在不同温度下的化学平衡常数(K)。
由表中数据判断该反应为________ 反应(填“吸热”或“放热”)。 某温度下,将2 mol CO和6 mol H2充入2 L的密闭容器中充分反应,达到平衡后,测得c(CO)=0.2 mol/L,则CO的转化率为______ ,此时的温度为______ (从表中选择)。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH1 kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH2 kJ/mol
③H2O(g)=H2O(l) ΔH3 kJ/mol
则反应 CH3OH(l)+O2(g)=CO(g)+2H2O(l) ΔH=_____________ kJ/mol(用ΔH1、ΔH2、ΔH3表示)。
(3)现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有Cr2O72‾)时,实验室利用如图装置模拟该法:
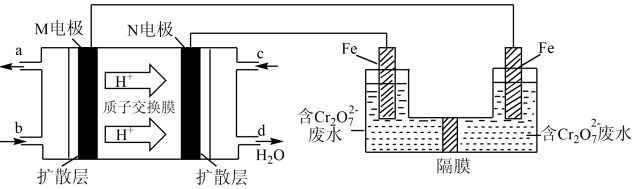
①N电极的电极反应式为___________________________________ 。
②请完成电解池中Cr2O72‾转化为Cr3+的离子反应方程式:
Cr2O72‾ +______ Fe2+ + ______ = ______ Cr3+ + ______ Fe3+ + ______
(4)处理废水时,最后Cr3+以Cr(OH)3形式除去,当c(Cr3+)=1×10‾5 mol/L 时,Cr3+沉淀完全,此时溶液的pH=______ 。(已知:Ksp=6.4×10‾31,lg2=0.3)
(1)工业上合成甲醇的反应为:CO(g)+2H2(g)
 CH3OH(g) ΔH。下表所列数据是该反应在不同温度下的化学平衡常数(K)。
CH3OH(g) ΔH。下表所列数据是该反应在不同温度下的化学平衡常数(K)。| 温度 | 250℃ | 300℃ | 350℃ |
| 平衡常数K | 2.041 | 0.270 | 0.012 |
由表中数据判断该反应为
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH1 kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH2 kJ/mol
③H2O(g)=H2O(l) ΔH3 kJ/mol
则反应 CH3OH(l)+O2(g)=CO(g)+2H2O(l) ΔH=
(3)现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有Cr2O72‾)时,实验室利用如图装置模拟该法:

①N电极的电极反应式为
②请完成电解池中Cr2O72‾转化为Cr3+的离子反应方程式:
Cr2O72‾ +
(4)处理废水时,最后Cr3+以Cr(OH)3形式除去,当c(Cr3+)=1×10‾5 mol/L 时,Cr3+沉淀完全,此时溶液的pH=
您最近一年使用:0次
2019-11-28更新
|
373次组卷
|
3卷引用:湖北省沙市中学2019-2020学年高二上学期期中考试化学(选考)试题
名校
解题方法
5 . 碳及其化合物广泛存在于自然界。请回答下列问题:
(1)反应Ⅰ:Fe(s)+CO2(g) FeO(s)+CO(g) ΔH1 平衡常数为K1
FeO(s)+CO(g) ΔH1 平衡常数为K1
反应Ⅱ:Fe(s)+H2O(g) FeO(s)+H2(g) ΔH2 平衡常数为K2
FeO(s)+H2(g) ΔH2 平衡常数为K2
不同温度下,K1、K2的值如下表:

现有反应Ⅲ:H2(g)+CO2(g) CO(g)+H2O(g),结合上表数据,反应Ⅲ是
CO(g)+H2O(g),结合上表数据,反应Ⅲ是_______ (填“放热”或“吸热”)反应。
(2)已知CO2催化加氢合成乙醇的反应原理为:
2CO2(g)+6H2(g) C2H5OH(g)+3H2O(g) ∆H<0。
C2H5OH(g)+3H2O(g) ∆H<0。
设m为起始时的投料比,即m= n(H2)/ n(CO2)。

①图1中投料比相同,温度从高到低的顺序为______________________ 。
②图2中m1、m2、m3从大到小的顺序为________________________ 。
③图3表示在总压为5MPa的恒压条件下,且m=3时,平衡状态时各物质的物质的量分数与温度的关系。则曲线d代表的物质化学名称为______________ ,T4温度时,该反应平衡常数KP的计算式为(不必化简)_______________________ 。
(3)已知:NH3·H2O的Kb=1.7×10-5,H2CO3的Ka1=4.3×10-7、Ka2=5.6×10-11。工业生产尾气中的CO2捕获技术之一是氨水溶液吸收技术,工艺流程是将烟气冷却至15.5℃~26.5℃后用氨水吸收过量的CO2。所得溶液的pH___________ 7(填“>”、“=”或“<”)。烟气需冷却至15.5℃~26.5℃的可能原因是____________ 。

(4)为了测量某湖水中无机碳含量,量取100mL湖水,酸化后用N2吹出CO2,再用NaOH溶液吸收。往吸收液中滴加1.0mol/L盐酸,生成的V(CO2)随V(盐酸)变化关系如图所示,则原吸收液中离子浓度由大到小的顺序为__________ 。
(1)反应Ⅰ:Fe(s)+CO2(g)
 FeO(s)+CO(g) ΔH1 平衡常数为K1
FeO(s)+CO(g) ΔH1 平衡常数为K1反应Ⅱ:Fe(s)+H2O(g)
 FeO(s)+H2(g) ΔH2 平衡常数为K2
FeO(s)+H2(g) ΔH2 平衡常数为K2不同温度下,K1、K2的值如下表:

现有反应Ⅲ:H2(g)+CO2(g)
 CO(g)+H2O(g),结合上表数据,反应Ⅲ是
CO(g)+H2O(g),结合上表数据,反应Ⅲ是(2)已知CO2催化加氢合成乙醇的反应原理为:
2CO2(g)+6H2(g)
 C2H5OH(g)+3H2O(g) ∆H<0。
C2H5OH(g)+3H2O(g) ∆H<0。设m为起始时的投料比,即m= n(H2)/ n(CO2)。

①图1中投料比相同,温度从高到低的顺序为
②图2中m1、m2、m3从大到小的顺序为
③图3表示在总压为5MPa的恒压条件下,且m=3时,平衡状态时各物质的物质的量分数与温度的关系。则曲线d代表的物质化学名称为
(3)已知:NH3·H2O的Kb=1.7×10-5,H2CO3的Ka1=4.3×10-7、Ka2=5.6×10-11。工业生产尾气中的CO2捕获技术之一是氨水溶液吸收技术,工艺流程是将烟气冷却至15.5℃~26.5℃后用氨水吸收过量的CO2。所得溶液的pH

(4)为了测量某湖水中无机碳含量,量取100mL湖水,酸化后用N2吹出CO2,再用NaOH溶液吸收。往吸收液中滴加1.0mol/L盐酸,生成的V(CO2)随V(盐酸)变化关系如图所示,则原吸收液中离子浓度由大到小的顺序为
您最近一年使用:0次
2019-11-22更新
|
604次组卷
|
6卷引用:湖北省荆州中学、宜昌一中、龙泉中学三校2020届高三期中联考理综化学试题
湖北省荆州中学、宜昌一中、龙泉中学三校2020届高三期中联考理综化学试题2020届高三《新题速递·化学》12月第01期(考点07-11)(已下线)《2020年新高考政策解读与配套资源》2020年山东新高考化学全真模拟卷(八)(已下线)考点10 化学平衡常数及其图象分析-2020年高考化学命题预测与模拟试题分类精编2020届高三化学二轮冲刺新题专练——化学反应原理综合题福建省福州第一中学2021届高三下学期开学考试化学试题
真题
名校
6 . 氢气与氧气生成水的反应是氢能源应用的重要途径。下列有关说法正确的是
| A.一定温度下,反应2H2(g)+O2(g) =2H2O(g)能自发进行,该反应的ΔH<0 |
| B.氢氧燃料电池的负极反应为O2+2H2O+4e−=4OH− |
| C.常温常压下,氢氧燃料电池放电过程中消耗11.2 L H2,转移电子的数目为6.02×1023 |
| D.反应2H2(g)+O2(g) =2H2O(g)的ΔH可通过下式估算:∆H=反应中形成新共价键的键能之和-反应中断裂旧共价键的键能之和 |
您最近一年使用:0次
2019-06-10更新
|
5085次组卷
|
30卷引用:湖北省荆州中学2020-2021学年高二12月月考化学试题
湖北省荆州中学2020-2021学年高二12月月考化学试题2019年江苏省高考化学试题(已下线)专题07 化学反应中的能量变化——2019年高考真题和模拟题化学分项汇编山西省祁县第二中学校2020届高三上学期期中考试化学试题陕西省渭南市临渭区尚德中学2020届高三上学期第三次月考化学试题陕西省西安中学2020届高三上学期第三次月考化学试题2019年秋高三化学复习强化练习——化学反应的方向及判断(已下线)专题九 化学能与热能(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训广西桂林市第十八中学2019-2020学年高二下学期开学考试化学试题(已下线)第六章能力提升检测卷-2021年高考化学一轮复习讲练测江苏省镇江市吕叔湘中学2019-2020学年高二下学期期中考试化学试题湖南省衡阳市第二十六中学2021届高三上学期9月月考化学试题江苏省苏州市新草桥中学2019-2020学年高二下学期6月月考化学试题(已下线)小题必刷23 焓变与热化学方程式——2021年高考化学一轮复习小题必刷(通用版)(已下线)小题必刷24 盖斯定律及反应热计算——2021年高考化学一轮复习小题必刷(通用版)(已下线)【镇江新东方】高二下21心湖期中安徽省淮北市树人高级中学2020-2021学年高二上学期第四阶段考试化学试题福建省厦门第一中学2020-2021学年高二上学期期中考试化学试题重庆市缙云教育联盟2020-2021学年高二上学期期末考试化学试题辽宁省沈阳市郊联体2021届高三上学期期末考试化学试题黑龙江省哈尔滨市呼兰区第一中学校等三校2020-2021学年高二上学期期末联考化学试题(已下线)专题05 化学反应与能量——备战2021年高考化学纠错笔记(已下线)【浙江新东方】高中化学20210304-003(已下线)课时29 盖斯定律及反应热计算-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点17 化学反应的热效应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)2019年高考江苏卷化学试题变式题(不定项选择题)天津市武清区城关中学2023-2024学年高三上学期第二次阶段性练习化学试题重庆十八中两江实验中学校2022-2023学年高二上学期第一次月考化学试题
名校
7 . 能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率,请回答下列问题。
(1)工业合成氨反应:N2+3H2 2NH3是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1 mol N2完全反应生成NH3可放出92 kJ热量。如果将10 mol N2和足量H2混合,使其充分反应,放出的热量
2NH3是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1 mol N2完全反应生成NH3可放出92 kJ热量。如果将10 mol N2和足量H2混合,使其充分反应,放出的热量________ (填“大于”、“小于”或“等于”)920kJ。
(2)实验室模拟工业合成氨时,在容积为2 L的密闭容器内,反应经过10 min后,生成10 mol NH3
①则用N2表示的化学反应速率为__________________ 。
②一定条件下,当该反应进行到最大限度时,下列说法正确的是______ (填编号)
a.N2的转化率达到最大值
b.N2、H2和NH3的体积分数之比为1 : 3 : 2
c.体系内气体的密度保持不变
d.体系内物质的平均相对分子质量保持不变
(3)某实验小组同学进行如下图所示实验,以检验化学反应中的能量变化。请根据你掌握的反应原理判断,②中的温度_______ (填“升高”或“降低”)。反应过程____ (填“①”或“②”)的能量变化可用图表示。
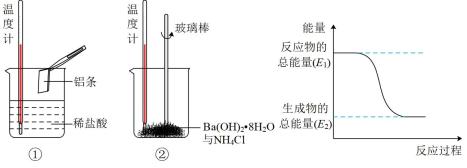
(4)用CH4和O2组合形成的质子交换膜燃料电池的结构如图:

①则d电极是____ (填“正极” 或“负极”),c电极的电极反应式为_____________________________ 。
②若线路中转移2 mol电子,则该燃料电池理论上消耗的O2在标准状况下的体积为______ L。
(1)工业合成氨反应:N2+3H2
 2NH3是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1 mol N2完全反应生成NH3可放出92 kJ热量。如果将10 mol N2和足量H2混合,使其充分反应,放出的热量
2NH3是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1 mol N2完全反应生成NH3可放出92 kJ热量。如果将10 mol N2和足量H2混合,使其充分反应,放出的热量(2)实验室模拟工业合成氨时,在容积为2 L的密闭容器内,反应经过10 min后,生成10 mol NH3
①则用N2表示的化学反应速率为
②一定条件下,当该反应进行到最大限度时,下列说法正确的是
a.N2的转化率达到最大值
b.N2、H2和NH3的体积分数之比为1 : 3 : 2
c.体系内气体的密度保持不变
d.体系内物质的平均相对分子质量保持不变
(3)某实验小组同学进行如下图所示实验,以检验化学反应中的能量变化。请根据你掌握的反应原理判断,②中的温度

(4)用CH4和O2组合形成的质子交换膜燃料电池的结构如图:

①则d电极是
②若线路中转移2 mol电子,则该燃料电池理论上消耗的O2在标准状况下的体积为
您最近一年使用:0次
2019-06-01更新
|
1143次组卷
|
7卷引用:【全国百强校】山西省临汾市第一中学2018-2019学年高一下学期期中考试化学试题
名校
8 . 已知X和Y能发生如下反应:X+Y=H2O+盐,下列有关物质X和Y所属种类的判断中一定不正确的是( )
| A.X为酸、Y为碱 | B.X为碱性氧化物、Y为酸 |
| C.X为盐、Y为碱 | D.X为碱性氧化物、Y为酸性氧化物 |
您最近一年使用:0次
2018-09-12更新
|
1835次组卷
|
31卷引用:云南省峨山彝族自治县峨山一中2018-2019学年高二入学考试化学试题
云南省峨山彝族自治县峨山一中2018-2019学年高二入学考试化学试题【全国百强校】山东省枣庄市第八中学东校区2019届高三9月月考化学试题贵州省毕节市织金县第一中学2018-2019学年高一上学期12月份考试化学试题鲁科版新教材(2019)化学同步2.1.1 元素与物质的关系 物质分类与物质性质福建省莆田市第六中学2019-2020学年高一上学期第一次月考化学试题(B)备战2020高考化学二轮专项训练:多角度考查物质变化云南省福贡县第一中学2019-2020学年高一上学期期末考试化学试题人教版高一化学必修1第二章《化学物质及其变化》测试卷(已下线)专题2.1 物质的分类 胶体 -巅峰冲刺山东省2020年高考化学一轮考点扫描《2020年新高考政策解读与配套资源》(已下线)2.1.1 元素与物质的关系 物质分类与物质性质练习(2)——《高中新教材同步备课》(鲁科版 必修第一册)(已下线)专题01 物质的分类及转化(核心素养卷)——【新教材精创】2019-2020学年高中化学新教材知识讲学广东省深圳市第七高级中学2020-2021学年高一上学期第一学段考试化学试题(已下线)练习2 物质的转化-2020-2021学年【补习教材·寒假作业】高一化学(苏教版)湖北省荆州市沙市中学2023-2024学年高一上学期9月月考化学试题(已下线)衔接点02 酸碱盐的分类和命名-2021年初升高化学无忧衔接(已下线)课时03 物质的组成、分类和性质-2022年高考化学一轮复习小题多维练(全国通用)福建省漳州市正兴学校2020-2021学年高二下学期期末考试化学试题陕西省西安市长安区第一中学2021-2022学年高二下学期期中考试化学试题(已下线)衔接点03 酸碱盐的分类和命名-2022年初升高化学无忧衔接(已下线)第01练 物质的分类及转化-2023年高考化学一轮复习小题多维练(全国通用)广东省揭阳华侨高级中学2021-2022学年高一上学期第一次阶段考试化学试题黑龙江省哈尔滨市第一中学2021-2022学年高一上学期期中考试化学试题 甘肃省兰州市西固区三校2021-2022学年高一上学期期中联考化学试题广西钦州市第四中学2021-2022学年高一上学期期中考试化学试题吉林省长春外国语学校2022-2023学年高一上学期第一次月考化学试题山东省“学情空间”区域教研共同体2022-2023学年高一上学期10月联考(人教版)化学试题甘肃省天水市第一中学2022-2023学年高一上学期第一学段检测化学试题(已下线)第二章 化学物质及其变化 第1讲 物质的变化及分类第2课时 物质的转化甘肃省部分学校2023-2024学年高一上学期10月期中考试化学试题河北省石家庄北华中学2023-2024学年高一上学期10月月考考试化学试题
名校
9 . 已知使36g焦炭发生不完全燃烧,所得气体中CO占1/3体积,CO2占2/3体积,已知:C(s)+1/2O2(g)=CO(g)△H=-Q1kJ/mol,CO(g)+1/2O2(g)=CO2(g)△H=-Q2kJ/mol,与这些焦炭完全燃烧相比较,损失的热量是中正确的是( )
| A.2Q2kJ | B.Q2kJ | C.3(Q1+Q2)kJ | D.3Q1KJ |
您最近一年使用:0次
2018-07-20更新
|
166次组卷
|
2卷引用:湖北省公安县车胤中学2018-2019学年高二上学期9月月考化学试题
名校
解题方法
10 . C、N、S的氧化物常会造成一些环境问题,科研工作者正在研究用各种化学方法来消除这些物质对环境的不利影响。
(1)已知:2CO(g)+O2(g)=2CO2(g) ΔH1=-566kJ/mol
S(l)+O2(g)=SO2(g) ΔH2=-296kJ/mol
一定条件下,可以通过CO与SO2反应生成S(1)和一种无毒的气体,实现燃煤烟气中硫的回收,写出该反应的热化学方程式_______________________________ 。
(2)一定温度下,向2L恒容密闭容器中通入2molCO和1molSO2,发生上述(1)中回收硫的反应。若反应进行到20min时达平衡,测得CO2的体积分数为0.5,则前20min的反应速率ν(CO)=_________ ,该温度下反应化学平衡常数K=____________ (L·mol-1)
(3)在不同条件下,向2L恒容密闭容器中通入2molCO和1molSO2,反应体系总压强随时间的变化如图(Ⅰ)所示:

①图(Ⅰ)中三组实验从反应开始至达到平衡时,v(CO)最大的为___________ (填序号)
②与实验a相比,c组改变的实验条件可能是_________________ 。
(4)“亚硫酸盐法”吸收烟气中的SO2。室温条件下,将烟气通入(NH4)2SO3溶液中,测得溶液pH与含硫组分物质的量分数的变化关系如图(Ⅱ)所示,b点时溶液pH=7,则n(NH4+)∶n(HSO3-)=______ 。

(5)间接电化学法可除NO。其原理如图(Ⅲ)所示,写出电解池阴极的电极反应式(阴极室溶液呈酸性)_______________________________ 。

(1)已知:2CO(g)+O2(g)=2CO2(g) ΔH1=-566kJ/mol
S(l)+O2(g)=SO2(g) ΔH2=-296kJ/mol
一定条件下,可以通过CO与SO2反应生成S(1)和一种无毒的气体,实现燃煤烟气中硫的回收,写出该反应的热化学方程式
(2)一定温度下,向2L恒容密闭容器中通入2molCO和1molSO2,发生上述(1)中回收硫的反应。若反应进行到20min时达平衡,测得CO2的体积分数为0.5,则前20min的反应速率ν(CO)=
(3)在不同条件下,向2L恒容密闭容器中通入2molCO和1molSO2,反应体系总压强随时间的变化如图(Ⅰ)所示:

①图(Ⅰ)中三组实验从反应开始至达到平衡时,v(CO)最大的为
②与实验a相比,c组改变的实验条件可能是
(4)“亚硫酸盐法”吸收烟气中的SO2。室温条件下,将烟气通入(NH4)2SO3溶液中,测得溶液pH与含硫组分物质的量分数的变化关系如图(Ⅱ)所示,b点时溶液pH=7,则n(NH4+)∶n(HSO3-)=

(5)间接电化学法可除NO。其原理如图(Ⅲ)所示,写出电解池阴极的电极反应式(阴极室溶液呈酸性)

您最近一年使用:0次
2018-05-01更新
|
359次组卷
|
2卷引用:【全国百强校】湖北省荆州中学2018届高三全真模拟考试(一)理综化学试题

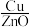 纳米棒
纳米棒