1 . 我国科学家研发的“液态阳光”计划通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢制备甲醇。
(1)制备甲醇的主反应:
 。
。
该过程中还存在一个生成CO的副反应,结合反应: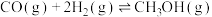
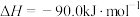 写出该副反应的热化学方程式:
写出该副反应的热化学方程式:______ 。
(2)将 和
和 按物质的量比1∶3混合,以固定流速通过盛放Cu/Zn/AI/Zr催化剂的反应器,在相同时间内,不同温度下的实验数据如右图所示。
按物质的量比1∶3混合,以固定流速通过盛放Cu/Zn/AI/Zr催化剂的反应器,在相同时间内,不同温度下的实验数据如右图所示。
①催化剂活性最好的温度为______ (填字母序号)。
a.483K b.503K c.523K d.543K
②温度由523K升到543K, 的平衡转化率降低,解释其原因:
的平衡转化率降低,解释其原因:______ 。
(3)使用 薄膜电极作阴极,通过电催化法将二氧化碳转化为甲醇。
薄膜电极作阴极,通过电催化法将二氧化碳转化为甲醇。
①将铜箔放入煮沸的饱和硫酸铜溶液中,制得 薄膜电极。反应的离子方程式为
薄膜电极。反应的离子方程式为______ 。
②用 薄膜电极作阴极,
薄膜电极作阴极, 溶液作电解液,采用电沉积法制备
溶液作电解液,采用电沉积法制备 薄膜电极,制备完成后电解液中检测到了
薄膜电极,制备完成后电解液中检测到了 。制备ZnO薄膜的电极反应式为
。制备ZnO薄膜的电极反应式为______ 。
③电催化法制备甲醇如图所示。______ 。
(1)制备甲醇的主反应:

 。
。该过程中还存在一个生成CO的副反应,结合反应:
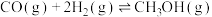
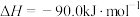 写出该副反应的热化学方程式:
写出该副反应的热化学方程式:(2)将
 和
和 按物质的量比1∶3混合,以固定流速通过盛放Cu/Zn/AI/Zr催化剂的反应器,在相同时间内,不同温度下的实验数据如右图所示。
按物质的量比1∶3混合,以固定流速通过盛放Cu/Zn/AI/Zr催化剂的反应器,在相同时间内,不同温度下的实验数据如右图所示。

①催化剂活性最好的温度为
a.483K b.503K c.523K d.543K
②温度由523K升到543K,
 的平衡转化率降低,解释其原因:
的平衡转化率降低,解释其原因:(3)使用
 薄膜电极作阴极,通过电催化法将二氧化碳转化为甲醇。
薄膜电极作阴极,通过电催化法将二氧化碳转化为甲醇。①将铜箔放入煮沸的饱和硫酸铜溶液中,制得
 薄膜电极。反应的离子方程式为
薄膜电极。反应的离子方程式为②用
 薄膜电极作阴极,
薄膜电极作阴极, 溶液作电解液,采用电沉积法制备
溶液作电解液,采用电沉积法制备 薄膜电极,制备完成后电解液中检测到了
薄膜电极,制备完成后电解液中检测到了 。制备ZnO薄膜的电极反应式为
。制备ZnO薄膜的电极反应式为③电催化法制备甲醇如图所示。

您最近一年使用:0次
解题方法
2 . 甲醇来源丰富、价格低廉,是一种重要的化工原料,有着重要的用途和应用前景。
2CO(g)+O2(g)=2CO2(g) △H = -570 kJ/mol
(1)计算2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g)△H =_______ 。
(2)若在绝热恒容 的容器内进行反应2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g),初始加入2mol CH3OH和3mol O2下列不能 表示该反应达到平衡状态的有__________ (填字母序号)。
A.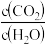 保持不变 B.容器中混合气体的密度不变化
保持不变 B.容器中混合气体的密度不变化
C.2v正(H2O)=v逆(CO2) D.容器中混合气体的压强不变化
E. 平均相对分子量保持不变 F. K值保持不变_______ ,初始压强为P,该反应的压强平衡常数Kp=______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)若再次向容器中充入0.5mol H2和0.5mol CO,则此时该反应v(正)_____ v(逆)(填“>”、“<”或“=”);
(5)某实验小组设计了甲醇以氢氧化钾为电解质溶液的燃料电池装置。该电池负极反应的离子方程式为______ 。
Ⅰ.工业生产甲醇的常用方法是:CO(g)+2H2(g)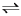 CH3OH(g) △H = -91 kJ/mol。
CH3OH(g) △H = -91 kJ/mol。
2CO(g)+O2(g)=2CO2(g) △H = -570 kJ/mol
(1)计算2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g)△H =
(2)若在
A.
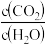 保持不变 B.容器中混合气体的密度不变化
保持不变 B.容器中混合气体的密度不变化C.2v正(H2O)=v逆(CO2) D.容器中混合气体的压强不变化
E. 平均相对分子量保持不变 F. K值保持不变
Ⅱ.制甲醇所需要的H2,可用下列反应制取:H2O(g)+CO(g)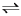 H2(g)+ CO2(g) △H<0,某温度下该反应,若起始时向2L容器中充入1 mol CO和1 mol H2O,5min达到平衡时,CO的转化率为60%,试回答下列问题:
H2(g)+ CO2(g) △H<0,某温度下该反应,若起始时向2L容器中充入1 mol CO和1 mol H2O,5min达到平衡时,CO的转化率为60%,试回答下列问题:
(4)若再次向容器中充入0.5mol H2和0.5mol CO,则此时该反应v(正)
(5)某实验小组设计了甲醇以氢氧化钾为电解质溶液的燃料电池装置。该电池负极反应的离子方程式为
您最近一年使用:0次
3 . I.中国科学家首次实现了二氧化碳到淀粉的全合成,相关成果由国际知名学术期刊《科学》在线发表。 的捕集、利用与封存是科学家研究的重要课题,利用
的捕集、利用与封存是科学家研究的重要课题,利用 与
与 制备“合成气”
制备“合成气” 、
、 ,合成气可直接制备甲醇,反应原理为:
,合成气可直接制备甲醇,反应原理为: 。
。
(1)若要该反应自发进行,___________ (填“高温”或“低温”)更有利。
(2)在恒温,恒容密闭容器中,对于合成气合成甲醇的反应,下列说法中能说明该反应达到化学平衡状态的是___________。(填字母序号)。
A.反应物的物质的量的比值不变
B.混合气体的密度不再变化
C. 的百分含量不再变化
的百分含量不再变化
D.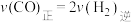
E.混合气体的平均相对分子质量不再变化
(3)把 转化为
转化为 是降碳并生产化工原料的常用方法,有关反应如下:
是降碳并生产化工原料的常用方法,有关反应如下:
①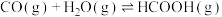
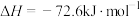
②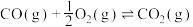
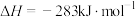
③
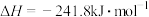
则 与
与 合成
合成 反应的热化学方程式:
反应的热化学方程式:___________ 。
(4)受绿色植物光合作用的启示,太阳能固碳装置被设计出来,则固碳电极反应为___________ 。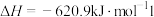 可有效降低汽车尾气污染物排放。
可有效降低汽车尾气污染物排放。
(5)探究温度、压强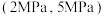 对反应
对反应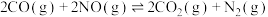 的影响,如图所示,表示
的影响,如图所示,表示 的是
的是___________ (填标号)。 的恒容密闭容器按体积
的恒容密闭容器按体积 比例充入
比例充入 和
和 ,压强为
,压强为 发生上述反应,当反应达到平衡时容器内压强变为起始时的
发生上述反应,当反应达到平衡时容器内压强变为起始时的 ,此温度下该反应的平衡常数
,此温度下该反应的平衡常数
___________ ( 为压强平衡常数)。
为压强平衡常数)。
 的捕集、利用与封存是科学家研究的重要课题,利用
的捕集、利用与封存是科学家研究的重要课题,利用 与
与 制备“合成气”
制备“合成气” 、
、 ,合成气可直接制备甲醇,反应原理为:
,合成气可直接制备甲醇,反应原理为: 。
。(1)若要该反应自发进行,
(2)在恒温,恒容密闭容器中,对于合成气合成甲醇的反应,下列说法中能说明该反应达到化学平衡状态的是___________。(填字母序号)。
A.反应物的物质的量的比值不变
B.混合气体的密度不再变化
C.
 的百分含量不再变化
的百分含量不再变化 D.
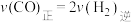
E.混合气体的平均相对分子质量不再变化
(3)把
 转化为
转化为 是降碳并生产化工原料的常用方法,有关反应如下:
是降碳并生产化工原料的常用方法,有关反应如下:①
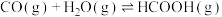
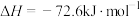
②
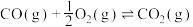
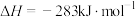
③

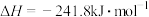
则
 与
与 合成
合成 反应的热化学方程式:
反应的热化学方程式:(4)受绿色植物光合作用的启示,太阳能固碳装置被设计出来,则固碳电极反应为
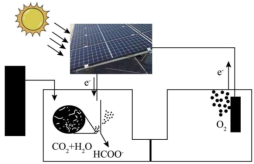
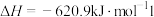 可有效降低汽车尾气污染物排放。
可有效降低汽车尾气污染物排放。(5)探究温度、压强
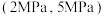 对反应
对反应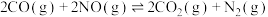 的影响,如图所示,表示
的影响,如图所示,表示 的是
的是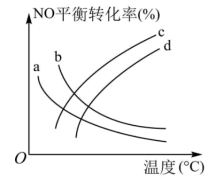
 的恒容密闭容器按体积
的恒容密闭容器按体积 比例充入
比例充入 和
和 ,压强为
,压强为 发生上述反应,当反应达到平衡时容器内压强变为起始时的
发生上述反应,当反应达到平衡时容器内压强变为起始时的 ,此温度下该反应的平衡常数
,此温度下该反应的平衡常数
 为压强平衡常数)。
为压强平衡常数)。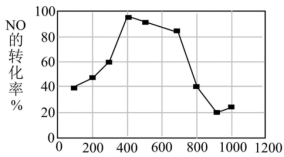
您最近一年使用:0次
4 . 由 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见图)中的重要反应之一
人工合成淀粉(节选途径见图)中的重要反应之一
反应②: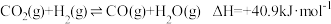
反应③: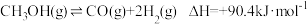
(1)反应①: 的
的
_______ 。
(2) 2的转化率与温度的关系如图所示。
2的转化率与温度的关系如图所示。_______ 逆反应速率(填“>或<或=”)。
②下列叙述能说明上述反应能达到化学平衡状态的是_______ 。(填字母)。
a.3v(CO2)=v(H2) b. 的体积分数不再改变
的体积分数不再改变
c.消耗1mol CO2的同时消耗3mol H2 d.混合气体的平均相对分子质量不再改变
③250℃后 2的平衡转化率降低的原因
2的平衡转化率降低的原因_______
(3)往一容积为 的密闭容器内,充入0.2mol CO2与
的密闭容器内,充入0.2mol CO2与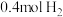 发生反应,反应达到c点时,从上图像可知在平衡时
发生反应,反应达到c点时,从上图像可知在平衡时 2的转化率是
2的转化率是_______ ,则c点时 的体积分数是
的体积分数是_______ ;平衡后再加入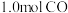 2后重新到达平衡,则H2的转化率
2后重新到达平衡,则H2的转化率_______ (填“增大”或“不变”或“减小”)。
 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见图)中的重要反应之一
人工合成淀粉(节选途径见图)中的重要反应之一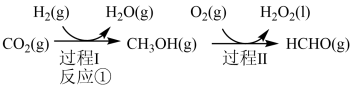
反应②:
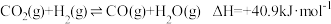
反应③:
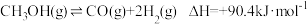
(1)反应①:
 的
的
(2)
 2的转化率与温度的关系如图所示。
2的转化率与温度的关系如图所示。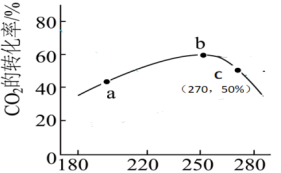
②下列叙述能说明上述反应能达到化学平衡状态的是
a.3v(CO2)=v(H2) b.
 的体积分数不再改变
的体积分数不再改变c.消耗1mol CO2的同时消耗3mol H2 d.混合气体的平均相对分子质量不再改变
③250℃后
 2的平衡转化率降低的原因
2的平衡转化率降低的原因(3)往一容积为
 的密闭容器内,充入0.2mol CO2与
的密闭容器内,充入0.2mol CO2与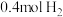 发生反应,反应达到c点时,从上图像可知在平衡时
发生反应,反应达到c点时,从上图像可知在平衡时 2的转化率是
2的转化率是 的体积分数是
的体积分数是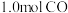 2后重新到达平衡,则H2的转化率
2后重新到达平衡,则H2的转化率
您最近一年使用:0次
5 . 反应①A+B→C ΔH1分两步进行:②A+B→X ΔH2,③X→C ΔH3.总反应过程中能量变化如图,下列说法正确的是
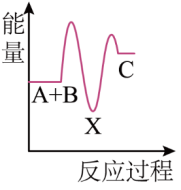
| A.总反应A+B→C ΔH1<0 |
| B.ΔH1=ΔH2 + ΔH3 |
| C.X的键能比C的键能小 |
| D.物质C比物质X稳定 |
您最近一年使用:0次
名校
6 . 氢气和碳氧化物反应生成甲烷,有利于实现碳循环利用。涉及反应如下:
反应Ⅰ: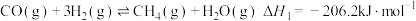
反应Ⅱ: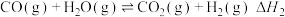
反应Ⅲ: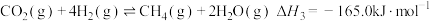
回答下列问题:
(1)
___________  。
。
(2)已知反应Ⅱ的速率方程为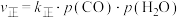 ,
, ,其中
,其中 、
、 分别为正、逆反应的速率常数。如图(lg k表示速率常数的对数,
分别为正、逆反应的速率常数。如图(lg k表示速率常数的对数, 表示温度的倒数)所示a、b、c、d四条斜线中,能表示
表示温度的倒数)所示a、b、c、d四条斜线中,能表示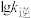 随
随 变化关系的是斜线
变化关系的是斜线___________ (填标号)。___________ (填“氧离子导体”或“质子导体”)。
②阳极的电极反应式为___________ 。
(4)温度为 时,在固定容积的容器中充入一定量的
时,在固定容积的容器中充入一定量的 和1mol CO,平衡时
和1mol CO,平衡时 和CO的转化率(α)及
和CO的转化率(α)及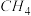 和
和 的物质的量(n)随
的物质的量(n)随 变化的情况如图所示。
变化的情况如图所示。___________ ;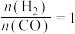 时,
时, 的选择性
的选择性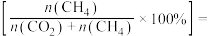
___________ 。
②已知起始充入1mol的CO和0.5mol的 进行上述反应时,起始压强为
进行上述反应时,起始压强为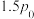 。反应Ⅰ的
。反应Ⅰ的
___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,用 表示);温度为
表示);温度为 ,
,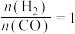 时,
时, 可能对应图中X、Y、Z、W四点中的
可能对应图中X、Y、Z、W四点中的___________ (填标号)。
反应Ⅰ:
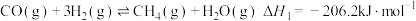
反应Ⅱ:
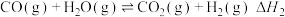
反应Ⅲ:
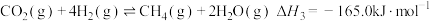
回答下列问题:
(1)

 。
。(2)已知反应Ⅱ的速率方程为
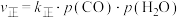 ,
, ,其中
,其中 、
、 分别为正、逆反应的速率常数。如图(lg k表示速率常数的对数,
分别为正、逆反应的速率常数。如图(lg k表示速率常数的对数, 表示温度的倒数)所示a、b、c、d四条斜线中,能表示
表示温度的倒数)所示a、b、c、d四条斜线中,能表示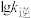 随
随 变化关系的是斜线
变化关系的是斜线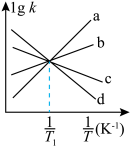
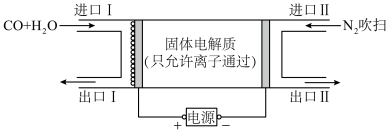
②阳极的电极反应式为
(4)温度为
 时,在固定容积的容器中充入一定量的
时,在固定容积的容器中充入一定量的 和1mol CO,平衡时
和1mol CO,平衡时 和CO的转化率(α)及
和CO的转化率(α)及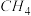 和
和 的物质的量(n)随
的物质的量(n)随 变化的情况如图所示。
变化的情况如图所示。
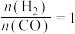 时,
时, 的选择性
的选择性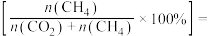
②已知起始充入1mol的CO和0.5mol的
 进行上述反应时,起始压强为
进行上述反应时,起始压强为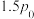 。反应Ⅰ的
。反应Ⅰ的
 表示);温度为
表示);温度为 ,
,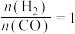 时,
时, 可能对应图中X、Y、Z、W四点中的
可能对应图中X、Y、Z、W四点中的
您最近一年使用:0次
解题方法
7 . 金属钛(Ti)在航空航天、医疗器械等工业领域有着重要用途,目前生产钛的方法之一是将金红石(TiO2)转化为TiCl4,再进一步还原得到钛。回答下列问题:
(1) 转化为
转化为 有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式及其平衡常数如下:(ⅰ)直接氯化:
有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式及其平衡常数如下:(ⅰ)直接氯化:
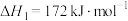 ,
,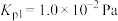
(ⅱ)碳氯化:
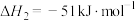 ,
,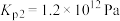
①反应 的
的 为
为________  。
。
②运用以上数据分析,你认为以上两种方法更优越的是__________ ,理由_________________ 。
(2)在压强为170kPa恒压作用下,将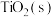 、
、 、
、 以物质的量之比为
以物质的量之比为 进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。
进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。 的平衡常数
的平衡常数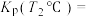
________  (分压
(分压 物质的量分数
物质的量分数 总压)。
总压)。
②图中显示,在T1℃平衡时TiO2几乎完全转化为TiCl4,但实际生产中反应温度却远高于此温度,其原因是___________ 。
(1)
 转化为
转化为 有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式及其平衡常数如下:(ⅰ)直接氯化:
有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式及其平衡常数如下:(ⅰ)直接氯化:
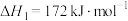 ,
,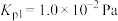
(ⅱ)碳氯化:

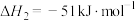 ,
,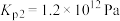
①反应
 的
的 为
为 。
。②运用以上数据分析,你认为以上两种方法更优越的是
(2)在压强为170kPa恒压作用下,将
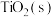 、
、 、
、 以物质的量之比为
以物质的量之比为 进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。
进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。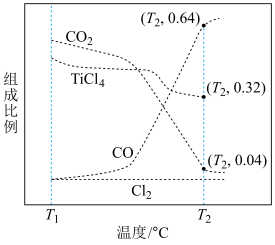
 的平衡常数
的平衡常数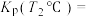
 (分压
(分压 物质的量分数
物质的量分数 总压)。
总压)。②图中显示,在T1℃平衡时TiO2几乎完全转化为TiCl4,但实际生产中反应温度却远高于此温度,其原因是
您最近一年使用:0次
解题方法
8 . 中国科学家首次实现了二氧化碳到淀粉的全合成,相关成果于北京时间 9 月 24 日由国际知名学术期刊《科学》在线发表。CO2的捕集、利用与封存是科学家研究的重要课题,利用 CH4与 CO2制备“合成气”(CO、H2),合成气可直接制备甲醇,反应原理为:

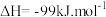 。
。
(1)已知:
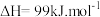 ,部分键能数据如下:(CO 的结构式为 C≡O)
,部分键能数据如下:(CO 的结构式为 C≡O)
计算 C—H 的键能 x= ______________ kJ/mol,(保留一位小数)。
(2)若要该反应自发进行,_______ (填“高温”或“低温”)更有利,该反应必须在高温下才能启动,原因是_______ 。
(3)已知:H2 (g)的燃烧热ΔH=-285.8kJ.mol-1,写出H2 (g)燃烧热的热化学反应方程式____________ 。
(4)在恒温,恒容密闭容器中,对于合成气合成甲醇的反应,下列说法中能说明该反应达到化学平衡状态的是_______(填字母序号)。
(5)T1℃下,在 2L 恒容密闭容器中充入 2molCO 和 6molH2合成 CH3OH(g),测得 CO 的物质的量浓度随反应时间的变化如图所示:_______ 。
②T1℃时,该反应的化学平衡常数 K=_______ 。
③10min 时,改变的外界条件可能是_______ 。
(6)T1℃下,在 1L 恒容密闭容器中充入 2molCO、2molH2和 3molCH3OH(g),此时反应将_______ (填“向左进行”“向右进行”“达到平衡”或“无法判断”)。

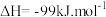 。
。(1)已知:

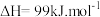 ,部分键能数据如下:(CO 的结构式为 C≡O)
,部分键能数据如下:(CO 的结构式为 C≡O)| 共价键 | C≡O | C—O | C—H | O—H | H—H |
| 键能/(kJ/mol) | 1072 | 326 | 464 | 436 |
(2)若要该反应自发进行,
(3)已知:H2 (g)的燃烧热ΔH=-285.8kJ.mol-1,写出H2 (g)燃烧热的热化学反应方程式
(4)在恒温,恒容密闭容器中,对于合成气合成甲醇的反应,下列说法中能说明该反应达到化学平衡状态的是_______(填字母序号)。
| A.混合气体的平均相对分子质量不再变化 |
| B.混合气体的密度不再变化 |
| C.CO 的百分含量不再变化 |
| D.CO、H2、CH3OH 的物质的量之比为 1∶2∶1 |
(5)T1℃下,在 2L 恒容密闭容器中充入 2molCO 和 6molH2合成 CH3OH(g),测得 CO 的物质的量浓度随反应时间的变化如图所示:
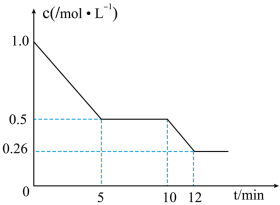
②T1℃时,该反应的化学平衡常数 K=
③10min 时,改变的外界条件可能是
(6)T1℃下,在 1L 恒容密闭容器中充入 2molCO、2molH2和 3molCH3OH(g),此时反应将
您最近一年使用:0次
9 . 下列有关热化学方程式的叙述中正确的是
| A.中和热的离子方程式为:OH-(aq)+H+(aq)=H2O(g) ∆H=-57.3 kJ·mol-1 |
| B.已知C(s)+O2(g)=CO2(g) ∆H1,C(s)+O2(g)=CO2(s) ∆H2,则∆H1>∆H2 |
| C.已知2H2(g)+O2(g)=2H2O(l) ∆H=-571.6 kJ·mol-1,则H2的燃烧热为-571.6 kJ·mol-1 |
| D.已知C(石墨,s)=C(金刚石,s) ∆H=+1.9 kJ·mol-1,则金刚石比石墨稳定 |
您最近一年使用:0次
10 . 氮及其化合物与我们的生产、生活联系非常密切。
(1)工业上以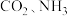 为原料生产尿素
为原料生产尿素 ,反应分两步进行:
,反应分两步进行:
Ⅰ:
Ⅱ: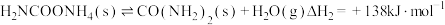
已知: 。
。
①请写出以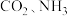 为原料,合成尿素和液态水的热化学方程式:
为原料,合成尿素和液态水的热化学方程式:___________ 。
② 时,在
时,在 的密闭容器中充入
的密闭容器中充入 和
和 模拟工业生产,
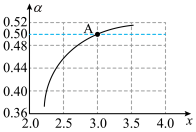
模拟工业生产, ,如图是
,如图是 平衡转化率
平衡转化率 与x的关系,计算图中A点
与x的关系,计算图中A点 的平衡转化率
的平衡转化率
___________ (填分数)。 转变为
转变为 ,其工作原理如图,M极接电源的
,其工作原理如图,M极接电源的___________ 极,N极的电极反应式为___________ 。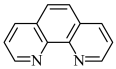 ,简写为phen,遇
,简写为phen,遇 溶液生成橙红色配合物
溶液生成橙红色配合物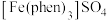 ,其中
,其中 的配位数为6。
的配位数为6。
① 中,phen的
中,phen的___________ 个N参与配位;
② 中,
中,___________ 提供空轨道,___________ 提供孤对电子。
(1)工业上以
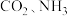 为原料生产尿素
为原料生产尿素 ,反应分两步进行:
,反应分两步进行:Ⅰ:

Ⅱ:
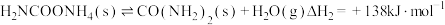
已知:
 。
。①请写出以
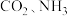 为原料,合成尿素和液态水的热化学方程式:
为原料,合成尿素和液态水的热化学方程式:②
 时,在
时,在 的密闭容器中充入
的密闭容器中充入 和
和 模拟工业生产,
模拟工业生产, ,如图是
,如图是 平衡转化率
平衡转化率 与x的关系,计算图中A点
与x的关系,计算图中A点 的平衡转化率
的平衡转化率
 转变为
转变为 ,其工作原理如图,M极接电源的
,其工作原理如图,M极接电源的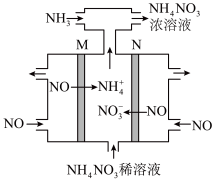
 ,简写为phen,遇
,简写为phen,遇 溶液生成橙红色配合物
溶液生成橙红色配合物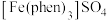 ,其中
,其中 的配位数为6。
的配位数为6。①
 中,phen的
中,phen的②
 中,
中,
您最近一年使用:0次



