1 . 根据所学知识,问答下列问题:
(1)在25℃、101kPa下,已知完全燃烧4.4g丙烷气体,生成 和液态水时,释放222.0kJ热量,
和液态水时,释放222.0kJ热量, 的燃烧热
的燃烧热
___________  。
。
(2)已知:
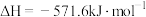 。现有
。现有 和
和 的混合气体共5mol,完全燃烧时释放3847kJ热量,则在混合气体中
的混合气体共5mol,完全燃烧时释放3847kJ热量,则在混合气体中 和
和 的体积比是
的体积比是___________ 。
(3)一个化学过程的示意图如图。已知甲池的总反应为 。
。

①图中甲池是___________ 装置;A(石墨)电极的名称是___________ 。
②写出通入 的电极的电极反应式:
的电极的电极反应式:___________ 。
③乙池中发生反应的化学方程式为___________ 。当乙池中B(Ag)电极的质量增加5.40g时,甲池中理论上消耗___________ mL(标准状况下) 。
。
(1)在25℃、101kPa下,已知完全燃烧4.4g丙烷气体,生成
 和液态水时,释放222.0kJ热量,
和液态水时,释放222.0kJ热量, 的燃烧热
的燃烧热
 。
。(2)已知:

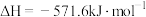 。现有
。现有 和
和 的混合气体共5mol,完全燃烧时释放3847kJ热量,则在混合气体中
的混合气体共5mol,完全燃烧时释放3847kJ热量,则在混合气体中 和
和 的体积比是
的体积比是(3)一个化学过程的示意图如图。已知甲池的总反应为
 。
。
①图中甲池是
②写出通入
 的电极的电极反应式:
的电极的电极反应式:③乙池中发生反应的化学方程式为
 。
。
您最近一年使用:0次
2024-03-06更新
|
53次组卷
|
2卷引用:山西省朔州市怀仁市第九中学高中部2023-2024学年高二上学期11月期中化学试题
解题方法
2 . 硫化氢((H₂S))为易燃危化品,与空气混合能形成爆炸性混合物,遇明火、高热能引起燃烧爆炸,并且硫化氢有剧毒。石油与天然气开采、石油化工、煤化工等行业废气中普遍含有硫化氢,需要回收处理并加以利用。根据所学知识回答下列问题:
(1)已知:Ⅰ.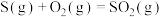
 kJ⋅mol
kJ⋅mol (
( )
)
Ⅱ.
 kJ⋅mol
kJ⋅mol (
( )
)
Ⅲ.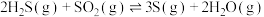
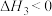
若反应Ⅲ中正反应的活化能为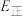 ,逆反应的活化能为
,逆反应的活化能为 ,则
,则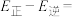
______ (填含a、b的代数式)kJ⋅mol ;在某恒温恒容体系中仅发生反应Ⅲ,下列叙述能说明反应Ⅲ达到平衡状态的是
;在某恒温恒容体系中仅发生反应Ⅲ,下列叙述能说明反应Ⅲ达到平衡状态的是______ (填标号)。
A.体系压强不再变化
B.断裂1 mol 键的同时断裂1 mol
键的同时断裂1 mol  键
键
C.混合气体的密度不再变化
D.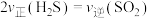
(2)利用工业废气 生产
生产 的反应为
的反应为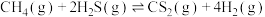 。向某容器中充入1 mol
。向某容器中充入1 mol 、2mol
、2mol 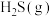 ,体系起始总压强为
,体系起始总压强为 kPa,保持体系总压强不变,反应达到平衡时,四种组分的物质的量分数(x)随温度(T/℃)的变化如图1。
kPa,保持体系总压强不变,反应达到平衡时,四种组分的物质的量分数(x)随温度(T/℃)的变化如图1。
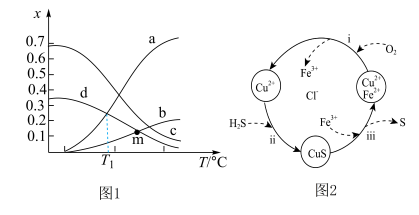
①图中表示 的曲线是
的曲线是______ (填标号)。
② ℃时,该反应的
℃时,该反应的
______ (列出表达式即可,用平衡分压代替平衡浓度,分压=总压×物质的量分数)。
(3)工业中先将废气与空气混合,再通入 、
、 、
、 的混合液中,其转化过程如图2所示。
的混合液中,其转化过程如图2所示。
已知:25℃时,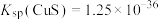 ,
, 的
的 ,
, 。则25℃时过程Ⅱ中的反应
。则25℃时过程Ⅱ中的反应______ (填“能”或“不能”)进行完全。(已知:通常情况下,反应平衡常数 时,认为反应已进行完全)
时,认为反应已进行完全)
(4)某科研小组将微电池技术用于去除废气中的 ,其装置如图3,主要反应:
,其装置如图3,主要反应: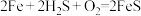
 (FeS难溶于水),室温时,
(FeS难溶于水),室温时, 的条件下,研究反应时间对
的条件下,研究反应时间对 的去除率的影响。
的去除率的影响。

①装置中NaCl溶液的作用是______ ,FeS在______ (填“正”或“负”)极生成。
②一段时间后,电流减小,单位时间内 的去除率降低,可能的原因是
的去除率降低,可能的原因是____________ 。
(1)已知:Ⅰ.
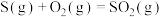
 kJ⋅mol
kJ⋅mol (
( )
)Ⅱ.

 kJ⋅mol
kJ⋅mol (
( )
)Ⅲ.
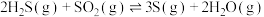
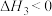
若反应Ⅲ中正反应的活化能为
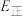 ,逆反应的活化能为
,逆反应的活化能为 ,则
,则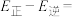
 ;在某恒温恒容体系中仅发生反应Ⅲ,下列叙述能说明反应Ⅲ达到平衡状态的是
;在某恒温恒容体系中仅发生反应Ⅲ,下列叙述能说明反应Ⅲ达到平衡状态的是A.体系压强不再变化
B.断裂1 mol
 键的同时断裂1 mol
键的同时断裂1 mol  键
键C.混合气体的密度不再变化
D.
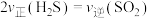
(2)利用工业废气
 生产
生产 的反应为
的反应为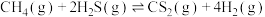 。向某容器中充入1 mol
。向某容器中充入1 mol 、2mol
、2mol 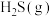 ,体系起始总压强为
,体系起始总压强为 kPa,保持体系总压强不变,反应达到平衡时,四种组分的物质的量分数(x)随温度(T/℃)的变化如图1。
kPa,保持体系总压强不变,反应达到平衡时,四种组分的物质的量分数(x)随温度(T/℃)的变化如图1。
①图中表示
 的曲线是
的曲线是②
 ℃时,该反应的
℃时,该反应的
(3)工业中先将废气与空气混合,再通入
 、
、 、
、 的混合液中,其转化过程如图2所示。
的混合液中,其转化过程如图2所示。已知:25℃时,
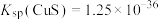 ,
, 的
的 ,
, 。则25℃时过程Ⅱ中的反应
。则25℃时过程Ⅱ中的反应 时,认为反应已进行完全)
时,认为反应已进行完全)(4)某科研小组将微电池技术用于去除废气中的
 ,其装置如图3,主要反应:
,其装置如图3,主要反应: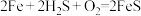
 (FeS难溶于水),室温时,
(FeS难溶于水),室温时, 的条件下,研究反应时间对
的条件下,研究反应时间对 的去除率的影响。
的去除率的影响。
图3
①装置中NaCl溶液的作用是
②一段时间后,电流减小,单位时间内
 的去除率降低,可能的原因是
的去除率降低,可能的原因是
您最近一年使用:0次
名校
解题方法
3 . 我国科学家在合成气直接制烯烃方面的研究获重大突破。已知:

下列说法不正确的是

下列说法不正确的是
| A.△H1-△H2<0 |
| B.反应②为吸热反应 |
C.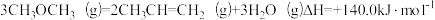 |
D.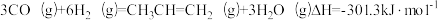 |
您最近一年使用:0次
4 . 纳米花状催化剂Cu/ZnO可用于催化乙酸甲酯加氢制备乙醇,反应历程如图所示,总反应经历如下两步:
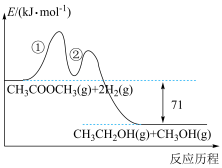
①
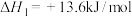
②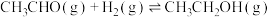

下列说法正确的是

①

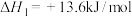
②
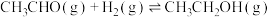

下列说法正确的是
A.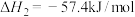 |
| B.反应①决定总反应的速率 |
| C.升高温度,反应①、②的平衡均正向移动 |
D.对于反应①,分离出 时,该反应的正反应增大,逆反应速率减小 时,该反应的正反应增大,逆反应速率减小 |
您最近一年使用:0次
5 . 已知N2O和CO反应进程的相对能量变化如图所示。已知CO(g)的燃烧热ΔH=-283kJ·mol-1。下列说法错误的是
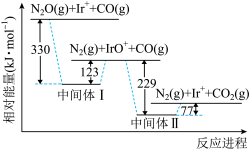

| A.中间体Ⅱ比中间体I稳定 |
| B.Ir+是上述反应的催化剂 |
| C.该反应过程中Ir元素的化合价发生了变化 |
D.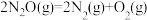 的反应热ΔH为-76kJ·mol-1 的反应热ΔH为-76kJ·mol-1 |
您最近一年使用:0次
6 . 我国是世界上最大的PO (环氧丙烷,C3H6O)生产国,环氧丙烷是一种高价值化工中间体,广泛用于化工、农药汽车、纺织等行业。回答下列问题:
(1)“丙烯与氧气直接环氧化法”是最经济和绿色的PO生产途径,有关反应为2CH2=CH-CH3(g)+O2(g)→2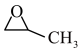 (g),该反应的△H=
(g),该反应的△H=_______ 。【已知:丙烯、环氧丙烷(C3H6O)的燃烧热(△H)分别为-2049 kJ/mol、-1887.6 kJ/mol。]
(2)在以上直接环氧化过程中,丙烯易被氧气部分氧化为丙烯醛,并进而被深度氧化为CO2.图(a)为丙烯反应速率(用★表示)、产物选择性与温度的关系曲线(以c-Cu2O纳米晶为催化剂)。
注:产物(X)选择性=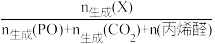 ×100%
×100%
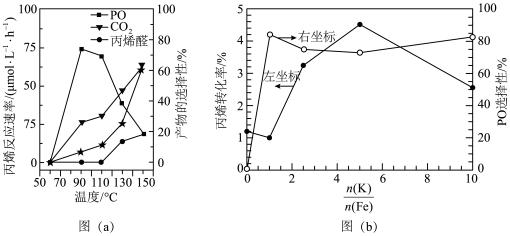
若在实际生产中选择110℃左右作为“丙烯与氧气直接环氧化法”的反应温度,其原因是_______ 。
(3)在KCl修饰的FeOx/SBA-15催化剂作用下,丙烯也可以被N2O氧化为环氧丙烷,该反应为CH2=CH-CH3(g)+N2O(g)
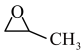 (g)+N2(g)。
(g)+N2(g)。
①已知在325℃时,该催化剂中的钾铁比 对以上反应中丙烯转化率和PO选择性的影响如图(b)所示,当钾铁比=2.5时,丙烯的转化率
对以上反应中丙烯转化率和PO选择性的影响如图(b)所示,当钾铁比=2.5时,丙烯的转化率_______ (填“是”或“不是”)对应温度下的平衡转化率,判断理由是_______ 。
②350℃下,在一恒容密闭容器进行上述反应,已知起始压强为p(C3H6)=2.5kPa,p(N2O)=25.3kPa.忽略其他副反应,丙烯的平衡转化率为α,则平衡时的p(PO)=_______ kPa(用含a的代数式表示,下同),以上反应用平衡分压代替平衡浓度表示的平衡常数Kp=_______ (列出计算式,分压=总压×物质的量分数)。
(1)“丙烯与氧气直接环氧化法”是最经济和绿色的PO生产途径,有关反应为2CH2=CH-CH3(g)+O2(g)→2
 (g),该反应的△H=
(g),该反应的△H=(2)在以上直接环氧化过程中,丙烯易被氧气部分氧化为丙烯醛,并进而被深度氧化为CO2.图(a)为丙烯反应速率(用★表示)、产物选择性与温度的关系曲线(以c-Cu2O纳米晶为催化剂)。
注:产物(X)选择性=
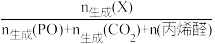 ×100%
×100%
若在实际生产中选择110℃左右作为“丙烯与氧气直接环氧化法”的反应温度,其原因是
(3)在KCl修饰的FeOx/SBA-15催化剂作用下,丙烯也可以被N2O氧化为环氧丙烷,该反应为CH2=CH-CH3(g)+N2O(g)

 (g)+N2(g)。
(g)+N2(g)。①已知在325℃时,该催化剂中的钾铁比
 对以上反应中丙烯转化率和PO选择性的影响如图(b)所示,当钾铁比=2.5时,丙烯的转化率
对以上反应中丙烯转化率和PO选择性的影响如图(b)所示,当钾铁比=2.5时,丙烯的转化率②350℃下,在一恒容密闭容器进行上述反应,已知起始压强为p(C3H6)=2.5kPa,p(N2O)=25.3kPa.忽略其他副反应,丙烯的平衡转化率为α,则平衡时的p(PO)=
您最近一年使用:0次
7 . 2023年7月28日,第31届世界大学生运动会在四川省成都市盛大开幕。已知:
回答下列问题:
(1)火炬“蓉火"采用了生物质丙烷为燃料。
①写出表示丙烷气体燃烧热的热化学方程式:_______ 。
②生物质丙烷由秸秆、稻壳、玉米芯等废弃物合成而来,与传统来自天然气加工和石油提炼的丙烷相比,其优点是_______ 。
(2)火炬“蓉火”通过优化燃料喷注和空气掺混等方式,减少了燃料的使用量,其原因是_______ 。
(3)我国科学家将甲烷无氧偶联制备乙烷和氢气,根据以上数据,计算该反应2CH4(g)=C2H6(g)+H2(g)的△H=_______ 。
| 物质 | 甲烷CH4 | 乙烷C2H6 | 丙烷C3H8 | H2 |
| 燃烧热△H/(kJ/mol) | -890.3 | -1559.8 | -2219.9 | -285.8 |
(1)火炬“蓉火"采用了生物质丙烷为燃料。
①写出表示丙烷气体燃烧热的热化学方程式:
②生物质丙烷由秸秆、稻壳、玉米芯等废弃物合成而来,与传统来自天然气加工和石油提炼的丙烷相比,其优点是
(2)火炬“蓉火”通过优化燃料喷注和空气掺混等方式,减少了燃料的使用量,其原因是
(3)我国科学家将甲烷无氧偶联制备乙烷和氢气,根据以上数据,计算该反应2CH4(g)=C2H6(g)+H2(g)的△H=
您最近一年使用:0次
解题方法
8 . 随着化石能源的减少,新能源的开发利用日益迫切。
(1)Bunsen热化学循环制氢工艺由下列三个反应组成:
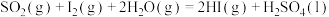
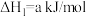
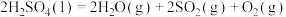
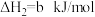
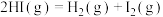
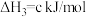
则: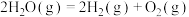

___________ kJ/mol。
(2)硅光电池作为电源已广泛应用于人造卫星、灯塔和无人气象站等,工业制备纯硅的反应为
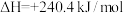 ,若将生成的HCl通入100mL1mol/L的NaOH溶液中恰好完全反应,则此制备纯硅反应过程
,若将生成的HCl通入100mL1mol/L的NaOH溶液中恰好完全反应,则此制备纯硅反应过程___________ (填“吸收”或“放出”)的热量是___________ kJ。
(3)甲醇是一种新型的汽车动力燃料。
①以 和
和 为原料合成甲醇,反应的能量变化如下图所示,则图中A处应填写的内容为
为原料合成甲醇,反应的能量变化如下图所示,则图中A处应填写的内容为___________ 。

②工业上利用CO和 来制备甲醇气体。已知某些化学键的键能数据如下表:
来制备甲醇气体。已知某些化学键的键能数据如下表:
设CO以 键构成,则工业制备甲醇的热化学方程式为
键构成,则工业制备甲醇的热化学方程式为___________ 。
(4)恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图所示:
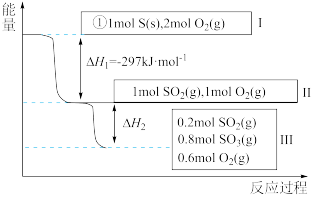
已知: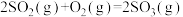

①表示硫的燃烧热的热化学方程式为___________ 。
②图中
___________ kJ/mol。
(1)Bunsen热化学循环制氢工艺由下列三个反应组成:
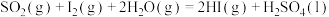
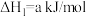
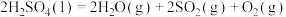
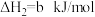
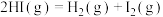
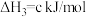
则:
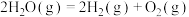

(2)硅光电池作为电源已广泛应用于人造卫星、灯塔和无人气象站等,工业制备纯硅的反应为

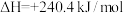 ,若将生成的HCl通入100mL1mol/L的NaOH溶液中恰好完全反应,则此制备纯硅反应过程
,若将生成的HCl通入100mL1mol/L的NaOH溶液中恰好完全反应,则此制备纯硅反应过程(3)甲醇是一种新型的汽车动力燃料。
①以
 和
和 为原料合成甲醇,反应的能量变化如下图所示,则图中A处应填写的内容为
为原料合成甲醇,反应的能量变化如下图所示,则图中A处应填写的内容为
②工业上利用CO和
 来制备甲醇气体。已知某些化学键的键能数据如下表:
来制备甲醇气体。已知某些化学键的键能数据如下表:| 化学键 |  |  |  |  |  |  |
键能/ | 348 | 413 | 436 | 358 | 1072 | 463 |
 键构成,则工业制备甲醇的热化学方程式为
键构成,则工业制备甲醇的热化学方程式为(4)恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图所示:

已知:
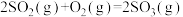

①表示硫的燃烧热的热化学方程式为
②图中

您最近一年使用:0次
2023-11-17更新
|
216次组卷
|
2卷引用:山西省临汾市2023-2024学年高二上学期11月期中考试化学试题
9 . 化学反应产生的巨大能量能把火箭送入太空,研究火箭推进剂的放热原理意义重大。回答下列问题:
(1)①已知16.0g气态肼( )在氧气中完全燃烧生成氮气和气态水,放出272kJ热量,
)在氧气中完全燃烧生成氮气和气态水,放出272kJ热量, 完全燃烧的热化学方程式是
完全燃烧的热化学方程式是___________ 。
②已知断裂1mol共价键所需能量如下表:
结合①,表中
___________ 。
(2)已知:①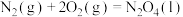
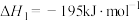
②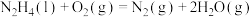

③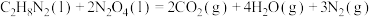
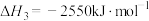
根据反应①②,1mol 与
与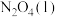 完全反应生成
完全反应生成 和水蒸气时放出的热量为
和水蒸气时放出的热量为___________ kJ,火箭推进剂使用 和
和 的主要优点是
的主要优点是___________ 。
(3)Ⅰ.已知部分物质的相对能量如图所示,则表示 的燃烧热的热化学方程式为
的燃烧热的热化学方程式为___________ 。
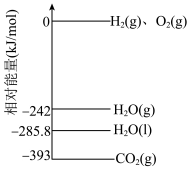
热值是火箭燃料的另一个指标,它是指单位质量的燃料完全燃烧放出的热量,单位为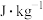 ,有高热值(氢元素产物为液态水)与低热值(氢元素产物为气态水)之分。三类火箭燃料中煤油的低热值高达
,有高热值(氢元素产物为液态水)与低热值(氢元素产物为气态水)之分。三类火箭燃料中煤油的低热值高达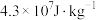 ,氢气的低热值为
,氢气的低热值为___________ 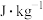 。
。
Ⅱ.三种催化剂催化甲烷脱氢制备 的过程能量变化如图。
的过程能量变化如图。
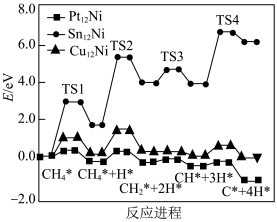
①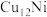 、
、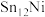 、
、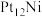 三种催化剂催化甲烷脱氢过程的脱氢速率分别为
三种催化剂催化甲烷脱氢过程的脱氢速率分别为 、
、 、
、 ,则脱氢速率由大到小的顺序为
,则脱氢速率由大到小的顺序为___________ 。
②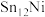 催化甲烷脱氢过程中,速率最快的基元反应的方程式是
催化甲烷脱氢过程中,速率最快的基元反应的方程式是___________ 。
(1)①已知16.0g气态肼(
 )在氧气中完全燃烧生成氮气和气态水,放出272kJ热量,
)在氧气中完全燃烧生成氮气和气态水,放出272kJ热量, 完全燃烧的热化学方程式是
完全燃烧的热化学方程式是②已知断裂1mol共价键所需能量如下表:
| 化学键 | N≡N | O=O | N―N | N―H | O―H |
| 断裂1mol共价键所需能量(kJ/mol) | x | 497 | 193 | 391 | 463 |

(2)已知:①
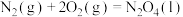
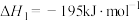
②
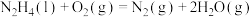

③
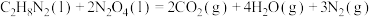
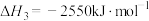
根据反应①②,1mol
 与
与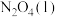 完全反应生成
完全反应生成 和水蒸气时放出的热量为
和水蒸气时放出的热量为 和
和 的主要优点是
的主要优点是(3)Ⅰ.已知部分物质的相对能量如图所示,则表示
 的燃烧热的热化学方程式为
的燃烧热的热化学方程式为
热值是火箭燃料的另一个指标,它是指单位质量的燃料完全燃烧放出的热量,单位为
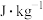 ,有高热值(氢元素产物为液态水)与低热值(氢元素产物为气态水)之分。三类火箭燃料中煤油的低热值高达
,有高热值(氢元素产物为液态水)与低热值(氢元素产物为气态水)之分。三类火箭燃料中煤油的低热值高达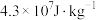 ,氢气的低热值为
,氢气的低热值为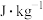 。
。Ⅱ.三种催化剂催化甲烷脱氢制备
 的过程能量变化如图。
的过程能量变化如图。
①
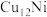 、
、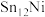 、
、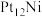 三种催化剂催化甲烷脱氢过程的脱氢速率分别为
三种催化剂催化甲烷脱氢过程的脱氢速率分别为 、
、 、
、 ,则脱氢速率由大到小的顺序为
,则脱氢速率由大到小的顺序为②
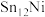 催化甲烷脱氢过程中,速率最快的基元反应的方程式是
催化甲烷脱氢过程中,速率最快的基元反应的方程式是
您最近一年使用:0次
名校
解题方法
10 . 已知:
①
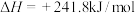
②
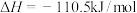
③
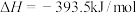
下列说法错误的是
①

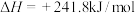
②

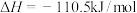
③

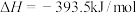
下列说法错误的是
| A.上述反应属于吸热反应的是① |
| B.表示C的燃烧热的热化学方程式是③ |
C.10g 完全燃烧生成水蒸气,放热2418kJ 完全燃烧生成水蒸气,放热2418kJ |
D.CO燃烧的热化学方程式为  |
您最近一年使用:0次
2023-11-14更新
|
146次组卷
|
5卷引用:山西省大同市2023-2024学年高二上学期11月期中考试化学试题



