18-19高二上·湖北宜昌·期末
名校
1 . 硝酸是一种重要的化工原料,工业上生产硝酸的过程如下:
(1)以氮气、氢气为原料合成氨
①下列措施可以提高H2的转化率是(填选项序号)___________ 。
a.选择适当的催化剂 b.增大压强 c.及时分离生成的NH3 d.升高温度
②一定温度下,在密闭容器中充入1molN2和3molH2发生反应。若容器容积恒定,达到平衡状态时,容器内的压强是原来的 15/16,则N2的转化率a1=_____________ ;若容器压强恒定,达到平衡状态时,N2的转化率为a2,则a2______ a1(填“>”、“<”或“=”)
(2)以氨气、空气为主要原料制硝酸。在容积恒定的密闭容器中进行反应2NO(g)+O2(g) 2NO2(g) △H>0,该反应的反应速率(v)随时间(t)变化的关系如下图所示。若t2、t4时刻只改变一个条件,下列说法正确的是(填选项序号)
2NO2(g) △H>0,该反应的反应速率(v)随时间(t)变化的关系如下图所示。若t2、t4时刻只改变一个条件,下列说法正确的是(填选项序号)_____________ 。
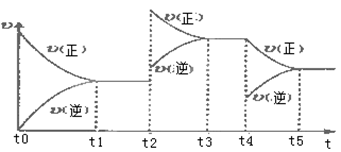
a.在t1~t2时,可依据容器内气体的压强保持不变判断反应已达到平衡状态
b.在t2时,采取的措施一定是升高温度
c.在t3~t4时,可依据容器内气体的密度保持不变判断反应已达到平衡状态
d.在t0~t5时,容器内NO2的体积分数在t3时值的最大
(3)硝酸工厂用H2将NO2还原为N2
已知:2H2(g)+O2(g)=2H2O(g) △H=-483.5kJ/mol
N2(g)+2O2(g)=2NO2(g) △H=+133kJ/mol
则H2还原NO2生成水蒸气反应的热化学方程式是___________________
(1)以氮气、氢气为原料合成氨
①下列措施可以提高H2的转化率是(填选项序号)
a.选择适当的催化剂 b.增大压强 c.及时分离生成的NH3 d.升高温度
②一定温度下,在密闭容器中充入1molN2和3molH2发生反应。若容器容积恒定,达到平衡状态时,容器内的压强是原来的 15/16,则N2的转化率a1=
(2)以氨气、空气为主要原料制硝酸。在容积恒定的密闭容器中进行反应2NO(g)+O2(g)
 2NO2(g) △H>0,该反应的反应速率(v)随时间(t)变化的关系如下图所示。若t2、t4时刻只改变一个条件,下列说法正确的是(填选项序号)
2NO2(g) △H>0,该反应的反应速率(v)随时间(t)变化的关系如下图所示。若t2、t4时刻只改变一个条件,下列说法正确的是(填选项序号)
a.在t1~t2时,可依据容器内气体的压强保持不变判断反应已达到平衡状态
b.在t2时,采取的措施一定是升高温度
c.在t3~t4时,可依据容器内气体的密度保持不变判断反应已达到平衡状态
d.在t0~t5时,容器内NO2的体积分数在t3时值的最大
(3)硝酸工厂用H2将NO2还原为N2
已知:2H2(g)+O2(g)=2H2O(g) △H=-483.5kJ/mol
N2(g)+2O2(g)=2NO2(g) △H=+133kJ/mol
则H2还原NO2生成水蒸气反应的热化学方程式是
您最近一年使用:0次
2 . 汽车尾气中含有CO、NO、NO2、碳氢化合物等多种污染物。回答下列问题:
(1)汽车燃料中不含氮元素,尾气中所含NO产生的原因是____________________ 。
(2)已知:2C8H18(1)+25O2(g)=16CO2(g)+18H2O(g) △H1=-10244kJ·mol-1
N2(g)+O2(g)=2NO(g) △H2
2NO(g)+2CO(g)=N2(g)+2CO2(g) △H3=-746kJ·mol-1
①若H2O(1)=H2O(g) △H=+44kJ·mol-1,则表示辛烷燃烧热的热化学方程式为____________________ 。
②部分化学键键能数据如下:
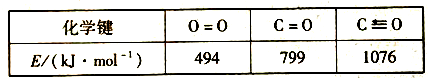
△H2=__________ kJ·mol-1
(3)1573K时,N2+O2 2NO平衡常数为2.0×10-6,若测得内燃机内平衡混合气中氮气、氧气的物质的量分别为0.2mol、0.001mol,则生成NO的物质的量为
2NO平衡常数为2.0×10-6,若测得内燃机内平衡混合气中氮气、氧气的物质的量分别为0.2mol、0.001mol,则生成NO的物质的量为__________ mol,N2的转化率为__________ 。
(4)反应NO(g)+CO(g)=N2(g)+CO2(g)的平衡常数为1.68×1060,从热力学角度看,该反应程度应该很大,实际汽车尾气中该反应的程度很小,原因是____________________ ,要增大汽车尾气净化装置中单位时间内该反应的程度,关键是要____________________ 。
(5)T<500K时,反应NO2(g)+CO(g)=NO(g)+CO2(g)分两步进行:
第一步:NO2(g)+NO2(g)→NO3(g)+NO(g) (慢反应)
第二步:NO3(g)+CO(g)→NO(g)+CO2(g) (快反应)
下列表述正确的是__________ (填标号)
A.反应速率与NO浓度有关 B.反应速率与NO2浓度有关
C.反应的中间产物只有NO3 D.第二步反应活化能较高
(1)汽车燃料中不含氮元素,尾气中所含NO产生的原因是
(2)已知:2C8H18(1)+25O2(g)=16CO2(g)+18H2O(g) △H1=-10244kJ·mol-1
N2(g)+O2(g)=2NO(g) △H2
2NO(g)+2CO(g)=N2(g)+2CO2(g) △H3=-746kJ·mol-1
①若H2O(1)=H2O(g) △H=+44kJ·mol-1,则表示辛烷燃烧热的热化学方程式为
②部分化学键键能数据如下:

△H2=
(3)1573K时,N2+O2
 2NO平衡常数为2.0×10-6,若测得内燃机内平衡混合气中氮气、氧气的物质的量分别为0.2mol、0.001mol,则生成NO的物质的量为
2NO平衡常数为2.0×10-6,若测得内燃机内平衡混合气中氮气、氧气的物质的量分别为0.2mol、0.001mol,则生成NO的物质的量为(4)反应NO(g)+CO(g)=N2(g)+CO2(g)的平衡常数为1.68×1060,从热力学角度看,该反应程度应该很大,实际汽车尾气中该反应的程度很小,原因是
(5)T<500K时,反应NO2(g)+CO(g)=NO(g)+CO2(g)分两步进行:
第一步:NO2(g)+NO2(g)→NO3(g)+NO(g) (慢反应)
第二步:NO3(g)+CO(g)→NO(g)+CO2(g) (快反应)
下列表述正确的是
A.反应速率与NO浓度有关 B.反应速率与NO2浓度有关
C.反应的中间产物只有NO3 D.第二步反应活化能较高
您最近一年使用:0次
3 . 回答下列问题。
(1)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g) =2Fe(s)+3CO2(g) △H= -24.8kJ/mol
3Fe2O3(s)+ CO(g) =2Fe3O4(s)+ CO2(g) △H= -47.2kJ/mol
Fe3O4(s)+CO(g) =3FeO(s)+CO2(g) △H= +640.4kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:__________ 。
(2)化学在环境保护中起十分重要的作用,电化学降解法可用于治理水中硝酸盐污染,电化学降解NO3—的原理如图所示。

①电源正极为____ (填“A”或“B”),阴极的电极反应式为___________________________ 。
②若电解过程中转移了2 mol电子,则膜两侧电解液的质量变化差(Δm左-Δm右)为___ g。
(1)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g) =2Fe(s)+3CO2(g) △H= -24.8kJ/mol
3Fe2O3(s)+ CO(g) =2Fe3O4(s)+ CO2(g) △H= -47.2kJ/mol
Fe3O4(s)+CO(g) =3FeO(s)+CO2(g) △H= +640.4kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:
(2)化学在环境保护中起十分重要的作用,电化学降解法可用于治理水中硝酸盐污染,电化学降解NO3—的原理如图所示。

①电源正极为
②若电解过程中转移了2 mol电子,则膜两侧电解液的质量变化差(Δm左-Δm右)为
您最近一年使用:0次
名校
4 . (Ⅰ)工业上可以用煤和水为原料通过一系列转化变为清洁能源氢气或者合成工业原料甲醇等。
(1)用煤制取氢气的反应是C(s)+2H2O(g) CO2(g)+2H2(g)△H>0,若已知碳的燃烧热和氢气的燃烧热,
CO2(g)+2H2(g)△H>0,若已知碳的燃烧热和氢气的燃烧热,____ (填“能”或“不能”)求出上述反应的△H。
(2)工业上也可以仅利用上述反应得到的CO2和H2进一步合成甲醇,反应方程式如下:CO2(g)+3H2(g)⇌ CH3OH(g)+H2O(g)△H=-49.0kJ/mol,则在工业生产中,CO2和H2的转化率_____________ (选填“前者大”、“后者大”、“无法确定”);若提供的氢气为12mol,达到平衡时放出的热量为137.2kJ,则氢气的转化率为_______________
(Ⅱ)某研究小组以Ag—ZSM—5为催化剂模拟汽车尾气的处理,实现NO和CO反应转化为无毒气体,同时利用反应放出的热量预热NO和CO。实验测得NO的转化率随温度的变化如图所示。
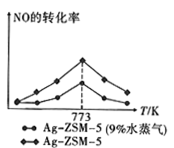
(3)低于773K时,NO的转化率______ (填“是”或者“不是”)对应温度下的平衡转化率,判断理由是______________________________________________________________
(4)为提高汽车尾气中NO的转化率,除了改变温度、压强外,还可以采取的措施有_________ 。
(1)用煤制取氢气的反应是C(s)+2H2O(g)
 CO2(g)+2H2(g)△H>0,若已知碳的燃烧热和氢气的燃烧热,
CO2(g)+2H2(g)△H>0,若已知碳的燃烧热和氢气的燃烧热,(2)工业上也可以仅利用上述反应得到的CO2和H2进一步合成甲醇,反应方程式如下:CO2(g)+3H2(g)⇌ CH3OH(g)+H2O(g)△H=-49.0kJ/mol,则在工业生产中,CO2和H2的转化率
(Ⅱ)某研究小组以Ag—ZSM—5为催化剂模拟汽车尾气的处理,实现NO和CO反应转化为无毒气体,同时利用反应放出的热量预热NO和CO。实验测得NO的转化率随温度的变化如图所示。

(3)低于773K时,NO的转化率
(4)为提高汽车尾气中NO的转化率,除了改变温度、压强外,还可以采取的措施有
您最近一年使用:0次
名校
解题方法
5 . (1)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如下:
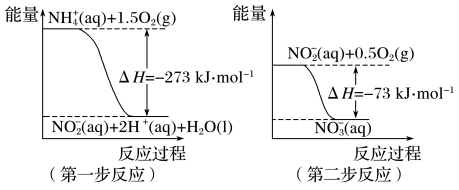
①第一步反应是______________ (填“放热”或“吸热”)反应,判断依据是___________ 。
②1molNH4+(aq)全部氧化成NO3-(aq)的热化学方程式是___________________ 。
(2)已知红磷比白磷稳定,则反应P4(白磷,s)+5O2(g)=2P2O5(s) ΔH1;4P(红磷,s)+5O2(g)=2P2O5(s) ΔH2;ΔH1和ΔH2的关系是ΔH1________ ΔH2(填“>”、“<”或“=”)。
(3)在298 K、101 kPa时,已知:①2H2O(g)=O2(g)+2H2(g) ΔH1;②Cl2(g)+H2(g)=2HCl(g) ΔH2;③2Cl2(g)+2H2O(g)=4HCl(g)+O2(g) ΔH3,则ΔH3与ΔH1和ΔH2之间的关系正确的是________ 。
A.ΔH3=ΔH1+2ΔH2
B.ΔH3=ΔH1+ΔH2
C.ΔH3=ΔH1-2ΔH2
D.ΔH3=ΔH1-ΔH2
(4)已知:
①2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ·mol-1②Na2O2(s)+CO2(g)=Na2CO3(s)+ O2(g) ΔH=-226 kJ·mol-1,则CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数目为
O2(g) ΔH=-226 kJ·mol-1,则CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数目为_____________ 。
(5)已知H2(g)+Br2(l)=2HBr(g) ΔH=-72 kJ·mol-1,蒸发1 mol Br2(l)需要吸收的能量为30 kJ,其他相关数据如下表:
则表中a=________ 。

①第一步反应是
②1molNH4+(aq)全部氧化成NO3-(aq)的热化学方程式是
(2)已知红磷比白磷稳定,则反应P4(白磷,s)+5O2(g)=2P2O5(s) ΔH1;4P(红磷,s)+5O2(g)=2P2O5(s) ΔH2;ΔH1和ΔH2的关系是ΔH1
(3)在298 K、101 kPa时,已知:①2H2O(g)=O2(g)+2H2(g) ΔH1;②Cl2(g)+H2(g)=2HCl(g) ΔH2;③2Cl2(g)+2H2O(g)=4HCl(g)+O2(g) ΔH3,则ΔH3与ΔH1和ΔH2之间的关系正确的是
A.ΔH3=ΔH1+2ΔH2
B.ΔH3=ΔH1+ΔH2
C.ΔH3=ΔH1-2ΔH2
D.ΔH3=ΔH1-ΔH2
(4)已知:
①2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ·mol-1②Na2O2(s)+CO2(g)=Na2CO3(s)+
 O2(g) ΔH=-226 kJ·mol-1,则CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数目为
O2(g) ΔH=-226 kJ·mol-1,则CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数目为(5)已知H2(g)+Br2(l)=2HBr(g) ΔH=-72 kJ·mol-1,蒸发1 mol Br2(l)需要吸收的能量为30 kJ,其他相关数据如下表:
物质 | H2(g) | Br2(g) | HBr(g) |
1mol分子中的化学键断 裂时需要吸收的能量(kJ) | 436 | 200 | a |
则表中a=
您最近一年使用:0次
2019-01-01更新
|
297次组卷
|
6卷引用:湖北省沙市中学2017-2018学年高二上学期第一次双周考化学试题
解题方法
6 . (1)广州亚运会“潮流”火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料。试回答下列问题:
①如图是一定量丙烷完全燃烧生成CO2和1 mol H2O(l)过程中的能量变化图,请在图中的括号内填入“+”或“-”_____ 。

②写出表示丙烷燃烧热的热化学方程式:___________________________________ 。
③二甲醚(CH3OCH3)是一种新型燃料,应用前景广阔。1 mol二甲醚完全燃烧生成CO2和液态水放出1 455 kJ热量。若1 mol丙烷和二甲醚的混合气体完全燃烧生成CO2和液态水共放出1835 kJ热量,则混合气体中,丙烷和二甲醚的物质的量之比为_______ 。
(2)科学家盖斯曾提出:“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的。”利用盖斯定律可测某些特别反应的热效应。
①P4(s,白磷)+5O2(g)===P4O10(s) ΔH1=-2 983.2 kJ·mol-1
②P(s,红磷)+5/4O2(g)===1/4P4O10(s) ΔH2=-738.5 kJ·mol-1
则白磷转化为红磷的热化学方程式为_________________________________________ 。相同的状况下,能量较低的是________ ;白磷的稳定性比红磷________ (填“高”或“低”)。
①如图是一定量丙烷完全燃烧生成CO2和1 mol H2O(l)过程中的能量变化图,请在图中的括号内填入“+”或“-”

②写出表示丙烷燃烧热的热化学方程式:
③二甲醚(CH3OCH3)是一种新型燃料,应用前景广阔。1 mol二甲醚完全燃烧生成CO2和液态水放出1 455 kJ热量。若1 mol丙烷和二甲醚的混合气体完全燃烧生成CO2和液态水共放出1835 kJ热量,则混合气体中,丙烷和二甲醚的物质的量之比为
(2)科学家盖斯曾提出:“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的。”利用盖斯定律可测某些特别反应的热效应。
①P4(s,白磷)+5O2(g)===P4O10(s) ΔH1=-2 983.2 kJ·mol-1
②P(s,红磷)+5/4O2(g)===1/4P4O10(s) ΔH2=-738.5 kJ·mol-1
则白磷转化为红磷的热化学方程式为
您最近一年使用:0次
名校
7 . (1)已知在常温常压下:
①CH3OH(l)+O2(g)===CO(g)+2H2O(g) ΔH=-354.8 kJ·mol-1
②2CO(g)+O2(g)===2CO2(g) ΔH=-566.0 kJ·mol-1
③H2O(g)===H2O(l) ΔH=-44.0 kJ·mol-1
则表示CH3OH(l)燃烧热的热化学方程式为______________________________________ 。
(2)由甲醇、氧气和NaOH溶液构成的新型手机电池,充电一次可使手机连续使用一个月。
①该电池负极的电极反应式为________________________________________________ 。
②若以该电池为电源,用石墨作电极电解200 mL含有如下离子的溶液。
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)。阳极上最先发生的反应为___________________________ ;从各阶段的电解总反应方程式来看,最初是电解__________ (填写化学式,下同)溶液,然后是电解________ 溶液,最后是电解H2O。
①CH3OH(l)+O2(g)===CO(g)+2H2O(g) ΔH=-354.8 kJ·mol-1
②2CO(g)+O2(g)===2CO2(g) ΔH=-566.0 kJ·mol-1
③H2O(g)===H2O(l) ΔH=-44.0 kJ·mol-1
则表示CH3OH(l)燃烧热的热化学方程式为
(2)由甲醇、氧气和NaOH溶液构成的新型手机电池,充电一次可使手机连续使用一个月。
①该电池负极的电极反应式为
②若以该电池为电源,用石墨作电极电解200 mL含有如下离子的溶液。
| 离子 | Cu2+ | H+ | Cl- | SO42- |
| c/(mol·L-1) | 0.5 | 2 | 2 | 0.5 |
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)。阳极上最先发生的反应为
您最近一年使用:0次
8 . 对机动车尾气中的N元素、C 元素进行处理,可以保护环境,减少污染。
(1)汽缸中生成 NO 的反应为:N2(g)+O2(g) 2NO(g) △H>0,NOx在铑(Rh)的催化下最终转化为无毒的产物,其中NO与CO的反应过程中经历如下两步(已知:1kcal=4.18kJ):
2NO(g) △H>0,NOx在铑(Rh)的催化下最终转化为无毒的产物,其中NO与CO的反应过程中经历如下两步(已知:1kcal=4.18kJ):
反应Ⅰ:NO(g)+CO(g)+Rh(s) RhN(s)+CO2(g) △H=-8kcal·mol-1
RhN(s)+CO2(g) △H=-8kcal·mol-1
反应Ⅱ:RhN(s)+NO(g) Rh(s)+N2O(g) △H =-76.4kcal·mol-1
Rh(s)+N2O(g) △H =-76.4kcal·mol-1
则由NO生成1mol N2O的△H =____ kcal·mol-1。若Ⅰ比Ⅱ的反应速率大,下列能正确表示反应2NO(g)+CO(g) N2O(g)+CO2(g) △H在有催化剂(a)和无催化剂(b)时反应进程的能量变化图的是
N2O(g)+CO2(g) △H在有催化剂(a)和无催化剂(b)时反应进程的能量变化图的是_____

⑵在体积为1L的恒温密闭容器中,发生反应:
2NO(g)+2CO (g)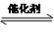 N2(g)+2CO2(g),有关物质的量如下表:
N2(g)+2CO2(g),有关物质的量如下表:
①上述反应的化学平衡常数表达式K=__________
②若达到平衡后气体的压强为开始时的0.875倍,则a =______
⑶汽车使用乙醇汽油并不能减少NOx的排放,某研究小组在实验室以耐高温试剂Ag-ZSW-5催化,测得NO转化为N2的转化率随温度变化情况如下图所示。

①在n(NO)/n(CO)=1条件下,最佳温度应控制在_____ 左右。
②若不使用CO,温度超过775 K,发现NO的分解率降低,其可能的原因为___
③用平衡移动原理解释为什么加入CO后NO转化为N2的转化率增大?______
(1)汽缸中生成 NO 的反应为:N2(g)+O2(g)
 2NO(g) △H>0,NOx在铑(Rh)的催化下最终转化为无毒的产物,其中NO与CO的反应过程中经历如下两步(已知:1kcal=4.18kJ):
2NO(g) △H>0,NOx在铑(Rh)的催化下最终转化为无毒的产物,其中NO与CO的反应过程中经历如下两步(已知:1kcal=4.18kJ):反应Ⅰ:NO(g)+CO(g)+Rh(s)
 RhN(s)+CO2(g) △H=-8kcal·mol-1
RhN(s)+CO2(g) △H=-8kcal·mol-1反应Ⅱ:RhN(s)+NO(g)
 Rh(s)+N2O(g) △H =-76.4kcal·mol-1
Rh(s)+N2O(g) △H =-76.4kcal·mol-1则由NO生成1mol N2O的△H =
 N2O(g)+CO2(g) △H在有催化剂(a)和无催化剂(b)时反应进程的能量变化图的是
N2O(g)+CO2(g) △H在有催化剂(a)和无催化剂(b)时反应进程的能量变化图的是
⑵在体积为1L的恒温密闭容器中,发生反应:
2NO(g)+2CO (g)
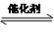 N2(g)+2CO2(g),有关物质的量如下表:
N2(g)+2CO2(g),有关物质的量如下表:| 起始物质的量/mol | 平衡物质的量/mol | |||
| NO | CO | N2 | CO2 | CO2 |
| 0.2 | 0.2 | 0 | 0 | a |
①上述反应的化学平衡常数表达式K=
②若达到平衡后气体的压强为开始时的0.875倍,则a =
⑶汽车使用乙醇汽油并不能减少NOx的排放,某研究小组在实验室以耐高温试剂Ag-ZSW-5催化,测得NO转化为N2的转化率随温度变化情况如下图所示。

①在n(NO)/n(CO)=1条件下,最佳温度应控制在
②若不使用CO,温度超过775 K,发现NO的分解率降低,其可能的原因为
③用平衡移动原理解释为什么加入CO后NO转化为N2的转化率增大?
您最近一年使用:0次
名校
9 . 二氧化碳是用途非常广泛的化工基础原料,回答下列问题:
(1)工业上可以用CO2来生产燃料甲醇。
已知:CO2(g)+3H2(g)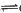 CH3OH(l)+H2O(l) △H=-130kJ·mol-1
CH3OH(l)+H2O(l) △H=-130kJ·mol-1
2H2(g)+O2(g)=2H2O(l) △H=-572kJ·mol-1
CH3OH(l)的燃烧热△H=___________ 。
(2)在催化剂作用下,CO2和CH4可直接转化为乙酸:CO2(g)+CH4(g)=CH3COOH(g) △H>0在不同温度下乙酸的生成速率变化如图所示。

①当温度在250℃—300℃范围时,乙酸的生成速率减慢的主要原因是_________ 。
②欲使乙酸的平衡产率提高,应采取的措施是_____________ (任写一条措施即可)。
(3)一定条件下,在密闭容器中发生反应:2CO(g)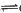 C(s)+CO2(g)。
C(s)+CO2(g)。
①下列能说明该反应达到平衡的是___________ 。
A.容器内混合物的质量不变 B.CO和CO2的物质的量之比不再变化
C.混合气体的平均摩尔质量不再变化 D.形成amolC=O键的同时断裂amolC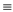 O键
O键
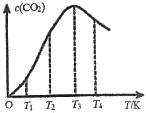
②向某恒容容器中通入一定量的CO发生上述反应,在不同温度下CO2的物质的量浓度c(CO2)随温度的变化如上图所示,则该反应为________ (填“放热”或“吸热”)反应。
③向容积可变的某恒压容器中通入amolCO,TC时反应经过10min达平衡,CO的体积分数为75%。CO的平衡转化率为_______ 。在容积改变的条件下,反应速率可用单位时间内反应物或生成物的物质的量变化来表示,则0-10min内平均反应速率v(CO2)=__________ 。
(1)工业上可以用CO2来生产燃料甲醇。
已知:CO2(g)+3H2(g)
 CH3OH(l)+H2O(l) △H=-130kJ·mol-1
CH3OH(l)+H2O(l) △H=-130kJ·mol-12H2(g)+O2(g)=2H2O(l) △H=-572kJ·mol-1
CH3OH(l)的燃烧热△H=
(2)在催化剂作用下,CO2和CH4可直接转化为乙酸:CO2(g)+CH4(g)=CH3COOH(g) △H>0在不同温度下乙酸的生成速率变化如图所示。

①当温度在250℃—300℃范围时,乙酸的生成速率减慢的主要原因是
②欲使乙酸的平衡产率提高,应采取的措施是
(3)一定条件下,在密闭容器中发生反应:2CO(g)
 C(s)+CO2(g)。
C(s)+CO2(g)。
①下列能说明该反应达到平衡的是
A.容器内混合物的质量不变 B.CO和CO2的物质的量之比不再变化
C.混合气体的平均摩尔质量不再变化 D.形成amolC=O键的同时断裂amolC
 O键
O键②向某恒容容器中通入一定量的CO发生上述反应,在不同温度下CO2的物质的量浓度c(CO2)随温度的变化如上图所示,则该反应为
③向容积可变的某恒压容器中通入amolCO,TC时反应经过10min达平衡,CO的体积分数为75%。CO的平衡转化率为
您最近一年使用:0次
2018-03-09更新
|
848次组卷
|
6卷引用:湖北孝感高中等五校2017-2018学年高二上学期期末联考化学试题
湖北孝感高中等五校2017-2018学年高二上学期期末联考化学试题(已下线)2018-2019学年同步单元双基双测AB卷:第二单元化学反应速率与化学平衡单元测试B卷四川省成都市实验中学2018-2019学年高二上学期期中模拟考试化学试题(已下线)练习3 化学反应速率的计算及其影响因素-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)四川省江油中学2020-2021学年高二下学期3月月考化学试题(已下线)期中试卷01-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版选择性必修1)
10 . 为了研究化学反应A+B═C+D的能量变化情况,某同学设计了如图所示装置.当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升.试回答下列问题:
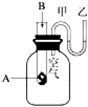
(1)该反应为__________ 反应(填“放热”或“吸热”).
(2)A和B的总能量比C和D的总能量__________ (填“高”或“低”).
(3)物质中的化学能通过化学反应转化成________________ 释放出来.
(4)反应物化学键断裂吸收的能量______ (填“高”或“低”)于生成物化学键形成放出的能量.
(5)写出一个符合题中条件的化学方程式:________________________________________________________________________________
Ⅱ.已知:P4(白磷,s)+5O2(g)═P4O10(s)△H=-2 983.2kJ•mol-1①
P(红磷,s)+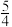 O2(g)═
O2(g)═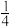 P4O10(s)△H=-738.5kJ•mol-1 ②
P4O10(s)△H=-738.5kJ•mol-1 ②
则白磷转化为红磷的热化学方程式为_________________________________________ .相同状况下,能量状态较低的是 __________ ;白磷的稳定性比红磷 ______ (填“高”或“低”).

(1)该反应为
(2)A和B的总能量比C和D的总能量
(3)物质中的化学能通过化学反应转化成
(4)反应物化学键断裂吸收的能量
(5)写出一个符合题中条件的化学方程式:
Ⅱ.已知:P4(白磷,s)+5O2(g)═P4O10(s)△H=-2 983.2kJ•mol-1①
P(红磷,s)+
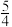 O2(g)═
O2(g)═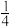 P4O10(s)△H=-738.5kJ•mol-1 ②
P4O10(s)△H=-738.5kJ•mol-1 ② 则白磷转化为红磷的热化学方程式为
您最近一年使用:0次



